文章编号:1004-0609(2009)02-0360-06
钽掺杂金红石型二氧化钛光催化分解水的析氧活性
吴道新1, 2,陈启元1,李 洁1,尹周澜1
(1. 中南大学 化学化工学院,长沙 410083;
2. 长沙理工大学 化学与生物工程学院,长沙 410077)
摘 要:以钛酸丁酯为原料,用低温超声水解方法合成不同Ta掺杂浓度的金红石型TiO2光催化剂,采用XRD、PL、DRS、BET等技术进行了催化剂表征。在光源为高压汞灯和氙灯、Fe3+为电子受体、悬浮液pH值为2.0的条件下,考察Ta掺杂对金红石型TiO2的光催化分解水析氧活性的影响。结果表明:Ta掺杂量(质量分数)在1.0%~5.0%范围时,Ta掺杂没有改变金红石型TiO2的晶型,表面形成氧空位,在导带底附近形成施主能级,有利于光生电子和空穴的分离,掺杂催化剂光致发光强度与其光催化析氧活性的变化趋势一致;当Ta掺杂量在1.0%时,掺杂催化剂的光催化分解水析氧活性最高,紫外光和可见光下光催化分解水的析氧速率分别为130.4和69.6 μmol/(L?h),比金红石型TiO2掺杂改性前的析氧速率分别提高14.6%和12.1%.
关键词:金红石型TiO2;掺杂钽;光催化分解水;析氧
中图分类号:O 643.32 文献标识码: A
Photocatalytic oxidation of water to O2 over Ta-dopant of rutile TiO2
WU Dao-xin1, 2, CHEN Qi-yuan1, LI Jie1, YIN Zhou-lan1
(1. School of Chemistry and Chemical Engineering, Central South University, Changsha 410083, China;
2. School of Chemistry and Biological Engineering, Changsha University of Science and Technology,
Changsha 410076, China)
Abstract: The photocatalyst of Ta-doped rutile TiO2 with different Ta doping concentrations were prepared by low temperature ultrasonic hydrolysis using tetrabutyl titanate(C16H36O4Ti) as raw material. This photocatalyst was characterized by XRD, PL, DRS and BET. Under the condition of Fe3+ as electron acceptor, pH=2.0 with UV irradiation and visible radiation, the effects of various Ta doping concentrations on the photocatalytic oxidation activity of Ta doped rutile TiO2 particles were investigated. The results show that with appropriate concentration ranging in 1.0%?5.0%, Ta can be doped into rutile TiO2 lattice without causing any change in rutile TiO2 crystal structure. Therefore, the surface oxygen vacancies and the donor energy level near the bottom of the conduction band lead to easier departure of photoinduced electrons from holes to achieve stronger photocatalytic activity. The highest photocatalytic oxygen evolution and PL Spectra intensity are achieved. When the concentration of Ta is 1.0%, the O2 evolution speeds are 130.4 and 69.6 umol/(L?h) under UV irradiation and visible radiation, which are 14.6% and 12.1% higher than those before doping, respectively.
Key words: rutile titania; Ta-doped; photocatalytic water splitting; oxygen evolution
氢能是人们期待的新的二次能源,利用太阳能光催化分解水(简称光解水)制取氢气[1],可望使廉价制氢气技术成为现实,具有广泛的应用前景。目前光解水的光催化量子化效率还比较低,效率难于提高,制备具有较高光催化活性的催化材料,以及光解水循环反应体系的实用化,是光解水研究领域的热点[2]。光解水分为析氢和析氧两个半反应,而析氧过程是一个难以实现的半反应,对催化材料的要求高。BAMWENDA等[3?5]研究CeO2,WO3,TiO2光催化分解水析氧活性,金红石型二氧化钛析氧活性较其他氧化物高。SAYAMA和ARAKAWA[6]研究负载Pt对TiO2分解水催化活性的影响,LEE等[7]研究了NiO对TiO2负载的光催化效果,在可见光下光催化活性不高。WONG等[8?13] 发现通过掺杂金属离子改善催化剂光催化性能。金红石型二氧化钛虽然在光催化分解水方面被用作催化剂,但其存在光利用率低、析氧速率不高等缺点,施主掺杂Nb能够提高TiO2的催化性能[14],但关于Ta掺杂对TiO2光解水析氧研究尚未见报道。本文作者用钛酸丁酯低温超声水解方法合成不同Ta掺杂浓度的金红石型TiO2,采用X射线衍射(XRD)、光致发光光谱(PL)和漫反射光谱(DRS)等技术进行催化剂形貌和结构表征,并研究Ta掺杂对金红石型TiO2光催化分解水析氧活性的影响。
1 实 验
1.1 实验仪器与试剂
XRD分析采用日本理学D/max2250 X射线衍射分析仪;BET分析采用美国Micromeritics Instrument Corporation公司ASAP2020 Surface Area and Porosity Analyzer;TG-DSC分析采用瑞士梅特勒?托力多公司TGA/SDTA851热重差热同步分析仪;DRS分析采用北京普析通用仪器有限责任公司的TU?1901型紫外?可见分光光度计;PL分析采用美国PE公司LS?45型原子荧光分光光度计;样品制备采用长沙华信合金机电有限公司SK2?6?13型程序控温高温管式电阻炉;产物氧气的检测采用上海天普分析仪器有限公司SP?2305型气相色谱仪(热导池检测器、氩气为载气、固定相为5A的分子筛)。
钛酸丁酯、无水乙醇和Ta2O5等试剂均为分析纯。
1.2 催化剂的制备
室温下,将一定量的钛酸丁酯和无水乙醇混合均匀,将混合物滴加到装有硝酸酸化蒸馏水烧杯中,冰水冷却,45 min滴加完毕,超声强化处理(100 W,20~25 kHz,4 min,间歇工作频率为5 s),磁力搅拌3 h,减压浓缩至粘稠,分别加入含Ta为0.5%、1.0%、2.0%、3.0%、4.0%、5.0%(摩尔分数)的Ta2O5(以Ti摩尔比计),继续搅拌1.5 h。静置陈化12 h,真空干燥。将前驱物置于高温管式炉中,程序控温,在850 ℃进行热处理3 h(晶相转变温度由前驱物TG-DSC测定得到),冷却,研磨,得到Ta掺杂TiO2催化剂。
1.3 光催化反应
光催化反应采用自制内置光源夹套式石英反应器(560.0 mL),光源为250 W高压汞灯(氙灯)。将蒸馏水煮沸,除溶解氧,冷却后加入到反应器中, 同时加入1.0 g 的催化剂和电子受体Fe3+。磁力搅拌器, 恒温水浴,反应温度为298 K,pH值为2.0。光催化分解水产生的氧气通过气相色谱分析。
2 结果与讨论
2.1 光解水析氧活性
在Fe3+的浓度为8.0 mmol/L(体系中Fe3+浓度为0时,没有氧气产生[14])、在高压汞灯和氙灯照射下,Ta掺杂浓度对金红石型TiO2催化剂光催化活性的影响见图1、图2和表1。由图和表所示结果可知,析氧活性与Ta掺杂量存在一定的关系:Ta掺杂能够提高TiO2催化剂的光催化活性,掺杂催化剂存在最佳的Ta掺杂浓度,即在低浓度1.0%~2.0%掺杂量范围内,Ta掺杂TiO2的析氧活性高于未掺杂TiO2的析氧活性,而高浓度3.0%~5.0%Ta掺杂的TiO2的析氧活性低于TiO2的析氧活性。在紫外和可见光源辐射下最佳掺杂浓度为1.0%,1.0%Ta掺杂的TiO2光催化析氧的活性最高,析氧速率分别达130.4和69.6 umol/(L?h),分别比TiO2掺杂改性前析氧速率提高了14.6%和12.1%。
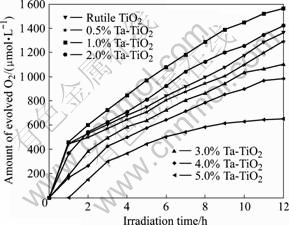
图1 紫外光辐射下Ta掺杂浓度对金红石型TiO2光催化活性的影响
Fig.1 Influence of Ta-dopant concentration on photocatalytic reactivity of rutile TiO2 for O2 evolution under ultraviolet radiation
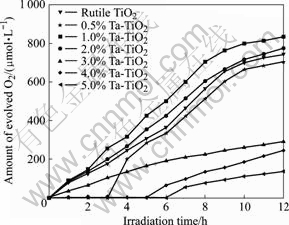
图2 可见光辐射下Ta掺杂浓度对金红石型TiO2光催化活性的影响
Fig.2 Influence of Ta-dopant concentration on photocatalytic reactivity of rutile TiO2 for O2 evolution under visible radiation
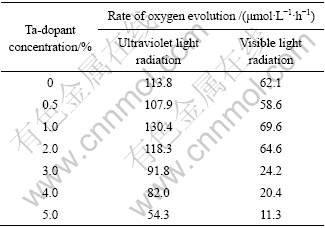
表1 Ta掺杂浓度对金红石型TiO2光催化活性的影响
Table 1 Dependence of Ta-dopant concentration on photocatalytic reactivity of TiO2 for oxygen production
2.2 催化剂XRD分析
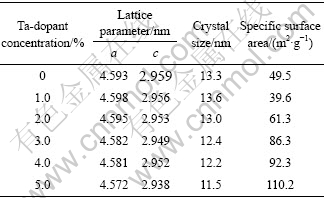
图3所示为不同Ta掺杂浓度改性后的金红石型TiO2的XRD谱。从图可知,所制得的掺杂TiO2催化剂晶型均为金红石型(2θ=27.38?,36.00?,54.25?)。Ta以Ta2O5状态掺入并没有引起TiO2的晶型改变。表2所列为不同的Ta掺杂浓度改性后的金红石型TiO2的特性变化中晶格参数变化的结果。由表可知,催化剂的晶格参数随Ta掺杂浓度增加而减小。Ta5+离子半径0.068 nm和Ti4+离子半径0.068 nm相等,Ta可能以取代方式掺入到金红石型TiO2的晶格中。随着Ta 掺杂量的增加,晶粒尺寸先增加后减小,催化剂比表面积增加,使得晶格内应力增加,晶格畸变增加,晶格参数c变小(见表2)。图4所示为紫外光辐射下光催化反应前后催化剂1.0%Ta掺杂金红石型TiO2的XRD谱,由图可知,经过12 h的光催化反应后催化剂在光催化反应前后结构没有发生改变, 没有发生光氧化或光溶解现象, 催化剂具有良好的稳定性。
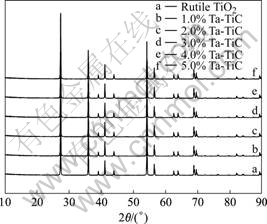
图3 不同Ta掺杂浓度改性后的金红石型TiO2的XRD谱
Fig.3 XRD patterns of rutile TiO2 with different Ta-dopant concentrations
表2 不同Ta掺杂浓度改性后金红石型TiO2的特性变化
Table 2 Influence of Ta-dopant concentration on morphology parameter of rutile TiO2
2.3 催化剂光吸收性能分析
图5所示为Ta掺杂浓度对金红石型TiO2光吸收性能的影响。由图5可知, 在波长为200~380 nm 紫外光范围内, Ta掺杂改性金红石型TiO2与未掺杂金红石型TiO2的光吸收强度基本相当,都表现出具有较强的紫外光光吸收性能,Ta掺杂并没有在紫外光区域内改变催化剂的光吸收性能;在l>400 nm可见光波长范围内,Ta掺杂的金红石型TiO2的光吸收强度较大,Ta掺杂能够使催化剂光吸收性能增强,而且随着Ta掺杂量的增加,改性金红石型TiO2的光吸收强度增强。
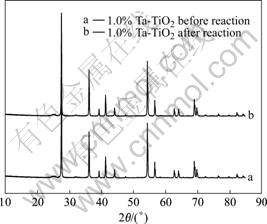
图4 紫外光辐射下光催化反应前后1.0% Ta掺杂金红石型TiO2的XRD谱
Fig.4 XRD patterns of 1.0% Ta-dopant rutile TiO2 before and after photocatalytic reaction under ultraviolet radiation
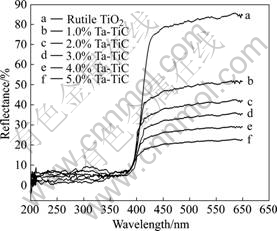
图5 Ta掺杂浓度对金红石型TiO2光吸收性能的影响
Fig.5 Diffuse reflection spectra of rutile TiO2 with different Ta dopant concentrations
上述现象的产生可能有两个原因:其一是由于Ta离子的替代引入,在TiO2晶格中出现缺陷位置,即产生了无序性。由于无序性的影响,以及存在着局域态以及迁移率边缘,会使TiO2导带和价带出现带尾,从而使其局部的带隙能变小,呈现出对可见光有一定强度的吸收。材料的无序性随着Ta掺杂浓度的增大而增加,在可见光区的吸收强度呈现出增强趋势。其二是由于Ta离子的引入,在金红石型TiO2的带隙中产生了施主杂质能级,使Ta离子改性TiO2受激所需的能量变小,故呈现出在λ>400 nm的可见光范围光谱响应向可见光区移动现象。Ta掺杂改性金红石型TiO2的光吸收性能得到提高,其光催化活性也相应得到改善。结合表1可以看出,在一定的掺杂浓度范围内,可见光辐射下Ta掺杂改性后催化剂的光催化析氧活性有一定 增强。
2.4 催化剂光致发光性能分析
图6所示为不同Ta掺杂浓度改性后的金红石型TiO2的PL谱。由图6可知,在激发波长225 nm条件下,波长为400~550 nm范围内,催化剂分别在420和480 nm处出现明显的PL峰,前者可能归属于带边自由激子发光,而后者可能为束缚激子发光。1.0%~ 3.0% Ta掺杂会使金红石型TiO2的光致发光强度增强,而4.0%~5.0% Ta掺杂时,金红石型TiO2的光致发光强度减弱,低于未掺杂金红石型TiO2的光致发光强度。
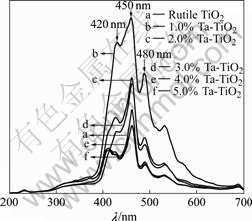
图6 不同Ta掺杂浓度改性后的金红石型TiO2的PL谱
Fig.6 PL spectra of rutile TiO2 with different Ta-dopant concentrations
Ta掺杂量增加时,Ta掺杂金红石型TiO2催化剂颗粒变小(见表2),光生电子从催化剂体相运动到表面的平均自由程短,致使催化剂表面氧空位和缺陷束缚的电子形成激子的几率增大[15],在带隙中接近导带底的位置形成激子能级,产生激子发光,使发光强度增加。Ta掺杂浓度过高时,使得颗粒变得更小,掺杂催化剂表面会产生过多的氧空位和缺陷,在其周围可能会束缚了较多的电子,光生电子与空穴的分离效果降低,导致光致发光性能减弱。
从表1与图6可知,金红石型TiO2经掺杂不同浓度Ta改性后,掺杂催化剂的光催化活性与其PL光谱变化趋势一致,即发光性能好的掺杂催化剂析氧活性高,发光性能差的掺杂催化剂析氧活性低。可见,Ta掺杂对金红石型TiO2光催化分解水析氧过程有促进作用。但光催化析氧与Ta掺杂的量有关,高浓度掺杂反而活性降低。所掺杂的Ta以取代方式掺入到TiO2的晶格中,由于Ta的电荷比Ti4+高,在TiO2的禁带中形成施主能 级[16],该能级位于半导体导带底附近,如图7所示。电子受激发可以很容易转移到杂质能级上,光生电子的数目就会增加,同时延长了空穴的寿命,有利于光催化;另一方面,由于Ta的电荷比Ti4+高,催化剂表面会出现氧空位[16],氧空位能俘获光生电子,一定程度上使得光生电子与空穴分离,提高光催化性能。但是, 高浓度掺杂导致氧空位过多, 可能会在其周围束缚了较多的电子,降低光生电子与空穴的分离效果[17],降低光催化活性。
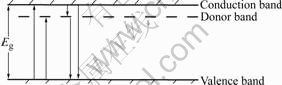
图7 具有施主能级的金红石型TiO2的能带图
Fig.7 Energy band structure of rutile TiO2 photocatalyst with donor doping
3 结 论
1) Ta掺杂金红石型TiO2的光催化分解水析氧活性与Ta掺杂的量有关,低浓度Ta掺杂能够提高金红石型TiO2析氧活性,高浓度掺杂Ta反而降低其析氧活性。
2) Fe3+的初始浓度为8.0 mmol/L,体系pH=2.0,Ta掺杂量在1.0%时,Ta掺杂催化剂的光催化分解水析氧活性最高,其紫外光和可见光下光催化分解水的析氧速率分别为130.4和69.6 umol/(L?h),比金红石型TiO2掺杂改性前的析氧速率分别提高14.6%和12.1%。
3) Ta的掺杂量在1.0%~5.0%范围时,Ta掺杂没有改变金红石型TiO2的晶型,掺杂催化剂光吸收、光致发光强度与其光催化析氧活性的变化趋势一致。
REFERENCES
[1] HONDA K, FUJISHIMA A. Electrochemical photolysis of water at a semiconductor electrode[J]. Nature, 1972, 238: 37?38.
[2] 杨亚辉, 陈启元, 尹周澜, 李 洁, 梁 胜. Fe3 + 和Cr3 + 掺杂对K4 Nb6O17光催化活性的影响[J]. 中国稀土学报, 2004, 22(5): 647?650.
YANG Ya-hui, CHEN Qi-yuan, YIN Zhou-lan, LI Jie, LIANG Sheng. Photocatalytic Activity of K4Nb6O17 Doped with Fe3 + and Cr3 +[J]. Journal of Rare Earth, 2004, 22(5): 647?650.
[3] BAMWENDA G R, UESIGI T, ABE Y. The photocatalytic oxidation of water to O2 over pure CeO2, WO3, and TiO2 using Fe3+ and Ce4+ as electron acceptors[J]. Applied Catalysis A: General, 2001, 205(1/2): 117?128.
[4] BAMWENDA G R, ARAKAWA H. Cerium dioxide as a photocatalyst for water decomposition to O2 in the presence of Ceaq4+ and Feaq3+ species[J]. Journal of Molecular Catalysis A: Chemical, 2000, 161(1/2): 105?113.
[5] BAMWENDA G R, ARAKAWA H. The photoinduced evolution of O2 and H2 from a WO3 aqueous suspension in the presence of Ce4+/Ce3+[J]. Solar Energy Materials and Cells, 2001, 70(1): 1?14.
[6] SAYAMA K, ARAKAWA H. Effect of carbonate salt addition on the photocatalytic decomposition of liquid water over Pt-TiO2 catalyst[J]. The Journal of Chemical Society: Faraday Transactions, 1997, 93(8): 1647?1654.
[7] LEE S G, LEE S, LEE H I. Photocatalytic production of hydrogen from aqueous solution containing CN? as a hole scavenger[J]. Applied Catalysis A: General, 2001, 207(1/2): 173?181.
[8] WONG W K, MALA M A. Doped TiO2 for solar energy applications[J]. Solar Energy, 1986, 36: 163?166.
[9] CHOI W Y, TERMIN A, MICHAEL R H. The role of metal ion dopants in quantumsized TiO2 correlation between photo reactivity and charge carrier recombination dynamics[J]. J Phys Chem, 1994, 98: 13669?13672.
[10] CUI H, D WIGHT K, WOLD A. Surface acidityand photocatalytic activity of Nb2O5/TiO2 photocatalysts[J]. Journal of Solid State Chemistry, 1995, 115: 187?191.
[11] ISHIBASHI K, FUJISHIMA A, WATANABE T, HASHIMOTO K. Quantum yields of active oxidative species formed on TiO2 photocatalyst[J]. Journal of Photochemistry and Photobiology A: Chemistry, 2000, 134: 139?142.
[12] HOFFMANN M R, MARTIN S T, CHOI W. Environmental applications of semiconductor photocatalysis[J]. Chemical Reviews, 1995, 95: 69?76.
[13] PICHAT P, HERRMANN V H, DISDIER J. Modification of the TiO2 Electron density by ion doping or metal deposit and consequences for photoassisded reactions[J]. Studies in Surface Science and Catalysis, 1984: 319?326.
[14] 吴道新, 陈启元, 李 洁, 尹周澜. Nb5+掺杂γ-TiO2的光催化分解水析氧活性研究[J]. 中国有色金属学报, 2008, 18(1): 171?176.
WU Dao-xin, CHEN Qi-yuan, LI Jie, YIN Zhou-lan. The photocatalytic oxidation of water to O2 over Nb5+-dopant of γ-TiO2[J]. The Chinese Journal of Nonferrous Metals, 2008, 18(1): 171?176.
[15] JING Li-qiang, SUN Xiao-jun, XIN Bai-fu, WANG Bai-qi, CAI Wei-min, FU Hong-gang. The preparation and characterization of La doped TiO2 nanoparticles and their photocatalytic activity[J]. Journal of Solid State Chemistry, 2004, 177: 3375?3382.
[16] 徐毓龙. 氧化物与化合物半导体基础[M]. 西安电子科技大学出版社, 1991.
XU Yu-long. Semiconductor basis on oxides and compounds[M]. Xi’an: Xi’an University of Electronic Sciences and Technology Press, 1991.
[17] 高友良, 陈启元, 尹周澜, 胡慧萍, 李 洁. 氧空位对WO3 光催化析氧活性影响的研究[J]. 无机化学学报, 2005, 21(10): 1510?1514.
GAO You-liang, CHEN Qi-yuan, YIN Zhou-lan, HU Hui-ping, LI Jie. Influence of oxygen vacancies of WO3 on photocatalytic activity for O2 evolution[J]. Chinese Journal of Inorganic Chemistry, 2005, 21(10): 1510?1514.
基金项目:国家高技术研究发展计划资助项目(2002AA327140);湖南省科技计划资助项目(2006GK3067);湖南省自然科学基金资助项目(08JJ3022)
收稿日期:2008-06-18;修订日期:2008-10-07
通讯作者:吴道新,高级实验师;电话:0731-8877364;E-mail: daoxinwu@126.com
(编辑 何学锋)