文章编号:1004-0609(2008)12-2291-07
Pb/Zn冶炼废渣生物浸提后余渣的潜在毒性
程 义1,郭朝晖1, 2,邱冠周2,孟 阳1,潘凤开1
(1. 中南大学 材料科学与工程学院,长沙 410083;
2. 中南大学 资源加工与生物工程学院,长沙 410083)
摘 要:在pH为1.5、温度为65 ℃、废渣浓度为5%的优化浸出条件下,通过摇瓶实验,结合扫描电子显微镜、X射线衍射仪和BCR法三步连续提取,研究生物浸提Pb/Zn冶炼废渣后余渣中重金属元素的潜在毒性。结果表明:生物浸出3d后,废渣中As、Cd、Cu和Zn含量分别由原渣中的5 055、20.7、10 718和29 681 g/t降至1 107、2.5、410和4 821 g/t;而Pb主要以硫酸铅及黄钾铁钒类物质等形式沉积在浸出渣中。余渣中As、Cd、Cu、Pb和Zn等重金属主要以残留态存在,其环境活性和潜在危害远低于中国有色金属工业固体废物污染控制标准(GB5085―85)的规定,生物浸出能有效实现Pb/Zn冶炼废渣的无害化机理。
关键词:Pb/Zn冶炼废渣;生物浸出;浸出毒性;无害化机理
中图分类号:X 142; X 705 文献标识码: A
Potential toxicity of bioleached residues from Pb/Zn smelting slag
CHENG Yi 1, GUO Zhao-hui1, 2, QIU Guan-zhou2, MENG Yang1, PAN Feng-kai1
(1. School of Metallurgical Science and Engineering, Central South University, Changsha 410083, China;
2. School of Resources Processing and Bio-engineering, Central South University, Changsha 410083, China)
Abstract: Shaking flask experiments were used to study the bioleaching of heavy metals from Pb/Zn smelting slag under the optimized conditions, which are determined to be pH1.5, 65 ℃ and pulp density of 5%. The residues from the bioleaching were analyzed by scanning electron microscopy, XRD and three-stage BCR sequential extraction procedure. The results show that the heavy metal contents (As, Cd, Cu and Zn) are sharply decreased after 3-day leaching, from 5 055, 20.7, 10 718 and 29 681 g/t to 1 107, 2.5, 410 and 4 821 g/t, respectively. However, the lead mainly deposits in the residues as lead sulfate and jarosite-type compounds. As, Cd, Cu, Pb and Zn in the residues mainly exist in residual form. The environmental availability and potential risk of heavy metals are significantly less than those commended by the Standard for Solid Wastes From Nonferrous Metal Industry of China (GB5085―85), proving that bioleaching can effectively reduce the potential toxicity of Pb/Zn smelting slags.
Key words: Pb/Zn smelting slag; bioleaching; leaching toxicity; innocuous treatment
铅锌冶炼过程中产生的大量废渣含有As、Cd、Cu、Pb和Zn等具有高度迁移性的有价金属元素和有毒元素,长期堆置不仅导致大量有价金属流失,而且对土壤、地下水等周边生态环境造成严重的潜在污染和危害[1?4]。降低废渣中毒性重金属元素含量,减小其环境危害性,实现废渣的资源化和无害化是我国建设资源节约型、环境友好型社会的必然要求。生物浸出技术因其具有处理对象范围广、过程简单、能耗低和环境友好等优点被广泛应用于处理低品位矿[5]、重金属污染土壤[6]和污泥[7]等。然而,应用生物浸出技术的研究主要集中在有价金属的回收率[5, 8?9]及其生物浸出机理[5, 10],对生物浸出后余渣中As、Cd、Cu、Pb和Zn等元素含量、环境活性以及潜在毒性等报道不多[9]。
本课题组利用高温菌群,在pH=1.5、温度65 ℃、矿渣浓度为5%的优化浸出条件下浸提Pb/Zn冶炼废渣,可以较好地浸出废渣中Cu、Zn、In和Ga等有价金属,为实现废渣中有价金属资源化提供可能[8]。然而,生物浸出渣中还含一定量的As、Cd和Pb等有毒重金属元素,这些重金属元素在浸后渣中的潜在毒性将直接影响到生物浸出技术对Pb/Zn冶炼废渣进行资源化与无害化处理的应用前景。因此,本研究通过收集在pH1.5、温度65 ℃、矿渣浓度5%的优化浸出条件[8]下不同浸出时间段的生物浸出渣,利用BCR三步提取法和浸出毒性分析,结合XRD、SEM-EDX等现代分析技术对该浸出余渣的矿物组成、渣中重金属赋存状态等进行分析,研究生物浸提Pb/Zn冶炼废渣后余渣中As、Cd、Cu、Pb和Zn等元素的含量、存在形态与潜在环境毒性,为废渣最终无害化处理和科学利用提供依据。
1 实验
1.1 废渣的来源与处理
实验所用废渣采自某大型铅锌冶炼厂废渣堆场。废渣经自然风干,球磨机磨细,过0.1 mm筛后于105 ℃下烘干。渣中含铁量高达34.80%,磨细后的废渣经磁选回收部分铁资源后,装袋,供实验用。有价金属元素主要为Zn、Cu、Pb、Ag、In和Ga等,其含量(质量分数)依次为2.67%、1.08%、0.47%、92 g/t、100 g/t和916 g/t;Cd和As的含量分别为21 g/t和0.51%。
1.2 实验方法
1.2.1 Pb/Zn冶炼废渣生物浸出渣的收集
在pH为1.5、温度为65 ℃、矿渣浓度为5%的优化浸出条件下[8],于250 mL锥形瓶中接种10%(体积比, 10×107 cell/mL)驯化的高温菌(主要为Bacillus sp、 Sporosarcina sp、Pseudomonas sp)进行Pb/Zn冶炼废渣的生物浸出实验,分别于第1、2、3、4、6、9和12 d取样。取样后全部转移至100 mL离心管中于3 000 r/min下分离5 min,余渣按水渣比(质量比)为1?10用去离子水(稀硫酸调节pH值至2)轻轻漂洗两次后于105 ℃下烘干,每时段共收集浸出渣约50 g,称量后装袋备用。生物浸出过程中蒸发散失的水分采用恒量法用蒸馏水补充。
1.2.2 BCR提取、浸出毒性及腐蚀性分析
利用BCR三步法对Pb/Zn冶炼废渣和经不同时间段生物浸出渣中重金属进行连续提取[11]。同时,取冶炼废渣和不同时间段生物浸出渣渣样约0.25 g于100 mL聚四氟乙烯坩埚中进行消解,测定重金属全量[4]。残留态含量为全量减去酸可提取态、可还原态和可氧化态含量之差。为进一步研究生物浸出渣的无害化程度,取部分生物浸出渣按《有色金属工业固体废物浸出毒性试验方法标准(GB5086―85)》[12]和《有色金属工业固体废物腐蚀性试验方法标准(GB5087―85)》[13]对生物浸出渣的浸出毒性和腐蚀性进行检验。
提取液和消解液中Cu、Zn、Pb、Cd和As含量采用电感耦合等离子体发射光谱仪(ICP,美国热电元素公司产IntrepidⅡXSP型)测定。分别取原渣和生物浸提2、4和6 d后渣样进行SEM-EDX(KYKY2800型)和XRD(SIMENS2500X型)分析。
2 结果与讨论
2.1 生物浸出过程中废渣基本特征的变化
2.1.1 废渣中重金属元素的生物浸出
表1所列为不同时间段生物浸出渣中重金属含量的变化。从表1可以看出,Pb/Zn冶炼废渣经生物浸出1 d后,废渣中As、Cd、Cu和Zn的含量显著降低,废渣中As、Cd、Cu和Zn的浸出率在70%以上。生物浸出3 d后,生物浸出渣中As、Cd、Cu和Zn含量分别降至1 107、2.5、410和4 821 g/t(见表1),说明生物浸出体系能有效浸出废渣中As、Cd、Cu和Zn等重金属,降低废渣中重金属的含量[8]。然而,废渣中Pb浸出率很低,其在生物浸出渣中的含量因废渣的减量而由4 678 g/t增加到5 534 g/t (见如表1)。随浸出时间的进一步延长,浸出后余渣中Cu、Zn、Pb和Cd的含量基本维持稳定(见表1),而As含量却呈上升趋势,这是由于浸出体系中Fe3+浓度增高,浸出液中As会重新转化为稳定的砷酸铁(FeAsO4)或随着Fe3+的水解而包裹到黄钾铁钒类物质中从而使As在浸出渣中的含量有所提高[14?15]。
表1 不同时间段生物浸出渣中重金属含量的变化
Table 1 Changes of metals content in bioleached residues during bioleaching process

2.1.2 生物浸出过程中浸出渣的矿物相特征
冶炼废渣中金属赋存矿物相复杂,主要呈非晶态的铁质玻璃体状物质,部分晶态结构如闪锌矿、硫化铜及方铅矿等矿物被包裹在铁质非晶态结构中[4]。在生物浸出初期(1 d),废渣非晶结构被破坏,废渣颗粒不断被侵蚀且越来越小(见图1),重金属被浸出,同时,生物浸出体系中开始形成硫酸铅、黄钾铁钒等新的矿物相(见图2)。进入生物浸出中期(2~4 d),废渣中黄钾铁钒则随着浸出体系中铁离子含量增加而逐渐升高,但部分Pb被包裹在黄钾铁钒沉淀中,使得废渣中独立晶相硫酸铅含量降低(见图2)。在废渣经生物浸出6 d后,其矿物相以炭、黄钾铁钒类和含硅化合物(主要为石英,少量硅酸盐)等矿物为主(见图2),其间夹杂着少量铁的硫化物以及微量Cu、Pb、Zn硫化物或硫酸盐等矿物。上述XRD和SEM-EDX分析结果表明,生物浸出能破坏Pb/Zn冶炼废渣中非晶结构,使废渣中闪锌矿、黄铜矿或硫化铜、铁的氧化矿物等硫化矿物以及包裹于非晶态矿物中重金属浸出,大大降低了废渣中As、Cd、Cu和Zn等含量,实现废渣中部分重金属的综合回收和废渣的无害化处理。
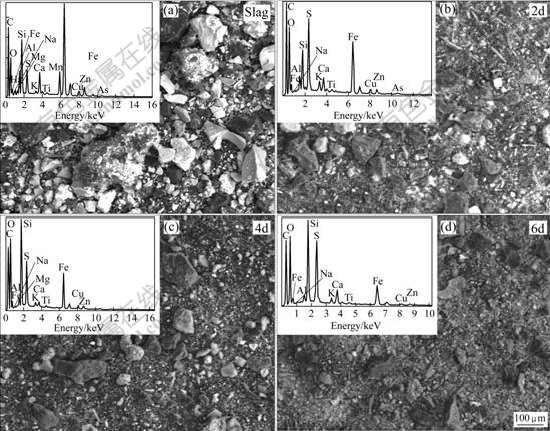
图1 不同时间段生物浸出渣的SEM-EDX图
Fig.1 SEM-EDX images for bioleached residues during bioleaching process: (a) Slag; (b) 2 d; (c) 4 d; (d) 6 d;

图2 不同时间段生物浸出渣的XRD谱
Fig.2 XRD patterns for bioleached residues during bioleaching process
2.2 生物浸出渣中重金属的形态变化
尽管Pb/Zn冶炼废渣中As、Cd、Cu、Pb和Zn等重金属元素及矿物大部分与硫铁结合并包裹在非晶态铁质玻璃体中,且主要以残留态和可氧化态等为 主[4],但由于其绝对含量高,对环境潜在危害非常明显。虽然生物浸出能有效地降低Pb/Zn冶炼废渣中As、Cd、Cu和Zn含量,但浸出渣中重金属的环境活性状况仍将直接影响到Pb/Zn冶炼废渣生物浸出渣的无害化程度和进一步处理处置。
表2所列为余渣中主要重金属毒性元素组分形态含量随生物浸出时间的变化。从表2可以看出,尽管原渣中As残渣态含量达到95%,但由于废渣中As含量很高,其对环境的潜在危害不可忽视[4]。在生物浸出前期(0~1 d),包裹在非晶态中的As及As矿物被释放出来,活性态(酸可提取态、可还原态、可氧化态之和)所占比例由原渣中的5%提高到61%,残留态As急剧降低。随着浸出时间延长,浸出液中Fe3+浓度提高和黄钾铁钒类物质的生成,废渣中部分浸出液中As再次重新转化为稳定的砷酸铁(FeAsO4)或共沉淀到黄钾铁钒类物质中,从而使As的环境活性逐渐降低[15]。经生物浸出3 d后,As残留态含量达到89%,这说明生物浸出使废渣中As的含量减少的同时,还能使其在浸出渣保持稳定,As对环境的潜在危害已经降低到一个较低水平。原渣中的Cd经生物浸出3 d后,80%以上被浸出,余渣中酸可提取态、可还原态和可氧化态Cd含量分别为0.14、0.06和1.10 g/t,而残留态Cd含量也仅为1.36 g/t,浸后余渣中Cd对环境的潜在危害已经降至很低水平。但废渣中Pb在生物浸出1 d后,Pb的酸可提取态、可氧化态和残留态含量均有所下降,而可还原态Pb则由原渣中的7%升高40%。结合XRD谱(见图2)可知,废渣中铅硫化物在生物浸出前期(0~1 d)被氧化生成PbSO4沉淀在浸出渣中[16]。随浸出时间增长,Pb能镶嵌到黄钾铁钒类物质中而使浸出渣中残留态Pb含量升高[17];生物浸出4 d后,浸出渣中Pb残留态所占比例超过80%,Pb环境活性已经很低。废渣中Cu和Zn经连续3 d的生物浸出,绝大部分Cu和Zn被浸出,浸后废渣中Cu、Zn活性组分维持在相对稳定的较低水平,残渣态含量分别为77%和81%,其潜在环境风险已经很低。
表2 余渣中主要重金属毒性元素组分形态含量随生物浸出时间的变化
Table 2 Changes of contents of toxic metals in residues during bioleaching process

2.3 生物浸出渣的浸出毒性分析
根据《有色金属工业固体废物浸出毒性试验方法标准(GB5086―85)》[12]和《有色金属工业固体废物腐蚀性试验方法标准(GB5087―85)》[13]对生物浸出渣中重金属的潜在毒性和浸出渣的腐蚀性进行检验。结果表明,Pb/Zn冶炼废渣中As、Cd、Cu、Pb、Zn等重金属在生物浸出过程中经历一个浸出毒性提高(1 d)-下降(2~3 d)-稳定(4~12 d)的变化过程(见图3)。废渣中Cd和Pb在整个生物浸出过程中都能满足有色金属工业固体废物浸出毒性标准(GB5085―85)[18]的要求,Cu、Zn在生物浸出2 d后即可达到标准,As则可在生物浸出6 d后达到有色金属工业固体废物浸出毒性标准。生物浸出渣的pH值约2.8±0.1,满足有色金属工业固体废物腐蚀性标准(GB5085―85,2.0<pH<12.5)[19],表明原为危险固体废物的Pb/Zn冶炼废渣经生物浸出后其浸出渣可以作为一般固体废物处理处置。
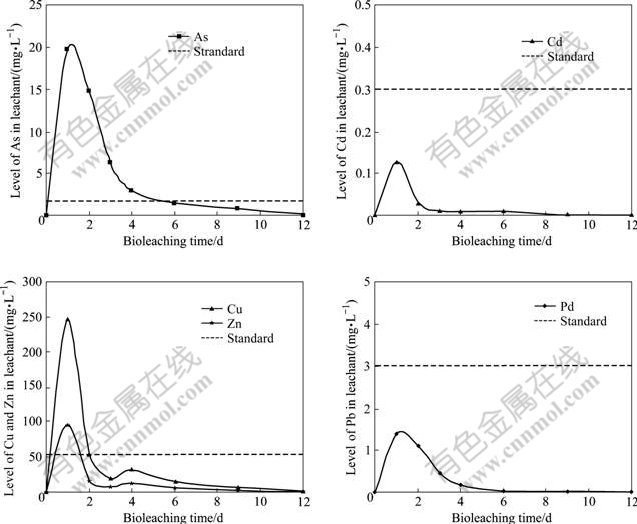
图3 浸出渣中重金属毒性水平随生物浸出时间的变化
Fig.3 Toxic levels of heavy metals in residues during bioleaching process: (a) As; (b) Cd; (c) Cu and Zn; (d) Pb
综上所述,Pb/Zn冶炼废渣中As、Cu、Pb、Zn具有很高的环境毒性。在自然堆放过程中受酸雨及微生物等外界条件作用,废渣中重金属易释放到环境中而具有很高的潜在危害性[2, 4]。生物浸出能破坏Pb/Zn冶炼废渣的非晶结构,有效浸出其中As、Cd、Cu和Zn等重金属元素[8]。经生物浸出3 d后,As、Cd、Cu和Zn浸出率分别达到78%、88%、96%和94%,能实现废渣中Cu和Zn等有价金属元素的资源化,同时将废渣中Cd和As等毒性较高的重金属的含量降低至较低水平。然而,生物浸出过程中Pb的浸出率不理想[7],这是由于生物浸出体系为铁?硫酸体系,废渣中Pb在浸出过程中生成PbSO4(Ksp=1.62×10?8)沉淀而使其浸出率低[16]。
在生物浸出前期阶段(0~1 d),废渣中As、Cd、Cu、Pb、Zn等重金属元素活性增强;随时间延长(2~3 d),废渣中酸可提取态、可还原态和可氧化态含量迅速降低,残留态比例迅速上升,余渣中重金属以残留态为主,其环境潜在危害性显著降低。随着浸出体系中黄钾铁钒类物质的生成,As、Cd、Cu、Pb和Zn等重金属能包裹到黄钾铁钒类物质的晶体结构中而更加稳定[17, 19]。由于原渣重金属和重金属矿物被包裹在铁质非晶结构中,因此其重金属浸出毒性低,但由于砷含量高(砷铁渣)被列入危险固体废物名录[19]。经生物浸出3~6 d后,不仅可以降低Pb/Zn冶炼废渣中重金属含量,实现Cu和Zn等有价金属的资源化,而且使废渣中重金属的浸出毒性能降低至一较低水平,表明生物浸出技术为实现Pb/Zn冶炼废渣的资源化和无害化提供了一条很好的途径。然而,余渣中Pb(5 000~ 5 600 mg/kg)、As(1 100~1 200 mg/kg)含量还很高,尽管研究表明能满足浸出毒性标准,但仍需采用其他方法回收余渣中Pb[8, 20]。同时,改善生物浸出条件,进一步提高As浸出率,最终实现废渣的资源化和无害化。
3 结论
1) 生物浸出大大降低了废渣中As、Cd、Cu和Zn的含量。经生物浸提3 d后,废渣中As、Cd、Cu和Zn含量分别由原渣中的5 055、20.7、10 718和29 681 g/t降至1 107、2.5、410和4 821 g/t;Pb主要以硫酸铅及黄钾铁钒类物质等形式沉积在余渣中。余渣中As、Cd、Cu、Pb和Zn等的重金属主要以残留态存在,余渣中重金属的环境活性和潜在危害已经降低至一较低水平。
2) 浸出毒性分析表明,Cd和Pb在整个生物浸出过程中都能满足有色金属工业固体废物浸出毒性标准(GB5085―85),Cu和Zn在生物浸出2 d后即可达到标准,As则可在生物浸出6 d后达到有色金属工业固体废物浸出毒性标准;腐蚀性分析进一步证明Pb/Zn冶炼废渣经生物浸出后可作为一般固体废物处理处置,使Pb/Zn冶炼废渣真正实现了无害化。
REFERENCES
[1] GBOR P K, HOQUE S, JIA C Q. Dissolution behavior of Fe, Co, and Ni from non-ferrous smelter slag in aqueous sulphur dioxide[J]. Hydrometallurgy, 2006, 81(2): 130?141.
[2] 吴 攀, 刘丛强, 杨元根, 张国平, 李思亮. 土法炼锌废渣堆中的重金属及其释放规律[J]. 中国环境科学, 2002, 22(2): 109?113.
WU Pan, LIU Cong-qiang, YANG Yuan-gen, ZHANG Guo-ping, LI Si-liang. Heavy metals and their release in the wastes residue pile at the indigenous zinc smelting area[J]. China Enviromental Science, 2002, 22(2): 109?113.
[3] MANZ M, CASTRO L J. The environmental hazard caused by smelter slags from the STA. Maria De La PAZ Mining district in Mexico[J]. Environmental Pollution, 1997, 98(1): 7?13.
[4] 郭朝晖, 程 义, 柴立元, 宋 杰. 有色冶炼废渣的矿物学特征及其环境活性研究[J]. 中南大学学报: 自然科学版, 2007, 38(6): 1100?1105.
GUO Zhao-hui, CHENG Yi, CHAI Li-yuan, SONG Jie. Mineralogical characteristics and environmental availability of non-ferrous slag[J]. Journal of Central South University: Natural Science, 2007, 38(6): 1100?1105.
[5] 杨显万, 沈庆峰, 郭玉霞. 微生物湿法冶金[M]. 北京: 冶金工业出版社, 2003: 106?244.
YANG Xian-wan, SHEN Qing-feng, GUO Yu-xia. Bio-hydrometallurgy[M]. Beijing: Metallurgical Industry Press, 2003: 106?244.
[6] NARESHKUMAR R, NAGENDRAN R, PARVATHI K. Bioleaching of heavy metals from contaminated soil using Acidithiobacillus thiooxidans: Effect of sulfur/soil ratio[J]. World J Microbiol Biotechnol, 2008, 24: 1539?1546.
[7] BABEL S, DACERA M D. Heavy metal removal from contaminated sludge for land application: A review[J]. Waste Management, 2006, 26(9): 988?1004.
[8] 郭朝晖, 程 义, 邱冠周, 刘学端, 潘凤开. Pb/Zn冶炼废渣中有价金属生物浸出条件优化[J]. 中国有色金属学报, 2008, 18(5): 1?6.
GUO Zhao-hui, CHENG Yi, QIU Guan-zhou, LIU Xue-duan, PAN Feng-kai. Optimization on bioleaching of metal values from Pb/Zn smelting slag[J]. The Chinese Journal of Nonferrous Metals, 2008, 18(5): 1?6.
[9] KREBS W, BROMBACHER C, BOSSHARD P P, BACHOFEN P, BRANDL H. Microbial recovery of metals from solids[J]. FEMS Microbiology Reviews, 1997, 20 (3/4): 605?617.
[10] MISHRA D, KIM D J, AHN J G, LEE J C. Bacterial leaching of metals from sulfide minerals and industrial wastes[J] KIGAM Bullentin, 2004, 9(1): 48?57.
[11] DAVIDSON C M, DUNCAN A L, LITTLEJOHN D, URE A M, GARDEN L M. A critical evaluation of the three-stage BCR sequential extraction procedure to assess the potential mobility and toxicity of heavy metals in industrially-contaminated land[J]. Analytica Chimica Acta, 1998, 363(1): 45?55.
[12] GB5086―85. 有色金属工业固体废物浸出毒性试验方法标准[S]. 1985.
GB5086―85. Test method standard for extraction procedure toxicity of solid waste in nonferrous metal industry[S]. 1985.
[13] GB5087―85. 有色金属工业固体废物腐蚀性试验方法标准[S]. 1985.
GB5087―85. Test method standard for corrosivity of solid waste in nonferrous metal industry[S]. 1985.
[14] DOGAN P, JOHN E D. Characterization of arsenate-for-sulfate substitution in synthetic jarosite using X-ray diffraction and X-ray absorption spectroscopy[J]. Canadian Mineralogist, 2003, 41(4): 905?919.
[15] MART?NEZ-S?NCHEZ M J, NAVARRO M C, P?REZ-SIRVENT C, MARIM?N J, GARC?A-LORENZO V M L, BECH J. Assessment of the mobility of metals in a mining-impacted coastal area (Spain, Western Mediterranean)[J]. Journal of Geochemical Exploration, 2008, 96(2/3): 171?182.
[16] SILVA G D. Kinetics and mechanism of the bacterial and ferric sulphate oxidation of galena[J]. Hydrometallurgy, 2004, 75(1/4): 99?110.
[17] CAPPUYNS V, SWENNEN R, NICLAES M. Application of the BCR sequential extraction scheme to dredged pond sediments contaminated by Pb-Zn mining: A combined geochemical and mineralogical approach[J]. Journal of Geochemical Exploration, 2007, 93(2): 78?90.
[18] GB5085―85. 有色金属工业固体废物污染控制标准[S]. 1985.
GB5085―85. Standard for pollution control of solid waste in nonferrous metal industry[S]. 1985.
[19] ROMERO F M, ARMIENTA M A, GONZ?LEZ- HERN?NDEZ G. Solid-phase control on the mobility of potentially toxic elements in an abandoned lead/zinc mine tailings impoundment, Taxco, Mexico[J]. Applied Geochemistry, 2007, 22(1): 109?127.
[20] FR?AS C, D?AZ G, OCA?A N, LOZANO J I. Silver, gold and lead recovery from bioleaching residues using the PLINT process[J]. Minerals Engineering, 2002, 15(11): 877?878.
基金项目:国家自然科学基金资助项目(20507022);中南大学博士后基金资助项目(1339-811640000)
收稿日期:2008-05-15;修订日期:2008-07-14
通讯作者:郭朝晖,副教授,博士;电话:0731-8836442;传真:0731-8710171;E-mail: zhguo@mail.csu.edu.cn
(编辑 何学锋)