文章编号:1004-0609(2013)06-1783-06
从硫酸锰两步法制备的四氧化三锰中除硫
李长安,陈 上,刘 伟
(吉首大学 化学化工学院,吉首 416000)
摘 要:采用硫酸锰两步法合成高纯四氧化三锰,研究水解物的生成及洗涤条件对水解物及四氧化三锰中硫酸根含量的影响。测定不同加料方式、氨锰比、硫酸锰浓度、反应温度、氨水滴加速度条件下生成的水解物及其四氧化三锰产品的硫酸根含量,并对水解物分别使用稀氨水硝酸铵溶液和水洗涤,测定匀浆及淋洗两种洗涤方式下水解物的硫酸根含量。结果表明:在硫酸锰浓度0.5 mol/L、温度60 ℃、氨水滴加时间20 min、氨锰比为3:1的条件下,采用向硫酸锰溶液中滴加稀氨水的加料方式,四氧化三锰产率可达86.1%;采用匀浆洗涤方法能明显降低水解物的硫酸根含量,其效果优于淋洗方法;使用2%稀氨水匀浆洗涤两次所得四氧化三锰的硫酸根含量可降低至0.09%。
关键词:硫酸锰;四氧化三锰;除硫
中图分类号:TF803.24 文献标志码:A
Removal of sulfur in Mn3O4 prepared by two-step method from manganese sulfate
LI Chang-an, CHEN Shang, LIU Wei
(College of Chemistry and Chemical Engineering, Jishou University, Jishou 416000, China)
Abstract: The effects of preparation and rinsing conditions for hydrolysate on sulfate content of MnSO4 were investigated in the process of high-purity Mn3O4 prepared by two-step method from MnSO4. The sulfate contents of hydrolysate and Mn3O4 prepared under different feeding sequences, ratio of ammonia to manganese, concentration of manganese sulfate solution, reaction temperature and feeding rate of ammonia solution were determined. The hydrolysates were washed with ammonia, ammonia nitrate solution and water, respectively, and their sulfate contents of hydrolysate washed by homogenate and rinsing method were determined. The results show that, under the following conditions of MnSO4 concentration of 0.5 mol/L, temperature of 60 ℃,ratio of ammonia to manganese of 3:1, feeding time of 20 min, using the feeding sequence of adding ammonia to manganese solution, the yield of Mn3O4 is 86.1%. Using homogenate washing method can sharply decrease the sulfate content of hydrolysate, which is better than using rinsing method. The sulfate content of Mn3O4 washed with 2% ammonia for 2 times can lower to 0.09%.
Key words: manganese sulfate; trimanganese tetroxide; sulfur removal
电子级四氧化三锰(以下简称四氧化三锰)作为电子工业大批量生产锰锌铁氧体软磁材料主要原料之一,其需求量随着世界软磁铁氧体市场的扩大一直稳步增长。高纯四氧化三锰作为原料可制备高品质的锰锌铁氧体[1]。近年来有研究发现,四氧化三锰是制备尖晶石LiMn2O4电池的优质原料,其使用效果优于二氧化锰,四氧化三锰由此成为极具发展前景的锂离子电池正极材料原料之一,拓展了电子级四氧化三锰应用领域[2-6]。
目前制备四氧化三锰主要有两种途径:1) 金属锰粉悬浮液氧化法,将粉碎的电解金属锰调制成一定固液比的悬浮液,在催化剂的作用下,使用空气氧化生成四氧化三锰[7-8];2) 使用硫酸锰溶液在弱碱性条件下水解-空气氧化一步法制备四氧化三锰[9-10]。前者原料纯度高,只要生产过程中没有外来杂质,就能有效地控制其杂质含量,包括硫含量,但是产品比表面积比较小,一般为5~7 m2/g(BET法),因此产品附加值较低[11];后者使用价格低廉的硫酸锰为原料,可获得高比表面积的电子级四氧化三锰,是四氧化三锰制备重点发展的方向。
MICHAEL等[12]最早研究了四氧化三锰制备过程中降低硫含量,通过多次高温高压处理的措施来降低产品中的硫含量,硫含量明显降低,但最低只能降低至约0.3%(以SO3计),多次高温高压的条件苛刻且繁琐,实现工业化的生产较难;邹兴等[13-15]较系统地分析了硫酸锰制备四氧化三锰的优缺点,指出钙、镁、硫等杂质含量偏高是其主要的缺点,比表面积较大是其优点,硫含量与碱式硫酸锰的含量有关,混合物中氢氧化锰优先于碱式硫酸锰被氧化,四氧化三锰产品中硫含量偏高是其碱式硫酸锰很难被完全氧化所致;邹兴等[16]在其专利中认为四氧化三锰中的硫主要以碱式硫酸锰存在,提出使用酸洗涤含硫量高的四氧化三锰,在保持收率的基础上,通过控制洗涤过程中温度及酸度,使碱式硫酸锰溶解,使被包裹的可溶性硫酸盐释放出来,但是酸洗涤会使部分四氧化三锰歧化生成三氧化二锰,最终产品为两者的混合物;骆艳华等[17]将硫酸锰水解,空气氧化分两步进行,比较了这种两步法与一步法制备四氧化三锰的差异,实验证实两步法氧化时间短,氧化更彻底,一步法制备的四氧化三锰由于容易被过氧化,锰含量只能达到68%,颜色较黑,对过程中影响硫含量的因素没有详细研究。
本文作者对两步法制备四氧化三锰过程中氧化时间、加料顺序、水解条件、水解物处理方法对水解物和四氧化三锰中的硫酸根含量的影响进行了详细研究,试验表明水解-氧化分步进行的两步法是控制硫酸根的有效方法。
1 实验
1.1 仪器与试剂
实验仪器:PHS-25酸度计(上海日岛科学仪器有限公司),ST-201B型浊度仪(北京中仪伟信科技有限公司),SHB循环水式多用真空泵(郑州长城科工贸有限公司),AN0905型电子天平(上海民桥精密科学仪器有限公司),JJ-3数显控温电动搅拌器(金坛市荣华仪器制造有限公司)。
主要实验试剂:硫酸锰,氨水,盐酸,氯化钡,实验所用试剂均为分析纯。
1.2 实验方法
1) 硫酸锰水解沉淀:将一定浓度的硫酸锰溶液与2.5%氨水反应,实验采用3种方式滴加:(A) 氨水加入到硫酸锰溶液中;(B) 硫酸锰溶液加入到氨水中;(C) 氨水和硫酸锰溶液同时加入到反应容器中。反应过程中不断搅拌,生成白色沉淀,过滤,使用一定体积的去离子水、稀氨水或稀硝酸铵溶液洗涤滤饼,50 ℃真空干燥,使用硫酸钡重量法检测水解物的硫酸根含量。
2) 水解物的氧化:将上述滤饼转移至反应器中,按液固比4:1(mL/g)加入水,化浆,悬浮液加热至60 ℃,在通入空气的同时滴加氨水,用pH计跟踪反应过程的pH值,控制pH在8.5~8.7之间,反应4 h,反应结束后,抽滤,烘干,得产品四氧化三锰,采用浊度法检测产品硫酸根含量。
1.3 实验原理
由Mn-H2O系的电位―pH图知,可用两步法制备四氧化三锰,第一步是锰离子在氨性介质中水解生成氢氧化锰,第二步是氢氧化锰在弱碱性中氧化成四氧化三锰,涉及的主要化学反应[14-15, 18]如下:
MnSO4+2NH3・H2O=Mn(OH)2(s)+(NH4)2SO4 (1)
2MnSO4+2NH3・H2O=Mn2(OH)2SO4(s) (2)
6Mn(OH)2(s)+O2=2Mn3O4(s)+6H2O (3)
在上述水解反应(1)和(2)中,式(1)为主要水解反应,通过式(2)生成碱式硫酸锰会导致水解物硫酸根含量的升高,必须抑制反应式(2)的进行,碱式硫酸锰可通过控制水解条件及洗涤来降低。
在含碱式硫酸锰的水解物通空气氧化过程中,其中的硫以硫酸或者硫酸铵的方式(反应(4)和(5))溶于水中而达到脱除,水解物中碱式硫酸锰越少,该步反应后得到的四氧化三锰中硫酸根含量也将越低,因此,对水解过程中已生成的碱式硫酸锰采用水、氨水、硝酸铵洗涤,通过化学反应或者离子交换作用以降低水解物硫酸根含量,反应(6)和(7)示意了采用稀氨水洗涤水解物而脱硫涉及的反应,并生成反应活性更好的氢氧化锰,同时洗涤过程可以除去沉淀中夹带的可溶性硫酸盐。
3Mn2(OH)2SO4(s)+O2 =2Mn3O4(s) +6H+ + 3SO42- (4)
3Mn2(OH)2SO4(s)+O2+6NH3・H2O=Mn3O4(s)+6H2O+3(NH4)2SO4 (5)
Mn2(OH)2SO4(s)+2NH3・H2O=2Mn(OH)2(s)+(NH4)2SO4 (6)
Mn2(OH)2SO4(s)+2OH-=2Mn(OH)2(s)+ SO42- (7)
2 结果与讨论
2.1 加料方式对四氧化三锰产率及硫酸根含量的影响
从表1中分析得出,硫酸锰与氨水不同的加料方式,影响着水解物及四氧化三锰硫酸根含量和产率。A方式中硫酸根含量最低,B、C方式相对偏高,可能是因为硫酸锰在B、C方式中沉淀过程分布不均匀造成生成较多碱式硫酸锰,以及局部沉淀包夹硫酸锰造成的。A方式四氧化三锰产率为86.1%;C方式产率比另外两种方式大约低5%,B方式收率较低主要是局部氨水是过量的,因此锰离子被大量络合,而C方式主要是因为锰离子沉降不完全。3种方式中,A方式中硫的含量最低,硫酸根含量为0.165%,但这种方式仍然高出了四氧化三锰产品标准的要求[19],需要进一步控制四氧化三锰中的硫酸根含量,使产品达到要求。
表1 不同加料方式对产率及硫酸根含量的影响
Table 1 Effect of feeding sequence on yield and sulfate content
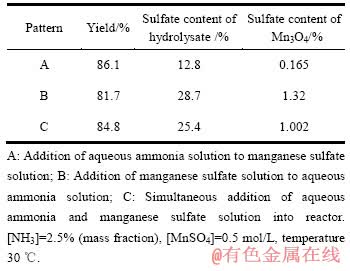
向硫酸锰溶液中滴加氨水的A方式产品收率最高,其硫酸根含量也最低,因此以下的研究都采用向硫酸锰溶液中滴加氨水的方法。
2.2 氨锰比对硫酸根含量的影响
在硫酸锰浓度为0.5 mol/L、反应温度为30 ℃、快速加入氨水的条件下,考察氨锰比对水解产物及四氧化三锰中硫酸根含量的影响,结果如图1所示。
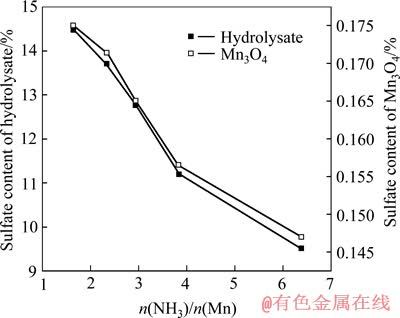
图1 氨锰比对硫酸根含量的影响
Fig. 1 Effect of ratio of ammonia to manganese on sulfate content
随着氨锰比变大,水解物与四氧化三锰中硫酸根含量逐渐减少,这是因为氨水用量越大,反应(1)易于发生,而抑制了反应(2),理论上高氨锰比能降低硫酸根,但是高氨锰比会造成大量锰离子与氨水络合,收率会明显降低。
2.3 硫酸锰浓度对硫酸根含量的影响
在反应温度为30 ℃、快速加入氨水、氨锰比为3:1的条件下,考察不同浓度硫酸锰对水解产物及四氧化三锰中硫酸根含量的影响,结果如图2所示。
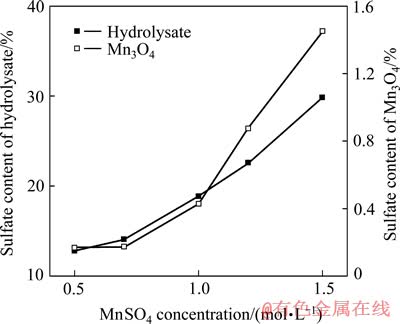
图2 硫酸锰浓度对硫酸根含量的影响的关系图
Fig. 2 Effect of MnSO4 concentration on sulfate content
随着硫酸锰浓度的提高,水解产物和四氧化三锰中的硫酸根含量明显增多,碱式硫酸锰含量增多是其主要原因,在式(6)和(7)的置换反应中,生成物硫酸盐浓度增大,抑制了反应(6)和(7)的继续进行。从图中数据可知,降低硫酸锰的浓度非常有利于减少碱式硫酸锰的生成,在实际过程中,为降低硫酸根含量,可根据需要配制较低浓度硫酸锰溶液,但是太低的硫酸锰浓度会增加生产成本,降低产量。
2.4 水解温度对硫酸根含量的影响
在硫酸锰浓度为0.5 mol/L,快速加入氨水,氨锰比为3:1的条件下,考察不同反应温度对水解产物及四氧化三锰中硫酸根含量的影响,结果如图3所示。
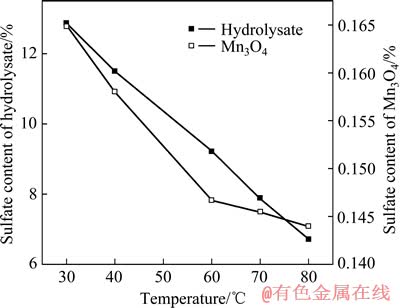
图3 水解温度对硫酸根含量的影响
Fig. 3 Effect of hydrolytic temperature on sulfate content
随温度的升高,水解物中硫酸根含量逐步下降,但在60~80 ℃之间,四氧化三锰中硫酸根下降趋缓,说明高温反应更有利于氢氧化锰的生成,从而降低碱式硫酸锰的生成量,但是温度过高会增加能耗以及氨水的挥发。
2.5 滴加速度对硫酸根含量的影响
在硫酸锰浓度为0.5 mol/L、反应温度为60 ℃、氨锰比为3:1的条件下,考察氨水的滴加速度对水解产物及四氧化三锰中硫酸根含量的影响,结果如图4所示。
随着滴加所用时间的延长,锰的水解产物中硫酸根含量会逐渐减少,其原因可能是在快速加入氨水情况下氨水浓度不均匀性增加,在氨水浓度小的区域,偏向于通过反应(2)生成碱式硫酸锰,而在局部氨水高的区域,瞬间生成大量氢氧化锰,从而在沉淀中容易包夹硫酸锰以及已经生成的碱式硫酸锰,这些包夹物在后续的洗涤过程中难以除去。
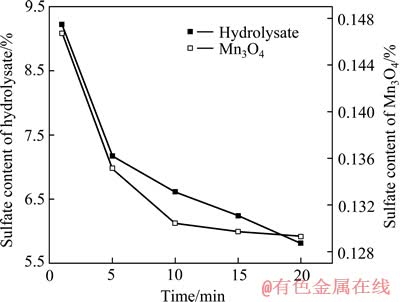
图4 氨水滴加时间对硫酸根含量的影响
Fig. 4 Effect of feeding time of ammonia solution on sulfate content
2.6 洗涤剂种类和洗涤次数对硫酸根含量的影响
在硫酸锰浓度为0.5 mol/L、反应温度为60 ℃、氨锰比为3:1、氨水滴加时间为20 min的条件下,制备锰的水解产物,滤饼用稀氨水,硝酸铵溶液或蒸馏水洗涤,前两者选择1%、2%和5% 3个浓度去洗涤,并且采用淋洗和匀浆洗涤2种方式,结果如表2所列。
表2 洗涤剂种类和洗涤次数对硫酸根含量的影响
Table 2 Effect of washing agent and washing times on sulfate content

对水解物采用淋洗除硫,氨水和硝酸铵洗涤后产物硫酸根含量相近,优于蒸馏水的洗涤效果;匀浆洗涤,氨水优于硝酸铵,硝酸铵优于蒸馏水;淋洗和匀浆洗涤都随着洗涤剂浓度的增大,硫酸根含量逐步降低,匀浆洗涤效果明显好于淋洗效果,水解物使用5%氨水匀浆洗涤一次硫酸根含量可降低到3.55%,但是洗涤后的滤液是土黄色,说明氢氧化锰与氨水络合,造成了锰离子大量损失,可以选择2%氨水匀浆洗涤。蒸馏水匀浆洗涤两次,水解物中硫酸根可降至1.45%,而氨水匀浆洗涤两次硫酸根可降至1.17%,相应的四氧化三锰产品硫酸根降至0.09%,因此,采用2%氨水洗涤两次可获得较好的除硫效果。水解产物硫酸根下降,源于两个原因:一是包夹的可溶性硫酸根被洗涤下来;二是碱式硫酸锰中的硫酸根被氢氧根通过类似离子交换作用被替换,从而被除去。
2.7 水解物氧化过程中pH值及锰含量随时间的变化
在300 mL的浓度为0.5 mol/L的硫酸锰溶液中加入氨水,氨锰比为3:1,反应温度为30 ℃,滴加时间为40 min的条件下,制备的硫酸锰水解沉淀,过滤后滤饼放在300 mL水溶液中氧化,使用酸度计监控pH值变化,研究水解沉淀氧化过程中溶液pH值和锰含量随氧化时间的变化。
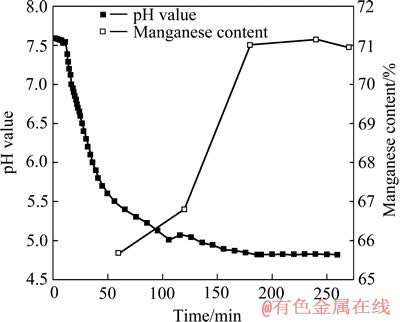
图5 氧化时间对锰含量及溶液pH值的影响
Fig. 5 Effect of oxidation time on manganese content and pH value of solution
从图5可以看出,滤饼的氧化分为3个阶段,第一个阶段前15 min,这一阶段pH值变化下降较慢,主要是氢氧化锰的氧化(反应(3));第二阶段就是15~150 min,这其间pH值下降较快,碱式硫酸锰开始氧化,分解成四氧化锰和硫酸氢离子致使pH值下降(反应(4)),使得四氧化三锰产品中硫酸根含量迅速降低,如果滤饼被氧化时,滴加氨水将更有利于反应向右移动,加快氧化和脱除硫酸根的速度;第三阶段是150 min之后,pH值趋于稳定,碱式硫酸锰氧化过程达到平衡终点,此时仍然有极少量碱式硫酸锰未完全氧化,其中的硫酸根作为产品杂质而存在。氧化4 h后,体系pH值趋于稳定,表明碱式硫酸锰氧化基本完成,此时产品中锰含量达到71%,已经符合标准要求,因此,氧化反应时间选取4h已足够,继续氧化可能造成过氧化生成三氧化二锰以及氧化锰,导致产品中锰含量低于标准要求。
3 结论
1) 水解反应条件,如加料方式、氨锰比、硫酸锰浓度、温度、滴加时间等对碱式硫酸锰的生成有明显影响,采用向硫酸锰中滴加氨水,以及采用适当的氨锰比(3:1)、较低的硫酸锰浓度(0.5 mol/L)和适当的温度(60 ℃)可以明显降低水解物中碱式硫酸锰的含量。
2) 水解物采用2%稀氨水匀浆洗涤效果最好,其原因是使用氨水洗涤存在离子交换作用,使碱式硫酸锰中的硫酸根洗脱得更为彻底。
3) 控制空气氧化4h洗涤过的水解物能有效降低硫酸根含量,锰含量达到71%。
4) 通过调控滴加方式、水解条件、洗涤等综合措施,能将产品中的硫酸根降低至0.09%。
REFERENCES
[1] 周叶青, 程 翔, 黄 昱, 全春平, 谭龙辉. Mn3O4纳米颗粒的制备及改性[J]. 应用化工, 2008, 33(11): 1335-1337.
ZHOU Ye-qing, CHEN Xiang, HUANG Yu, QUAN Chun-ping, TAN Long-hui. Preparation and modification of nano material Mn3O4[J]. Applied Chemical Industry, 2008, 33(11): 1335-1337.
[2] 秦 伟, 韦 华, 甘永乐, 文衍宣, 粟海锋. 碳酸锂和四氧化三锰合成锰酸锂的工艺优化研究[J]. 无机盐工业, 2009, 41(4): 15-17.
QIN Wei, WEI Hua, GAN Yong-le, WEN Yan-xuan, SU Hai-feng. Optimization for synthesis process of lithium manganate from lithium carbonate and trimanganese tetroxide[J]. Inorganic Chemicals Industry, 2009, 41(4): 15-17.
[3] BERBENNI V, MARINI A. Solid state synthesis of lithiated manganese oxides from mechanically activated Li2CO3-Mn3O4 mixtures[J]. Journal of Analytical and Applied Pyrolysis, 2003, 70(2): 437-456.
[4] 张国昀, 姜长印, 万春荣, 何培炯. 以Mn3O4为前驱体的LiMn2O4及其电化学性能[J]. 无机材料学报, 2001, 16(4): 667-671.
ZHANG Guo-yun, JIANG Chang-yin, WAN Chun-rong, HE Pei-jiong. Electrochemical performance of LiMn2O4 synthesized from precursor Mn3O4[J]. Journal of Inorganic Materials, 2001, 16(4): 667-671.
[5] 王英平, 王先友, 隗小山, 魏启亮, 杨秀康, 杨顺毅, 舒洪波, 白艳松, 吴 强. 以Mn3O4为前驱体制备尖晶石型LiMn2O4及其性能[J]. 中国有色金属学报, 2012, 22(8): 2276-2282.
WAGN Ying-ping, WANG Xian-you, KUI Xiao-shan, WEI Qi-liang, YANG Xiu-kang, YANG Shun-yi, SHU Hong-bo, BAI Yan-song, WU Qiang. Preparation process and performance of spinel LiMn2O4 using Mn3O4 as precursor[J]. The Chinese Journal of Nonferrous Metals, 2012, 22(8): 2276-2282.
[6] HE Xiang-ming, LI Jian-jun, CAI Yan, JIANG Chang-yin, WAN Chun-rong. Preparation of spherical spinel LiMn2O4 cathode material for Li-ion batteries[J]. Materials Chemistry and Physics, 2006, 95(1): 105-108.
[7] LAUGHLIN W C, SCHULKE D A. Process for preparing high purity Mn3O4. US Patent, 4812302[P]. 1989-03-14.
[8] 姚震江. 高纯Mn3O4和锰系列化合物的制备[J]. 中国锰业, 1992, 10(2): 114-117.
YAO Zhen-jiang. Preparation of high purity Mn3O4 and manganese-series compounds[J]. China’s Manganese Industry, 1992, 10(2/3): 114-117.
[9] 马子川, 谢亚勃. Mn(OH)2空气氧化反应实验与产物表征[J]. 化学研究与应用, 2001, 13(4): 417-418.
MA Zi-chuan, XIE Ya-bo. Air-oxidation of Mn(OH)2 and characterization of the products[J]. Chemical Research and Application, 2001, 13(4): 417-418.
[10] 陈飞宇, 梅光贵, 谭柱中. 硫酸锰溶液制备电子级四氧化三锰的研究[J]. 中国锰业, 2003, 21(3): 14-16.
CHEN Fei-yu, MEI Guang-gui, TAN Zhu-zhong. Study on producing mangano-manganic oxide from manganous sulphate solution[J]. China’s Manganese Industry, 2003, 21(3): 14-16.
[11] 王红太. 国内四氧化三锰的生产工艺现状及发展方向[J]. 山西化工, 2006, 26(3): 55-57.
WANG Hong-tai. Mangano-manganic oxide production craft present situation and development direction in China[J]. Shanxi Chemical Industry, 2006, 26(3): 55-57.
[12] MICHAEL B, WILLIAM L S. Preparation of trimanganese tetroxide. GB Patent, 1374975[P]. 1974-11-20.
[13] 邹 兴, 孙宁磊, 王国承. 用空气直接氧化游离二价锰离子制备高纯四氧化三锰[J]. 北京科技大学学报, 2007, 29(12): 1250-1253.
ZOU Xing, SUN Ning-lei, WANG Guo-cheng. Preparation of trimanganese tetroxide by air oxidizing free divalent manganese ions[J]. Journal of University of Science and Technology Beijing, 2007, 29(12): 1250-1253.
[14] 邹 兴, 孙宁磊, 方克明. 用硫酸锰溶液不经电解直接制备四氧化三锰的过程中除硫的研究[J]. 中国稀土学报, 2004, 22(S): 469-471.
ZOU Xing, SUN Ning-lei, FANG Ke-ming. Study on removal of sulfate in the process of direct preparation Mn3O4 from manganese sulfate solution and without electrolysis[J]. Journal of Rare Earths, 2004, 22(S): 469-471.
[15] 邹 兴, 朱鸿民.硫酸锰在氨性介质中制备四氧化三锰的研究[J]. 中国锰业, 2009, 27(4): 4-6.
ZOU Xing, ZHU Hong-min. A study on preparation of Mn3O4 by oxidizing hydrolysis of manganese sulfate with air in ammonia alkaline media[J]. China’s Manganese Industry, 2009, 27(4): 4-6.
[16] 邹 兴, 邹瑞瑞. 一种锰的氧化物制备过程中分离硫的方法. 中国, CN 101215007A[P]. 2008-07-09.
ZOU Xing, ZOU Rui-rui. The method of the separation sulfur in the preparation of manganese oxide process. China, CN 101215007A[P]. 2008-07-09.
[17] 骆艳华, 陈思学, 王 凡, 王克玉. 硫酸锰直接制备四氧化三锰的研究[J]. 矿业快报, 2002(2): 17-19.
LUO Yan-hua, CHEN Si-xue, WANG Fan, WANG Ke-yu. Research on direct preparation of Mn3O4 by MnSO4[J]. Express Information of Mining Industry, 2002(2): 17-19.
[18] ARDIZZONE S, BIANCH C L, TIRELLI D. Mn3O4 and MnOOH powers, Preparation, phase composition and XPS characterization[J]. Colloids and Surface, 1998, 134: 305-312.
[19] GB/T 21835―2008. 软磁铁氧体用四氧化三锰[S]. GB/T 21835―2008. Manganous-manganic oxide for soft magnetic ferrites[S].
(编辑 李艳红)
基金项目:湖南省自然科学基金资助项目(07JJ6012);湖南省教育厅自然科学基金资助项目(07B060)
收稿日期:2012-08-15;修订日期:2012-12-05
通信作者:陈 上,副教授,博士;电话:13508430595;E-mail: shangchen@jsu.edu.cn