文章编号:1004-0609(2014)03-0725-08
Li(1+x)Ni0.166Co0.166Mn0.667O(2.175+x/2)正极材料的喷雾干燥法合成及电化学性能
黄 果1, 2,杨顺毅2, 3,雷钢铁1,黄友元2,岳 敏2,胡社军3,任建国2,侯贤华3
(1. 湘潭大学 化学学院,湘潭 411105;
2. 深圳市贝特瑞新能源材料股份有限公司,深圳 518106;
3. 华南师范大学 物理与电信工程学院,广州 510631)
摘 要:采用喷雾干燥法制备锂离子电池用层状富锂锰基正极材料Li(1+x)Ni0.166Co0.166Mn0.667O(2.175+x/2)(x=0.3,0.4,0.5,0.6),通过X射线衍射(XRD)、扫描电子显微镜(SEM)、等离子体发射光谱(ICP)、热重-差热分析(TG-DSC)、比表面积、粒度分布和恒流充放电等测试手段对材料的结构、形貌及电化学性能进行表征。结果表明:所制得的富锂锰基正极材料为三方层状结构(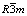 )的 LiNi1/3Mn1/3Co1/3O2和单斜层状结构(C2/m)的Li2MnO3组成的固溶体,且具有多孔球形形貌。当x=0.4时,材料具有最优的电化学性能。在2.0~4.8 V电压范围内,25 mA/g电流密度下材料的首次放电比容量高达277.5 mA・h/g,20周循环后容量保持率达95.3%,500 mA/g电流密度下放电比容量仍达192.5 mA・h/g。
)的 LiNi1/3Mn1/3Co1/3O2和单斜层状结构(C2/m)的Li2MnO3组成的固溶体,且具有多孔球形形貌。当x=0.4时,材料具有最优的电化学性能。在2.0~4.8 V电压范围内,25 mA/g电流密度下材料的首次放电比容量高达277.5 mA・h/g,20周循环后容量保持率达95.3%,500 mA/g电流密度下放电比容量仍达192.5 mA・h/g。
关键词:锂离子电池;正极材料;富锂锰基;喷雾干燥法
中图分类号:O646 文献标志码:A
Spray drying synthesis and electrochemical performance of Li(1+x)Ni0.166Co0.166Mn0.667O(2.175+x/2) cathode materials
HUANG Guo1, 2, YANG Shun-yi2, 3, LEI Gang-tie1, HUANG You-yuan2, YUE min2,
HU She-jun3, REN Jian-guo2, HOU Xian-hua3
(1. School of Chemistry, Xiangtan University, Xiangtan 411105, China;
2. Shenzhen BTR New Energy Materials Inc., Shenzhen 518106, China;
3. School of Physics and Telecommunication Engineering, South China Normal University, Guangzhou 510631, China)
Abstract: The layered lithium-riched manganese-based cathode materials Li(1+x)Ni0.166Co0.166Mn0.667O(2.175+x/2) (x=0.3, 0.4, 0.5, 0.6) for Li-ion batteries were synthesized by spray drying method. The structures, morphologies and electrochemical performance of the as-prepared materials were characterized by X-ray diffractometry (XRD), scanning electron microscopy (SEM), inductively coupled plasma (ICP), thermo-gravimetric/differential scanning calorimeter analysis (TG/DSC), specific surface area, particle size distribution and galvanostatic charge-discharge tests. The results indicate that the obtained lithium-riched manganese-based cathode materials consist of the layered trigonal LiNi1/3Mn1/3Co1/3O2 phase (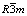 ) and monoclinic Li2MnO3 phase (C2/m), and show the special porous spherical morphology. When x is 0.4, the cathode shows the best electrochemical performance. It exhibits the initial discharge capacity of 277.5 mA・h/g and the capacity retention after 20 cycles reaches 95.3% between 2.0 and 4.8 V at current density of 25 mA/g. The discharge capacity of the cathode still approaches to 192.5 mA・h/g, even when the cathode is cycled at 500 mA/g.
) and monoclinic Li2MnO3 phase (C2/m), and show the special porous spherical morphology. When x is 0.4, the cathode shows the best electrochemical performance. It exhibits the initial discharge capacity of 277.5 mA・h/g and the capacity retention after 20 cycles reaches 95.3% between 2.0 and 4.8 V at current density of 25 mA/g. The discharge capacity of the cathode still approaches to 192.5 mA・h/g, even when the cathode is cycled at 500 mA/g.
Key words: lithium ion battery; cathode material; lithium-riched manganese based; spray drying
当前,新能源汽车的快速发展和锂离子电池电力储能的应用,使市场对锂离子电池的要求除了需要满足环保、安全、成本低及寿命长等基本条件外,对能量密度指标也提出了更高的要求,相对负极材料普遍的高容量(>300 mA・h/g),提高正极材料能量密度是提高锂离子电池能量密度的关键[1]。目前商用的正极材料多为具有α-NaFeO2结构的层状氧化LiMO2(M为过渡金属元素)和聚阴离子型LiFePO4,容量均小于200 mA・h/g[2-4]。富锂锰基材料自报道以来,就以其超大比容量(>200 mA・h/g)、优异的高温及循环性能、低成本和高安全性迅速成为备受关注的新型锂离子电池正极材料之一[5-7],被认为是未来动力锂离子电池市场最具应用前景的正极材料。
目前,富锂锰基正极材料合成方法有共沉淀法[8-11]、固相法[5]、溶胶凝胶法[11]、熔融盐法[12]、微波合成法[13]、燃烧法[14]和冷冻干燥法[15]等。不同的合成方法对材料的物理 (形貌、粒度等)和电化学性能影响较大。共沉淀法是正极材料大规模生产最常用的方法,但是其工艺复杂,对设备要求高,控制变量多,不利于控制成本及批次间的稳定性。溶胶-凝胶法能实现分子水平混合,但是反应消耗大量价格昂贵的有机原料,凝胶需要很长的干燥过程,不适应大规模生产。采用熔融盐法、微波合成法、燃烧法和冷冻干燥法等制备的材料虽然具有较好的电化学性能,但受设备和其他条件限制,仅限于研究领域。
喷雾干燥法是系统化技术应用于物料干燥的一种方法。该法生产设备简单,流程易于实现,能将溶液、乳浊液快速干燥成粉状或颗粒状制品,可省去蒸发和洗涤工序,提高产品生产效率,节约成本,实现大规模生产[16]。喷雾干燥法在锂离子电池材料制备领域已有较广泛的应用。WU等[17]采用喷雾干燥法合成了LiFePO4/C正极材料,在0.1C、1C和10C倍率下的放电容量分别为162.5、154.7 和117.8 mA・h/g,倍率性能优越。YUE等[18]通过喷雾干燥工艺制备了LiNi0.6Co0.2Mn0.2O2三元正极材料,其0.1C首次放电容量高达173.1 mA・h/g,且具有较好的循环稳定性。目前,采用喷雾干燥法制备富锂锰基正极材料的报道很少。基于此,本文作者采用喷雾干燥法合成富锂锰基正极材料Li(1+x)Ni0.166Co0.166Mn0.667O(2.175+x/2) (0.3≤x≤0.6),并对其物理和电化学性能进行研究。
1 实验
1.1 样品制备
按照金属摩尔比n(Ni):n(Co):n(Mn):n(Li)为0.166:0.166:0.667:(1+x)(0.3≤x≤0.6)的比例,称取相应质量的Ni(Ac)2・4H2O(AR,98.0%)、Co(Ac)2・4H2O(AR,99.5%)、Mn(Ac)2・4H2O(AR,99.0%)和LiOH・H2O (AR,99.0%,过量5%),加入去离子水,搅拌成均匀浆料,经喷雾干燥制备前驱体,将前驱体置于箱式炉中,在550 ℃下预烧10 h,然后在920 ℃下焙烧24 h制得最终产物。
1.2 样品的表征与测试
采用梅特勒-托利多公司生产的TG/DSC 1 SF型热重-差热分析仪对前驱体进行热分析实验,载气为空气,以10 ℃/min的升温速率从常温升至1000 ℃,获得TG-DSC曲线;晶体结构分析采用荷兰PANalytical公司生产的X′pert PRO粉末X射线衍射仪,测试条件如下:石墨单色器、 Cu靶(Kα,λ=0.15406 nm)、管电压40 kV、管电流40 mA、扫描范围10°~90°;材料形貌采用日本日立公司生产的HITACHIS-4800扫描电子显微镜进行观察;元素分析采用美国PE公司生产的Optima2100DV ICP 光谱仪进行检测;粒度分布采用英国马尔文公司生产的MASTERSIZER 2000激光粒度仪进行测试;比表面积采用北京市北分仪器技术公司生产的ST-08比表面积测试仪进行测试。
1.3 电化学性能测试
将制备好的正极材料与S-P(导电剂)、粘结剂按质量比 90:5:5混合,滴加少量N-甲基-2-吡咯烷酮(NMP) 后,搅拌成均匀糊状,涂膏于铝箔上,经 120 ℃真空干燥24 h后作为正极;以金属锂片作为负极,l mol/L LiPF6/(EC+DMC)(体积比为1:1) 溶液为电解液,采用日本UBE 25 μm PP/PE/PP隔膜,在充满氩气的手套箱中装配成模拟电池。采用 NewWare CT-3008W测试柜在恒温25 ℃下对电池进行恒流充放电测试,充放电电压范围为2.0~4.8 V,电流密度分别为25、50、125、250和500 mA/g(理论比容量按250 mA・h/g计)。
2 结果与讨论
2.1 前驱体分析
2.1.1 前驱体形貌
图1所示为喷雾干燥前驱体(以Li1.4Ni0.166Co0.166- Mn0.667O2.325样品前驱体为例)的SEM像。从图1中可以看出,前驱体具有良好的球形形貌,粒径分布均匀,其D10、D50和D90分别为8.435、14.905和25.269 μm,分布相对集中。从其放大图(见图1(b))可以看出,球形颗粒表面较为粗糙,为无定形态。

图1 前驱体的SEM像
Fig. 1 SEM images of precursor
2.1.2 前驱体的TG-DSC分析
为了研究喷雾干燥前驱体的热反应过程和相转变情况,在25~1000 ℃温度范围内对前驱体进行热分析实验(TG-DSC测试)。图2所示为前驱体的TG-DSC曲线。从图2中TG曲线可以看出,喷雾干燥前驱体制备富锂锰基材料的过程分为3个阶段:1)脱水阶段,对应质量损失区为室温至210℃,质量损失率为5%,归因于前驱体失去表面物理吸附水和分子间结晶水;2)金属氢氧化物及醋酸盐的分解阶段,质量损失区为210~420℃,质量损失率达21%,主要是喷雾干燥前驱体中未分解的金属氢氧化物和醋酸盐分解引起,从DSC曲线上可以观察到,在270和365 ℃处有一强一弱两个放热峰,分别与氢氧化物和醋酸盐的分解相对应;3) 物相形成和晶体发育阶段,质量损失区间在420~1000 ℃,损失率达4.2%,主要是新物相形成和晶化调整时析氧所致。
根据上述分析,本文作者采用两段控温烧结制备Li(1+x)Ni0.166Co0.166Mn0.667O(2.175+x/2)。 首先在550 ℃保温10 h,脱去所含的吸附水和结晶水,保证氢氧化物及醋酸盐分解完全,然后升温至920 ℃焙烧24 h,各原子相互迁移扩散,形成晶体,并进一步晶化调整,得到结晶完整的目标产物。
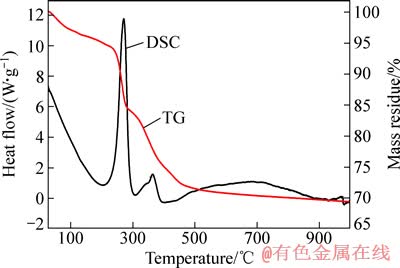
图2 前驱体的TG-DSC曲线
Fig. 2 TG-DSC curves of precursor
2.2 组分分析
采用等离子体发射光谱仪(ICP)对材料的组分进行分析,结果如表1所列。从表1中可以看出,n(Ni):n(Co):n(Mn)基本与理论值(0.166:0.166:0.667)接近,n(Li)/[n(Ni)+n(Co)+n(Mn)]比值稍高于理论值,为所加的5%过量锂未完全挥发所致。元素分析结果表明,采用喷雾干燥法能制备出各元素实际含量与理论配比相符合的富锂锰基正极材料。
2.3 XRD分析
表1 Li(1+x)Ni0.166Co0.166Mn0.667O(2.175+x/2)(0.3≤x≤0.6)的元素分析结果
Table 1 Elemental analysis results of Li(1+x)Ni0.166Co0.166Mn0.667O(2.175+x/2)(0.3≤x≤0.6)
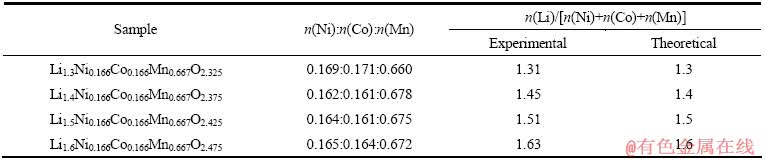
图3所示为喷雾干燥法制得的不同锂含量样品的XRD谱。从图3中可以看出,各样品均出现归属于典型三方层状α-NaFeO2结构(空间群: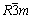 )的(003)、(104)、(101)、(006)、(012)、(018)和(110)特征衍射峰,且(006/012)和(018/110)峰存在明显的分裂现象,说明各材料层状结构良好,晶型发育完整。在20°~25°范围内存在一系列相对较弱的特征峰,该系列峰归属于六方单斜晶系的Li2MnO3结构(空间群为C2/m),是由其过渡金属层内LiMn6短程有序超结构引起的衍射 峰[19]。由XRD谱分析可知,富锂锰基正极材料为三方层状(
)的(003)、(104)、(101)、(006)、(012)、(018)和(110)特征衍射峰,且(006/012)和(018/110)峰存在明显的分裂现象,说明各材料层状结构良好,晶型发育完整。在20°~25°范围内存在一系列相对较弱的特征峰,该系列峰归属于六方单斜晶系的Li2MnO3结构(空间群为C2/m),是由其过渡金属层内LiMn6短程有序超结构引起的衍射 峰[19]。由XRD谱分析可知,富锂锰基正极材料为三方层状(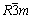 )结构的 LiNi1/3Mn1/3Co1/3O2和单斜层状结构(C2/m)的Li2MnO3组成的固溶体。
)结构的 LiNi1/3Mn1/3Co1/3O2和单斜层状结构(C2/m)的Li2MnO3组成的固溶体。
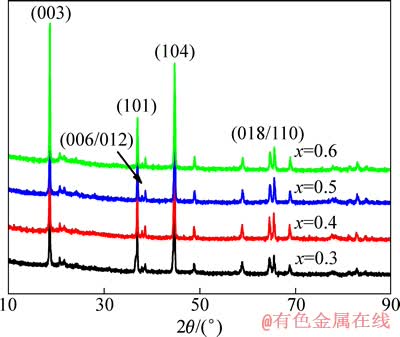
图3 Li(1+x)Ni0.166Co0.166Mn0.667O(2.175+x/2)(0.3≤x≤0.6)的XRD谱
Fig. 3 XRD patterns of Li(1+x)Ni0.166Co0.166Mn0.667O(2.175+x/2) (0.3≤x≤0.6)
2.4 微观形貌及物理性能
锂含量的细微变化对富锂锰基材料的微观形貌和物理性能影响显著。图4所示为Li(1+x)Ni0.166Co0.166- Mn0.667O(2.175+x/2)(0.3≤x≤0.6)系列样品的SEM像。图4(a)、(c)、(e)和(g)直观地表征了样品的二次颗粒形貌,各样品均保持了前驱体良好的球形形貌,为疏松多孔的球形颗粒。该球形多孔结构有利于增大材料比表面积、增加电解液渗透程度,在一定程度上对提高电化学性能有利,其形成与烧结时醋酸盐分解产生大量气体有关。
从图4(b)、(d)、(f)和(h)可以观察到一次粒子的形貌变化特点。由图4(b)可见,Li1.3Ni0.166Co0.166- Mn0.667O2.325样品的一次粒子为多直线型边角的无规则颗粒,粒子间结合紧密,间隙不明显。从图4(d)、(f)和(g)可以看出,当x≥0.4时,样品的一次粒子为边角圆润的颗粒状,粒子间结合较为疏松,空隙较多,且随着锂含量的增加,颗粒尺寸逐渐增大。
图5所示为样品的粒度分布;图6所示为样品的D50和比表面积随着x值的变化曲线。如图5和6所示,随着x增大,样品颗粒平均粒径分布呈先减小后增大的趋势,而比表面积则呈现先增大后减小的趋势。当x=0.4时,制得的样品颗粒平均粒径最小(D50为11.624 μm),比表面积最大 (3.38 m2/g)。小的颗粒粒径能够有效缩短锂离子扩散路径,便于离子嵌入和脱出,将有利于提高电化学反应活性;大比表面积有利于增加活性物质与电解液的接触面积,提高电化学反应速率和反应程度,增加材料利用率和首周循环时的结构转变程度,从而提高比容量[20]。
2.5 电化学性能
为了研究喷雾干燥制备的富锂锰基正极材料的电化学性能,在2.0~4.8 V电压范围内和25 mA/g电流密度下对各材料进行恒流充放电测试。样品的首次充放电曲线如图7所示。从图7中可以看出,各样品的充电曲线存在两个明显电压平台:第一个平台在3.75~4.5 V之间,这是过渡金属层中Ni2+发生氧化反应,形成Ni4+所致[21],放出约100 mA・h/g的容量;第二个平台为4.5 V处的较长充电平台,为富锂锰基正极材料的充放电特征平台,此平台为Li2MnO3相的活化过程,Li2MnO3微结构中的O 2p键氧化(析氧)同时伴随着Li+脱出,形成Li2O化合物[22]。通过理论计算可知,Li1.5Ni0.166Co0.166Mn0.667O2.425(x=0.5)材料的Li2MnO3结构全部脱锂后,将产生229.5 mA・h/g的容量。锂含量低时,Li2MnO3含量越低,对应的Li2MnO3相理论放电容量越小,平台越短,与图7中不同锂含量下的高电压充电平台长度变化完全对应。图7放电曲线上,各样品表现出类似LiNi1/3Mn1/3Co1/3O2的长且平滑的放电平台。3.5 V以上的放电平台对应 Ni4+/Ni2+的可逆还原过程,低于3.5 V处的平台则与少量Mn4+/Mn3+还原有关。伴随着还原反应的进行,脱出的大量锂离子回嵌至活性材料中,表现出富锂的高容量特性。从图7中各曲线可见,锂含量对富锂锰基正极材料的首次放电比容量和首次库仑效率影响显著。当x为0.3、0.4、0.5和0.6时,样品的充电和放电比容量分别为263.2、199.4,341.7、277.5,362.7、247.1和325.5、220.4 mA・h/g,首次效率分别为75.8%、81.2%、68.1%和67.7%。随着锂含量的增加,材料的首周充放电比容量及首次库仑效率呈先增大后减小的趋势,当x=0.4时,材料表现出最优异的电化学性能。从测试结果明显可见,该系列材料还表现出67%~81%的低首次库仑效率。这主要与高电压状态下,晶格O2-随着锂离子以Li2O化合物形式脱出后,表层金属离子占据体相中的离子空位,致使体相晶格无法完全容纳充电过程中脱出的锂离子有关。富锂材料的这种低首次库仑效率是其实际应用中必须解决的问题,根据已有文献报道,掺混宿主材料[23]和氧化物包覆[24]等均能有效地提高材料的首次库仑效率,大大降低不可逆容量。

图4 Li(1+x)Ni0.166Co0.166Mn0.667O(2.175+x/2)的SEM像
Fig. 4 SEM images of Li(1+x)Ni0.166Co0.166Mn0.667O(2.175+x/2)
图8所示为样品在2.0~4.8 V电压范围内和25 mA/g电流密度下的循环寿命曲线。从图8中可以看出,不同锂含量富锂锰基正极材料均具有较好的循环稳定性,20周后放电容量分别为193.1、264.6、236.5和220.9 mA・h/g,容量保持率(η)分别达到94.4%、95.3%、95.7%和96.6%,但是与普通三元材料相比[25],其循环性能仍然有待提高。随着锂含量增加,材料的循环性能趋于稳定,这与材料中具有稳定晶体结构的Li2MnO3相增加有关[26]。
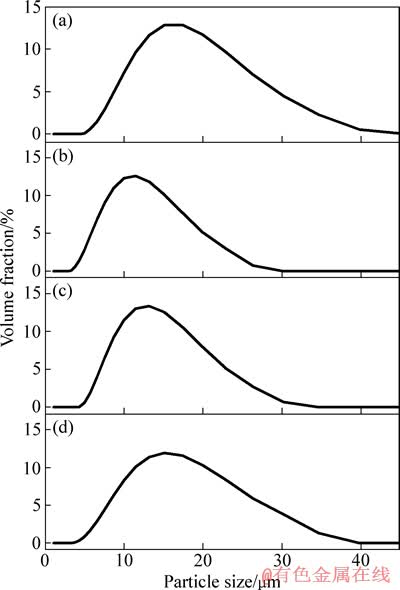
图5 Li(1+x)Ni0.166Co0.166Mn0.667O(2.175+x/2)(0.3≤x≤0.6)的粒度分布
Fig. 5 Particles size distribution for samples of Li(1+x)Ni0.166Co0.166Mn0.667O(2.175+x/2)(0.3≤x≤0.6)

图6 Li(1+x)Ni0.166Co0.166Mn0.667O(2.175+x/2)(0.3≤x≤0.6)样品的D50与比表面积随x的变化曲线
Fig. 6 Variation of D50 and specific surface area (SSA) of Li(1+x)Ni0.166Co0.166Mn0.667O(2.175+x/2)(0.3≤x≤0.6) with x value
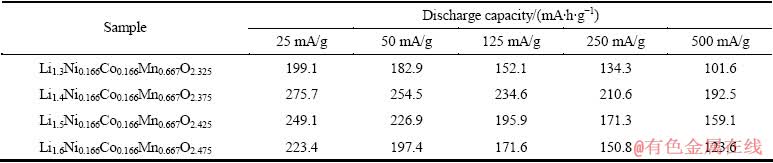
倍率性能是锂离子电池正极材料的关键性能指标。为了研究不同锂含量富锂锰基正极材料的倍率性能,在2.0~4.8 V电压范围内对电池依次以25、50、125、250和500 mA/g电流密度进行恒流充放电测试,每个电流密度下循环5周。表2所列为各样品不同倍率下的放电比容量;图9 所示为Li(1+x)Ni0.166Co0.166- Mn0.667O(2.175+x/2)(0.3≤x≤0.6)样品的倍率性能曲线。从图9中可以看出,与其他材料相比,Li1.4Ni0.166Co0.166- Mn0.667O2.325(x=0.4)在不同电流密度下均具有较高的放电比容量。在25、50、125、250和500 mA/g电流密度下其放电比容量分别277.5、254.5、234.6、210.6和192.5 mA・h/g;在50、125、250和500 mA/g电流密度下相对容量保持率分别达到92.3%、85.1%、76.4%和69.8%(相对于25 mA/g电流密度下的放电比容量)。
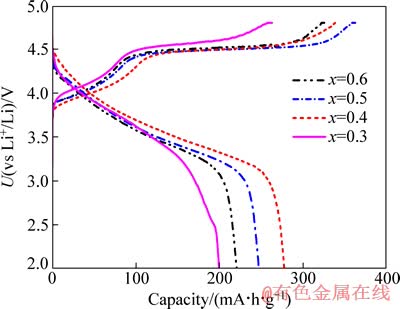
图7 Li(1+x)Ni0.166Co0.166Mn0.667O(2.175+x/2)(0.3≤x≤0.6)的首次充放电曲线
Fig. 7 Initial charge-discharge curves of Li(1+x)Ni0.166- Co0.166Mn0.667O(2.175+x/2)(0.3≤x≤0.6)
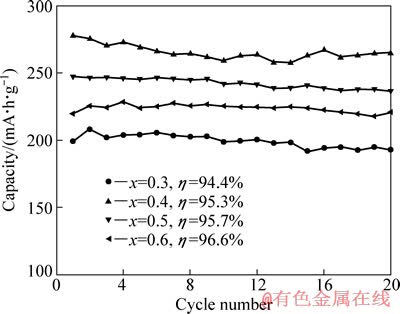
图8 Li(1+x)Ni0.166Co0.166Mn0.667O(2.175+x/2)(0.3≤x≤0.6)循环寿命曲线
Fig. 8 Cycling life curves of Li(1+x)Ni0.166Co0.166- Mn0.667O(2.175+x/2)(0.3≤x≤0.6)
表2 Li(1+x)Ni0.166Co0.166Mn0.667O(2.175+x/2)(0.3≤x≤0.6)的倍率放电性能
Table 2 Discharge capacities of Li(1+x)Ni0.166Co0.166Mn0.667O(2.175+x/2)(0.3≤x≤0.6) samples at various current rates
高电流密度下,电化学反应速度较快,锂离子扩散成为电化学反应的控制步骤,而当x=0.4时,样品颗粒尺寸小,其一次粒子颗粒尺寸仅为100~200 nm,比表面积大,有利于缩短锂离子的扩散路径并增加离子迁移通道,加速电化学反应速率及反应程度,从而提高材料的倍率性能。
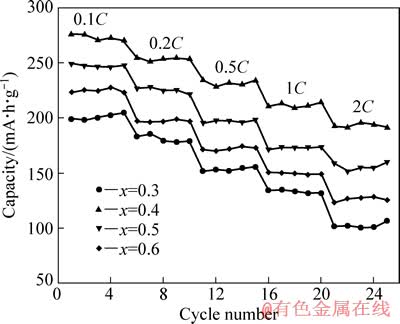
图9 Li(1+x)Ni0.166Co0.166Mn0.667O(2.175+x/2)(0.3≤x≤0.6)的倍率性能曲线
Fig. 9 Rate performance curves of Li(1+x)Ni0.166Co0.166- Mn0.667O(2.175+x/2)(0.3≤x≤0.6)
3 结论
1) 采用喷雾干燥法制备的富锂锰基正极材料由稳定的固溶体结构组成,且具有多孔球形形貌。
2) 锂含量是影响富锂锰基材料相结构、形貌和其他物理特性的关键因素,从而影响材料的电化学性能。当x=0.4时,材料(Li1.4Ni0.166Co0.166Mn0.667O2.375)具有最好的电化学性能。在2.0~4.8 V电压范围内和25 mA/g电流密度下其放电比容量高达277.5 mA・h/g,首次效率为81.2%,20周循环后的容量保持率达95.3%,50、125、250和500 mA/g电流密度下相对容量保持率分别达到92.3%、85.1%、76.4%和69.8%。
3) 喷雾干燥法工艺简单,是一种制备锂离子电池富锂锰基正极材料的有效方法,未来有望在大规模商业化生产中得到应用。
REFERENCES
[1] 吴承仁, 赵长春, 王兆翔, 陈立泉. 锂离子电池用富锂层状正极材料[J]. 化学进展, 2011, 23(10): 2038-2044.
WU Cheng-ren, ZHAO Chang-chun, WANG Zhao-xiang, CHEN Li-quan. Li-rich layer-structured cathode materials for Li-ion batteries[J]. Progress in Chemistry, 2011, 23(10): 2038-2044.
[2] JACOB C, LYNCH T, CHEN A P, JIAN J, WANG H Y. Highly textured Li(Ni0.5Mn0.3Co0.2)O2 thin films on stainless steel as cathode for lithium-ion battery[J]. Journal of Power Sources, 2013, 241: 410-414.
[3] 岳 鹏, 彭文杰, 王志兴, 李新海, 李灵均, 郭华军, 胡启阳, 张云河. 正极材料LiNi0.8Co0.1Mn0.1O2的合成及电化学性能[J]. 中国有色金属学报, 2011, 21(7): 1601-1607.
YUE Peng, PENG Wen-jie, WANG Zhi-xing, LI Xin-hai, LI Ling-jun, GUO Hua-jun, HU Qi-yang, ZHANG Yun-he. Synthesis and electrochemical performance of LiNi0.8Co0.1Mn0.1O2 cathode material[J]. The Chinese Journal of Nonferrous Metals, 2011, 21(7): 1601-1607.
[4] 彭忠东, 唐代春, 胡国荣, 杜 柯, 曹雁冰. 均匀沉淀法制备LiFePO4/C及其电化学性能[J]. 中国有色金属学报, 2012, 22(5): 1319-1325.
PENG Zhong-dong, TANG Dai-chun, HU Guo-rong, DU Ke, CAO Yan-bing. Synthesis and electrochemical performance of LiFePO4/C by homogeneous precipitation method[J]. The Chinese Journal of Nonferrous Metals, 2012, 22(5): 1319-1325.
[5] TANG Zhao-hui, WANG Zhi-xing, LI Xin-hai, PENG Wen-jie. Influence of lithium content on the electrochemical performance of Li1+x(Mn0.533Ni0.233Co0.233)1-xO2 cathode materials[J]. Journal of Power Sources, 2012, 208: 237-241.
[6] SHI S J, TU J P, TANG Y Y, YU Y X, ZHANG Y Q, WANG X L, GU C D. Combustion synthesis and electrochemical performance of Li[Li0.2Mn0.56Ni0.16Co0.08]O2 with improved rate capability[J]. Journal of Power Sources, 2013, 228: 14-23.
[7] CROY J R, KIM D, BALASUBRAMANIAN M , GALLAGHE K, KANG S H, THACKERAY M M. Countering the voltage decay in high capacity xLi2MnO3・(1-x)LiMO2 electrodes (M=Mn, Ni, Co) for Li-ion batteries[J]. Journal of the Electrochemical Society, 2012, 159(6): A781-A790.
[8] SON J T, JEON H J, LIM J B. Synthesis and electrochemical characterization of Li2MnO3-LiNixCOyMnzO2 cathode for lithium battery using co-precipitation method[J]. Advanced Powder Technology, 2013, 24: 270-274.
[9] ZHANG Jing-wen, GUO Xun, YAO Su-mei, ZHU Wen-tao, QIU Xin-ping. Tailored synthesis of Ni0.25Mn0.75CO3 spherical precursors for high capacity Li-rich cathode materials via a urea-based precipitation method[J]. Journal of Power Sources, 2013, 238: 245-250.
[10] DENG H, BELHAROUAK I, WU H, DAMNOURNET D, AMINE, K. Effect of cobalt incorporation and lithium enrichment in lithium nickel manganese oxides[J]. Journal of the Electrochemical Society, 2010, 157(7): A776-A781.
[11] SHOJAN J, RAO C V, TORRES L, SINGH G, KATIYAR R S. Lithium-ion battery performance of layered 0.3Li2MnO3-0.7LiNi0.5Mn0.5O2 composite cathode prepared by co-precipitation and sol-gel methods[J]. Materials Letters, 2013, 104: 57-60.
[12] YU Chuang, LI Guang-she, GUAN Xiang-feng, ZHENG Jing, LI Li-ping. Composite Li[Li0.11Mn0.57Ni0.32]O2: Two-step molten-salt synthesis, oxidation state stabilization, and uses as high-voltage cathode for lithium-ion batteries[J]. Journal of Alloys and Compounds, 2012, 528: 121-125.
[13] WANG Jun, ZHANG Ming-hao, TANG Chang-lin, XIA Yong-gao, LIU Zhao-ping. Microwave-irradiation synthesis of Li1.3NixCoyMn1-x-yO2.4 cathode materials for lithium ion batteries[J]. Electrochem Acta, 2012, 80: 15-21.
[14] ZHONG Zhuo-hong, YE Nai-qing, WANG Hai, MA Zhen. Low temperature combustion synthesis and performance of spherical 0.5Li2MnO3-LiNi0.5Mn0.5O2 cathode material for Li-ion batteries[J]. Chemical Engineering Journal, 2011, 175: 579-584.
[15] SHI S J, TU J P, TANG Y Y, YU Y X, ZHANG Y Q, WANG X L. Synthesis and electrochemical performance of Li1.131Mn0.504Ni0.243Co0.122O2 cathode materials for lithium ion batteries via freeze drying[J]. Journal of Power Sources, 2013, 221: 300-307.
[16] 赵军峰. 三元系锂离子电池正极材料的制备与研究[D]. 长沙: 中南大学, 2011.
ZHAO Jun-feng. Preparation and study of the performance of lithium-nickel-cobalt-manganese oxides cathode material for lithium-ion batteries[D]. Changsha: Central South University, 2011.
[17] WU Ling, ZHONG Sheng-kui, LIU Jie-qun,  Fan, WAN Kang. High tap-density and high performance LiFePO4/C cathode material synthesized by the combined sol spray-drying and liquid nitrogen quenching method[J]. Materials Letters, 2012, 89: 32-35.
Fan, WAN Kang. High tap-density and high performance LiFePO4/C cathode material synthesized by the combined sol spray-drying and liquid nitrogen quenching method[J]. Materials Letters, 2012, 89: 32-35.
[18] YUE Peng, WANG Zhi-xing, PENG Wen-jie, LI Ling-jun, CHEN Wei, GUO Hua-jun, LI Xin-hai. Spray-drying synthesized LiNi0.6Co0.2Mn0.2O2 and its electrochemical performance as cathode materials for lithium ion batteries[J]. Powder Technology, 2011, 214: 279-282.
[19] THACKERY M M, KANG S H, JOHNSON C S, VAUGHEY J T, BENEDEK R HACKNEY S A. Li2MnO3-stabilized LiMO2(M=Mn, Ni, Co) electrodes for lithium-ion batteries[J]. Journal of Materials Chemistry, 2007, 17: 3112-3125.
[20] RYU J H, PARK B G, KIM S B, PARK Y J. Effects of surface area on electrochemical performance of Li[Ni0.2Li0.2Mn0.6]O2 cathode material[J]. Journal of Applied Electrochemistry, 2009, 39: 1059-1066.
[21] KOBAYASHI H, TAKENAKA Y, ARACHI Y, NITANI H, OKUMURA T, SHIKANO M, KAGEYAMA H, TATSUMI K. Study on Li deintercalation/intercalation mechanism for a high capacity layered Li1.20Ni0.17Co0.10Mn0.53O2 material[J]. Solid State Ionics, 2012, 225: 580-584.
[22] ARMSTRONG A R, HOLZAPFEL M, NOVAK P, JOHNSON C S, KANG S H, THACKERAY M M, BRUCE P G. Demonstrating oxygen loss and associated structural reorganization in the lithium battery cathode Li[Ni0.2Li0.2Mn0.6]O2[J]. Journal of the American Chemical Society, 2006, 128: 8694-8698.
[23] GAO J, KIM J, MANTHIRAM A. High capacity Li[Li0.2Mn0.54Ni0.13Co0.13]O2-V2O5 composite cathodes with low irreversible capacity loss for lithium ion batteries[J]. Electrochemistry Communications, 2009, 11: 84-86.
[24] WEST W C, SOLER J, SMART M C, RATNAKUMAR B V, FIRDOSY S, RAVI V, ANDERSON M S, HRBACEK J E, LEE S, MANTHIRAM A. Electrochemical behavior of layered solid solution Li2MnO3・LiMO2(M=Ni, Mn, Co) Li-ion cathodes with and without alumina coatings[J]. Journal of the Electrochemical Society, 2011, 158(8): A883-A889.
[25] NOH H J, YOUN S, YOON C S, SUN Y K. Comparison of the structural and electrochemical properties of layered Li[NixCoyMnz]O2(x=1/3, 0.5, 0.6, 0.7, 0.8 and 0.85) cathode material for lithium-ion batteries[J]. Journal of Power Sources, 2013, 233: 121-130.
[26] ARUNKUMAR T A, WU Y, MANTHIRAM A. Factors influencing the irreversible oxygen loss and reversible capacity in layered Li[Li0.33Mn0.67]O2-Li[M]O2(M=Mn0.5-yNi0.5-yCo2y and Ni1-yCoy) solid solutions[J]. Chemistry of Materials, 2007, 19: 3067-3073.
(编辑 陈卫萍)
基金项目:国家自然科学基金资助项目(51201066,51171065);中国博士后科学基金资助项目(2013M531864);广东省自然科学基金重点项目(S2012020010937);广东高校优秀青年创新人才培育项目(2012LYM_0048);广东省教育部科技部产学研结合项目(2011A091000014);湖南省教育厅重点项目(12A133)
收稿日期:2013-06-03;修订日期:2013-10-19
通信作者:雷钢铁,教授,博士;电话:0731-58292206;传真:0731-58292251;E-mail:lgt@xtu.edu.cn