DOI: 10.11817/j.ysxb.1004.0609.2020-35783
ʪ����пΣ��������ˮ�ȷֽ⼰������ת����Ϊ
�� ��������֣��� �������ı�κ �ƣ���־�ң����˱� �գ���F͢
(����������ѧ ұ������Դ����ѧԺ������ 650093)
ժ Ҫ��ʪ����п���̲��������������д������м۽���п��Ǧ�Լ���������������ˮ�������£�Σ����������������Ч�ֽ���ת�����м۽���ת����Һ��������ת��Ϊ����������ʪ����п��ҵ������������Ϊ�о������о��˷�Ӧ�¶ȡ���Ӧʱ�䡢Һ�̱ȡ���ʼ��ȡ�����Ũ�ȵȺ�ۼ����������������ֽ���ת����Ӱ����ɡ����ۼ����ʵ�����������ڸ���ˮ����ϵ�У��������еĻƼ��������������������п���������Чת��Ϊ������Ǧ���������ȶ�����ת���������¶Ȳ��ӳ���Ӧʱ�������ڻƼ��������������������п�����ˮ�ȷֽ���ת������220 ���·�Ӧ1 h����������ת��������ɣ���ת���ʴ�94%����Ӧ4 h������п�����������ȫ��ʧ��п�����ʴ�87%��ת�����г���������68%���ʵ���߳�ʼ�������������п��ת����������ϵ��ʼ��ȸ���15 g/Lʱ��������������ת�����ڷ�Ӧ�¶�220 �桢��Ӧʱ��4 h��Һ�̱�(mL/g) 10:1����ʼ���0.01 g/L�������£�п������Ϊ89%�����������ת���ʿɴ�95%������ת��������Ҫ����Ϊ�������京��Ϊ68%��
�ؼ��ʣ���������ˮ�ȷֽ⣻������ת����Ϊ
���±�ţ�1004-0609(2020)-05-1119-12���� ��ͼ����ţ�TF813���� ���ױ�־�룺A
�ҹ�80%���ϵ�п����ʪ����п����������п��������ʪ����п����Ҫ�Ļ��ڡ�Ŀǰ���Ӻ�������п����Һ�з���п�������й�ҵ��Ӧ�õķ����лƼ���������������������[1-3]�����У��Ƽ�������������ɱ��͡��м۽��������ʸߡ�������ϵ��ƽ����ŵ�ռ����������λ[4-5]���ڻƼ��������������չ����У������п��ɰ���кͼ�����ɰ�д���п��ͭ�������м۽������ӡ�Ǧ������ж�Ԫ������������һ������������У�����������ɷּ��临�ӣ�����Ȼ�Ѵ��������ؽ������ж�Ԫ�ز����ܳ���Ⱦ����ˮ�����������������Ⱦ���ֽ��������ѱ�����Σ�չ�����������С���ͳ�ƣ���ʪ����п������ÿ����1 t��п������0.3~0.5 t��������Ŀǰ����ÿ�꽫��������100��t��Σ��������[6-11]������������������Դ�������غ�ʪ����п��ҵ�������뷢չ��
����������������й����߲��û���ʪ�����ϻ�ʪ���ȹ��ս������������������̶������ͻ��������м۽������о�������������ɽұ�������õ�����Ausemelt¯���մ���������Ψһʵ�ֹ�ҵ���Ĵ�������[12]����ѧ��[13-14]���û��ն��������������м۽���Ǧ��п�Ƚ�����Դ�����ã����û��մ������������й��ռ��ɲ�����ǿ���ŵ㣬�������ܺĸߡ�����������������ɶ�������ĵͿ���Ⱦ�����ٻ���[15]���ſ�����[16]�ֱ���õ��±���-NH4Cl����-������ͱ���-ˮ������������������п��Ǧ��ͭ�������м۽������л������ã��ֱ�õ�����53.84%�ļ����������Ǧ�����Ľ����������û�ʪ�������ڴ���������ʱ�����м۽��������ʸߡ��м۽�����������ȫ���ŵ㣬�����ڹ��ո��ӡ��ɱ��ߵȲ��㡣��ˣ������������ʪ��������ȡ�������е��м۽��������ÿ��Լ�������������ʱ���ɽ��������е���������п���м۽����ֱ��ڽ������ͽ���Һ��[17-19]��ʪ��������������ܺĵ͡����������ʸߵ��ײ�����Һ����������ɶ�����Ⱦ��̷����[20]��ASOKAN��[21]�����������й̻��������̻�����Ϲ��ұ�Ҫ�̻�������Σ���������ɱ��ͣ�������ǿ�������������м۽����Ļ��ղ������ƣ�����������м۽������˷ѡ�
����ֵ�[22-25]���о���������ˮ�ȳ������������������̬����������Խ�һ���������ת����ͨ�������¶ȡ����Ӿ��֡��ӳ���Ӧʱ����ֶΣ��ɴٽ�������̬����ת��Ϊ�����������ø��о�˼·����ʪ����п���̲�����������Ϊ�о�������ˮ��������ʹ�䷢���ֽ���ת�����м۽���ת����Һ��������ת��Ϊ����DZ�����ü�ֵ�ij�����ͨ���о���Ӧ�¶ȡ���Ӧʱ�䡢Һ�̱ȡ���ʼ��ȡ�����Ũ�ȵȺ�ۼ���������������������������п����ֽ���ת����Ӱ����ɣ�����Ż�����������Ϊ��һ�����������м۽����ĸ�Ч��ȡ�ṩ������
1 ʵ��ԭ��
ʪ����п��ҵ������Σ��������������ɼ��临�ӣ�ͨ���������е����������ǻ������(NH4Fe3(SO4)2(OH)6)����������(NaFe3(SO4)2(OH)6)���Ƽ�����(KFe3(SO4)2(OH)6)��Ǧ����(PbFe6(SO4)4-(OH)12)�е�һ�ֻ��ֵĻ�������������ˮ�������°���Ӧʽ(1)������Ӧ��������������ת��Ϊ������ת������������ʽ���С��ͬʱ�������������е�п��ͭ���м۽���Ҳ��֮�ܽ������Һ��
2AFe3(SO4)2(OH)6=A2SO4+3Fe2O3+3H2SO4+3H2O
(A=Na, K, NH4, 0.5Pb) (1)
�������������������༰��ɲ�ͬ�䷴Ӧ����Ҳ��ͬ������Material Studio�����Ի�������������������Ƽ�������Ǧ�������м����Ż�������ȶ��ṹ���ó�����4�������Ľṹ�������������ͼ1��ʾ��4���������������ڣ��������(-9833 eV)����������(-10241 eV)���Ƽ�����(-10651 eV)��Ǧ����(-29574 eV)���ɴ˿�֪����������ˮ�ȷֽ���ת�����������ȶ����ɴ�С����ΪǦ�������Ƽ����������������ͻ����������������������ֽ⣬Ǧ�������ѷֽ⡣

ͼ1 ��������������������ͼ
Fig.1 Final energy convergence of jarosite
ʪ����п�Ƽ����������������У���������п��ɰ��Ϊ�кͼ�������п��ɰ�д�����п������п��ʽ��������������ˮ�������£�����������ת������Ӧ��ϵ������ߣ�����п�����ֽ⡣����HSC���ݿ���Ƴ�220����Fe-Zn-S-H2Oϵ��λ-pHͼ����ͼ2��ʾ����ͼ2��֪���ڸ���ˮ������������п����Ӧʽ(2)�����ֽ⣬�ڸ���ˮ�������£���������ϵ�е�Zn2+�� ����γ�ZnSO4��H2O�ᾧ��������ϵ�¶Ƚ���ZnSO4��H2O�ᾧ���ܽ���ת��Һ�У������м۽���п����������ת��Һ��
����γ�ZnSO4��H2O�ᾧ��������ϵ�¶Ƚ���ZnSO4��H2O�ᾧ���ܽ���ת��Һ�У������м۽���п����������ת��Һ��
ZnFe2O4(s)+ (aq)+H+(aq)=ZnSO4��H2O(s)+Fe2O3(s) (2)
(aq)+H+(aq)=ZnSO4��H2O(s)+Fe2O3(s) (2)

ͼ2 220 �� Fe-Zn-S-H2Oϵ��λ-pHͼ
Fig. 2 Potential-pH patterns for Fe-Zn-S-H2O system at 220 �� (a=1)
��������ˮ�ȷֽ⼰ת�������У���ϵ������������ɵij������ַ��ܣ�����Ӧ(3)�ܽ���ת��Һ��[26]��
Fe2O3(s)+6H+(aq)=2Fe3+(aq)+3H2O(l) (3)
2 ʵ��
2.1 ԭ��
��ʵ������ԭ��Ϊ����ijʪ����п��ҵ����������������������ˮϴ����ˣ�����70 �����������������ĥ��100Ŀɸ(��150 ��m)��װ���Ա��������仯ѧ�ɷ֡�XRD��������1��ͼ3��ʾ�����÷�����Fe2O3��Ϊʵ�龧�֣�D50Ϊ0.691 ��m�������ȷ�����ͼ4��ʾ��
�ɱ�1��֪���������г����д�������(29.37%)�����п(6.37%)��Ǧ(1.36%)���м۽��������ͼ3��֪����������������ҪΪ����������Ƽ�����������п�Ͷ�ˮ����ơ��Ƽ����������������У�п��ɰ����ˮ���кͼ���ʹ�õ�����������ĸ��Ӷ�䲢����һ����������п��
2.2 ʵ�鷽��
ʵ�鰴ͼ5��ʾ���̽��У�ȡһ��������������Ԥ�辧��Ũ�Ⱥ�Һ�̱ȼ���һ��������(Fe2O3)��ˮ�������1 L��������ѹ�����ڡ��̶�����ת��Ϊ500 r/min��Ԥ��ʵ���¶ȣ��ﵽԤ���¶Ⱥ�ʼ��ʱ������Ԥ�跴Ӧʱ�������ȴ�����ó����豸�Խ�������Һ�̷��룬�õ�ת��Һ��ת��������ȡת��Һ���������ת����ʪ�ز�����70 ����ո�������У�������������ز�ȡ���ͼ졣
��1 ����������Ҫ��ѧ�ɷ�
Table 1 Major chemical composition of jarosite residue

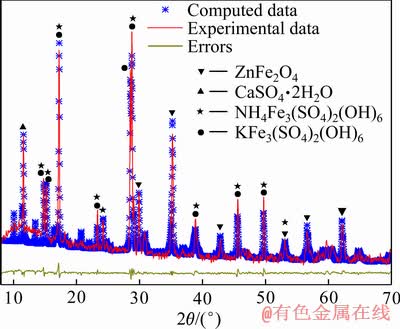
ͼ3 ��������XRD��
Fig. 3 XRD patterns of jarosite residue
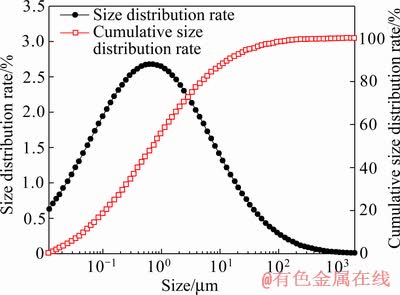
ͼ4 Fe2O3���ֵ������ֲ�ͼ
Fig. 4 Particle size distribution of hematite seed crystal
2.3 ������������
��ʵ���о���ת����������п�����Ԫ�ؼ��ί������ұ���о�Ժ�����ⶨ����������������ʡ�п�����ʽ��б�����������XPS��������ס�XRD�ľ����������ת���ʺ�ת������Fe2O3�ĺ���������֤������ת��������ʽ(4)���м���[27]��
 (4)
(4)
ʽ�У�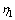 Ϊ����ת���ʣ�%��m1Ϊԭ�ϵ�������g��m2Ϊת������������g��w1Ϊԭ�������������Fe������%��w2ΪXRD��������ת���������������Fe������%��
Ϊ����ת���ʣ�%��m1Ϊԭ�ϵ�������g��m2Ϊת������������g��w1Ϊԭ�������������Fe������%��w2ΪXRD��������ת���������������Fe������%��

ͼ5 ����ʾ��ͼ
Fig. 5 Flow diagram
3 ���������
3.1 ��Ӧ�¶ȶ�������ˮ�ȿ�����ת����Ӱ��
�ڷ�Ӧʱ��4 h��Һ�̱�(mL/g)10:1����ʼ���0.01 g/L�������£������˷�Ӧ�¶ȶ�������ˮ��ת����Ӱ�졣ת������XRD����ͼ6��7��ʾ��ת������������ʡ�����ת���ʡ�п�����ʡ�ת������Fe2O3��������ȴǰ��ת��Һ��Fe3+Ũ����ͼ8��ʾ��

ͼ6 ��ͬ��Ӧ�¶ȵ�ת����XRD��
Fig. 6 XRD patterns of precipitates for various temperatures
��ͼ6��7��֪������Ӧ�¶���160 ��������180 ��ʱ����47��~53��������ڳ��ֳ���������壻�����¶�������200 ��ʱ���Ƽ������ͻ�����������������ʧ�������������������ǿ����220 ��ʱ��������ת����Ϊ95%�����������80%����Ϊ17%����ת����Ӧ������ɣ���������ҪΪ����ƺ�����Ǧ�е���ʱת��������Ҫ�������Ϊ����������ƺ�����Ǧ����������Ǧ������������Ϊ��������ˮ��ת���ֽ�����У�Ǧ���������ȶ�����ת����������������������������ͼ(��ͼ1)������������

ͼ7 160��170��200 ��ת������XRD�Ŵ�ͼ
Fig. 7 XRD enlarge pattern of precipitates at 160, 180 and 200 ��
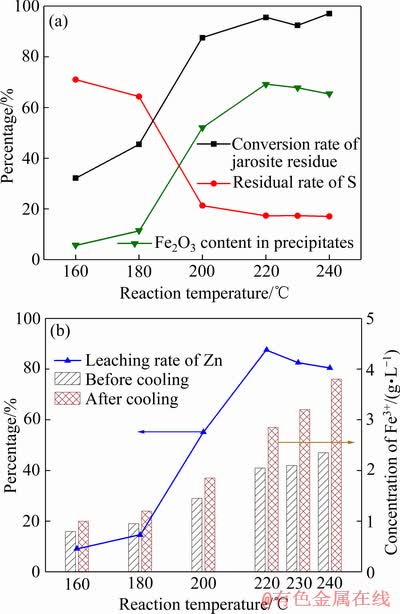
ͼ8 ��Ӧ�¶ȶ�������ת����Ӱ��
Fig. 8 Effect of reaction temperature on transformation of jarosite residue
�ڷ�Ӧ�¶���160 ��������220 ��Ĺ����У��������������ת������Ӧ��ϵ������ߣ�����п���Ϸֽ⣬����������ͣ�п������Ҳ��9%�����87%��
�����¶�����������������п�����������ת�䣬ʹ��ת����������������������160 ���6%������220 ���69%������ͼ8(b)��֪����Ӧ���������ŷ�Ӧ�¶ȵĽ��ͣ����ֳ������ܣ��ڷ�Ӧ�¶���160 ��������240 �����ȴǰ��ת��Һ��Fe3+Ũ�Ȳ���0.2 g/L������1.45 g/L����������Ӿ磬ͨ��ǰ�ڽ���ʵ����������ͨ����߽������ʿ���Ч��ֹת��������������������ķ��ܡ�
3.2 ��Ӧʱ���������ˮ�ȿ�����ת����Ӱ��
�ڷ�Ӧ�¶�220 �桢Һ�̱�10:1����ʼ���0.01 g/L�������£����췴Ӧʱ���������ת����Ӱ�졣ת������XRD����ͼ9��10��ʾ��ת������������ʡ�����ת���ʡ�п�����ʺ�ת������Fe2O3������ͼ11��ʾ��
��ͼ9��10��11��֪����220 ���·�Ӧ1 h�Ƽ������ͻ��������������������ʧ����������ת���ʴ�94%�������ӳ���Ӧʱ����5 h������ת����ԼΪ95%���ɴ˿ɼ�����Ӧ1 h������ת��������ɣ������ӳ�ʱ�������ת���ʺ�ת����������Ӱ�첻������п��������淴Ӧʱ����ӳ�����������Ӧ4 h������п�����������ȫ��ʧ��п��������68%������87%��ת�����г���������56%������69%������ת�����г���������������ת��������п����ֽ������

ͼ9 ��ͬ��Ӧʱ���ת����XRD��
Fig. 9 XRD patterns of precipitates for various time

ͼ10 ��ͬ��Ӧʱ��ת������XRD�Ŵ�ͼ
Fig. 10 XRD enlarge patterns of precipitates for various time

ͼ11 ��Ӧʱ���������ת����Ӱ��
Fig. 11 Effect of reaction time on transformation of jarosite residue
3.3 Һ�̱ȶ�������ˮ�ȿ�����ת����Ӱ��
�ڷ�Ӧ�¶�220 �桢��Ӧʱ��4 h����ʼ���0.01 g/L�������£�����Һ�̱ȶ�������ת����Ӱ�죬ת������XRD����ͼ12��ʾ��ת������������ʡ�����ת���ʡ�п�����ʺ�ת������Fe2O3������ͼ13��ʾ��

ͼ12 ��ͬҺ�̱���ת������XRD��
Fig. 12 XRD patterns of precipitates for various liquid-solid ratios

ͼ13 Һ�̱ȶ�������ת����Ӱ��
Fig. 13 Effect of liquid-solid ratio on transformation of jarosite residue
��ͼ12��13��֪����Һ�̱���5:1������30:1ʱ��XRD����ʾ�Ƽ������ͻ�������������������ֱ����ʧ������ת������90%������96%����ת�����г���������п����������ϵҺ�̱�5:1������20:1����������֮���һ������Һ�̱Ⱥͣ�����������ϵ�����Ӱ������п�ֽ���ת������Ҫ����֮һ[28]����ͼ12֤��������Һ�̱ȵ���������п��������������������ʧ��֮����Һ�̱�Ϊ25:1ʱ�����֣�����п�����ʵĽ��ͺ�ת�����г��������ļ��١�
3.4 ��ʼ��ȶ�����ˮ�ȿ�����ת����Ӱ��
�ڷ�Ӧ�¶�220 �桢��Ӧʱ��4 h��Һ�̱�10:1�������£������˳�ʼ��ȶ�������ת����Ӱ�졣ת������XRD����ͼ14��ʾ��ת������������ʡ�����ת���ʡ�п�����ʺ�ת������Fe2O3������ͼ15��ʾ��
��ͼ14��15��֪����ʼ�����0.01 g/L������5 g/L��п��������87%������92%������ת���ʡ�ת�����г�����������ʼ������ֲ��䣻��ʼ��ȴ�15g/L����������ȣ�ת�����в����д���δת��������������п���࣬����������ߣ�ת�����г����������罵�͡��ɼ�����ʼ��ȶ�����ˮ��ת��Ӱ����������������ת��Ϊ���ᷴӦ�����ߵ���Ƚ���������ת����

ͼ14 ��ͬ��ʼ��ȵ�ת����XRD��
Fig. 14 XRD patterns of precipitates for various acidities
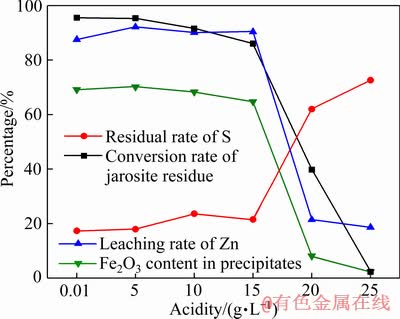
ͼ15 ��ʼ��ȶ�������ת����Ӱ��
Fig. 15 Effect of acidity on transformation of jarosite residue
3.5 ���ֶ�������ˮ�ȿ�����ת����Ӱ��
�ڷ�Ӧ�¶�220 �桢��Ӧʱ��4 h��Һ�̱�10:1����ʼ���0.01 g/L�������£���Fe2O3��Ϊ���֣��Ա�0��5��10 g/L����Ũ�ȶ�������ת����Ӱ�죬���Է�Ӧ0 h(�¶ȴﵽ220 ��ʱ��ʼ��ʱ)�ͼ���1 h(������(183��2) ��)����ȡ����ת�����ĺ��ͼ��ͼ16��ʾ����ͬʱ�䡢��ͬ����Ũ�ȵ�ת����XRD����ͼ17��ʾ����ͬ����Ũ�ȶ�������ת���ķ��������ͼ18��19��ʾ��

ͼ16 ��ͬ����Ũ�ȵ�ת�������ͼ
Fig. 16 Macro graphs of precipitates for various crystalline concentrations

ͼ17 ��ͬ����Ũ���ڷ�Ӧ0 h��4 h��ת����XRD��
Fig. 17 XRD patterns of precipitates after reactions of 0 h and 4 h for various crystalline concentrations
��ͼ16��֪�����뾧�ִﵽ��Ӧ�¶�ʱ��ת��������ɫ�ʽۺ�ɫ����δ���뾧��ʱ�Ļ�ɫ�����ɫ�����XRD�������ͼ16��ʾ�����ž���Ũ��������5 g/L��ת�������������ຬ����46%������30%�����ֵļ���ӿ������������ת����
�ɷ�Ӧ4 h��ת����XRD��Ԫ�ؼ���֪��0��5��10 g/L����Ũ���µ�����ת����Ϊ94.8%��0.7%��������ʺ�п�����ʻ������䣬ת�����г��������ӵ����������ľ���������ȣ�������D50�ֱ�Ϊ1.84��2.06��1.82 ��m����֪���뾧�ֽ���������Ӧ�ٶȣ�ʹ��Ӧ�ӿ���У��Է�Ӧ���еij̶ȡ�ת�������Ⱦ���Ӱ�졣

ͼ18 ����Ũ�ȶԷ�Ӧ0 h��4 h��������ת����Ӱ��
Fig. 18 Effect of crystalline concentration on transformation of jarosite residue after reactions of 0 h(a) and 4 h(b)
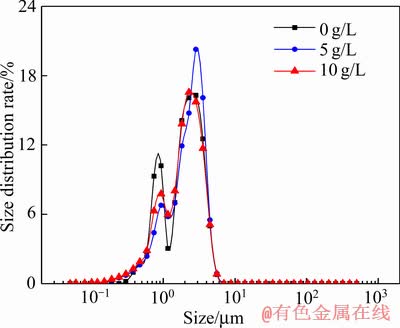
ͼ19 ��ͬ����Ũ���·�Ӧ4 h��ת�����������ֲ�ͼ
Fig. 19 Particle size distribution of precipitates after reaction of 4 h for various crystalline concentrations
4 �ۺ�����ʵ��
��������������ʵ��������������������ˮ��������ת��Ϊ�����������ڷ�Ӧ�¶�220 �桢��Ӧʱ��4 h��Һ�̱�10:1����ʼ���0.01 g/L�Ҳ��Ӿ��ֵ������½�һ����չ���ۺ���֤�о���
���ۺ�����ʵ��ת�������к������⣬��ͼ20��ʾ���Ա���������ת������900~1300 cm-1��Χ�ڵ� ���շ壬�������ർ��
���շ壬�������ർ�� �γ���λ������ʹ���ӵĶԳ��Խ��ͣ����������ѣ������г��־����������Ե���ģʽ����������������ת��Ϊ���������к�
�γ���λ������ʹ���ӵĶԳ��Խ��ͣ����������ѣ������г��־����������Ե���ģʽ����������������ת��Ϊ���������к� �����ʣ����ƺ�����Ǧ��
�����ʣ����ƺ�����Ǧ��  �ĶԳ�����ǿ��ֻ����1095.50 cm-1�������շ�[29]��ͬʱ��ͼ21��22��֪����������O 1s������Ϊ˫�壬��������531.59 eV��ΪCaSO4��2H2O�ᾧˮ�������壬��ˮ�ȴ���ת��Ϊת������530.06 eV��Fe2O3��������[30]�����ת������XRD��(��ͼ23)��֪����ˮ�ȴ��������в�����
�ĶԳ�����ǿ��ֻ����1095.50 cm-1�������շ�[29]��ͬʱ��ͼ21��22��֪����������O 1s������Ϊ˫�壬��������531.59 eV��ΪCaSO4��2H2O�ᾧˮ�������壬��ˮ�ȴ���ת��Ϊת������530.06 eV��Fe2O3��������[30]�����ת������XRD��(��ͼ23)��֪����ˮ�ȴ��������в����� Ϊ����ơ�����Ǧ�����࣬ת��������Ҫ����Ϊ������������������������塣ת������Ҫ��ѧ�ɷ����2��ʾ��
Ϊ����ơ�����Ǧ�����࣬ת��������Ҫ����Ϊ������������������������塣ת������Ҫ��ѧ�ɷ����2��ʾ��

ͼ20 ��������ת�����ĺ������ͼ
Fig. 20 FT-IR spectra of jarosite residue and precipitates

ͼ21 ��������ת������ȫ��ɨ����
Fig. 21 Full spectrum scanning spectrogram of jarosite residue and precipitates

ͼ22 ��������ת������OԪ�ص�խ��ɨ��ͼ��
Fig. 22 Resolved narrow scan spectra of element O in jarosite residue (a) and precipitates (b)
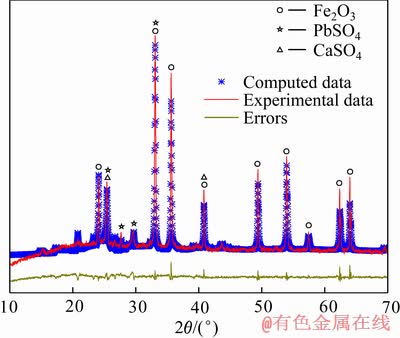
ͼ23 �ۺ�ʵ��ת������XRD��
Fig. 23 XRD patterns of precipitates of comprehensive experiment
�ۺ����������������ˮ�ȴ���������������������ת���ʿɴ�95%���м۽���п�����ʿɴ�89%�������������и��������ɴ�48%��ת�������������ϸߣ�������������Ǧ�������м۽��������Ϊ����ԭ�ϣ�����Ϊ��ɫ��[31]�������ˮ��̻��Ʊ��ս�ש[18]��ʵ��Σ���������а���������Դ�����á�
��2 ת������Ҫ��ѧ�ɷ�
Table 2 Major chemical composition of precipitates (mass fraction, %)

5 ����
1) ���ۼ����ʵ����������������ˮ��ת���ֽ������������ķֽ��������Ϊ��������������������Ƽ�������Ǧ������Σ����������ˮ�ȴ�����ת��Ϊ����������ת�����г���������������ת��������п����ֽ���ɡ�
2) �¶���Ӱ��������ת���Ĺؼ����أ������¶ȿɴٽ��������������п������������ת������220���ˮ����ϵ�У�94%�����������ڷ�Ӧ1 h���ת����п�������ڷ�Ӧ4 h���87%�����Һ�̱ȿɴٽ�����������������ת���������ߵ�Һ�̱Ƚ��谭����п�ķֽ⣻��ȴ���15 g/L���谭��������ת����������������ת���ʵĽ��ͣ����Ӿ��ֿ��Լ�����������ת��������ˮ���������γɵij�������������С���ڽ��¹����г�������ڷ���������߽�����������ֹת�����������������ܵ���Ч������
3) �ڷ�Ӧ�¶�220 �桢��Ӧʱ��4 h��Һ�̱�10:1����ʼ���0.01 g/L�Ҳ����뾧�ֵ������£����������ת���ʿɴ�95%��п�����ʴ�89%������ת��������Ҫ����Ϊ�������京��Ϊ68%��
REFERENCES
[1] KAKSONEN A H, MORRIS C, HILARIO F, REA S M, LI J, USHER K M, WYLIE J, GINIGE M P, CHENG K Y, DU PLESSIS C. Iron oxidation and jarosite precipitation in a two-stage airlift bioreactor[J]. Hydrometallurgy, 2014, 150: 227-235.
[2] ÷���, ������, �ܾ�Ԫ, �� ��. ʪ����пѧ[M]. ��ɳ: ���ϴ�ѧ������, 2001: 197-198.
MEI Guang-gui, WANG De-run, ZHOU Jing-yuan, WANG Hui. Zinc hydrometallurgy[M]. Changsha: Central South University Press, 2001: 197-198.
[3] �� ��, ��־��, κ ��, �����, ���˱�. ���ó�����ȥ��������п�����Һ�е���[J]. �й���ɫ����ѧ��, 2014, 24(9): 2387-2391.
YANG Fan, DENG Zhi-gan, WEI Chang, LI Cun-xiong, LI Xing-bin. Iron-removal by hematite from leaching liquor of high iron sphalerite[J]. The Chinese Journal of Nonferrous Metals, 2014, 24(9): 2387-2391.
[4] ���㾲. �ؽ���ұ��ѧ[M]. ����: ұ��ҵ������, 2013: 197-198.
ZHAI Xiu-jing. Metallurgy of heavy metals[M]. Beijing: Metallurgical Industry Press, 2013: 197-198.
[5] CRABBE H, FERMANDEZ N, JONES F. Crystallization of jarosite in the presence of amino acids[J]. Journal of Crystal Growth, 2015, 416: 28-33.
[6] KENDALL M R, MADDEN A S, MADDEN M E E, HU Qin-hong. Effects of arsenic incorporation on jarosite dissolution rates and reaction products[J]. Geochimica et Cosmochimica Acta, 2013, 112(3): 192-207.
[7] ����ƽ, ������, ����ϲ, ����ƽ, �� ʤ. ��п�������Ļ�������[J]. ��ұ, 2009, 18(1): 23-28.
LIU San-ping, WANG Hai-bei, JIANG Kai-xi, FENG Ya-ping, HUANG Sheng. Utilization of jarosite containing zinc[J]. Mining & Metallurgy, 2009, 18(1): 23-28.
[8] MEHRA P, GUPTA R C, THOMAS B S. Properties of concrete containing jarosite as a partial substitute for fine aggregate[J]. Journal of Cleaner Production, 2016, 120: 241-248.
[9] DUTRIZAC J E, JAMBOR J L. Jarosites and their application in hydrometallurgy[J]. Reviews in Mineralogy and Geochemistry, 2000, 40(1): 405-452.
[10] KAKSONEN A H, MORRIS C, REA S M JIANLI, USHER K M, MCDONALD R G, HILARIO F, HOSKEN T, JACKSON M, PLESSIS C A. Biohydrometallurgical iron oxidation and precipitation: Part ��Jarosite precipitate characterisation and acid recovery by conversion to hematite[J]. Hydrometallurgy, 2014, 147/148: 264-272.
[11] ������, ������, �����, ������, �� ʤ. �û����������Ʊ�������п������[J]. ���ϴ�ѧѧ��(��Ȼ��ѧ��), 2006, 37(4): 685-691.
YANG Zheng-hui, GONG Zhu-qing, LI Hong-xu, CHEN Wen-mi, GONG Sheng. Preparation of Ni-Zn ferrite from sodium jarosite residue[J]. Journal of Central South University (Science and Technology), 2006, 37(4): 685-691.
[12] Ѧ����, ���ٻ�, �����, ������. ����-�����Ƽ��������ж����м۽���[J]. ���̹���ѧ��, 2011, 11(1): 56-60.
XUE Pei-yi, JU Shao-hua, ZHANG Yi-fei, WANG Xin-wen. Recovery of valuable metals by leaching of roasted jarosite residue[J]. The Chinese Journal of Process Engineering, 2011, 11(1): 56-60.
[13] ������. ����ֱ�ӻ�ԭ��������������Ǧп����ͬ����������о�[D]. ����: �����Ƽ���ѧ, 2018: 24-30.
WANG Yun-xue. Fundamental study on recovery of lead,zinc an iron and simultaneous sulfur from jarosite residues based on direct reduction[D]. Beijing: Civil and Resource Engineering University of Science and Technology Beijing, 2018: 24-30.
[14] ·����, ������, л ��, �� ��. ��������ԭ�����Ʊ���������о�[J]. ͭҵ����, 2013(1): 6-11.
LU Dian-kun, JIN Zhe-nan, XIE Feng, WANG Meng. Research on magnetite preparation by reductive baking of jarosite residue[J]. Copper Engineering, 2013(1): 6-11.
[15] JU S H, ZHANG Y F, ZHANG Y, XUE P Y, WANG Y H. Clean hydrometallurgical route to recover zinc, silver, lead, copper, cadmium and iron from hazardous jarosite residues produced during zinc hydrometallurgy[J]. Journal of Hazardous Materials, 2011, 192(2): 554-558.
[16] �ſ���, ��־ǿ, ������, ����ϼ. ��������������ˮ��������п����[J]. �й���ɫ����ѧ��, 2017, 27(5): 1045-1050.
ZHANG Kui-fang, LIU Zhi-qiang, DAI Zi-lin, GAO Li-xia. Recovery of Zn and In from ammonium jarosite residue bearing indium by roasting-water leaching method[J]. The Chinese Journal of Nonferrous Metals, 2017, 27(5): 1045-1050.
[17] ������, ������, ������, �� ��, �Ƴ���, ���, ³����. NaOH�ֽ⺬���������¹���[J]. �й���ɫ����ѧ��, 2009, 19(7): 1322-1331.
CHEN Yong-ming, TANG Mo-tang, YANG Sheng-hai, HE Jing, TANG Chao-bo, YANG Jian-guang, LU Jun-yue. Novel technique of decomposition of ammonium jarosite bearing indium in NaOH medium[J]. The Chinese Journal of Nonferrous Metals, 2009, 19(7): 1322-1331.
[18] ������, �����, ������, �� ��, ��С��. ����������ջƼ����������м�Ԫ��[J]. ���̹���ѧ��, 2016, 16(4): 584-589.
LIU Peng-fei, ZHANG Yi-fei, YOU Shao-wei, BO Jing, JIANG Xiao-duo. Recovery of valuable elements in jaroaite residue by hot acid leaching[J]. The Chinese Journal of Process Engineering, 2016, 16(4): 584-589.
[19] �� ��, �ƽ, ������, ������, ������. ����������ֽ⼰��������[J]. �й���ɫ����ѧ��, 2017, 27(7): 1504-1512.
HE Jing, YANG Jian-ping, YANG Sheng-hai, CHEN Yong-ming, WANG Xia-yang. Decomposition of jarosite residue in sulfuric acid medium and recovery of silver with thiourea solution[J].The Chinese Journal of Nonferrous Metals, 2017, 27(7): 1504-1512.
[20] ̷���, ��Сǿ, ֣����, ����ʢ. ������ˮ������������Ӧ���P�̻�[J]. ��ɫ��������, 2015, 5(6): 74-77.
TAN Hong-bin, HOU Xiao-qiang, ZHENG Xu-tao, GUO Cong-sheng. Reaction product and solidification of portland cement and jarosite slag[J]. Nonferrous Metals Engineering, 2015, 5(6): 74-77.
[21] ASOKAN P, SAXENA M, ASOLEKAR S R. Hazardous jarosite use in developing non-hazardous product for engineering application[J]. Journal of Hazardous Materials, 2006, 137(3): 1589-1599.
[22] �����, κ ��, ��־��, ���˱�, �� ��, ������, ��˸��, ��F͢. FeSO4-H2O ��ϵ��ˮ�ȳ��������������̬������ת����Ϊ[J]. �й���ɫ����ѧ��, 2018, 28(3): 628-634.
LI Cun-xiong, WEI Chang, DENG Zhi-gan, LI Xing-bin, FAN Gang, WANG Yi-zhao, YI Shuo-wen, LI Min-ting. Hydrothermal hematite precipitation and conversion behavior of metastable iron phase in FeSO4-H2O system[J]. The Chinese Journal of Nonferrous Metals, 2018, 28(3): 628-634.
[23] DENG Zhi-gan, ZHU Bei-ping, ZENG Peng, WEI Chang, LI Xing-bin, LI Cun-xiong, FAN Gang. Behavior and characterization of hematite process for iron removal in hydrometallurgical production[J]. Canadian Metallurgical Quarterly, 2019, 60(2): 222-231.
[24] ������, �����, κ ��, ��־��, ���˱�, �� ��, ��˸��. ʪ����п�����г��������ɼ��������ת��[J]. �й���ɫ����ѧ��, 2017, 27(10): 2145-2153.
WANG Yi-zhao, LI Cun-xiong, WEI Chang, DENG Zhi-gan, LI Xing-bin, FAN Gang, YI Shuo-wen. Production of hematite and conversion of adsorption S in zinc hydrometallurgy process[J]. The Chinese Journal of Nonferrous Metals, 2017, 27(10): 2145-2153.
[25] LI Cun-xiong, DENG Zhi-gan, WEI Chang, FAN Gang, LI Xing-bin, LI Min-ting, WANG Yi-zhao. Production of low-sulfur hematite by hydrothermal oxydrolysis of ferrous sulfate[J]. Hydrometallurgy, 2018, 178: 294-300.
[26] DUTRIZAC J E, SUNYER A. Hematite formation from jarosite type compounds by hydrothermal conversion[J]. Canadian Metallurgical Quarterly, 2012, 51(1): 11-23.
[27] �Ƽ���, �� ��. �ྦྷ����X��������[M]. ����: ұ��ҵ������, 2012: 241-263.
HUANG Ji-wu, LI Zhou. Polycrystalline material X-ray diffraction[M]. Beijing: Metallurgical Industry Press, 2012: 241-263.
[28] ֣ ��, ��־��, �� ��, κ ��, �� ��, ���˱�, �����, ��F͢. ��������ԭ�ֽ�����п��п��������[J].�й���ɫ����ѧ��, 2019, 29(1): 170-178.
ZHENG Yu, DENG Zhi-gan, FAN Gang, WEI Chang, FAN Guang, LI Xing-bin, LI Cun-xiong, LI Min-ting. Reductive decomposition of zinc ferrite and zinc residues by sulfur dioxide[J]. The Chinese Journal of Nonferrous Metals, 2019, 29(1): 170-178.
[29] �б�һ��, �Ƶ���. ������λ������ĺ������������[M]. ����: ��ѧ��ҵ������, 1986: 244-248.
NAKAMOTO Kazuo, HUANG De-ru. Infrared and Raman spectra of inorganic and coordination compounds[M]. Beijing: Chemical Industry Press,1986: 244-248.
[30] MOULDER J F, STICKLE W F, SOBOL P E, BOMBEN K D. Handbook of X-ray photoelectron spectroscopy[M]. Minnesota, USA: Physical Electronics Inc, 1995: 44-45.
[31] �� ��, �����, ������. �ӻ�ѧ�ɷ�̽�����̷ֹ������ҳ���ս�ש������[J]. �й����ĿƼ�, 2017(6): 69-70.
CHEN Jian, LI Bi-xiong, LIANG Xin-xiao. The feasibility of the fired brick incorporating three kinds of solid waste based on chemical components[J]. China Academic Journal Electronic Publishing House, 2017(6): 69-70.
Hydrothermal decomposition of hazardous jarosite residue produced in zinc hydrometallurgy and transformation behavior of iron containing phase
CHU Ming, LI Cun-xiong, ZHANG Peng, JI Wen-bin, WEI Chang, DENG Zhi-gan, LI Xing-bin, FAN Gang, LI Min-ting
(Faculty of Metallurgical and Energy Engineering, Kunming University of Science and Technology, Kunming 650093, China)
Abstract: The jarosite produced in the process of zinc hydrometallurgy contains a large amount of valuable metal Zn, Pb and associated metal Fe. Under hydrothermal conditions, the jarosite will decompose and transform efficiently, the valuable metal will be transferred into solution, and the associated Fe will be transformed into hematite. In this paper, the jarosite produced by the zinc-iron separation process in the wet zinc smelting enterprise was taken as the research object, the effects of macroscopic technical parameters such as reaction temperature, reaction time, liquid-solid ratio, acidity and crystalline concentration on the decomposition and transformation of jarosite and zinc ferrite phases in precipitates were studied. Theoretical calculation and experimental results show that in high-temperature hydrothermal system, jarosite, ammoniojarosite and zinc ferrite phase in jarosite slag can be effectively transformed into hematite, while the plumbojarosite are stable and difficult to be transformed. Increasing the temperature and prolonging the reaction time are beneficial to the hydrothermal decomposition and transformation of the phase of jarosite, ammoniojarosite and zinc ferrite. After reaction of 1 h at 220 ��, jarosite phase transformation is basically completed, the conversion rate is 94%; and after the reaction of 4 h, the diffraction peak of zinc ferrite phase disappears completely, zinc leaching rate is 87%, and the transformation of precipitates in hematite content is 68%. Appropriately increasing the acidity of the system is conducive to the transformation of zinc ferrite, but when the initial acidity of the system is higher than 15 g/L, the phase transformation of ferrite will be inhibited. Under the conditions of reaction temperature of 220 ��, reaction time of 4 h, liquid-solid ratio(mL/g) of 10:1, and initial acidity of 0.01 g/L, the zinc leaching rate is 89%, the conversion rate of jarosite phase can reach 95%. Hematite is the main phase in precipitates, and its content is 68%.
Key words: jarosite; hydrothermal decomposition; hematite; transformation behavior
Foundation item: Project(51664038, 51474117, 51804146) supported by the National Natural Science Foundation of China
Received date: 2019-04-23; Accepted date: 2019-07-05
Corresponding author: LI Cun-xiong; Tel: +86-13518764748; E-mail: licunxiong@126.com
(�༭ ��ѧ��)
������Ŀ��������Ȼ��ѧ����������Ŀ(51664038��51474117��51804146)
�ո����ڣ�2019-04-23�������ڣ�2019-07-05
ͨ�����ߣ�����֣����ڣ���ʿ���绰��13518764748��E-mail��licunxiong@126.com