文章编号:1004-0609(2012)05-1311-08
液相沉淀-多元醇还原法合成
LiFePO4/C正极材料的电化学性能
李绍敏1,刘 恒1,陈 亮1,李 渊1,郝保青2
(1. 四川大学 材料科学与工程学院,成都 610064;
2. 西南民族大学 生命科学与技术学院,成都610041)
摘 要:以钛白工业副产物七水硫酸亚铁为铁源,用液相沉淀制得无定形FePO4・xH2O前躯体,然后在多元醇中与锂源反应制得LiFePO4材料,过程在常压下进行,无需煅烧与惰性气体保护。用XRD、SEM及电化学分析考察多元醇乙二醇(EG)、二甘醇(DEG)和三甘醇(TEG)对材料物相和形貌的影响。结果表明:三甘醇所得样品的锂离子扩散速率最小;此样品的晶粒尺寸最小,结晶最完整,无明显杂相生成。在室温下放电倍率为0.1C、1C和5C时,该正极材料的首次放电比容量分别达到148.8、129.3和102.8 mA・h/g,其碳包覆样品的首次放电比容量分别达到155.6、139.9和112.2 mA・h/g,且循环性能良好。
关键词:LiFePO4;液相沉淀;多元醇;锂离子电池;正极材料
中图分类号:O614.111;TM912 文献标志码:A
Electrochemical performance of LiFePO4/C cathode materials synthesized by liquid-precipitation and polyol reduction route
LI Shao-min1, LIU Heng1, CHEN Liang1, LI Yuan1, HAO Bao-qing2
(1. School of Materials Science and Engineering, Sichuan University, Chengdu 610064, China;
2. College of Life Science and Technology, Southwest University of Nationalities, Chengdu 610041, China)
Abstract: Amorphous FePO4・xH2O was prepared by liquid precipitation using FeSO4・7H2O by-product of titanium dioxide industry, and LiFePO4 was synthesized by a polyol route under ordinary pressure without further calcinating or inert gas protection. The effects of different polyols of EG, DEG and TEG on the phase composition and morphology were investigated by X-ray diffraction(XRD), scanning electron microscope (SEM) and electrochemical analysis. The results demonstrate that LiFePO4 prepared by TEG shows the smallest diffusion rate of lithium ion, the smallest particle size, the best crystalline integrity and the highest phase purity. The LiFePO4 prepared by TEG has the first discharge specific capacities of 148.8, 129.3 and 102.8 mA・h/g at 0.1C, 1C and 5C discharge rate and room temperature, respectively. The improved first discharge specific capacity of its carbon-coating sample reaches 155.6, 139.9 and 112.2 mA・h/g at 0.1C, 1C and 5C, respectively, exhibiting a favorable capacity cycling maintenance.
Key words: LiFePO4; liquid-precipitation; polyol; lithium-ion battery; cathode material
1997年,GOODENOUGH等[1]研究发现,橄榄石型LiFePO4是一种极具应用潜力的锂离子电池正极材料,但其最主要的缺点是本征导电率和振实密度低。改善LiFePO4导电性的方法主要集中在:掺杂金属离子进入LiFePO4晶格,表面包覆导电剂以提高其本征导电性能[2-3];采用不同的制备方法或合成工艺,以改善LiFePO4的尺寸大小和形貌[4]。LiFePO4正极材料充放电辐射模型[1]认为,锂离子脱嵌过程是在LiFePO4/FePO4两相界面进行的,随着循环次数的增加,非活性物质相FePO4包裹活性物质相LiFePO4,使其不能被充分利用,从而造成容量损失,且大倍率放电性能较差。根据这个理论,大比表面积和细小粒径的LiFePO4可缩短锂离子的扩散路径,有利于电化学反应的进行。有许多方法与工艺能制备出颗粒粒径在200~300 nm的LiFePO4;如实验室常用的溶胶-凝胶法[5]、软模板法[6]和水热法[7],工业上常用的高温固相法、碳热还原法和湿法沉淀-高温烧成法。以上方法大都采用分析纯试剂作为原料,或需要在高压容器或惰性气体和还原性气体的保护下煅烧才能得到LiFePO4及其复合材料。
多元醇具有强还原性,近年来已被用来制备高结晶度的金属、合金及氧化物粉末[8],此法为在常压较低温度下制备结晶良好的超微粉体材料提供了一条有效途径。CAO等[9]利用三甘醇还原分析纯的三价铁源制备LiFePO4,获得了较好的结果。CHOI等[10]采用四甘醇一步合成得到LiFePO4,现有文献报道多以价格较昂贵的分析纯试剂为原料。结合以上方法的优点,本文作者以价格低廉的钛白工业副产物七水硫酸亚铁为铁源,采用液相沉淀法制备无定形FePO4前躯体,再利用多元醇还原方法制备LiFePO4正极材料。制备过程在常压下进行,无需煅烧与惰性气体保护,且多元醇可回收利用,从原料与工艺过程能耗两方面降低生产成本。通过实验比较3种多元醇对最终产物物相、粒径、形貌和电化学性能的影响。所制得的LiFePO4正极材料具有物相单一和粒径细小的优点,且电化学性能较优异。
1 实验
1.1 实验所用原料
亚铁盐溶液的精制:将钛白工业副产物七水硫酸亚铁溶解、加入少量铁粉后加热还原其中的三价铁杂质、调节pH值为5~6,生成的沉淀用絮凝剂沉降过滤除去大部分杂质,最后得到含有微量Mn2+和Mg2+的亚铁盐溶液,再用硫酸调节pH值至2~3以利于保存。
实验所用原料:精制FeSO4、NH4H2PO4(工业纯)、H3PO4(工业纯)、LiOH(电池级)、柠檬酸和聚乙二醇(PEG,相对分子质量为6 000)均为分析纯。
1.2 液相沉淀法制备FePO4・xH2O
将NH4H2PO4与FeSO4混合,用双氧水氧化Fe2+,NH3・H2O调节pH,搅拌反应一段时间后过滤、洗涤溶液中的SO42-,干燥沉淀得到FePO4・xH2O,其中铁含量和磷含量的测定分别按文献[11-12]所列方法进行。
1.3 LiFePO4/C的制备
按化学计量比n(Fe):n(P)=1:1称取自制FePO4・
xH2O和LiOH。首先将FePO4・xH2O分散到液相还原剂多元醇(醇与Fe3+的摩尔比为10:1)中,转移至旋转真空蒸发器反应,然后将LiOH水溶液慢慢滴加到体系中。电热套加热,先形成砖红色悬浊液,然后在多元醇沸点温度回馏10 h,最后减压蒸馏回收多元醇,蒸干沉淀即得产物。多元醇有乙二醇、二甘醇和三甘醇,分别在其沸点198、245和290 ℃下得到样品S1、S2和S3。为了对比后续热处理对材料的影响,高能球磨样品S3、柠檬酸和聚乙二醇的混合物,干燥后在氮气保护下于650 ℃煅烧1 h,得到碳包覆样品S4。
1.4 材料的表征
采用X射线衍射仪(Philips X’Pert Pro MDP)检测晶相组成(管压40 kV、管流100 mA、Cu Kα射线、扫描范围10°~70°、λ=0.154 05 nm)。样品形貌采用JEOL公司生产的JSM-5900LV型扫描电子显微镜观察(无水乙醇作为分散剂,超声分散)。碳含量测量采用CS-902红外碳硫分析仪(北京万联达公司生产)。
1.5 电化学性能测试
将合成产物LiFePO4/C(80%,质量分数)与导电剂乙炔黑(15%,质量分数)、黏结剂PVDF(5%,质量分数)及一定量的N-甲基-2-吡咯烷酮(NMP)球磨混合均匀,用涂膜器均匀涂布在铝箔上,在真空于120 ℃下干燥12 h,冷却至室温,冲切成直径为1.6 cm的圆片,10 MPa下压平得到扣式电池正极片并称取质量。采用金 属直径为1.7 cm锂片作负极,直径为1.8 cm的Celguard 2400 PE膜作隔膜,以1 mol LiPF6溶解在体积比为1:1的碳酸乙烯酯(EC)和碳酸二甲酯(DMC)的混合液作为电解液。在充满氩气的无水、无氧的手套箱内组装成CR2032扣式电池,用Neware BTS-610 (中国深圳生产)多通道电池测试系统,在电压为2.5~ 4.3 V范围对电池进行恒流充放电测试。采用美国生 产的Pastart2273分析仪进行电化学交流阻抗谱测试(EIS),频率范围为1 mHz~100 kHz,扰动电压为5 mV。
2 结果与讨论
2.1 前躯体物相与形貌
图1所示为FePO4・xH2O前躯体的红外光谱,在 1 053 cm-1波数处为与P=O伸缩振动相关的吸收峰,528 cm-1波数处为PO4的弯曲振动吸收峰[13],3 000~ 3 600 cm-1范围内强而宽的吸收谱带是水分子对称伸缩振动和反对称伸缩振动产生的吸收,l 628 cm-1处是水分子面内弯曲振动谱带;400~900 cm-1是水分子面外弯曲振动谱带[13]。从红外光谱可以看出:以经过净化的钛白工业副产物七水硫酸亚铁为铁源制备的FePO4・xH2O前躯体的基本结构单元是PO4四面体,含一定量的化学吸附水。图2(a)所示为自制FePO4・xH2O的XRD谱,说明此FePO4・xH2O前躯体呈无定形态,PO4四面体并不是有序的生长。图2(b)所示为FePO4・
xH2O的SEM像。从图2(b)可以看出:FePO4・xH2O颗粒尺寸较小,在0.2~0.5 μm范围,且粒径分布较均匀。

图1 前躯体FePO4・xH2O的红外光谱
Fig. 1 FTIR spectrum of FePO4・xH2O precursor
2.2 样品物相与形貌分析
图3所示为在乙二醇、二甘醇和三甘醇沸点温度下回馏得到的样品S1、S2和S3的XRD谱。从图3可以看出:3个样品的衍射峰与LiFePO4材料的标准衍射峰(JCPDS标准卡号81-1173)一致,均为正交晶系橄榄石结构,属于Pnma空间群,特征峰明显,背底较为平整,说明多元醇法反应过程无需惰性气体保护可一步制备结晶良好的LiFePO4。与LiFePO4标准XRD谱相比,样品S1存在少许杂质峰,经分析,杂相主要为Fe2PO5,其他3个样品无杂质峰,且随着还原温度的升高,特征峰趋于尖锐,结晶度更高。多元醇在其沸点下具有强还原性[8],可将前躯体中的Fe3+还原成Fe2+,S1所得杂相为Fe2PO5,其中铁元素为三价,可能是乙二醇的还原作用没有二甘醇和三甘醇的强而造成的。由谢乐公式[14]可得样品S1、S2和S3的平均晶粒尺寸分别为30.6、30.3和28.0 nm,即在这个反应体系中较高的还原温度有利于得到晶粒尺寸更小的LiFePO4。多元醇相对分子质量的增大导致其沸点升高,在较高沸点温度下生成的晶粒可能因毛细收缩而减小,从而抑制一次粒子的凝并长大,较大相对分子质量的多元醇具有更明显的空间位阻效应,也可抑制一次晶粒的凝并长大[15]。
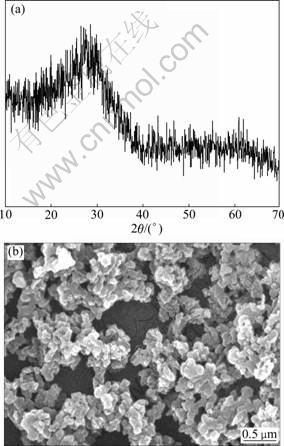
图2 前躯体FePO4・xH2O的XRD谱和SEM像
Fig. 2 XRD pattern (a) and SEM image (b) of FePO4・xH2O precursor

图3 不同反应条件下S1、S2、S3和S4的XRD谱
Fig. 3 XRD patterns of LiFePO4 samples S1, S2, S3 and S4 prepared under different reaction conditions
图3中还比较了以三甘醇为还原剂所得样品S3与煅烧后样品S4的XRD谱。从图3可以看出:经过碳包覆后的样品S4的衍射峰比S3的更尖锐,特征峰更清晰,且没有观察到碳的晶态衍射峰,经碳硫分析仪分析检测样品S4的碳含量为5.44%(质量分数),说明柠檬酸煅烧分解的碳是以无定形的形式存在,且不会影响LiFePO4的晶体结构。根据正交晶系面间距公式及布拉格方程[1]可计算出样品S4的晶胞参数a= 1.031 6 nm,b=0.599 5 nm,c=0.468 8 nm,与标准卡片中的晶胞参数(a=1.033 2 nm,b=0.601 0 nm,c= 0.469 2 nm)基本吻合。
图4所示为S1、S2、S3和S4样品的SEM像。由图4可以看出:S1的粒径分布不均,且颗粒较粗;S2的颗粒较S1细化;三甘醇还原得到的LiFePO4材料S3的一次颗粒更细小,尺寸在100~200 nm,但一次粒子小、表面能高,导致团聚现象较严重;碳包覆后LiFePO4/C 复合材料S4并没有聚集生长成为大颗粒,粒径分布较均匀,主要是由于柠檬酸和PEG(6 000)在煅烧过程热解后的无定形碳包裹在LiFePO4表面,使得颗粒表面粗糙,产生的空间阻隔在一定程度上避免了粒子凝并长大成粗颗粒[16]。可见,多元醇还原法可获得粒径分布均匀、颗粒细小的LiFePO4材料,这有利于缩短Li+的的固相扩散距离,提高Li +扩散速率,改善材料的电化学动力学性能,且还原温度越高,样品平均晶粒尺寸越小。这一结论也可由XRD谱分析结果得到证实。
2.3 多元醇液相还原反应机理
为探讨液相还原反应机理,本文作者以三甘醇为还原剂,对每隔2.5 h所得产物T0、T1、T2、T3和S3进行X射线衍射分析和pH值测量,各反应时间点所取样品的数据列于表1。图5所示为各样品的XRD谱。从表1和图5可以看出:各反应时间点XRD谱的峰型变化较大,T0处于反应初期,原料随温度升高逐渐熔融,有少量新产物生成,呈非晶态;随回馏时间的增加,物质自发充填颗粒而致密化,粒度逐渐增大,LiFePO4特征峰趋于尖锐,结晶更完整。因T0还处于非晶态,衍射峰不易辨认,不能正确计算晶粒度。其余各时间点粒度为根据谢乐公式D=kλ/(βcosθ) (k=0.9, λ=0.154 06 nm)[14]采用2θ<40°的3个主要衍射峰的半高峰宽(β)计算的平均粒度,可以看出,在体系保温7.5 h后,晶体生长较快。
结合体系的pH值和XRD谱,推测各反应物之间发生的化学反应可能按照以下步骤进行:
FePO4+3LiOH=Fe(OH)3+Li3PO4 (1)
Fe(OH)3=Fe3++3OH- (2)
4Fe3++2HOCH2CH2OCH2CH2OCH2CH2OH=(3)

H++OH-=H2O (4)
FePO4+3OH-=Fe(OH)3+ (5)
(5)
Li3PO4+3Fe2++2 =3LiFePO4 (6)
=3LiFePO4 (6)

图4 不同条件下S1、S2、S3和S4样品的SEM像
Fig. 4 SEM images of LiFePO4 samples prepared under different conditions: (a) Sample S1; (b) Sample S2; (c) Sample S3; (d) Sample S4
表1 各反应时间点所取样品参数
Table 1 Parameters of samples at different reaction times
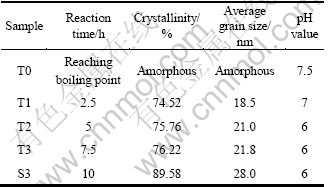

图5 反应各时间点样品的XRD谱
Fig. 5 XRD patterns of samples at different reaction times
以上反应进行时,由于FePO4呈无定形态,Li3PO4与LiFePO4同属正交晶系,根据相变晶体学中的惯习现象[17],即保持晶型的相变更容易进行,故反应极有可能是由于FePO4中Fe3+与PO4四面体的结合较弱,Fe3+与OH-重新结合后被还原成Fe2+,同游离的 进入Li3PO4晶格生成LiFePO4。为证明三甘醇与Fe3+的反应产物,对反应前后的三甘醇进行红外图谱对比分析,结果见图6。
进入Li3PO4晶格生成LiFePO4。为证明三甘醇与Fe3+的反应产物,对反应前后的三甘醇进行红外图谱对比分析,结果见图6。
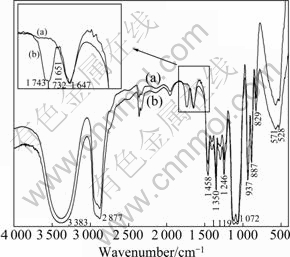
图6 三甘醇在反应前后的红外光谱
Fig. 6 FTIR spectra of TEG samples before (a) and after (b) reaction
对比图6中反应前后溶剂的两条红外光谱曲线可见,其大部分峰的位置与形状没有明显变化,只是红外透过率增大,即红外吸收率减小。反应后在1 743和1 732 cm-1处出现了一个新峰,生成羰基,有可能是羧酸羰基、醛羰基或酮羰基。故推测三甘醇液相还原Fe3+时首先被氧化生成醛羰基,醛羰基进一步被氧化为羧酸,羧酸在高温下与溶剂中过量未反应的三甘醇发生酯化反应生成环酯,且 在1 651 cm-1处反应后向低波数移动到1 647 cm-1处,可能是羧酸与羟基形成分子内氢键的缘故。总反应方程式为
在1 651 cm-1处反应后向低波数移动到1 647 cm-1处,可能是羧酸与羟基形成分子内氢键的缘故。总反应方程式为
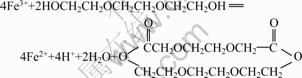 (7)
(7)
2.4 电化学性能测试与分析
图7所示为样品S1、S2、S3和S4在0.1C放电倍率下的首次充放电曲线。放电平台均在3.4 V左右,其放电比容量分别为142、148、152和158 mA・h/g。可以看出,随多元醇还原反应温度的升高,产物的电化学性能得以改善,这是由于升高温度有利于得到粒径更小、结晶更好的LiFePO4[13],使得材料在充放电过程中的极化减小。
图8(a)所示为三甘醇还原合成的纯相LiFePO4样品S3在不同倍率下的首次放电曲线。在0.1、0.5、 1、2、5和10C 下样品的放电比容量分别为148.8、134.0、129.3、119.3、102.8和84.1 mA・h/g,考虑到未进行碳包覆处理,纯相LiFePO4材料在2C以及更高放电倍率下平台保持较差,这是由于材料的电子电导率较低,在大电流放电下可逆容量较低。图8(b)所示为碳包覆后的LiFePO4/C材料在不同倍率下的首次放电性能, 在0.1、0.5、1和2C下材料的放电比容量分别为155.6、146.2、139.9和129.3 mA・h/g。与纯相LiFePO4相比,LiFePO4/C 材料具有更好的倍率性能,主要是柠檬酸和聚二乙醇在高温下分解形成的碳在颗粒表面或颗粒之间改善了LiFePO4的电子导电和倍率放电性能。

图7 样品S1、S2、S3和S4在0.1C倍率下的首次充放电曲线
Fig. 7 Initial charge-discharge curves of different samples at 0.1C
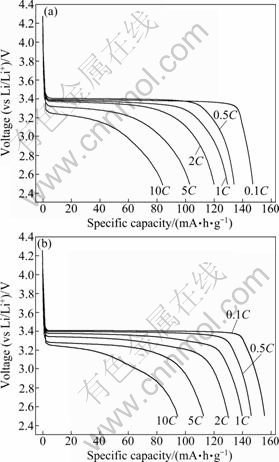
图8 S3和S4样品在不同倍率下的首次放电曲线
Fig. 8 Initial discharge curves of LiFePO4 samples S3 (a) and S4 (b) at different rates
图9所示为样品S3和S4在各放电倍率下的循环稳定性能对比。其中样品S3和S4在10C倍率下经10次循环后容量保保持率分别为97.3%和98.1%。图9说明材料均具有良好的循环稳定性,这得益于样品结晶良好、无杂相、颗粒细小。结晶度好保证了材料在充放电过程中的结构稳定性;样品颗粒细小缩短了Li+扩散路径,相应地提高了Li+的扩散速率;柠檬酸与PEG裂解的碳提高了材料的电子导电率,这些都使得合成的LiFePO4/C材料具有良好的电化学性能。
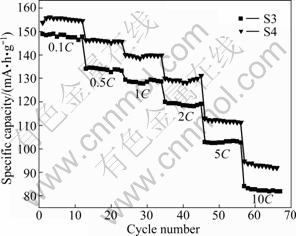
图9 不同放电倍率样品S3和S4的循环性能比较
Fig. 9 Comparison of cycle performance of LiFePO4 samples S3 and S4 at different rates
图10(a)所示为各样品在首次半嵌锂态时的交流阻抗谱。曲线由高频区的一个半圆和低频区的一条与实轴约成45°夹角的直线组成。前者直径代表因电极反应而导致的电荷转移阻抗,后者代表锂离子扩散所引起的Warburg阻抗。测试结果表明:在高频区,S1、S2和S3的电荷转移阻抗逐渐减小,这有利于克服材料在充放电过程中的动力学限制,说明随着多元醇沸点的升高,材料的导电性能逐渐得到改善,电极上由电荷传导引起的电化学反应阻抗不断减小;在低频区,S3直线斜率略大于S1和S2的,表明S3由扩散引起的浓差极化小于S1和S2的,这可能是样品S3的晶粒尺寸偏小,使锂离子的扩散路径减小,扩散系数相应增大,从而降低了扩散引起的浓差极化所致。图 10(b)所示为各样品低频处Z″与ω-1/2(ω为角频率)的关系图。由图10(b)可见,Z″与ω-1/2之间呈良好线性关系,由斜率可拟合出Warburg阻抗系数σ。根据以下公式[18]:
 (8)
(8)
式中:σ为Warburg阻抗系数;n为锂离子转移数;F为法拉第常数;A为电极的反应面积;R为摩尔气体常数;T为热力学温度;C为嵌锂浓度;D为锂离子的扩散系数。由式(8)可看出:斜率越小,样品LiFePO4/C的扩散系数越大。可见,更高沸点的多元醇确实可以提高锂离子的扩散速率,此结果与图10(a)所得结论一致。
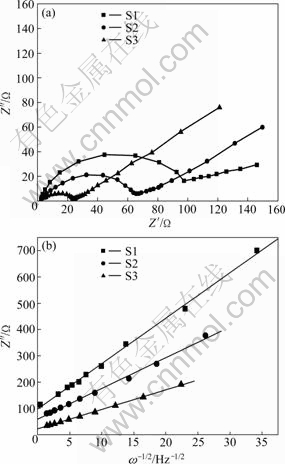
图10 样品S1、S2和S3的交流阻抗谱及低频处Z″与ω-1/2的关系
Fig. 10 AC impedance (a) and relationship between Z″ and ω-1/2 at low frequencies (b) of samples S1, S2 and S3
3 结论
1) 以廉价的钛白工业副产物七水硫酸亚铁为铁源,用液相沉淀法制得颗粒细小的无定形FePO4・xH2O前躯体,利用多元醇还原法可制得结晶良好、粒径细小且分布均匀的纯相LiFePO4正极材料。
2) 随着多元醇沸点的升高,所得材料粒径减小,放电比容量明显增大。在三甘醇沸点温度(290 ℃)下制得的纯相LiFePO4在0.1、0.5、1、2、5和10C下放电比容量分别为148.8、134.0、129.3、119.3、 102.8和84.1 mA・h/g;经650 ℃煅烧1 h后碳包覆LiFePO4/C材料的放电比容量分别为153.6、146.2、139.9、129.3、112.2和94.9 mA・h/g;纯相和碳包覆样品在10C倍率下循环10次后,容量保持率分别为97.3%和98.1%,说明由高沸点多元醇制得的材料具有较好的倍率和循环稳定性能。
3) 液相沉淀结合多元醇还原的工艺流程节约能源,设备投资少,多元醇可以回收重新利用,使生产成本有所降低,有利于工业化生产。
REFERENCES
[1] GOODENOUGH J B, PADHIA K, NANJUNDAWAMY K S. Phospho-olivines as positive-electrode materials for rechargeable lithium batteries [J]. J Electrochern Soc, 1997, 144(4): 1188- 1191.
[2] LU Jun-biao, TANG Zi-long. Influence of Mg ion doping on the battery properties of LiFePO4/C [J]. Acta Physico-Chimica Sinica, 2005, 21(3): 319-323.
[3] RAVET N, CHOUINARD Y, MAGNAN J F. Electroacitivity of natural and synthetic triphylite [J]. J Power Sources, 2001, 97/98: 503-507.
[4] LIU Xiao-hong, WANG Jin-qing, ZHANG Jun-yan, YANG Sheng-rong. Fabrication and characterization of LiFePO4 nanotubes by a sol-gel-AAO template process [J]. Chinese J Chemical Physics, 2006, 19(6): 530-534.
[5] KIM J K, CHOI J W, CHAUHAN C S. Enhancement of electrochemical performance of lithium iron phosphate by controlled sol-gel synthesis [J]. Electrochimica Acta, 2008, 53: 8258-8264.
[6] YANG Shu-ting, ZHAO Na-hong, YIN Yan-hong, DONG Hong-yu, YUE Hong-yun, YANG Jin-xin. Synthesis of LiFePO4/C nano-structure intergrowth by PAM soft templating method [J]. Battery Bimonthly, 2005, 35(4): 263-265.
[7] JIN En-mei, BO Jin, JUN D K, PARK K H, GU H B, KIM K W. A study on the electrochemical characteristics of LiFePO4 cathode for lithium polymer batteries by hydrothermal method [J]. J Power Sources, 2008, 178: 8801- 8806.
[8] 李启厚, 毕丹丹, 刘志宏, 刘志勇, 何 峰. 多元醇法制备超微粉体材料的特点及应用[J]. 粉末冶金材料科学与工程, 2008, 13(2): 79-83.
LI Qi-hou, BI Dan-dan, LIU Zhi-hong, LIU Zhi-yong, HE Feng. Characteristics and application of polyol method preparing ultrafine particles [J]. Chin Mater Sci Eng Powder Metal, 2008, 13(2): 79-83.
[9] CAO Yan-bing, HU Guo-rong, DU Ke, PENG Zhong-dong, TANG Chun, ZHANG Luo-hu. Synthesis of LiFePO4 cathode materials by polyol reduction processing [J]. Chinese Journal of Inorganic Materials, 2010, 26(6): 1061-1065.
[10] CHOI E S, KIM D H, WOO C H, CHOI C H, KIM J. Synthesis and electrochemical properties of LiFePO4/carbon nano- composites in polyol medium [J]. Journal of Nanoscience and Nanotechnology, 2010, 10: 3416-3419.
[11] 董丙坤, 董菊芬, 苗富贵. 铁矿石中全铁的分析方法[J]. 河北化工, 2008, 31(1): 72-74.
DONG Bing-kun, DONG Ju-fen, MIAO Fu-gui. Improvement of iron analysis methods of full iron [J]. Hebei Chemical Engineering and Industry, 2008, 31(1): 72-74.
[12] 张允湘, 冯余倩, 应建康, 曾祥森. 料浆法制磷铵的生产与操作[M]. 成都: 成都科技大学出版社, 1999: 159-161.
ZHANG Yun-xiang, FENG Yu-qian, YING Jian-kang, ZENG Xiang-sen. Production and operations of the slurry process on phosphate [M]. Chengdu: Chengdu University of Science and Technology Press, 1999: 159-161.
[13] 吴瑾光. 近代傅里叶变换红外光谱技术及应用(下卷)[M]. 北京: 科学技术文献出版社, 1994: 270-272, 297-299.
WU Jing-guang. Technology and applications of modern Fourier transform infrared spectroscopy technology (Ⅱ) [M]. Beijing: Science and Technology Literature Publishing House, 1994: 270-272, 297-299.
[14] 钱逸泰. 结晶化学导论[M]. 合肥: 中国科学技术大学出版社, 2002: 89-93.
QIAN Yi-tai. Introduction of crystal chemistry [M]. Hefei: Press of University of Science and Technology of China, 2002: 89-93.
[15] 柴诚敬, 张国亮. 化工流体流动与传热[M]. 北京: 化学工业出版社, 2000: 492-502.
CHAI Cheng-jing, ZHANG Guo-liang. Chemical fluid flow and heat transmission [M]. Beijing: Chemical Industry Press, 2000: 492-502.
[16] 陶丽丽, 徐云龙, 黄花庆. PEG对LiFePO4/C结构与性能的影响[J]. 电源技术, 2009, 33(4): 284-290.
TAO Li-li, XU Yun-long, HUANG Hua-qing. Effect of PEG on structure and performance of LiFePO4/C [J]. Chinese Journal of Power Sources, 2009, 33(4): 284-290.
[17] 邓永瑞, 许 洋, 赵 青. 固态相变[M]. 北京: 冶金工业出版社, 1994: 52-60.
DENG Yong-rui, XU Yang, ZHAO Qing. Solid-state phase transition [M]. Beijing: Metallurgical Industry Press, 1996: 52-60.
[18] 吴 彬. 锂离子电池正极材料LiFePO4的制备与改性研究[D]. 合肥: 合肥工业大学, 2008: 14-15.
WU Bing. Preparation and performance modification research of LiFePO4 for cathode material of lithium-ion battery [D]. Hefei: Hefei University of Technology, 2008: 14-15.
(编辑 陈卫萍)
基金项目:国家“十一五”科技支撑计划资助项目(2007BAE58B07)
收稿日期:2011-03-11;修订日期:2011-07-10
通信作者:刘 恒,教授,博士;电话:028-85410272;E-mail: h_liu@scu.edu.cn