文章编号:1004-0609(2009)09-1700-06
钒冶金废水微生物异化还原过程
李浩然1,冯雅丽2,邹晓阎2,罗小兵2
(1. 中国科学院 过程工程研究所 生化工程国家重点实验室,北京 100080;
2. 北京科技大学 土木与环境工程学院,北京 100083)
摘 要:以微生物燃料电池为研究工具,研究Rhodoferax ferrireducens(R.f )异化还原钒(Ⅴ)的过程。在对R.f进行NaVO3耐性驯化实验的基础上,考查NaVO3废水浓度、pH值和温度对R.f还原钒(Ⅴ)的影响。结果表明:适量钒元素对微生物生长具有促进作用,微生物的生长趋势及周期与钒(Ⅴ)的还原趋势及周期基本相同;初期由于钒化合物的生物效应促进葡萄糖消耗量增加,葡萄糖氧化分解过程产生小分子有机酸,使溶液pH降低,但钒(Ⅴ)还原过程需要H+的参与,且R.f异化作用也消耗部分小分子有机酸,后期溶液pH升高。经优化其培养条件为:温度30 ℃、搅拌速度150 r/min、pH为7.5时,在NaVO3含量为300 mg/L的钒废水中,R.f对钒(Ⅴ)的还原率为76%,细菌总数达到1.1×109 cfu/mL。
关键词:钒冶金废水;Rhodoferax ferrireducens;微生物燃料电池;异化还原
中图分类号:X 703;TM 911.4 文献标识码:A
Dissimilatory reduction process of vanadium(V) in metallurgical wastewater by Rhodoferax ferrireducens
LI Hao-ran1, FENG Ya-li2, ZOU Xiao-yan2, LUO Xiao-bing2
(1. State Key Laboratory of Biochemical Engineering, Institute of Process Engineering,
Chinese Academy of Sciences, Beijing 100080, China;
2. School of Civil and Environmental Engineering, University of Science and Technology Beijing,
Beijing 100083, China)
Abstract: The process of Rhodoferax ferrireducens (R.f ) dissimilatory reduction of V5+ in waste water was studied by the means of microbial fuel cell (MFC). Based on the inoculation test of tolerance to NaVO3 of R.f, the effects of NaVO3 concentration in the wastewater, pH and temperature on R.f reducing V5+ were investigated. The results show that adequate vanadium can promote the growth of microbes, and the tendency and cycle of R.f growth are essentially the same as that of V5+ reducing. In beginning period, the bioeffect of vanadium compound increases the consumption of glucose, and the glucose is oxidized to the small molecule organic acids, which leads to pH value fall. But H+ should be engaged in V5+ reduction, and the dissimilatory reduction of R.f will also consume some small molecule organic acids, which makes pH increase later. The optimized culture conditions are as follows: temperature 30 ℃, stirring speed 150 r/min, pH 7.5, NaVO3 concentration in the vanadium wastewater 300 mg/L. The reduction rate of V5+ by R.f is 76%, and the total R.f count reaches 1.1×109 cfu/mL.
Key words: vanadium metallurgical waste water; Rhodoferax ferrireducens; microbial fuel cell; dissimilatory reduction
钒是一种重要的合金元素,以其强度高、韧性大、耐磨性好等优点,广泛用于机械、汽车、造船、铁路、桥梁等行业。无论采用哪种方法提取钒,废水和废渣中都会含有一定浓度的高价钒[1-3]。目前,含钒废水的处理主要采用铁屑(或硫酸亚铁)沉淀法和SO2沉淀法。处理含钒废水包括还原和中和两个化学反应过程,德国鲁奇公司、意大利艾姆科公司以及四川川投峨眉铁合金厂都采用类似方法处理含钒废水,但此种废水处理方法易产生腐蚀钝化现象,影响净水效果的稳定性。研究者们[4]提出了一些改进措施,但没有从根本上消除其不利因素。SO2沉淀法主要是利用SO2的还原性将V5+还原成V4+。德国纽伦堡电冶金公司以及中国锦州铁合金厂都曾采用此种方法处理沉钒废水,但还原剂SO2的来源问题严重限制了此方法的实际应用范围[5]。采用上述方法的成本高而且可能会造成二次污染[6-7]。
近年来,生物法处理重金属废水越来越受到国内外学者的重视。CARPENTIER等[8]利用沙雷菌在厌氧条件下与乳酸盐、甲酸盐和丙酮酸盐共同作用,将V5+还原成V4+。但引入试剂过多,给金属提取带来不便。官纯[9]利用复合功能菌对钒冶金废水进行常规的生物吸附处理,但存在金属不易回收,易出现二次污染的问题。
本文作者探索了一种基于微生物燃料电池处理钒冶金废水的方法,利用异化金属还原菌还原高价钒过程中产生的电子进行发电,在处理高价钒金属污染、回收金属的同时获得能源。该方法将钒冶金废水的治理、钒金属的回收及能源回收有机结合。
1 实验
微生物:异化还原菌Rhodoferax ferrireducens (R.f)来自德国菌种保藏中心,R.f为厌氧菌,以氧化分解葡萄糖等有机物的形式获得生长能量。以R.f为模式微生物构建微生物燃料电池,其装置结构如图1所示[10-11]。
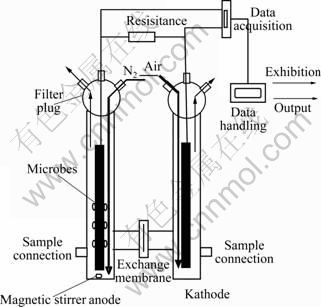
图1 双室微生物燃料电池装置示意图
Fig.1 Schematic diagram of double-room microbial fuel cell
数据采集:微生物燃料电池的电压通过数据采集卡直接测得。数据采集设备为A/D板 8201H(瑞博华),16位,32通道,采集精度0.05 mV,电流及输出电能通过连接的已知电阻计算得出。
检测方法:溶液中微生物的菌落总数采用ATP生物发光快速检测法[12-14];钒(Ⅳ)化合物浓度采用苯胺蓝紫外分光光度法;钒(Ⅴ)化合物浓度采用二苯胺磺酸钠分光光度法;葡萄糖浓度采用DNS法。
2 异化还原菌R.f对NaVO3耐性的 驯化
铵盐沉钒废水中钒(Ⅴ)化合物主要以NaVO3分子形式存在,含量在200~400 mg/L之间, pH值为7~8。国家规定的废水排放标准中全钒浓度小于2 mg/L,微量钒元素是微生物生长所必须的,对微生物生长具有促进作用,但NaVO3在一定浓度时对微生物有毒性作用,抑制其生长。为了提高微生物在较高NaVO3含量废液中的成活能力,需要对微生物进行驯化培养。
按照微生物驯化的要求,分别配制含NaVO3 50、100、150、200、250、300、350和400 mg/L的废水培养液,并将培养液pH值调到8左右,在厌氧箱中进行所有转接等必要操作,整个过程严格厌氧培养。异化还原菌R.f驯化过程如表1所列。
表1 异化还原菌R.f对NaVO3耐性驯化过程
Table 1 Process of domesticating duration of R.f for NaVO3
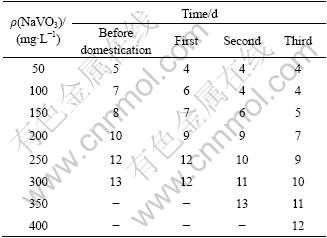
R.f经过在不同浓度NaVO3培养液多次转接驯化培养后,4~6 d时细菌进入对数生长期,可在含有较高NaVO3浓度的培养液中生长。在浓度不同的培养液中都可以发现,在刚接菌时,溶液皆呈微黄色,随后溶液颜色呈现蓝色,随着NaVO3浓度的提高,蓝色越来越深。溶液的颜色不同说明还原生成钒(Ⅳ)的量不同。
3 结果与讨论
3.1 NaVO3浓度对还原率的影响
试验条件:温度30 ℃,电池阳极搅拌速度150 r/min,接菌量15%,溶液pH 7.5,NaVO3浓度分别为200(接菌和不接菌)、250、300和350 mg/L,每天测阳极液中钒(Ⅳ)的浓度,分别考查菌种及NaVO3浓度对还原率的影响。
由图2可知,不接菌时,钒(Ⅴ)浓度没有变化。当NaVO3的浓度小于300 mg/L时,钒(Ⅴ)的还原率逐渐增大,300 mg/L时还原率最高达72%。大于300 mg/L时,还原率开始降低。实验结果表明,微生物的生长和钒的还原率之间有一定的联系,微生物的生长与溶液中钒化合物浓度有关。

图2 R..f菌及NaVO3的浓度对还原率的影响
Fig.2 Effect of R.f and concentration of NaVO3 on reduction rate of V5+
钒是微生物生长所必须的元素,钒酸根离子与铁离子作用相似,是微生物体内一些酶的辅酶,可提高微生物体内酶的活性,加快葡萄糖在微生物体内的运转、代谢。但随着NaVO3浓度的加大,钒(Ⅴ)的毒性增加,对微生物生长具有抑制作用,细菌总数逐渐减小,且NaVO3的还原率也开始下降。这说明适量NaVO3对微生物的生长起促进作用,过量则抑制微生物的生长,其原因可能是适量的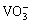 在细胞中能增加葡萄糖的转运和氧化而促进微生物的生长,但
在细胞中能增加葡萄糖的转运和氧化而促进微生物的生长,但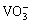 浓度过大时,钒又可能对微生物细胞的分裂起阻断作用。
浓度过大时,钒又可能对微生物细胞的分裂起阻断作用。
3.2 温度对钒(Ⅴ)还原率的影响
试验条件:pH 7.5,搅拌速度150 r/min,接菌量15%,NaVO3浓度300 mg/L,考察温度分别为25、30和33 ℃时,R.f对钒(Ⅴ)的还原率。
由图3所示,培养温度为30 ℃时,R.f培养到第6 d时还原率可达73.4%,而25 ℃时,钒(Ⅴ)的还原率为70.5%。当R.f在33 ℃培养时,第5 d钒(Ⅴ)的还原率达到69%,但之后钒(Ⅴ)的还原率有所下降。随着培养温度的升高,微生物生长的迟滞期缩短,生长加速,厌氧时分解有机物的速度也加快,可以在较短时间内到达R.f生长的平稳期。但在较高温度下,微生物细胞内的酶容易失活,R.f衰老速度也加快,对钒(Ⅴ)的还原周期也相应缩短,钒(Ⅴ)总的还原率较低。因此,30 ℃为R.f还原钒(Ⅴ)的最适温度。
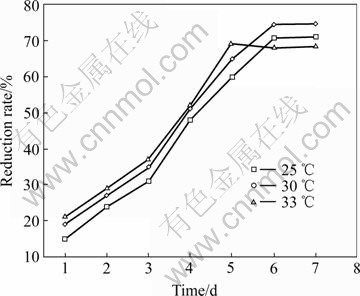
图3 不同温度对钒(Ⅴ)还原率的影响
Fig.3 Effect of different temperatures on reduction rate of V5+
3.3 pH对钒(Ⅴ)还原率的影响
试验条件:温度30 ℃、搅拌速度150 r/min,接菌量15%,NaVO3浓度300 mg/L,在微生物燃料电池中考察pH恒定为7、7.3、7.5、7.8和8时,pH对R.f还原钒(Ⅴ)过程的影响。
由图4可知,pH值对R.f还原钒(Ⅴ)有较大影响,当pH恒定为7和8时,钒(Ⅴ)的还原率较低,为60.2%和62.1%,而pH恒定为7.5时,钒(Ⅴ)的还原率最高,达到75.8%。

图4 pH对钒(Ⅴ)还原率的影响
Fig.4 Effect of pH on reduction rate of V5+
R.f分解葡萄糖过程中有小分子有机酸生成,导致溶液pH下降0.5~0.8。当生存环境pH变化时,细胞膜所带电荷状态发生变化,改变细胞膜的通透性,影响微生物的跨膜pH梯度,对微生物的生长及代谢产物的分泌都有影响。同时,pH变化也影响细胞内酶的活性,阻碍菌体的新陈代谢。试验中可通过调节NaVO3 溶液的pH,使微生物在几乎恒定pH环境中生长,以保证微生物的活性[15]。
3.4 微生物异化还原钒(Ⅴ)的过程分析
该试验的试验条件与3.1节的相同。接菌后分别在24、48、72、96、120、144和168 h测定钒(Ⅴ)的还原率和培养液中生物量、葡萄糖消耗和pH变化,由此来分析微生物生长过程中钒(Ⅴ)的还原过程。
微生物生长过程中,钒(Ⅴ)的还原率呈曲线上升,如图2所示。R.f经过2 d左右的生长迟滞期,进入对数期和稳定期,生长迅速,此时钒(Ⅴ)还原率也迅速增加,而在未接菌的NaVO3废液中,钒(Ⅴ)浓度没有变化。NaVO3浓度为300 mg/L时,钒(Ⅴ)的还原率最高,第6 d时达到了72.35%;NaVO3浓度为200 mg/L时,第6 d时还原率为68.72%;NaVO3浓度为350 mg/L时,第6 d时还原率为62.47%。由于本试验的试验条件与3.1节的相同,唯一不同的是NaVO3浓度,说明钒(Ⅴ)的还原是在微生物生长过程中完成的,随着微生物生长代谢的进行,钒(Ⅴ)还原率也相应变化。图5中微生物的生长曲线也可以证实这一点。由图5可知,微生物的生长曲线均呈上升趋势,在第6 d时,不加NaVO3废液的溶液中,细菌总数(N)为2.3×107 cfu/mL;当NaVO3浓度为200 mg/L时,细菌总数最大,达到8.5×108 cfu/mL,而NaVO3浓度为250和300 mg/L时,细菌总数分别为7.2×108和7.9×108 cfu/mL,再一次证明适量浓度的NaVO3对微生物生长是有利的。对比图2与图5可知,接菌第6 d后,钒(Ⅴ)的还原率变化逐渐平缓,生物量增长也在第6 d后趋于平缓,由此说明R.f的生长周期为6~7 d,钒(Ⅴ)的还原周期也在6 d左右。当NaVO3浓度为200 mg/L时R.f总数最大,但是R.f对钒(Ⅴ)的还原率比NaVO3浓度为300 mg/L时低。原因可能是R.f在NaVO3含量为200 mg/L时以同化作用为主,而在NaVO3含量为300 mg/L时以异化作用为主,同化作用氧化分解葡萄糖产生的能量没有异化作用氧化分解体内有机物产生的能量多,钒(Ⅴ)化合物在微生物处于异化作用时更容易获得电子,加速钒(Ⅴ)的还原速度。

图5 NaVO3浓度对R.f细菌总数的影响
Fig.5 Effect of concentration of NaVO3 on total number(N) of R.f
微生物生长代谢过程中需要消耗一定量的葡萄糖,因此培养液中葡萄糖浓度的变化可以间接反映出微生物生长代谢状况[16]。培养液中葡萄糖在培养周期内的浓度变化如图6所示。接菌15%的培养液中,R.f经过1~2 d的迟滞期后,迅速进入生长对数期,与之相应的葡萄糖消耗也迅速上升,而未加NaVO3溶液的葡萄糖浓度变化缓慢。这说明钒化合物促进了微生物的生长,导致葡萄糖消耗速度加快,R.f在代谢葡萄糖等有机物过程中还原钒(Ⅴ),培养到第6 d时,葡萄糖几乎完全消耗,细菌总数在1~6 d内逐渐增大,7 d后变化趋于平缓。
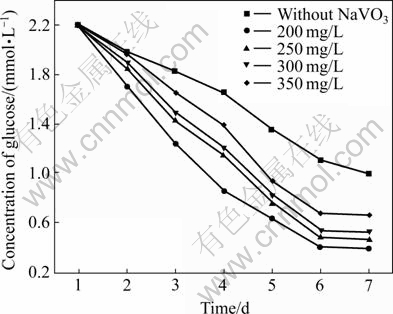
图6 NaVO3浓度对葡萄糖消耗速率的影响
Fig.6 Effect of concentration of NaVO3 on consumption rate of glucose
由于葡萄糖代谢过程中会产生酸性物质(乙酸和丁酸等),导致培养液的pH下降。随着葡萄糖的消耗,培养液的pH的变化曲线如图7所示。在R.f培养第 3 d后,含有300 mg/L NaVO3废水的pH最低(6.59),随着培养时间的增加,pH逐步上升,说明代谢可能是分步进行的。代谢开始时,代谢物主要是葡萄糖,生成小分子有机酸等有机物,导致pH下降,随着代谢进程的推进,葡萄糖浓度减小,小分子有机酸成主要代谢物,pH又开始升高,在代谢小分子有机酸的同时还原NaVO3中的钒(Ⅴ),导致培养液中pH的升高。其反应方程式如下。

图7 NaVO3浓度对还原过程中pH的影响
Fig.7 Effect of concentration of NaVO3 on pH in reduction process
阳极:

阴极:

阳极室中不加NaVO3时,其阳、阴极反应为式(1)和(3)。即在厌氧条件下,阳极室中的有机底物在微生物催化下分解为碳氧化合物(如CO2),同时释放电子和质子。电子通过外电路传递到阴极,质子通过质子交换膜传递到阴极。电子和质子与阴极室中的电子受体(如O2)反应生成水。
阳极室中加入NaVO3时,反应方程如式(1)~(3)所示。已有研究表明[17-18]:电能的输出很大程度上受到阴极微弱的氧气还原反应的影响,且氧气易通过质子交换膜扩散至阳极。阳极室内微生物催化分解有机物产生的质子和电子被高价钒的还原过程所利用,缓解了质子交换膜传递质子的压力,加速电子的转移,同时适量的钒也加速了微生物的生长代谢,加速了有机物分解和钒还原的进程。
4 结论
1) R.f在还原钒(Ⅴ)过程中受温度、搅拌速度、pH等影响,经优化后,其培养条件为:温度30 ℃、搅拌速度150 r/min、pH 7.5,钒废水中NaVO3含量300 mg/L,R.f对钒(Ⅴ)的还原率为76%,细菌总数达到1.1×109 cfu/mL。
2) 不加微生物时,单纯的钒(Ⅴ)化合物对电池产电没有影响。适量钒元素对微生物生长具有促进作用,微生物的生长趋势及周期与钒(Ⅴ)的还原趋势及周期基本相同,在含有200 mg/L NaVO3的培养液中细菌总数最高可达到8.5×108 cfu/mL,而不含NaVO3的培养液中细菌总数最高为2.3×107 cfu/mL。
3) 异化金属还原菌R.f还原钒(Ⅴ)过程中,溶液pH经历先降后升的过程,但在微生物完成生长周期后溶液pH下降0.5~0.8。由于钒化合物生物效应促进葡萄糖消耗量增加,葡萄糖氧化分解过程产生小分子有机酸,使溶液pH降低,但钒(Ⅴ)还原过程需要H+的参与,且R.f异化作用也消耗部分小分子有机酸,使溶液pH升高。
REFERENCES
[1] WECKHUYSEN B M, DAPHNE E K. Chemistry, spectroscopy and the role of supported vanadium oxides in heterogeneous catalysis[J]. Catalysis Today, 2003, 78: 25-46.
[2] BISWAJIT M, BALARAM P, SUSHMITA M, PRATIK B, AMIT T, MALAY C. Vanadium―An element of atypical biological significance[J]. Toxicology Letters, 2004, 150: 135-143.
[3] LI Hao-ran, FENG Ya-li, LIANG Jiang-long, DU Zhu-wei. Vanadium recovery from clay vanadium mineral using an acid leaching[J]. Rare Metals, 2008, 27(2): 116-120.
[4] 胡明松, COETZEE P P, FISCHER J L. 色谱分离和原子发射光谱检测工业废水中的四价和五价钒[J]. 化学通报, 2004, 4: 147-148.
HU Ming-song, COETZEE P P, FISCHER J L. Chromatographic separation and ICP-OES determination of V(Ⅳ) and V(Ⅴ) in industrial fluid[J]. Chemistry, 2004, 4: 147-148.
[5] 张清明, 艾南山, 徐 帅, 吴洪英. 含钒废水的处理现状及发展趋势[J]. 科技情报开发与经济, 2007, 17(2): 142-144.
ZHANG Qing-ming, AI Nan-shan, XU Shuai, WU Hong-ying. the present situation and developing trends of the treatment of vanadium containing wastewater[J]. Sci-Tech Information Development & Economy, 2007, 17(2): 142-144.
[6] REU1B A, SCAN S, JEAN-PIERRE. Effects of vanadium complexes with organic ligands on glucose metabolism: A comparison study in diabetic rats[J]. Br J Pharmacol, 1999, 126: 467-470.
[7] SAFAVI M R, HORMOZI N, SHAMS E. Highly selective and sensitive kinetic spectrophotometric determination of vanadium(Ⅳ) in the presence of vanadium(Ⅴ)[J]. Analytical Chimica Acta, 2000, 409: 283-289.
[8] CARPENTIER W, SANDRA K, de SMET I, BRIGE A, de SMET L, Van BEEUMEN J. Microbial reduction and precipitation of vanadium by shewanella oneidensis[J]. Applied and Environmental Microbiology, 2003, 69(6): 3636-3639.
[9] 官 纯. 微生物法处理含钒废水中钒铬的应用研究[J]. 四川冶金, 2006(5): 22-46.
GUAN Chun. The experimental research for treatment of V(5+), Cr(6+) in containing-vanadium wastewater by microbiological method[J]. Sichuan Metallurgy, 2006(5): 22-46.
[10] 连 静, 冯雅丽, 李浩然, 刘志丹, 周 良. 直接微生物燃料电池的构建及初步研究[J]. 过程工程学报, 2006, 6(3): 408-412.
LIAN Jing, FENG Ya-li, LI Hao-ran, LIU Zhi-dan, ZHOU Liang. Construction and preliminary studies on the direct microbial fuel cell[J]. The Chinese Journal of Process Engineering, 2006, 6(3): 408-412.
[11] 冯雅丽, 周 良, 祝学远, 连 静, 李少华. Geobacter metalli reducens 异化还原铁氧化物三种方式[J]. 北京科技大学学报, 2006, 28(6): 524-529.
FENG Ya-li, ZHOU Liang, ZHU Xue-yuan, LIANG Jing, LI Shao-hua. Three paths to reduce ferric oxides taken by geobacter metallireducens[J]. Journal of University of Science and Technology Beijing, 2006, 28(6): 524-529.
[12] SUZUKI S, KARUBE I, MATSUNAGA T. Harnessing microbially generated power on the seafloor[J]. Biotechnol Bioeng Symp, 1978, 8: 501-511.
[13] WINGARD L B, SHAW C H, CASTNER J F. Lack of production of electron-shuttling compounds or solubilization of Fe(Ⅲ) during reduction of insoluble Fe(Ⅲ) oxide by geobacter metallireducens[J]. Enzyme Microb Technol, 1982: 137-142.
[14] BOND D R, LOVLEY D R. Electricity production by geobacter sulfuerreducens attached to electrodes[J]. Appl Environ Microbiol, 2003, 69(3): 1548-1555.
[15] 李浩然, 冯雅丽, 周 良, 祝学远, 杜竹玮. 微生物异化还原金属氧化物的机理及应用[J]. 中国矿业大学学报, 2007, 36(5): 680-683.
LI Hao-ran, FENG Ya-li, ZHOU Liang, ZHU Xue-yuan, DU Zhu-wei. Mechanism and application of microbial dissimilatory reduction metal oxide[J]. Journal of China University of Mining & Technology, 2007, 36(5): 680-683.
[16] 冯雅丽, 李浩然, 祝学远. 单室直接微生物燃料电池性能影响因素分析[J]. 北京科技大学学报, 2007, 29(S2): 162-165.
FENG Ya-li, LI Hao-ran, ZHU Xue-yuan. Analysis of influencing factors on the performance of single chamber direct microbial fuel cell[J]. Journal of University of Science and Technology Beijing, 2007, 29(S2): 162-165.
[17] LIU Zhi-dan, LI Hao-ran. Effects of bio- and abio-factors on electricity production in a mediatorless microbial fuel cell[J]. Biochemical Engineering Journal, Biochemical Engineering Journal, 2007, 36(3): 209-214.
[18] 连 静, 冯雅丽, 李浩然, 杜竹玮. 微生物燃料电池的研究进展[J]. 过程工程学报, 2006, 6(2): 334-338.
LIAN Jing, FENG Ya-li, LI Hao-ran, DU Zhu-wei. Progress in research on microbial fuel cells[J]. The Chinese Journal of Process Engineering, 2006, 6(2): 334-338.
基金项目:国家自然科学基金资助项目(20876160);国家高技术研究发展计划资助项目(2007AA05Z158);“十一五” 国家科技支撑计划资助项目(2006BAB02A11)
收稿日期:2008-09-03;修订日期:2009-06-17
通信作者:冯雅丽,教授,博士;电话:010-62332467;E-mail: ylfeng126@126.com
(编辑 李向群)