三维电极电化学反应器降解有机废水中的EDTA
柴立元,尤翔宇,舒余德,杨杰,王云燕,赵娜
(中南大学 冶金科学与工程学院,湖南 长沙,410083)
摘 要:研究一种基于三维电极电化学反应器处理有机废水的新方法。研究结果表明:采用活化后的活性炭作为粒子电极,通过产生?OH自由基有效降解废水中的EDTA,其去除率受进水pH、电流和电导率等影响较大;在?OH自由基的作用下,EDTA首先被降解成伯胺等中间产物,进而又被矿化为CO2,H2O和NH3。在进水pH为6.0,进水流量为200 mL/min,水温为25 ℃,电导率为0.15 S/m,电流为200 mA时,电解1 h,总有机碳(TOC)的去除率可以达到96.40%;经50次循环实验,TOC去除率仍可保持在90%以上。
关键词:三维电极;电催化氧化;有机废水;羟基自由基;乙二胺四乙酸二钠
中图分类号:X703.1,O646.5 文献标志码:A 文章编号:1672-7207(2010)04-1240-06
Electrochemical degradation of organic wastewater containing EDTA with three-dimensional electrode reactor
CHAI Li-yuan, YOU Xiang-yu, SHU Yu-de, YANG Jie, WANG Yun-yan, ZHAO Na
(School of Metallurgical Science and Engineering, Central South University, Changsha 410083, China)
Abstract: The electrochemical degradation of organic wastewater containing EDTA was investigated using a novel three-dimensional electrode reactor. The results show that using activated carbon as particle electrode, EDTA in organic wastewater can be efficiently removed by ?OH radicals produced in the reactor, while its removal efficiency is significantly dependent on current, electric conductivity and pH of the wastewater. EDTA is firstly degraded into primary amine during the action of ?OH radicals, then mineralized into CO2, H2O and NH3. The removal efficiency of total organic carbon (TOC) is 96.40% at 200 mA, 0.15 S/m of electric conductivity, 1 h of electrolysis time, 25 ℃, 200 mL/min of influent flow rate, pH 6.0. The removal efficiency of TOC maintains 90% when it is circulated times is 50.
Key words: three-dimensional electrode; electro-catalytic oxidation; organic wastewater; ?OH radical; EDTA-2Na
毒性大、浓度高且难以生化降解的有机废水已成为当前国内外水处理研究的热点。近年来,深度氧化技术(Advanced oxidation processes)作为治理此类有机污染物的一条重要途径,受到了人们的广泛关注。该技术主要是通过氧化性极强的?OH自由基与有机物之间的加合、取代和电子转移等使污染物矿化[1]。目前,产生?OH自由基的主要方法有化学氧化法[2]、电化学法、光氧化法[3]及超声法等,其中以电化学产生?OH自由基的方法最受青睐。因该法废水深度氧化工艺比较容易控制,易建立密闭性循环和无二次污染[4]等优点,可望发展成为一项体现“绿色”特征的高效处理有机废水的新技术[5]。目前,相关研究多限于二维平板电极,这种传统的平板电极由于面体比小,传质问题未能根本解决,电流效率低,能耗高,故未能在实际中得到普遍应用。而三维电极具有很大的比表面,粒子间距离小,体反应速度高,时空转换效率高,传质效果好,能以较低的电流密度提供较大的电流。以此设计的电化学反应器在有机合成[6-7]、重金属废水处理[8-9]及有机废水处理[10-12]等领域的应用逐渐成为研究热点。但是,由于粒子电极催化活性低,有机物降解效率低,限制了其在工业中的应用。另一方面,目前主要采用先化学氧化再生化[13]处理EDTA有机废水的方法,存在工艺复杂、实用性差等缺点。在此,本文作者从新型三维电极反应器入手,采用石墨电极作为反应器的阳极和阴极,阴极与阳极之间填充活性炭粒子电极,通过分析改性后炭粒子电极电解反应前后的变化特征及降解有机废水的电化学机理,得到提高粒子电极催化活性的方法,组成高效的三维电极反应器,并考察含EDTA的有机废水处理的工艺影响因 素,旨在为难降解EDTA有机废水的处理提供一种新途径。
1 实验
1.1 实验装置
实验装置是一个带隔膜的三维电极电化学反应器,如图1所示。它主要由2个平板电极(阳极和阴极)、粒子电极和槽体组成。起馈电极作用的2个平板电极均为高纯石墨,极板面积为5 cm×10 cm,粒子电极为活性炭颗粒(粒径为830~2 360 μm),它们作为工作电极被填充在阳极和隔膜间形成三维电极,粒子电极有效填充体积为5 cm×5 cm×10 cm。槽体由PVC材料黏结而成,隔膜板为1块打满1 mm微孔的PVC板,隔膜板距阴极0.5 cm,距阳极5 cm。外加电源采用DF1797B-8003型程控开关电源以直流方式供电,输出电压0~80 V,输出电流0~2.5 A。
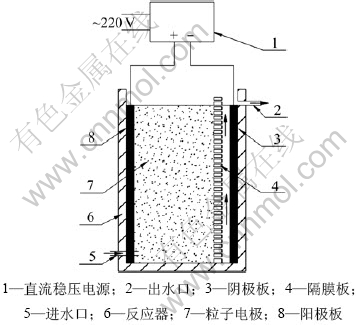
图1 三维电极反应器结构示意图
Fig.1 Schematic diagram of a three-dimensional electrode reactor
1.2 模拟废水的配制及分析
称取一定量的乙二胺四乙酸二钠,用超纯水溶解即得到模拟废水。用TOC-VCPH型总有机碳分析仪(日本岛津产)测得总有机碳(TOC)质量浓度为200 mg/L,pH用PHS-3B型精密pH计(上海雷磁产)测得,电导率用DDS-307型电导率仪(上海虹益产)测定。红外光谱采用NEXUS670型傅里叶红外光谱仪(美国Nicolet公司产)测定。
TOC去除率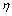 用以下公式计算:
用以下公式计算:
 (1)
(1)
式中:m0为处理前溶液的TOC质量;mt为处理时间为t时溶液的TOC质量。
1.3 电化学氧化
电解前,石墨电极用稀硫酸浸泡,用去离子水反复冲洗以去除表面附着的污染物,然后,置于电化学反应器中,在阳极和隔膜板间填充150 g预先活化好的活性炭。量取500 mL模拟废水置于烧杯中,将烧杯放在恒温水浴锅中以控制水温,用恒流泵使废水从阳极底端流入反应器,从阴极上部流出,返回到烧杯中,依此循环。同时,于主电极两端施加一定的电压,调节电流,开始进行电化学氧化,反应一段时间后取槽内溶液对TOC质量进行分析。
1.4 活性炭再生
活性炭每次使用后,残存着部分中间产物。因此,在进行下一次实验前,需将活性炭进行活化,使残存的有机物矿化。方法是:采用稀酸浸泡消除通过微孔填充和毛细管凝结吸附的有机物质,然后,通过电解进行活化。活化后再进行下一次实验。
2 结果与讨论
2.1 活性炭吸附效应消除实验
图2所示为活性炭对EDTA的吸附等压线。由图2可知:当温度小于20 ℃时,发生物理吸附;当温度大于20 ℃时,出现化学吸附,可见,活性炭具有范德华力及多种化学键。因此,活性炭吸附EDTA及中间产物时可以形成非催化活性配合物和催化活性配合物,非催化活性配合物在三维电极电解过程中将不发生分解,永久性占据活性炭的活性点。
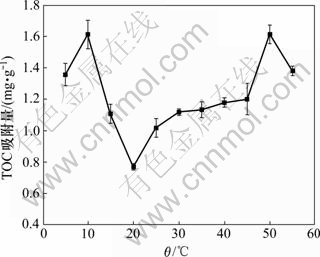
图2 活性炭对EDTA的吸附量与温度的关系
Fig.2 Effect of temperature on adsorption capacity of EDTA adsorbed using activated carbon
由于新使用的活性炭能生成非催化活性配合物,对有机物的去除率提供虚假的贡献,故必须消除对新使用的活性炭所产生的虚假去除率。采用的方法是取新的活性炭置于阳极和隔膜板之间,在pH为8.0,电流为200 mA时,模拟废水500 mL,电解2 h。连续进行多次实验,实验后取样分析溶液的TOC质量,得到了处理效果与活性炭使用次数的关系,与活化后的活性炭进行对比,如图3所示。
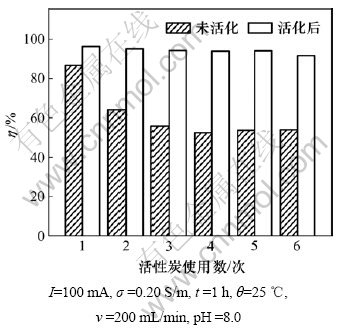
图3 活性炭使用次数对TOC去除率的影响
Fig.3 Effect of used times of activated carbon on TOC removal efficiency
从图3可以看出:未活化的活性炭初次使用时处理效果较好,TOC的去除率达到86.79%;当运行次数增加时,处理效果随之降低,当使用4次后,TOC的去除率由最初的86.79%下降到50%左右;再继续增加实验次数去除率已趋于稳定,表明活性炭所产生的虚假去除率已消除。而采用活化的活性炭,TOC的去除率基本保持在95%左右。为了消除电解生成非催化活性配合物所产生的虚假去除率,在进行单因素实验前,新的活性炭需采用模拟废水运行5次后再进行各项条件实验。
2.2 电解反应机理
文献[14]表明,在阳极电流作用下酸性溶液中O2的析出机理为:
H2O吸→?OH吸+H++e- (2)
?OH吸→O吸+H++e- (3)
2O吸→O2 (4)
其中反应式(2)为控制步骤。在碱性溶液中,氧析出机理是:
OH-吸→OH吸+e- (5)
OH-吸+OH吸→O吸+H2O+e- (6)
2O吸→O2 (7)
在低电流密度时,反应式(6)为控制步骤,高电流密度时,反应式(5)为控制步骤。
反应式(2)及式(5)表明:在阳极电流作用下,氧在酸性溶液和碱性溶液析出时都会产生中间产物羟基自由基,并吸附在活性炭上,它的标准电极电势为2.80 V,表明其有很强的电子亲和能力,容易进攻高电子云密度点。
由活性炭电解后的红外光谱图(见图4)可以看 出:在波数3 000~3 500 cm-1之间出现双峰,其中,波数为3 523.57 cm-1处的峰是N―H键对称伸缩振 动,波数为3 438.57 cm-1处的峰是N―H键反对称伸缩振动。在波数为1 564.44 cm-1处又出现了N―H键弯曲振动吸收峰,表明活性炭中有伯胺中间产物存 在[15]。对处理后的废水进行分析也检测到大量的NH3。据此,推测在羟基自由基的攻击下,EDTA按下列历程发生降解反应:EDTA→R3N(叔胺)→R2NH(仲胺)→H2NR(伯胺)→NH4++HOOC―COOH→CO2+H2O+ NH3,与Gilbert等[16]分析的EDTA在臭氧作用下可能的矿化反应路径相吻合。
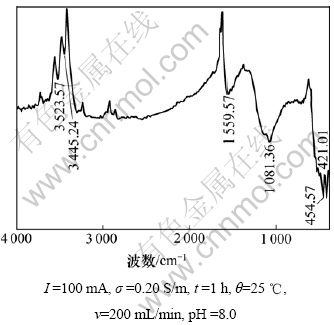
图4 电解实验后活性炭的红外光谱图
Fig.4 Infrared spectrum of activated carbon after electrolysis reaction
2.3 影响有机物去除率的工艺因素
2.3.1 进水流量对有机物去除率的影响
控制不同的进水流量,在出水口用40 mL瓶子连续取样监测出水TOC的浓度变化,结果如图5所示。从图5可见:随着进水流量的加快,废水在反应器内的停留时间缩短,去除效果逐渐下降;TOC的去除率开始下降很快,随后逐渐保持稳定,200 mL/min时去除率稳定在20%左右,275 mL/min时去除率稳定在25%左右,变化不大,从实际操作考虑,进水流量稳定在200 mL/min为宜。
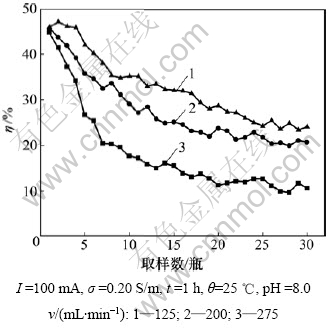
图5 进水流量对TOC去除率的影响
Fig.5 Effect of influent flow on TOC removal efficiency
2.3.2 电导率对有机物去除率的影响
溶液的电导率对有机物的降解影响较大,实验中以Na2SO4作为电导率调节剂加入到废水中,结果如图6所示。由图6可知:当电导率从0.10 S/m提高到0.15 S/m时,60 min时去除率升至94.71%;随着电导率的进一步增大,有机物的去除率逐步下降,并趋于稳定;在电导率为0.40 S/m时,60 min时去除率为84.03%。
电导率为0.15 S/m时,有机物的去除率高,表明此时溶液的电导率与活性炭的电导率接近或者相 等,因而在三维电极反应器内,两相中的电势变化方式相似。因此,活性炭不同点上固-液界面电位差近似恒定[17],电流分布均匀,故得到较好的降解效果。
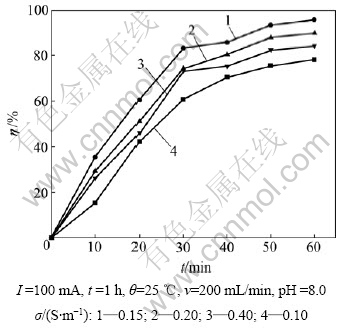
图6 电导率对TOC去除率的影响
Fig.6 Effect of electric conductivity on TOC removal efficiency
2.3.3 电流对有机物去除率的影响
电流对有机物去除率的影响见图7。从图7可知:随着电流的增加,有机物的去除率逐渐下降,在200 mA时,60 min去除率为96.40%;在500~800 mA时,60 min的去除率约92%;当电流升高到1 100 mA时,去除率迅速下降,60 min时去除率为75.22%。可见:电流过大,对TOC去除率有明显的不利影响。当电流为200~800 mA时,TOC去除率较高。
电极反应机理表明:在碱性(pH=9.0)溶液中,当电流密度较低时,反应式(6)为控制步骤,因此,反应式(5)生成的羟基自由基在电极表面上能保持较高的浓度,有利于EDTA的氧化分解,因而TOC去除率较高;但当电流增加到1 100 mA时,反应式(5)成为控制步骤,反应式(6)处在准平衡状态,电解反应生成的羟基自由基被很快消耗,故羟基自由基的浓度很低,TOC去除率变小。
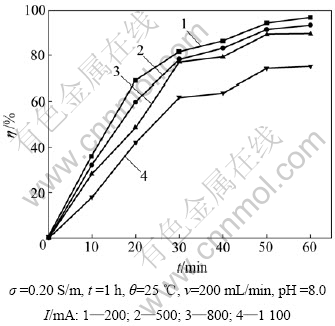
图7 电流对TOC去除率的影响
Fig.7 Effect of current on TOC removal efficiency
2.3.4 进水pH对有机物去除率的影响
溶液的pH对TOC的去除率影响较大,结果见图8。图8表明:当溶液pH为4~11时,TOC的去除率均保持在85%~90%;当pH小于3时,TOC的去除率由80%迅速下降至40%左右。因pH小于3时,Tafel斜率[18]为 ,表明反应式(2)为控制步骤,反应式(3)和(4)处于准平衡状态,故羟基自由基浓度低,不利于降解反应。
,表明反应式(2)为控制步骤,反应式(3)和(4)处于准平衡状态,故羟基自由基浓度低,不利于降解反应。
图8还表明:当pH大于11时,TOC的去除率突然下降,当pH过大时,Tafel斜率[18]为 ,表明反应式(5)为控制步骤,反应式(6)和(7)为准可逆状态,因而使EDTA去除率下降。
,表明反应式(5)为控制步骤,反应式(6)和(7)为准可逆状态,因而使EDTA去除率下降。
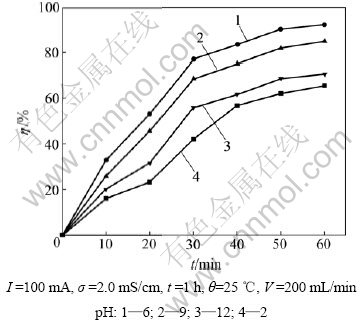
图8 进水pH值对TOC去除率的影响
Fig.8 Effect of inlet water pH on TOC removal efficiency
在pH为3~7的酸性溶液范围内时,反应式(3)为控制步骤;在pH为7~10的碱性溶液范围内时,反应式(6)为控制步骤。可见:当pH为3~10时,均可得到较高的TOC去除率。
2.3.5 进水温度对有机物去除率的影响
水温对TOC去除率的影响见图9。从图9可知:电解温度对TOC去除率有着显著的影响;随着水温的升高,TOC的去除率下降很快,25 ℃时,60 min时TOC的去除率为95.26%;当温度增加到45 ℃时,60 min时TOC的去除率下降到77.48%;再继续增加温度,去除率趋于稳定。在研究的温度范围内,最佳的电解温度为25 ℃。
Tafel斜率[18]会随着温度的升高而减小,当减小到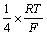 时,反应式(7)成为控制步骤,反应式(5)及(6)处于准平衡状态,羟基自由基浓度变小,因而EDTA的去除率下降。从图8可知:当温度大于45 ℃时,EDTA的去除率趋于稳定,表明温度为45 ℃时,反应式(7)已成为电极过程控制步骤,同时也说明控制步骤再也不随温度的变化而变化,故去除率能保持恒定。
时,反应式(7)成为控制步骤,反应式(5)及(6)处于准平衡状态,羟基自由基浓度变小,因而EDTA的去除率下降。从图8可知:当温度大于45 ℃时,EDTA的去除率趋于稳定,表明温度为45 ℃时,反应式(7)已成为电极过程控制步骤,同时也说明控制步骤再也不随温度的变化而变化,故去除率能保持恒定。
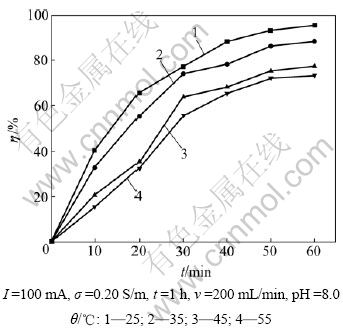
图9 水温对TOC去除率的影响
Fig.9 Effect of inlet water temperature on TOC removal efficiency
3 结论
(1) 通过活化再生处理消除活性炭粒子电极的吸附效应,TOC的去除率可稳定在90%以上。
(2) 获得三维电极反应器降解EDTA有机废水的优化工艺参数:pH为6.0~8.0,进水流量为200 mL/min,水温为25 ℃,电导率为0.15 S/m,电流为200 mA,循环电解1 h。在此优化工艺参数下,EDTA的去除率可以达到96.40%。
(3) EDTA在?OH自由基的作用下按下列历程发生降解反应:EDTA→R3N(叔胺)→R2NH(仲胺)→H2NR(伯胺)→NH4++HOOC―COOH→CO2+ H2O + NH3。
参考文献:
[1] Huang C P, DONG C D, Tang Z H. Advanced chemical oxidation: Its present role and potential future in hazardous waste treatment[J]. Waste Management, 1993, 13: 5-7.
[2] 徐夫元, 宋天顺, 陈英文, 等. Cu(Ⅱ)-Fe(Ⅱ)-H2O2协同催化氧化降解甲基橙[J]. 中南大学学报: 自然科学版, 2007, 38(6): 480-485.
XU Fu-yuan, SONG Tian-shun, CHEN Ying-wen, et al. Oxidation degradation of cationic red GTL by photo-Fenton[J]. Journal of Central South University: Science and Technology, 2007, 38(6): 480-485.
[3] 张亚平, 韦朝海. 光Fenton氧化降解染料阳离子红GTL[J]. 中南大学学报: 自然科学版, 2008, 39(4): 688-693.
ZHANG Ya-ping, WEI Chao-hai. Oxidation degradation of cationic red GTL by photo-Fenton[J]. Journal of Central South University: Science and Technology, 2008, 39(4): 688-693.
[4] Brillas E, Calpe J C, Casado J. Mineralization of 2,4-D by advanced electrochemical oxidation processes[J]. Water Research, 2000, 34(8): 2253-2262.
[5] Rajeshwar K, Ibanez J G, Swain G M. Electrochemistry and environment [J]. J Appl Electrochem, 1994, 24(11): 1077-1091.
[6] Belmant C, Cognet P, Berlan J, et al. Application of an electrochemical pulsed flow reactor to electroorganic synthesis: Part I. Reduction of acetophenone[J]. J Appl Electrochem, 1997, 28(2): 185-191.
[7] Szanto D, Trinidad P, Walsh F. Evaluation of carbon electrodes and electrosynthesis of coumestan and catecholamine derivatives in the FM01-LC electrolyser[J]. J Appl Electrochem, 1998, 28(3): 251-258.
[8] Didckmann G R, Langer S H. Selective electrogenerative oxidation of benzyl alcohol with platinum-graphite packed-bed anodes[J]. J Appl Electrochem, 1997, 27(1): 1-8.
[9] Bisang J M. Electrochemical treatment of waste solutions containing ferrous sulfate by anodic oxidation using an undivided reactor[J]. J Appl Electrochem, 2000, 30(4): 399-404.
[10] El-Deab M S, Saleh M M, El-Anodouli B E, et al. Electrochemical removal of lead ions from flowing electrolytes using packed bed electrodes[J]. J Electrochem Soc, 1999, 146(1): 208-213.
[11] Ragnini C A R, Di I R A, Bizzo W. et al. Recycled niobium felt as an efficient three-dimensional electrode for electrolytic metal ion removal[J]. Water Research, 2000, 34(13): 3269-3276.
[12] Walsh F, Reade G. Design and performance of electrochemical reactors for efficient synthesis and environmental treatment. Part 2. Typical reactors and their performance[J]. Analyst, 1994, 119(5): 797.
[13] Pitter P, Sykora V. Biodegradability of ethylenediamine-based complexing agents and related compounds[J]. Chemosphere, 2001, 44(4): 823-826.
[14] 查全性. 电极过程动力学导论[M]. 3版. 北京: 科学出版社, 2002: 192-197.
ZHA Quan-xing. Introduction to electrode kinetics[M]. 3rd ed. Beijing: Science Press, 2002: 192-197.
[15] 邹定平. 有机化合物结构分析[M]. 北京: 科学出版社, 2005: 53.
ZOU Ding-ping. Structure analysis of organic compounds[M]. Beijing: Science Press, 2005: 53.
[16] Gilbert E, Hoffmann-Glewe S. Ozonation of ethylenediaminetetraacetic acid (EDTA) in aqueous solution, influence of pH value and metal ions[J]. Water Reasearch, 1990, 24(1): 39-44.
[17] Newman J, Tiedemann W. Porous-electrode theory with battery applications[J]. American Institute of Chemical Engineers, 2004, 21(1): 25-41.
[18] Antropov L I. Theoretical electrochemistry[M]. Moscow: Mir Publishers, 1977: 196-201.
收稿日期:2009-09-05;修回日期:2010-01-18
基金项目:国家水体污染控制与治理科技重大专项(2009ZX07212-001-01);国家杰出青年科学基金资助项目(50925417);国家自然科学基金重点项目(50830301);湖南省节能减排科技重大专项(2008FJ1013)
通信作者:王云燕(1975-), 女,山西闻喜人,博士,副教授,从事环境电化学研究;电话:0731-88830875;E-mail: wyy@mail.csu.edu.cn
(编辑 任楚威)