微/纳米ZnO的控制合成及其光催化性能
谢娟1, 2,边丽1,王延吉3,魏雨2
(1. 河北工程大学 理学院,河北 邯郸,056038;
2. 河北师范大学 河北省无机纳米材料重点实验室,河北 石家庄,050024;
3. 河北工业大学 化工学院,天津,300130)
摘要:以锌盐和碱为主要原料,采用低温液相法,通过控制反应前驱液的组成,制得针状、花状、棒状和枣核状4种不同形貌的微/纳米ZnO。利用扫描电子显微镜(SEM)、X线能谱仪(EDS)、X线粉末衍射仪(XRD)、傅里叶变换红外光谱(FT-IR)、紫外-可见漫反射光谱(UV-Vis DRS)和热重-差热分析(TG-DTA)等多种手段对产物进行表征,并探讨不同形貌ZnO微/纳米晶的形成机制。以甲基橙模拟有机污染物,考察紫外光照下所得ZnO样品的降解效果。研究结果表明:ZnO晶体的粒度和形貌由其生长习性及成核、生长速率共同控制。ZnO的光催化性能与其颗粒粒度及形貌密切相关,棒状和枣核状ZnO表现出很高的光催化活性,120 min内即可将甲基橙完全降解。
关键词: ZnO;液相;光催化性能;甲基橙
中图分类号:O614 文献标志码:A 文章编号:1672-7207(2013)01-0060-07
Controlled-synthesis and photocatalytic performance of micro/nano ZnO
XIE Juan1, 2, BIAN Li1, WANG Yanji3, WEI Yu2
(1. College of Science, Hebei University of Engineering, Handan 056038, China;
2. Key Laboratory of Inorganic Nanomaterials of Hebei Province, Hebei Normal University, Shijiazhuang 050024, China;
3. College of Chemical Engineering and Technology, Hebei University of Technology, Tianjin 300130, China)
Abstract: Using zinc chloride and sodium hydroxide as the reactants, needle-, flower-, rod- and jujubestone-like ZnO micro-/nano-crystals were prepared via a low-temperature liquid phase method by controlling the composition of precursor solution. SEM, EDS, XRD, FT-IR, UV-Vis DRS and TG-DTA were used to characterize the products. Possible formation mechanism for these ZnO micro-/nanocrystals with different morphologies was discussed. The as-prepared ZnO powders were applied in photocatalytic degradation of methyl orange as model of organic pollutant during UV irradiation. The results show that the size and morphology of ZnO crystal are determined by its growth habit as well as nucleation and growth rates. A close relationship exists between the photocatalytic performance and the particle morphology and size. Rod- and jujubestone-like ZnO exhibit very strong photocatalytic activity, and methyl orange was completely degraded within 120 min.
Key words: ZnO; liquid phase; photocatalytic performance; methyl orange
目前,用作光催化剂的材料主要是TiO2,SnO2,CdS,WO3,ZrO2和Fe2O3等一些n型半导体化合物。尽管TiO2因氧化还原能力强、化学性质稳定、无毒无害和广谱适用等优点一直处于光催化研究的核心地位,但其至今仍存在光生电子与空穴易复合,量子效率较低(<4%),仅对紫外光有响应,无法充分利用太阳光中的可见光部分等问题[1]。ZnO拥有与TiO2相近的禁带宽度(Eg=3.2 eV)和价带能级位置,且两者的光催化降解机理完全相同[2],因此,近年来用微/纳米ZnO光催化降解各种有机化合物的报道不断增多。有研究表明,ZnO光催化降解罗丹明6G、酸性红18和酸性橙Ⅱ等[3-5]的效果比TiO2更好。加之ZnO利用太阳光的能力和量子效率均高于TiO2[6],所以,其极有可能成为继TiO2之后的又一种具有广阔应用前景的光催化剂。液相法与气相法和固相法相比具有生产成本和工艺要求较低、产品纯度高、组成均匀、颗粒形状统一和不需要后处理等优点,因此,被公认为最具发展前途的ZnO绿色合成方法[7]。国内外学者现已采用沉淀法、溶胶-凝胶法、微乳液法、沸腾回流法等液相法制备出了包括棒状、管状、坚果状、片状、花状、线状和带状等多种微/纳米结构ZnO,但有关粒度及形貌对ZnO光催化剂性能影响的研究报道还不多[8-11]。本文作者采用低温液相法,以廉价氯化锌为锌源,通过控制反应前驱液的组成,制备一系列形貌可控的微/纳米ZnO晶体,并探讨不同粒度及形貌ZnO的形成机制;同时,以甲基橙模拟有机污染物,考察所制备ZnO的光催化性能。
1 实验
1.1 试剂及仪器
试剂为:氯化锌(ZnCl2),氢氧化钠(NaOH),氢氧化锂(LiOH),十二烷基硫酸钠(SDS),甲基橙(MO)及无水乙醇均为分析纯;溶液用一次蒸馏水配制;德国Degussa公司生产的纳米TiO2(P25)。
仪器为:DC-3005A型低温恒温槽;HH-6型数显电热恒温水浴锅。
1.2 ZnO制备
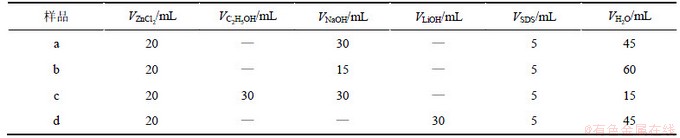
在磁力搅拌条件下,在与3 ℃恒温槽相连的200 mL玻璃套杯中,依次加入ZnCl2(1 mol/L)、无水乙醇以及NaOH/LiOH(4 mol/L),SDS(0.2 mol/L)和蒸馏水,定容100 mL。不同ZnO样品反应前驱液的组成见表1。将恒温槽的温度调至室温,继续搅拌1.5 h,再把所得包含白色物质的反应前驱液转移到250 mL具塞锥形瓶中,浸入85 ℃水浴锅陈化5 h。抽滤,洗涤,自然干燥,收集产品。
1.3 样品测试及表征
样品形貌用日立S-570扫描电子显微镜观察;Zn和O元素的原子数分数用INCA Energy 350型X线能谱仪(英国Oxford公司)检测;物相用德国Bruker AXS D8 ADVANCE X线粉末衍射仪鉴定;红外光谱和紫外-可见漫反射光谱分别用M-1730傅里叶变换红外光谱仪(美国Perkin-Elmer 公司)和日立 UV-3010紫外-可见分光光度计进行分析。热重-差热分析在TGA/SDTA 851e 型热分析仪(瑞士Mettler-Toledo 公司)上进行。以铬黑T为指示剂,用EDTA标准溶液(0.005 mol/L)配位滴定法测定2.5 mL反应液中Zn(Ⅱ)离子的浓度。
1.4 光催化性能评价
烧杯中加入100 mL甲基橙溶液(20 mg/L)和0.1 g ZnO粉体,超声分散15 min,暗处静置30 min,然后在磁力搅拌下,采用125 W高压汞灯(365 nm)照射(灯与样品距离12 cm)并开始计时。间隔取样,离心分离后取上清液经微孔滤膜过滤,测定其在甲基橙最大吸收波长(λmax=462 nm)处的吸光度,并依下式计算甲基橙的降解率(η):
η=(A0-At)/A0×100%
式中:A0为光照前甲基橙溶液的吸光度;At为光照时间t后甲基橙溶液的吸光度。
表1 不同ZnO样品反应前驱液的组成
Table 1 Composition of precursor solution of different ZnO samples
2 结果与讨论
2.1 ZnO晶体形貌、物相及光学性质表征
图1所示为不同ZnO样品的SEM照片。可以看出:样品a为粒径约500 nm、长约9 μm、一端是平面、一端呈尖锥形的长针状ZnO;样品b为花状ZnO,它由多个以某点为核心放射性伸展的纳米棒组成,每个纳米棒直径约为650 nm,长径比约为3,顶端亦是尖锥形。在反应前驱液中添加体积分数为30%的乙醇得到的是直径约为100 nm、长约为1.1 μm的短棒状ZnO(样品c)。将NaOH替换为LiOH,可得到直径约为40 nm,长径比约为1的枣核状ZnO(样品d)。EDS分析表明:所有样品只有Zn和O特征峰,专业软件拟合计算的Zn和O半定量解析数据表明,二者的原子数分数均为50%,即晶格Zn与O的原子数分数之比为1:1。
图2所示为不同ZnO样品的XRD图谱。样品a~d的各衍射峰均与标准ZnO卡片(JCPDS 89-0510)中的峰一一对应,属于六方晶系纤锌矿ZnO。没有杂质峰,说明产物的纯度很高;样品a和b较c和d的衍射峰强度高且宽度窄,表明样品c和d的结晶度有所下降,这是微/纳米尺度的晶粒尺寸减小,晶体中的缺陷相对增加,点阵间距发生变化所造成的[12]。
不同ZnO样品的FT-IR光谱(图3)与UV-Vis DRS光谱(图4)反映出不同粒度及形貌ZnO的光学性质差异。图3中,3 441 cm-1及1 636 cm-1附近的宽吸收带可分别归结为ZnO表面吸附水的伸缩振动和弯曲振动,2 359 cm-1处属于CO2的红外特征吸收;520~419 cm-1范围内出现的是对应于Zn―O晶格振动的较强红外光谱特征吸收峰[13],其随着ZnO颗粒粒度的减小,不断宽化和红移,吸收强度显著增大,该结果与相关文献报道结果一致[14]。吸收带宽化是由颗粒粒度减小,比表面增大,表面原子平均配位数随之下降,不饱和键和悬键逐渐增多,以致键振动模分布变宽,红外吸收频率分布也相应展宽所造成的;红移则由粒度减小导致的ZnO晶格膨胀,键长增大,键的平均频率下降引起;同时,界面极化和多重散射作为重要的吸收机制,还使得颗粒的光吸收能力随比表面的增大、表面原子比例的升高及悬键的增多越来越强[15]。由图4可以看出:此法制备的ZnO均具有较强的紫外光吸收性能;且随着ZnO颗粒粒度的减小,吸收强度逐渐增大,吸收边带不断蓝移,其中样品d相对于样品b的吸收边带蓝移了近10 nm。该现象归因于半导体材料尺寸效应导致的电子能级变化,通常颗粒粒径减小,能级间隔变大[16]。因此,只有频率更高的紫外线才能将价带的电子激发到导带。
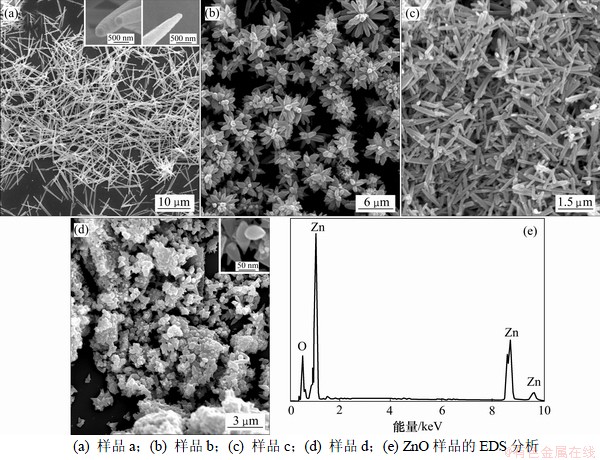
图1 不同ZnO样品的SEM照片及EDS分析
Fig.1 SEM images and EDS analysis of different ZnO samples
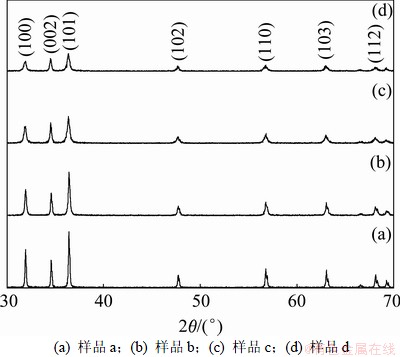
图2 不同ZnO样品的XRD图谱
Fig.2 XRD patterns of different ZnO samples
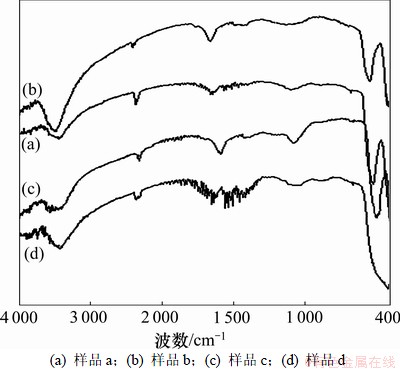
图3 不同ZnO样品的FT-IR图谱
Fig.3 FT-IR spectra of different ZnO samples
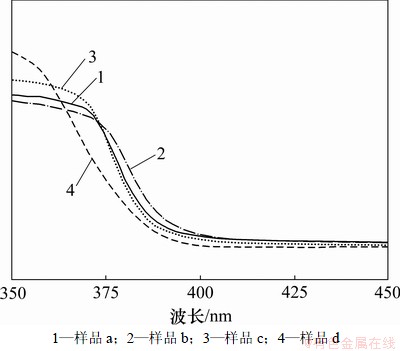
图4 不同ZnO样品的UV-Vis DRS图谱
Fig.4 UV-Vis DRS spectra of different ZnO samples
2.2 不同粒度及形貌ZnO生长机理初探
样品a和b反应前驱物Zn(OH)2的SEM照片及XRD图谱见图5。从图5可以看出:样品a和b反应前驱液中白色物质的形状明显不同,但XRD图谱证实二者均为Zn(OH)2(JCPDS 89-0138)。样品a的前驱物Zn(OH)2呈粒径均匀的颗粒状,晶化程度较高;样品b的前驱物Zn(OH)2不具有规则外形,且晶化程度偏低。

图5 样品a和样品b反应前驱物Zn(OH)2的SEM照片及XRD图谱
Fig.5 SEM images and XRD patterns of precursors Zn(OH)2 for samples a and b
图6所示为前驱物Zn(OH)2的TG-DTA曲线。DTA曲线在100~200 ℃之间有1个吸热峰,154.20 ℃时达到最大吸热量,TG曲线对应出现明显的质量变化,质量损失率为17.24%,该数值与Zn(OH)2分解生成ZnO的理论质量损失率(18.11%)基本吻合,此后TG和DTA曲线上再未出现任何变化。
图7所示为陈化过程中Zn(Ⅱ)离子浓度随时间的变化曲线。样品a的陈化步骤开始后,体系中Zn(Ⅱ) 离子浓度缓慢增大,并最终保持在约0.043 mol/L;而样品b的反应体系中Zn(Ⅱ)离子浓度在陈化之初就快速下降,并于50 min左右基本达到平衡(约0.001 mol/L)。综合分析认为,该反应体系中ZnO的形成机制为85 ℃陈化温度下的Zn(OH)2溶解-ZnO再结晶相变过程。
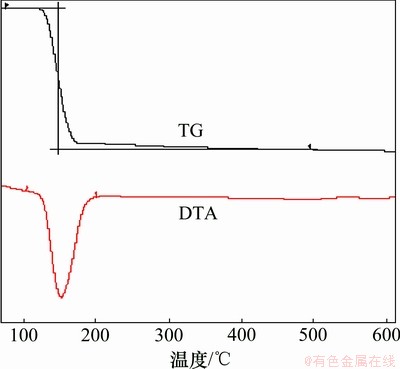
图6 前驱物Zn(OH)2的TG-DTA曲线
Fig.6 TG-DTA curves of precursor Zn(OH)2
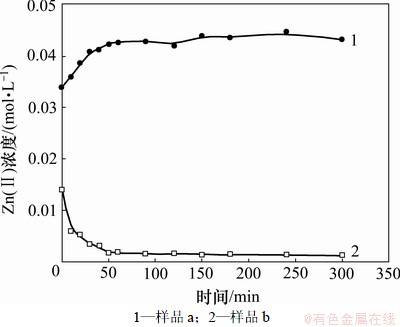
图7 样品a和样品b陈化过程中Zn(Ⅱ)离子浓度随时间变化曲线
Fig.7 Relationship between the aging time and Zn(Ⅱ) concentration for samples a and b
由于体系中OH-离子的浓度较高,而Zn(OH)42-又被普遍看作高碱度条件下Zn(Ⅱ)离子的主要存在形式和ZnO的生长基元[17],所以,相变反应可表示为:
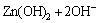 →
→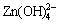 (1)
(1)
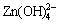 →ZnO+H2O+2OH- (2)
→ZnO+H2O+2OH- (2)
在85 ℃陈化过程中,Zn(OH)2溶解成为Zn(OH)42-,当其浓度满足ZnO析出条件时,Zn(OH)42-之间便通过氧桥合作用和阴离子基团质子化反应析出ZnO晶核;而后Zn(OH)42-继续通过脱水反应在晶界上进行叠合,并最终得到ZnO晶体。
众所周知,液相反应过程中,ZnO各晶面生长速率v不同:v[0001]>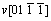 >
>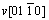 >
>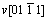 >
>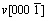 [17],即晶体生长沿[0001]方向最快,柱面方向居中,
[17],即晶体生长沿[0001]方向最快,柱面方向居中, 方向最慢,而且晶体的生长行为除受其内在生长习性控制外,还要受外部环境和生长条件的制约。在85 ℃下,由于颗粒状Zn(OH)2较无规则外形Zn(OH)2更为稳定,因而可起到降低溶液过饱和度、涵养锌源的作用。陈化步骤开始后,Zn(OH)2缓慢溶解,Zn(Ⅱ)离子浓度逐渐升高,并于约2 h建立起Zn(OH)2溶解与ZnO析出间的平衡。此过程不仅有利于均匀地析出ZnO晶核,还使得溶液中有限的Zn(OH)42-被优先提供到[0001]方向进行生长,最终得到一维针状ZnO。相反,无规则外形的Zn(OH)2因在高温下极易溶解,促使反应速率异常加快,体系中ZnO瞬间爆发性成核,导致陈化步骤开始阶段Zn(II)离子浓度迅速下降,无法观察到浓度的上升阶段;同时,由于比表面较大和表面自由能较高,这些粒度仅为数个纳米的ZnO 晶核极不稳定,为了降低总界面能,它们又在高频碰撞中通过粒子间引力相互粘附形成了无数小聚集体。而后每个晶核继续按照ZnO的固有习性生长,最后得到三维花状ZnO。样品a和b在不同陈化时间的中间产物的XRD图谱(图8)进一步佐证了上述判断。
方向最慢,而且晶体的生长行为除受其内在生长习性控制外,还要受外部环境和生长条件的制约。在85 ℃下,由于颗粒状Zn(OH)2较无规则外形Zn(OH)2更为稳定,因而可起到降低溶液过饱和度、涵养锌源的作用。陈化步骤开始后,Zn(OH)2缓慢溶解,Zn(Ⅱ)离子浓度逐渐升高,并于约2 h建立起Zn(OH)2溶解与ZnO析出间的平衡。此过程不仅有利于均匀地析出ZnO晶核,还使得溶液中有限的Zn(OH)42-被优先提供到[0001]方向进行生长,最终得到一维针状ZnO。相反,无规则外形的Zn(OH)2因在高温下极易溶解,促使反应速率异常加快,体系中ZnO瞬间爆发性成核,导致陈化步骤开始阶段Zn(II)离子浓度迅速下降,无法观察到浓度的上升阶段;同时,由于比表面较大和表面自由能较高,这些粒度仅为数个纳米的ZnO 晶核极不稳定,为了降低总界面能,它们又在高频碰撞中通过粒子间引力相互粘附形成了无数小聚集体。而后每个晶核继续按照ZnO的固有习性生长,最后得到三维花状ZnO。样品a和b在不同陈化时间的中间产物的XRD图谱(图8)进一步佐证了上述判断。
作为一种典型的阴离子表面活性剂,SDS可在水中完全电离,得到DS-。DS-与Zn(OH)42-之间的静电斥力在某种程度上抑制了Zn(OH)2的溶解,在规则Zn(OH)2基础上进一步减缓了反应速率,因此,SDS的加入对ZnO生长成一维结构起到了一定的积极作用。然而,极低的浓度使得SDS的作用十分有限,以致它的存在无法从根本上改变反应前驱物自身性质对反应速率的影响,所以,样品b依旧生长成为了三维结构。乙醇分子可以通过羟基中的氧原子与ZnO晶核表面上的Zn(Ⅱ)发生配位反应,被强烈吸附在晶核表面,形成一层―CH2―CH3疏水膜[18]。该膜的存在可使晶核表面活性大大降低,严重阻碍生长基元在晶核上的沉积,抑制ZnO各晶面的生长,因此,当乙醇的体积分数为30%时得到的是棒状ZnO。由于Li+较Na+半径小而电荷密度高,所以,Li+在ZnO晶体表面的吸附强度远高于Na+的吸附强度[19],致使LiOH为反应物时生长基元在ZnO晶核表面的叠合速率比NaOH为反应物时显著降低,各个晶面生长极其缓慢,从而得到了粒径和长径比均非常小的枣核状ZnO颗粒。
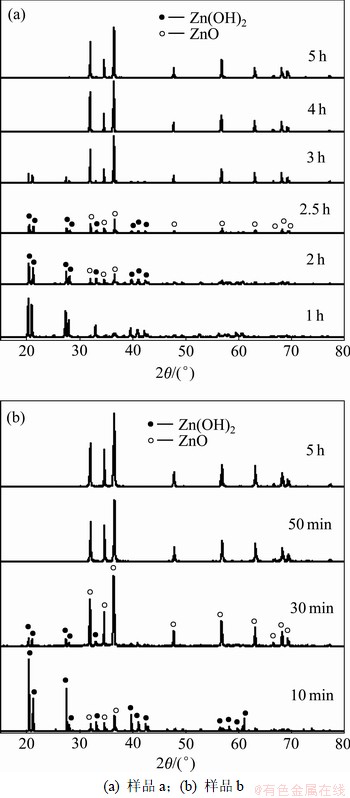
图8 样品a和样品b不同陈化时间中间产物的XRD图谱
Fig.8 XRD patterns of intermediate products at different aging time for samples a and b
2.3 粒度及形貌对ZnO光催化性能的影响
染料废水是一类很难降解的工业废水,而醌式及偶氮结构是碱性和酸性条件下染料化合物的主体结构,因此,以甲基橙模拟有机污染物具有较强的代表性。图9所示为所制不同ZnO样品光催化降解甲基橙效率与反应时间的关系曲线。空白实验结果显示:高压汞灯照射时,120 min后甲基橙的降解率仅为14.3%,该现象为甲基橙的自分解。各种ZnO样品光催化降解甲基橙效率的变化趋势基本一致,其中样品a,c和d的降解效果均优于相同条件下的商品光催化剂P25的降解效率。在所考察的光照时间内,样品b作催化剂时,甲基橙降解率约为86%;而以样品a为催化剂时,甲基橙的降解率可达96%;样品c和d则表现出更高的光催化活性,甲基橙几乎被完全降解。
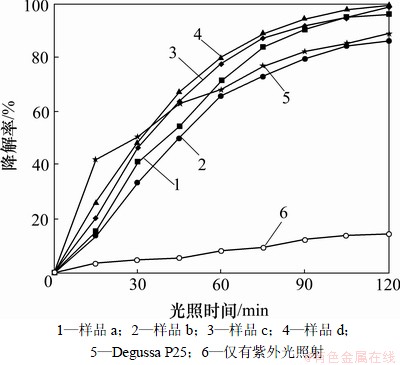
图9 不同ZnO样品光催化降解甲基橙效率与反应时间的关系
Fig.9 Relationship between degradation efficiency of MO and irradiation time with different ZnO samples
以上结果表明:ZnO的光催化活性与其颗粒粒度及形貌均有联系。首先,颗粒比表面积随粒度的减小不断增大,这不仅有利于光生电子/空穴向ZnO表面传输,而且有助于目标降解物在ZnO表面上的吸附与富集[11, 20],结果使催化剂的氧化活性和电荷流动性逐渐升高,光催化反应效率随之增大。其次,图2证实ZnO的晶粒尺寸减小,晶体中的缺陷相对增加,而晶格缺陷作为光催化反应的活性位,能够起到俘获光生电子的势阱作用,有助于抑制光生电子和空穴的复合,提高量子利用效率。因此,粒度减小明显提高了ZnO的光催化性能。ZnO颗粒不同晶面所包含的光催化活性位数目亦有区别[21-22]。由于不同形貌ZnO颗粒各晶面的展露程度和比例不尽相同,所以,活性位数目及光催化效果必然存在差异。至于上述ZnO样品颗粒中具体哪个晶面所含的光催化活性位最多,其展露度及比例又各为多少还有待于进一步深入探究。
3 结论
(1) 采用低温液相法,通过控制反应前驱液的组成制得了针状、花状、棒状和枣核状4种ZnO微/纳米晶。
(2) 该反应体系中ZnO的形成机制为Zn(OH)2溶解-ZnO再结晶相变过程。ZnO晶体的固有极性生长习性及反应条件对其成核、生长速率的影响共同控制着产物的粒度和形貌。
(3) 所制ZnO粉体均能在紫外光照下降解甲基橙模拟污染物,其光催化性能与颗粒的粒度及形貌密切相关。
参考文献:
[1] 刘春艳. 纳米光催化及光催化环境净化材料[M]. 北京: 化学工业出版社, 2008: 2-3.
LIU Chunyan. Nano-photo-catalysis and photo-catalytic environment purifying materials[M]. Beijing: Chemical Industry Press, 2008: 2-3.
[2] Hariharan C. Photocatalytic degradation of organic contaminants in water by ZnO nanoparticles: Revisited[J]. Appl Catal A, 2006, 304(1): 55-61.
[3] Kansal S K, Singh M, Sud D. Studies on photodegradation of two commercial dyes in aqueous phase using different photocatalysts[J]. J Hazard Mater, 2007, 141(3): 581-590.
[4] Sobana N, Swaminathan M. The effect of operational parameters on the photocatalytic degradation of acid red 18 by ZnO[J]. Sep Purif Technol, 2007, 56(1): 101-107.
[5]  V, Bakardjieva S, et al. Nanostructure materials for destruction of warfare agents and eco-toxins prepared by homogeneous hydrolysis with thioacetamide: Part 1. Zinc oxide[J]. J Phys Chem Solids, 2007, 68(5/6): 716-720.
V, Bakardjieva S, et al. Nanostructure materials for destruction of warfare agents and eco-toxins prepared by homogeneous hydrolysis with thioacetamide: Part 1. Zinc oxide[J]. J Phys Chem Solids, 2007, 68(5/6): 716-720.
[6] Kaneco S, Katsumata H, Suzuki T, et al. Solar photo-catalytic degradation of endocrine disruptor di-n-butyl phthalate in aqueous solution using zinc oxide[J]. Bull Catal Soc India, 2007, 6(3): 22-33.
[7] 王辉虎. 纳米氧化锌的控制制备及其光催化性能的研究[D]. 武汉: 华中科技大学材料科学与工程学院, 2006: 4-6.
WANG Huihu. Study on controlled synthesis and photocatalytic performance of nanometer-sized zinc oxide[D]. Wuhan: Huazhong University of Science and Technology. College of Materials Science and Engineering, 2006: 4-6.
[8] Li D, Haneda H. Morphologies of zinc oxide particles and their effects on photocatalysis[J]. Chemosphere, 2003, 51(2): 129-137.
[9] Wan Q, Wang T H, Zhao J C. Enhanced photocatalytic activity of ZnO nanotetrapods[J]. Appl Phys Lett, 2005, 87(8): 083105-083107.
[10] 吴建锋, 张敏, 徐晓虹, 等. ZnO微晶晶面与其光催化性能的关系[J]. 硅酸盐学报, 2009, 37(6): 1038-1043.
WU Jianfeng, ZHANG Min, XU Xiaohong, et al. Crystal planes of ZnO crystallite and its photocatalytic property[J]. J Chin Ceram Soc, 2009, 37(6): 1038-1043.
[11] 吕红金, 江萍, 刘宇珊, 等. 不同形貌纳米ZnO的合成及其光催化性能研究[J]. 功能材料, 2010, 41(2): 292-295.
L Hongjin, JIANG Ping, LIU Yüshan, et al. Preparation and photocatalytic degradation properties of ZnO nanopowders with different morphologies[J]. J Funct Mater, 2010, 41(2): 292-295.
Hongjin, JIANG Ping, LIU Yüshan, et al. Preparation and photocatalytic degradation properties of ZnO nanopowders with different morphologies[J]. J Funct Mater, 2010, 41(2): 292-295.
[12] 孙萍, 熊波, 张国青, 等. 氧化锌纳米晶体的光谱分析[J]. 光谱学与光谱分析, 2007, 27(1): 143-146.
SUN Ping, XIONG Bo, ZHANG Guoqing, et al. Spectral analysis of ZnO nanocrystals[J]. Spectrosc Spectral Analysis, 2007, 27(1): 143-146.
[13] Wu L L, Wu Y S, Shi Y C, et al. Synthesis of ZnO nanorods and their optical absorption in visible-light region[J]. Rare Met, 2006, 25(1): 68-73.
[14]  S. Influence of synthesis route on the formation of ZnO particles and their morphologies[J]. J Alloys Compd, 2007, 429(1/2): 242-249.
S. Influence of synthesis route on the formation of ZnO particles and their morphologies[J]. J Alloys Compd, 2007, 429(1/2): 242-249.
[15] 袁吉仁, 李要球, 邓新华. 纳米ZnO的光吸收特性研究[J]. 南昌大学学报: 工科版, 2006, 28(4): 329-331.
YUAN Jiren, LI Yaoqiu, DENG Xinhua. Study on the light absorption properties of nano-ZnO[J]. J Nanchang Univ: Eng & Technol, 2006, 28(4): 329-331.
[16] 张立德, 牟季美. 纳米材料和纳米结构[M]. 北京: 科学出版社, 2002: 80-82.
ZHANG Li-de, MOU Ji-mei. Nanomaterial and nanostructure[M]. Beijing: Science Press, 2002: 80-82.
[17] Li W J, Shi E W, Zhong W Z, et al. Growth mechanism and growth habit of oxide crystals[J]. J Cryst Growth, 1999, 203(1/2): 186-196.
[18] Burnett G R, Atkin R, Hicks S, et al. Surfactant-free “Emulsions” generated by freeze-thaw[J]. Langmuir, 2004, 20(14): 5673-5678.
[19] Uekawa N, Yamashita R, Wu Y J, et al. Effect of alkali metal hydroxide on formation processes of zinc oxide crystallites from aqueous solutions containing Zn(OH)42- ions[J]. Phys Chem Chem Phys, 2004, 6(2): 442-446.
[20] 王虎, 谢娟, 段明. 特殊形貌的ZnO晶体: 水热法生长及光催化性能[J]. 无机化学学报, 2011, 27(2): 321-326.
WANG Hu, XIE Juan, DUAN Ming. ZnO crystals of special morphologies: preparation by hydrothermal method and photocatalytic properties[J]. Chin J Inorg Chem, 2011, 27(2): 321-326.
[21] Bowker M, Houghton H, Waugh K C, et al. Crystal plane dependence of adsorption and reaction on zinc oxide[J]. J Catal, 1983, 84(1): 252-255.
[22] Bolis V, Fubini B, Giamello E, et al. Effect of form on the surface reactivity of differently prepared zinc oxides[J]. J Chem Soc, Faraday Trans, 1989, 85(1): 855-867.
(编辑 何运斌)
收稿日期:2012-01-07;修回日期:2012-04-09
基金项目:国家自然科学基金资助项目(21206026);河北省自然科学基金资助项目(B2012402011);邯郸市科学技术研究与发展计划项目(1223120094);河北省高等学校科学技术研究优秀青年基金资助项目(Y2012028)
通信作者:谢娟(1981-),女,河北石家庄人,博士,副教授,从事微/纳米材料合成及催化化学研究;电话:15226951585;E-mail: xiejuan_katy@yeah.net