文章编号:1004-0609(2013)S1-s0331-05
多孔钛表面羟基磷灰石形貌及形成机理
李若琳1,寇宏超1,徐广胜1,李金山1,周 廉1,卢婷丽2
(1. 西北工业大学 凝固技术国家重点实验室,西安 710072;
2. 西北工业大学 生命科学学院,西安 710072)
摘 要:由于预钙化对HA有诱导沉积作用,进而形成均匀涂层,而未预钙化的多孔钛表面由于表面张力作用形成团簇状HA涂层。采用碱热处理+模拟体液(SBF)等化学方法在多孔钛表面制备羟基磷灰石(HA)涂层,采用扫描电镜观察多孔钛表面形貌,采用能谱分析仪对表面的HA涂层成分进行分析,对比研究预钙化对HA形貌的影响,并探讨不同形貌HA的形成机理。结果表明:采用预钙化处理的多孔钛表面形成均匀附着且有一定厚度的HA,而未预钙化多孔钛表面则形成以团簇状不均匀分布的HA。
关键词:多孔钛;碱热处理;预钙化;团簇;羟基磷灰石
中图分类号:TG146.2 文献标志码:A
Morphology and formation mechanism of hydroxyapatite on porous titanium surface
LI Ruo-lin1, KOU Hong-chao1, XU Guang-sheng1, LI Jin-shan1, ZHOU Lian1, LU Ting-li2
(1. State Key Laboratory of Solidification Processing, Northwestern Polytechnical University, Xi’an 710072, China;
2. School of Life Science, Northwestern Polytechnical University, Xi’an 710072, China)
Abstract: The formation of HA is induced by pre-calcified, leading to form a uniform coating. However, because of the effect of surface tension, cluster-like HA is formed. A hydroxyapatite (HA) coating on the porous titanium surface was prepared by NaOH heat treatment and heat treatment followed by immersing into the simulated body fluid (SBF). The influence of pre-calcified on HA morphology and element content was studied, the formation mechanisms of HA with different morphologies were explored. The results show the hydroxyapatite of porous titanium surface after pre-calcified is attached uniformly and has a certain thickness. However, the hydroxyapatite without pre-calcified is unevenly distributed on porous titanium surface in clusters.
Key words: porous titanium; NaOH heat treatment; pre-calcification; cluster-like; hydroxyapatite
钛及钛合金因其良好的生物相容性、耐蚀性及优异的综合性能成为临床医用金属材料的首要选择[1],但是,钛合金植入人体后会产生应力屏蔽,且始终作为宿主的异体存在,容易变形和松动,这些缺点严重影响了钛合金人工关节的长期应用效果[2]。为了解决以上问题,采用在钛及钛合金中引入孔隙的方法,并对其进行表面改性[3]。多孔结构可通过调控孔隙率使材料的弹性模量接近人骨而减少应力屏蔽[4-5],且其独特的三维连通孔能使体液和营养物质在多孔植入体中传输,促进组织再生与重建,加快愈合过程。
人工植入材料的基本要求是不仅具有生物相容性,而且与相邻宿主骨间存在生物活性[6-7]。羟基磷灰石(HA)是脊椎动物硬组织的矿物质成分[8-9],具有良好的生物相容性及生物活性,HA涂层的溶解刺激了骨组织的结合,它植入人体后能在短时间内与人体的软组织紧密结合。在钛或钛合金表面涂覆HA活性涂层,改变了原多孔钛的表面形态,具有与人骨相近的钙磷比,有利于成骨细胞的粘附、增殖和分化,促使新骨组织长入孔隙,使植入体同骨之间形成生物固定[10]。ZHUANG等[11]利用粉末的单结晶羟基磷灰石纤维合成磷灰石凝胶,成功研发出一种新型高择优取向致密的羟基磷灰石陶瓷复合活性骨。LEE等[12]采用微弧氧化法在海绵复制法制备的多孔钛支架表面制备HA/TiO2复合涂层,这种混合涂层提高成骨细胞活性的多孔钛支架显著。徐淑华等[13-14]用扫描电镜和透射电镜对未经热处理的钛合金基体等离子喷涂HA生物材料的界面结合进行了观察与分析,发现HA以结晶态和非晶态两种形态存在,且HA和基体的界面结合是以物理结合为主, 界面明显,加入ZrO2后,涂层和基体之间的界面结合力显著增强。以上研究主要将视线集中于采用不同制备工艺对HA涂层进行设计,但对材料表面不同HA形貌及形成机理探讨较少。
本文作者通过化学法在多孔钛表面沉积涂覆羟基磷灰石,研究预钙化前后HA表面形貌的变化,探讨多孔钛表面均匀HA及团簇状HA的形成机理。
1 实验
1.1 表面HA涂层制备
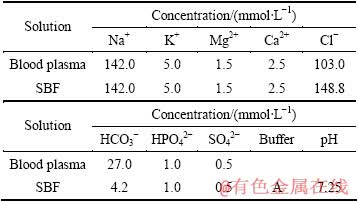
实验所用多孔钛为采用专利[15]钛网层叠烧结法制备的d16 mm×0.4 mm样品,在丙酮/酒精、去离子水依次中超声波清洗20 min后放入NaOH水溶液(浓度5.0 mol/L),于60 ℃密封保温处理24 h。取出后用去离子水清洗,在空气中干燥。处理后的样品以3 ℃/min的速率升温至630 ℃,保温1 h后随炉冷却,取A组碱热处理后的多孔钛试样进行预钙化处理,另取B组碱热处理后多孔钛样品不进行预钙化处理。预钙化处理的步骤为:将A组样品放入0.5 mol/L Na2HPO4溶液中24 h,再在饱和Ca(OH)2溶液中浸泡5 h,取出后用去离子水清洗。A组与B组均置于36.5 ℃模拟体液(Simulated body fluid,SBF,离子浓度见表1)中浸泡,制成HA涂层多孔钛。浸泡过程中每48 h更换1次SBF,以(CH2OH)3CNH2溶液作为缓冲液,调节pH到7.25。将2组样品于5 d和14 d后取出进行观察分析。
表1 模拟体液(SBF) 和人体血清离子浓度对照
Table 1 Ion concentrations of simulated body fluid and human blood plasma
1.2 观察分析
采用TESCAN VEGA3扫描电镜(SEM)对改性前后试样形貌进行观察,用扫描电镜配备的能谱分析仪对表面的HA涂层进行成分分析。
2 结果与分析
2.1 多孔钛表面碱热处理
对钛网预压烧结制备的多孔钛基体进行碱热处理。图1所示为碱热处理前后的多孔钛表面形貌,其中,图1(a)所示为酸洗后多孔钛表面形貌,表面呈阶梯型层片结构,表面平整光滑,提高了HA附着力和结合力。多孔钛表面产生大量气体,热处理使气体释放出来,表面形成纳米或几微米的三维孔隙结构,如图1(b)所示,这是由于多孔钛表面发生以下化学反应:
Ti+3OH-→Ti(OH)3++4e
Ti(OH)3++e→TiO2・H2O+1/2H2↑
碱热处理后钛表面形成非晶的钛胶层,热处理后表面形成钛酸钠,浸泡到 SBF 中钛表面的 Na+与模拟体液 SBF 中的 H3O+交换,钛表面形成活性 Ti-OH,为表面磷灰石形核提供活性位。

图1 碱热处理前后的多孔钛表面形貌
Fig. 1 Morphologies of porous titanium surface before (a) and after (b) NaOH and heat treatment
2.2 多孔钛表面HA沉积
将A和B 2组多孔钛试样在SBF中浸泡5 d后取出,利用扫描电镜观察钙磷涂层的生长情况,如图2所示,其中,图2(a)所示为A组预钙化后多孔钛表面磷灰石附着形貌,图2(b)所示为B组未经预钙化的多孔钛表面磷灰石附着形貌。
从图2(a)可以看出:预钙化的样品表面磷灰石附着均匀,涂层具有一定厚度,碱热处理后形成的微米级孔基本上观察不到,涂层分布比较均匀,一些盐类析出物没有看到。而图2(b)中所示的未预钙化多孔钛表面磷灰石分布比较分散,有些地方的原始表面片层纹路依稀可见,且一些结晶物分布比较明显,多孔钛表面碱热处理后的微米级孔洞还可以看到,磷灰石涂层分布不均匀,一些白色的盐类析出物比较多,且分布没有规律。

图2 多孔钛在SBF中浸泡5 d后钙磷涂层生长照片
Fig. 2 Surface morphologies of apatite coating on porous titanium immersed in SBF for 5 d

图3 多孔钛在SBF中浸泡14 d后钙磷涂层生长照片及能谱分析
Fig. 3 Surface morphologies and EDS analysis of apatite coating on porous titanium immersed in SBF for 14 d
将2组样品在SBF中继续浸泡至14 d后取出,图3所示为A和B 3组多孔钛浸泡SBF 14 d后的扫描电镜照片及能谱分析,其中,图3(a)所示为A组预钙化后进行SBF浸泡的样品,磷灰石涂层均匀地附着在多孔钛表面。对图3(a)框图区域进行EDS分析得到表面涂层的摩尔分数分别为Ca 6.36%、P 3.67%、O 72.44%,钙与磷摩尔比为1.73;而标准HA的钙磷摩尔比为1.67:1,说明浸泡SBF 14 d后A组多孔钛表面形成的磷灰石涂层为HA涂层。图3(b)所示为B组未预钙化样品浸泡SBF 14 d的表面形貌,磷灰石已完全覆盖多孔体表面,而且变成更大的簇状和团状。在对图3(b)框图区域内的团簇状物质进行EDS分析可知,团簇状磷灰石的摩尔分数分别为Ca 19.38%、P 11.60%、O 60.57%,钙磷原摩尔为1.67,B组多孔钛表面形成了HA涂层,且表面不均匀分布了少许NaCl和MgCl等其他盐类。
2.3 多孔钛表面磷灰石涂层形成机理
图4所示为碱热处理后多孔钛表面诱导磷灰石形核机理示意图,其中,图4(a)所示为均匀磷灰石涂层形成机理示意图,预钙化过程中样品表面的钛酸钠水解,形成带负电的活性Ti-OH,Ca2+被静电引力均匀吸附到表面的活性羟基位上。在浸泡SBF过程中,PO43-与Ca2+发生反应,均匀附着在Ca2+表面,同时,又有Ca2+均匀吸附到PO43-表面,层层叠加吸附,形成了均匀分布的HA。图4(b)所示为团簇状磷灰石涂层形成机理示意图,未预钙化的多孔钛表面,Ca2+与PO43-同时吸附到多孔钛表面,由于表面张力的作用,使磷酸钙发生球化,并以此为核心,结晶生长,形成团簇状HA。有些研究人员认为,多孔钛表面形成团簇状HA是由于浸泡的SBF中含有Mg2+和HCO3-,在模拟体液环境中,HCO3-对镁的腐蚀具有保护和破坏的双重作用,在这种交互作用下,会在表面形成团簇状HA。但在本实验中,A组和B组均浸泡了同样的含有Mg2+和HCO3-的SBF,唯一区别在于浸泡前后是否进行了预钙化这一过程,因此,本文作者认为未进行预钙化是团簇状HA的形成原因。
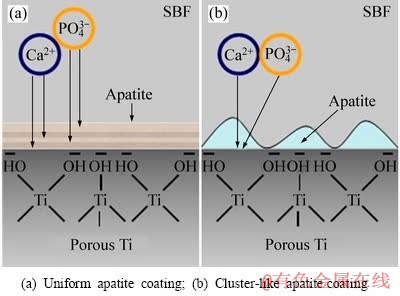
图4 多孔钛表面磷灰石涂层形成机理
Fig. 4 Formation mechanism of porous titanium apatite coating
3 结论
1) 碱热处理后,多孔钛表面形成丰富的三维微纳米级孔隙结构,便于HA的形核。
2) 采用预钙化处理的多孔钛表面形成均匀附着且有一定厚度的HA,预钙化对HA有诱导沉积作用,进而形成均匀涂层。
3) 未预钙化的多孔钛表面形成以团簇状不均匀分布的HA,Ca2+与PO43-同时吸附到多孔钛表面,由于表面张力的作用,使磷酸钙发生球化,形成团簇状HA。
REFERENCES
[1] NISHIQUCHI S, KATO H, FUJITA H, OKA M, KIM H M, KOKUBO T, NAKAMURA T. Titanium metals form direct bonding to bone after alkali and heat treatments[J]. Biomaterials, 2001, 22(18): 2525-2533.
[2] HUISKES R, WEINANS H, RIEBERGER B. Natural factors that affect the shape and strength of the aging human femur[J]. Clin Orthop Relat Res, 1992, 274:124.
[3] LIU Xuan-yong, CHU P K, DING Chuan-xian. Surface modification of titanium, titanium alloys, and related materials for biomedical applications[J]. Materials Science and Engineering, 2004, 47(3/4): 49-121.
[4] 刘 辉, 憨 勇. 医用多孔金属的制备及其生物活化研究进展[J]. 中国材料进展, 2012(5): 40-56.
LIU Hui, HAN Yong. Research progress on preparation and surface activation of porous biomedical metal materials[J]. Materials China, 2012(5): 40-56.
[5] 姜淑文, 齐 民. 生物医用多孔金属材料的研究进展[J]. 材料科学与工程, 2002, 20(4): 597-600.
JIANG Shu-wen, QI Min. Development of porous metals used as biomaterials[J]. Materials Science and Engineering, 2002, 20(4): 597-600.
[6] SYKARAS N, LACOPINO A M, MARKER V A, TRIPLETT R G, WOODY R D. Implant materials, designs and surface topographies: their effect on osseointegration. A literature review[J]. The International Journal of Oral & Maxillofacial Implants, 2000, 15(5): 675-690.
[7] PONSONNET L, REYBIER K, JAFFREZIC N, COMTE V, LAGNEAU C, LISSAC M, MARTELET C. Relationship between surface properties (Roughness, wettabillity) of titanium an titanium alloys and cell behaviour[J]. Materials Science & Engineering C, 2003, 23(4): 551-560.
[8] AKAO M, AOKI H, KATO K. Mechanical properties of sintered hydroxyapatite for prosthetic application[J]. Journal of Materials Science, 1981, 16(3): 809-812.
[9] ZHOU H, LEE J. Nanoscale hydroxyapatite particles for bone tissue engineering[J]. Acta Biomater, 2011, 7(7): 2769-2781.
[10] ANSELME K. Osteoblast adhesion on biomaterials[J]. Biomaterials, 2000, 21(7): 667-681.
[11] ZHUANG Z, FUJIMI T J, NAKAMURA M, KONISHI T, YOSHIMURA H, AIZAWA M. Development of a,b-plane-oriented hydroxyapatite ceramics as models for living bones and their cell adhesion behavior[J]. Acta Biomater, 2013, 9(5): 6732-6740.
[12] LEE J H, KIM H E, KOH Y H. Highly porous titanium (Ti) scaffolds with bioactive microporous hydroxyapatite/TiO2 hybrid coating layer[J]. Materials Letters, 2009, 63(23): 1995-1998.
[13] 徐淑华, 罗承萍, 王迎军. 羟基磷灰石生物涂层材料界面的电镜观察与分析[J]. 中国有色金属学报, 2001, 11(2): 190-194.
XU Shu-hua, LUO Cheng-ping, WANG Ying-jun. Electron microscopic study on interfacial characterization of hydroxyapatite biomaterial coating[J]. The Chinese Journal of Nonferrous Metals, 2001, 11(2): 190-194.
[14] 徐淑华, 罗承萍, 王迎军. 羟基磷灰石生物活性梯度涂层材料的界面特点[J]. 中国有色金属学报, 2002, 12(1): 163-167.
XU Shu-hua, LUO Cheng-ping, WANG Ying-jun. Interfacial characterization of hydroxyapatite Bioactive gradient coating[J]. The Chinese Journal of Nonferrous Metals, 2002, 12(1): 163-167.
[15] 寇宏超, 李金山, 徐广胜, 唐 斌, 王 军, 周 廉. 一种梯度多孔钛合金的制备方法[P]. 中国专利: 201310005574.3. 2013-01-08
KOU Hong-chao, LI Jin-shan, XU Guang-sheng, TANG Bin, WANG Jun, ZHOU Lian. A fabricated method of gradient porous titanium and titanium alloys[P]. China Patent: 201310005574.3. 2013-01-08.
[16] WITTE F, FISCHER J. In vitro and in vivo corrosion measurements of magnesium alloys[J]. Biomaterials, 2006, 27(7): 1013-1018.
(编辑 陈灿华)
基金项目:国家重点基础研究发展计划资助项目(2012CB619101)
收稿日期:2013-07-28;修订日期:2013-10-10
通信作者:寇宏超,副教授,博士;电话:029-88460568;E-mail:hchkou@nwpu.edu.cn