���±�ţ�1004-0609(2014)05-1375-08
�������������ٺ����������ѧ
��ΰ��1������ΰ1, 2
(1. ���ϴ�ѧ ұ���뻷��ѧԺ����ɳ 410083��
2. ���ϴ�ѧ ϡ�н���ұ��������Ʊ�����ʡ�ص�ʵ���ң���ɳ 410083)
ժ Ҫ��Ŀǰ��ұ����ҵ�㷺Ӧ�õij��ⷽ���ǻ����������������IJ��죬��Ը÷����д��ڵ��������������Ҽ۸�ߵ����⣬�����������P2S5��Ϊ��������ͨ����ˮ����������Ϊ������ṩ��Դ�����룬��������ѧ�Ƕȿ���P2S5��ˮ��Һ�е�ˮ����̼��١��������Ϊ�����������P2S5ˮ�������������Ҫ���������ͬʱ����pHֵ7~9����������Һ�У�n(S)/n(Mo)Ϊ8ʱ���������ʹ��Һ�е�MoO42-��ȫ��Ϊ������������WO42-����������������P2S5ˮ�������PO43-������ұ�������п������м�����ȥ����ˣ���������빤���У�P2S5������Ϊһ������Ч��������
�ؼ��ʣ��٣��⣻�����������ף����룻ˮ��ƽ�⣻������ѧ
��ͼ����ţ�TF801���� ���ױ�־�룺A
Thermodynamics of W and Mo sulfidation by using new sulfiding agent P2S5
ZHANG Wei-guang1, ZHAO Zhong-wei1,2
(1. School of Metallurgy and Environment, Central South University, Changsha 410083, China;
2. Hunan Key Laboratory for Metallurgy and Material Processing of Rare Metals,
Central South University, Changsha 410083, China)
Abstract: Currently, molybdenum is removed from tungstate solution by taking the advantage of different affinity towards S between W and Mo. Aiming at the problem of low sulfur content and high price of Mo sulfiding agent existing in tungsten extractive industry, we try to utilize the phosphorus pentasulfide as a new sulfiding agent and wish the generated HS- in the hydrolysis of P2S5 to provide the needed sulfur for Mo-sulfidation. Thus, the hydrolysis equilibrium of P2S5 in aqueous solution and thermodynamic behaviour of W amd Mo sulfidation were studied detail. The results show that the generated HS- in the hydrolysis of P2S5 can provide HS- for Mo-sulfidation. And, when n(S)/n(Mo) is 8 and the solution pH value is 7-9, MoO42- can be completely sulfurized to MoS42-, while tungsten still exists as WO42-. In addition, although the impurity PO43- is generated in the hydrolysis of P2S5, it can be removed easily and economically through the current technology in tungsten extractive industry. Therefore, P2S5 is expected to be a new efficient Mo sulfiding agent in the separation process of W and Mo.
Key words: tungsten; molybdenum; Mo-sulfidation agent; phosphorus pentasulfide; separation; hydrolysis equilibrium; sulfidation; thermodynamics
�������һֱ����������ȡұ��ļ������⡣һ�����������ٲ�Ʒ�������⺬����Ҫ�����ϸ���GB 10116-88����APT-0����Ʒ�������������������0.002%����һ���棬����ϵ������Ӱ�죬�١�������Ӱ뾶������ȣ�����ѧ����ʮ������[1-2]������Ԫ�ص���ȷ�����Ҫ����������������ѧ�����ϵ�ϸ���죬������ĵ���ѧ���ʿ�֪������������������ˣ�����ͨ������һ����������ʹ�������������������������Ȼ��WO42-��ʽ����[3]����������������������WO42-���ʵĽϴ���죬ͨ������������������ӽ��������ܼ���ȡ��������̿�������Լ�ѡ���Գ�����������������Һ�е���ѡ���Գ�ȥ��������������������������Ὣ����Һ��pHֵ������2.5~3.0����ʹ�����������������ȥ[4]�����ӽ������ܼ���ȡ�����ǻ��ڼ�炙�����������ǿ�ҵ�������ʹ����������������ȡ�����ӽ�����֬������ȡ���ϣ�ʵ���������Ч����[5-8]������̿�������ǻ��ڻ���̿���������ԣ�������������Һ�е�����������WO42-������������ [9-10]��ѡ���Գ�����������ijЩ����������������������������ã��������������Һ�г�ȥ[11-13]��������о�ʱ��ϳ���������Ϊ���죬�Ѿ�����ұ����ҵ�㷺Ӧ�ã���Ϊ��������[14-15]��
Ŀǰ����ұ����ҵ�еij������Ҫ�����������Һ�н��У�������Ϊ(NH4)2S��Һ��Ȼ����(NH4)2S��Һ��������Ϊ8%�����ҽϸߵļ۸��������������ijɱ�����ˣ����������ijɱ���Ϊ�ֽ����������̵Ĺؼ�[16]��
������ұ���Ƽ������߽����˴������������������о��������л�������CS2��SC(NH2)2[17]�������S��Ϊ����[18]����Щ������ҪNaOHǿ������Һ�ܽ���ټ������á�
P2S5�������ߴ�72%������Ƽۣ�P2S5�ļ۸����Ϊ(NH4)2S��Һ��1/5������ˮ��Һ����ˮ�⡣ͬʱ��Ϊһ�ֹ����Լ��������(NH4)2S��Һ���ӱ��������봢�档��ˣ���P2S5�ܹ���Ϊ��ʹ�ã�Ӧ�ÿ��Դ�������������ijɱ���ͬʱ��������õĹ�ҵӦ��ǰ��[19]��
Ϊ���о�P2S5��Ϊ�����Ŀ����ԣ��������߽�������ѧ�Ƕ�������P2S5��ˮ��Һ�е�ˮ��ƽ������Լ���Ϊ��ʱ���١��������Ϊ��
1 ����ѧ���ݵĹ��㼰����ѧƽ��ļ���
1.1 ����ѧ���ݵĹ���
����ȱ�����������ѧ���ݣ���ֱ�ӵó�P-S-H2Oϵ��ƽ�ⷴӦ��ƽ�ⳣ�����ڴˣ��������������������������ѧ���ݺ����������ܹ�ϵԭ���������PO3S3-��PO2S23-��POS33-��PS43-�����ɼ���˹������DfGQֵ���Ӷ��ó�P-S-H2Oϵ��ƽ�ⷴӦ��ƽ�ⳣ����������㷽�����¡�
��������SbO43-��SbS43-��DfGQֵ��
��֪H2S��S2-��H2O��DfGQ����ѧ���ݷֱ�Ϊ[20] -33.4��85.8��-237.14 kJ/mol���������·�Ӧ����ʽ������˹�ط���ʽ[21-22]��

 (1)
(1)

 (2)
(2)

 (3)
(3)

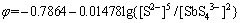 (4)
(4)
ͨ��DrGmQ=-zEQF�Լ�DrGmQ=-RTlnKaQ����ʽ�����Եõ�SbO43-��SbS43-��DfGQֵ�ֱ�Ϊ-596.84��-24.17 kJ/mol��EQΪԭ��صı��綯�ơ�
ͬʱ��ͨ������[23]���Եó���AsO3S3-��AsO2S23-��AsS3O3-��AsS43-��DfGQֵ�ֱ�Ϊ-275.08��-309.33��-138.33��30.39 kJ/mol����֪������ó���DfGQ���1���С�
��1 25 ��ʱ�ס��顢���������Ӽ����������ļ���˹����������ֵ
Table 1 DfGQ of MeO43-��MeO3S3-��MeO2S23-��MeOS33- and MeS43- (Me=P, As, Sb)

�ס��������ͬ����Ԫ�أ��������Լ�������ε����������������Ϻ��ס�����ͺ����ͬϵ���ӵļ���˹������ֵ֮��������Թ�ϵ(���������ܹ�ϵ���л�����ͬϵ�������й㷺����)[24-27]����ˣ���MeS43-��DfGQֵ��MeO43-��DfGQֵ��ͼ��3����һ��ֱ���ϣ���ͼ1��ʾ��������Եõ�PS43-��DfGQֵΪ393.61 kJ/mol��ͬʱ������������Լ���������ε�DfGQ�������μ���������ε�DfGQ��ͼ��5����ͬһ��ֱ���ϣ���ͼ2��ʾ���Ӷ��õ�PO3S3-��PO2S23-��PS3O3-��DfGQֵ�ֱ�Ϊ-238.54��-309.40��44.40 kJ/mol��

ͼ1 �ס��顢��ĺ������������������εļ���˹������ֵ���ͬϵ���Թ�ϵ
Fig. 1 Linear relation of DfGQ between MeO43- and MeS43- (Me=P, As, Sb)

ͼ2 ���������εĸ����������ļ���˹������ֵ���ͬϵ���Թ�ϵ
Fig. 2 Linear relation of DfGQ between P compounds and As compounds
1.2 �������ѧƽ��ļ���
��Me-S-H2O��ϵ�У���������ƽ��(Me=P��Mo�� W��n=2��3)��
 (5)
(5)
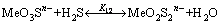 (6)
(6)
 (7)
(7)
 (8)
(8)
 (9)
(9)
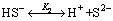 (10)
(10)
ʽ�У�KΪƽ�ⳣ�����ο���������pHֵ��Χֻ�������������ԣ�����������������������������ӵ�ˮ�ⷴӦ��
����������������Ӽ������������ӵ�DfGQֵ������ʽ(5)��(6)��(7)��(8)�����P-S-H2Oϵ��ƽ�ⷴӦ��ƽ�ⳣ���ֱ�Ϊ1��10-0.101��1��100.048��1��10-0.026��1��10-0.025��25 ��ʱ��Ӧʽ(5)~(10)��ƽ�ⳣ�����2��ʾ��
��2 25 ��ʱMe-S-H2Oϵ��ƽ�ⷴӦ��ƽ�ⳣ��
Table 2 Equilibrium constants of relevant reaction formulas at 25 ��

����ȱ�ٸ��й������ر��Ǻ������ӡ��������Ӽ��������ӵĻ��ϵ���������ڴˣ������о���Ũ�ȴ����ȡ�������ѧ���ۣ����Եó�������ѧ��ϵʽ��
 (11)
(11)
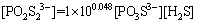 (12)
(12)
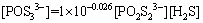 (13)
(13)
 (14)
(14)
 (15)
(15)
 (16)
(16)
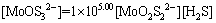 (17)
(17)
 (18)
(18)
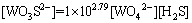 (19)
(19)
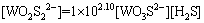 (20)
(20)
 (21)
(21)
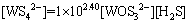 (22)
(22)
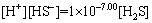 (23)
(23)
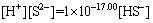 (24)
(24)
2 ���������
2.1 P2S5��ˮ��ƽ��
P2S5��ˮ��Һ�е�ˮ��ƽ�⣬�������غ㶨�ɿɵã�
 (25)
(25)

 (26)
(26)
�����ס����Ũ�ȼ���ϵ��pHֵ������ʽ(11)~(14)��ʽ(23)~(26)���ɵõ�1����8��δ֪���ķ����飬��˷�����ɵú������Ӽ��������ӵ�Ũ�ȡ���һ��ȡ�����ֵ���ɵõ��������Ӻͺ���������pHֵ�仯��Ũ�ȶ���ֵ�����������˽�ƽ��pHֵ����P2S5��ˮ��Һ��ˮ����̵�Ӱ�졣����ѧ����ȡ [S]=0.15 mol/L, ��������������P2S5���ṩ����������Ħ����1:2.5�����[P]=0.06 mol/L������ƽ��pHֵ����P2S5ˮ����Ϊ��Ӱ�졣
ͼ3��ʾΪƽ��pHֵ��P2S5ˮ����Ϊ��Ӱ�졣��ͼ3��֪��pHֵΪ7ʱ��P2S5ˮ�������������Ҫ��H2S��HS-��PO43-��Ũ�ȷֱ�Ϊ0.073��0.073��0.056 mol/L�����������������������ڡ�����pHֵ�����ߣ�H2S����ΪHS-����pHֵ����10ʱ��P2S5ˮ����������Ӽ���ȫ��ΪHS-��PO43-����ˣ���pHֵ7~14�ķ�Χ�ڣ�P2S5ˮ�Ⲣ��������������������������HS-�ṩ����������Ҫ����Դ����ΪP2S5��Ϊһ���µ������ṩ��ǿ����������ѧ֤������ȻP2S5ˮ���������PO43-�������������Һ�е�PO43-������ͨ���ɱ������������þ�η�����ȥ������Ѿ�������ѧ��������ҵʵ��������֤[1, 28]��

ͼ3 ƽ��pHֵ��P2S5ˮ����Ϊ��Ӱ��
Fig. 3 Effect of equilibrium pH value on hydrolysis of P2S5
2.2 P2S5Ϊ��ʱ���������Ϊ
2.2.1 ��-����ϵ
�ڵ�����-����ϵ�У�����P2S5��Ϊ��ʱ���������ѧ��Ϊ���������غ㶨�ɿ��Եó���

 (27)
(27)

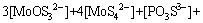
 (28)
(28)
�����ס��⡢���Ũ�ȼ���ϵ��pHֵ������ʽ(11)~(18)��ʽ(23)~(25)��ʽ(27)~(28)���ɵõ�1����13��δ֪���ķ����飬��˷�����ɵø��������ӵ�Ũ�ȣ���һ��ȡ�����ֵ���Ϳɵõ����������ӵ�Ũ�ȶ�������������P2S5��Ϊ��ʱ���������ѧ��Ϊ��ȡ[Mo]=3��10-3 mol/L��[S]=0.15 mol/L������P2S5������Ħ����1:2.5����[P]=6��10-2 mol/L���������������Ũ����pHֵ�仯������������ͼ4(a)��
ͬʱΪ�˿���P2S5��������������Ϊ��Ӱ�죬ȡ[Mo]=3��10-3 mol/L��pH=7.5��P2S5��������������Ħ�����������㣬�����ͼ5(a)��
��ͼ4(a)��ʾ����pH=14ʱ����Һ�к�������ȫ��ΪMoO42-��������ҺpHֵ�Ľ��ͣ�MoO42-����������������Ũ���������ߣ���pHֵΪ11~12ʱ��MoS42-Ũ�����������pH��9ʱ����Һ�е��⼸��ȫ����MoS42-����ʽ���ڣ�Ũ��ԼΪ3��10-3 mol/L����ˣ�������ҺpHֵ�Ľ��ͣ�MoO42-�����Ӹ�pHֵ��MoO42-Ϊ��Ҫ���Ӵ�����ʽ��ת��Ϊ��pHֵ��MoS42-Ϊ��Ҫ������ʽ���ڡ�
��ͼ5(a)��ʾ������P2S5������������MoO42-������n(S)/n(Mo)Ϊ4ʱMoO42-�Ѿ����������ڣ���ʱMoS42-��Ũ���Ѿ�������2.61��10-3 mol/L����n(S)/n(Mo)��8ʱ��MoS42-��Ũ�ȴﵽ3��10-3 mol/L����Һ�к��������Ѿ�ȫ����ΪMoS42-����ˣ�����P2S5������������MoO42-���ս�����ΪMoS42-��
����������֪��������������pHֵ��Χ��һ����P2S5�����������£���Һ�е���ᱻ��Ч����ΪMoS42-������Ϊ��Ľ�һ����ȥ��û�����

ͼ4 pHֵ�仯������������Ϊ��Ӱ��
Fig. 4 Effect of changing pH value on Mo (a) and W (b) sulfidation process
2.2.2 ��-����ϵ
�ڵ�����-����ϵ�У�����P2S5��Ϊ��ʱ�ٵ�������ѧ��Ϊ���������غ㶨�ɿ��Եó���
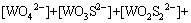
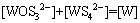 (29)
(29)

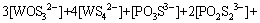
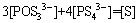 (30)
(30)
�����ס��١����Ũ�ȼ���ϵ��pHֵ������ʽ(11)~(18)��ʽ(23)~(25)��ʽ(29)~(30)���ɵõ�1����13��δ֪���ķ����飬��˷�����ɵø��������ӵ�Ũ�ȣ���һ��ȡ�����ֵ���Ϳɵõ����������ӵ�Ũ�ȶ��������������˽�P2S5Ϊ��ʱ�ٵ�������ѧ��Ϊ��
����ѧ����ȡ[W]=1 mol/L��[S]=0.15 mol/L������P2S5������Ħ����Ϊ1:2.5����[P]=6��10-2 mol/L���������������Ũ����pHֵ�仯������������ͼ4(b)��ͬʱ��Ϊ�˿���P2S5��������������Ϊ��Ӱ�죬ȡ[W]=1 mol/L��pH=7.5��P2S5����������-����ϵ��ͬ������[Mo]= 3��10-3 mol/L����Ħ�����������㣬�����ͼ5(b)��
��ͼ4(b)��ʾ����pHֵΪ7~14ʱ����Һ�еĺ���������Ҫ��WO42-����ʽ���ڡ����Ի���������ҺpHֵ�£��м�������WO42-��ΪWO3S2-������������������Ũ�Ȳ����ڣ�����pH�����ߣ�WO3S2-����ˮ�⣬�ڼ�����Һ��Χ���ټ���ȫ����WO42-��ʽ���ڡ�
��ͼ5(b)��ʾ��������P2S5���������췶Χ�ڣ���Һ��������WO42-Ϊ������n(S)/n(Mo)Ϊ8ʱ��WO42-Ũ��Ϊ0.99 mol/L�����������������������ڡ�����P2S5�����������࣬���ٲ��ֵ�WO42-���ᱻ����������n(S)/n(Mo)Ϊ50ʱ��WO42-Ũ�Ƚ���Ϊ0.86 mol/L��ͬʱ 0.14 mol/L ��WO3S2-���ɡ�
����������֪����ʹ������P2S5ʱ����Һ�к���������Ҫ����WO42-��ʽ���ڣ�ֻ�����������������£��Ż��к�Сһ���ֵ�WO42-����WO3S2-��

ͼ5 P2S5������������������Ϊ��Ӱ��
Fig. 5 Effect of P2S5 dosage on Mo (a) and W (b) sulfidation process
2.2.3 ��-��-����ϵ
�ں�����������Һ�У���P2S5Ϊ��ʱ�������غ㶨�ɿ��Եó���



 (31)
(31)
�������ס��⡢�١����Ũ�ȼ���ϵ��pHֵ������ʽ(11)~(25)��(27)��(29)��ʽ(31)���ɵõ�1����18��δ֪���ķ����飬��˷�����ɵú������Ӽ��������ӵ�Ũ�ȡ���һ��ȡ�����ֵ���Ϳɵõ��������Ӻͺ������ӵ�Ũ�ȶ���ֵ��
���չ�ҵ��ҺҪ��ȡ[Mo]=3��10-3 mol/L��[W]=1 mol/L��[S]=0.15 mol/L��[P]=6��10-2 mol/L��������������Һ��P2S5Ϊ��ʱpHֵ���⼰������Ϊ��Ӱ�죬�����ͼ6(a)��ͼ6(b)��
ͬʱΪ�˿�����������Һ��P2S5���������⼰������Ϊ��Ӱ�죬ȡ[Mo]=3��10-3 mol/L��[W]=1 mol/L��pH=7.5��P2S5��������������Ħ�����������㣬�����ͼ7(a)��ͼ7(b)��

ͼ6 ��������Һ��pHֵ�仯������������Ϊ��Ӱ��
Fig. 6 Effect of pH value on Mo (a) and W (b) sulfidation process in tungstate solution

ͼ7 ��������Һ��P2S5������������������Ϊ��Ӱ��
Fig. 7 Effect of changing P2S5 dosage on Mo (a) and W (b) sulfidation process in tungstate solution
��ͼ6(a)��ʾ����pHֵ����13ʱ����Һ�к���������ҪΪMoO42-��Ũ��Ϊ2.93��10-3 mol/L������pHֵ�Ľ��ͣ�MoO42-����������������Ũ���������ߣ���pHֵΪ11~12ʱ��MoS42-Ũ�������������ҺΪ���Լ�������(pH��9)����Һ�е�����Ҫ��MoS42-����ʽ���ڣ�Ũ��Ϊ2.84��10-3 mol/L��ͬʱ���ں�Сһ���ֵ�MoOS32-��Ũ��Ϊ0.15��10-3 mol/L��
��ͼ7(a)��ʾ������P2S5������������MoO42-������Ũ�����ͣ���n(S)/n(Mo)Ϊ8ʱ��MoO42-��ȫ��ת��Ϊ��������������������n(S)/n(Mo)Ϊ50ʱ����Һ����ҪΪMoS42-��Ũ�ȴﵽ2.84��10-3 mol/L��
��������Һ���������Ϊ����-����ϵ���������Ϊ������ͬ(ͼ4(a)��ͼ5(a))����������������pHֵ��Χ��һ����P2S5�����������£���������Һ�е��ⱻ��Ч����ΪMoS42-��
��ͼ6(b)��ʾ����pHֵΪ7~14ʱ����Һ�еĺ���������Ȼ��Ҫ��WO42-����ʽ���ڡ������Լ�������pHֵʱ���м�������WO42-��ΪWO3S2-������pH�����ߣ�WO3S2-����ˮ�⣬�ڼ�����Һ��Χ���ټ���ȫ����WO42-��ʽ���ڡ�
��ͼ7(b)��ʾ��������P2S5���������췶Χ�ڣ���Һ������Ҫ����WO42-Ϊ������n(S)/n(Mo)Ϊ8ʱ��WO42-Ũ��Ϊ0.99 mol/L�����������������������ڡ�����P2S5�����������࣬��С���ֵ�WO42-���ᱻ����������n(S)/n(Mo)Ϊ50ʱ�����м�С���ֵ�WO3S2-���ɣ�Ũ��Ϊ0.13 mol/L��
������������������Һ���ٵ�����Ϊ����-����ϵ���ٵ�����Ϊ������ͬ(ͼ4(b)��ͼ5(b))������������Һ������Ȼ��Ҫ����WO42-��ʽ���ڣ�����û�и����������������ɡ�
��ˣ�P2S5Ϊ��ʱ�������ʵ��������£���������Һ�����������ѡ���Եر���������ѧ��֤����P2S5��һ������Ч��������������õ�ʵ����������Һ���ȥ����
3 ����
1) ��pHֵ7~14��Χ��Һ�ڣ�P2S5����ˮ�⣬������HS-�ṩ����������Ҫ����Դ��
2) ʹ������P2S5ʱ����������Һ�У�n(S)/n(Mo)Ϊ8ʱ��P2S5ˮ�����ɵ������ʹ��������Һ�е�MoO42-��ȫ��Ϊ������������WO42-����������������ѧ��֤����P2S5 ��Ϊ����Ч���Ŀ����ԣ����Ը��õ�ʵ����������Һ�����ȥ����
3) ����ѧ���������P2S5ˮ�������Ҫ��PO43-����̬���ڣ����ǵ�Ŀǰ��ұ�����������ȥ���Ѿ����൱����Ĺ��ա���ˣ���������������빤ҵ��Ӧ�þ������õĹ�ҵӦ��ǰ����
REFERENCES
[1] ����, ��, �� ��. ��ұ��ѧ[M]. ��ɳ: ���ϴ�ѧ������, 2010: 211-228.
LI Hong-gui, YANG Jian-gao, LI Kun. Tungsten metallurgy[M]. Changsha: Central South University Press, 2010: 211-228.
[2] WIBERG E, WIBERG N, HOLLEMAN A F. Inorganic chemistry[M]. San Diego: Academic Press, 2001: 1386.
[3] ����. ϡ�н���ұ��ѧ[M]. ��ɳ: ���ϴ�ѧ������, 1990: 55-56.
LI Hong-gui. Rare metal metallurgy[M]. Beijing: Metallurgical Industry Press, 1990: 55-56.
[4] LASSNER E, SCHUBERT W D. Tungsten, properties, chemistry, technology of the element, alloys, and chemical compounds[M]. New York: Kluwer Academic/Plenum Publishers, 1999: 35-44.
[5] HUANG W, ZHANG Q, GONG B, HUANG S, LUO A. Production of pure ammonium tungstate by one-step removal of P, As, Si, Mo through ion-exchange[J]. Int J Refract Met Hard Mater, 1995, 13(4): 217-220.
[6] ��εׯ, ���ط�, ������. �ܼ���ȡ��������η�������[J]. �й���ɫ����ѧ��, 1995, 5(1): 45-47.
HUANG Wei-zhuang, GONG Bai-fan, ZHANG Qi-xiu. The separation of tungsten and molybdenum by solvent extraction of thiomolybdate[J]. The Chinese Journal of Nonferrous Metals, 1995, 5(1): 45-47.
[7] MACINNIS M, KIM T. Separation molybdenum values from an aqueous solution containing tungsten by solvent extraction: USA 4288413[P]. 1981-09-08.
[8] MACINNIS M, KIM T. Method for removing molybdenum from tungstate solution by solvent extraction: USA 4278642[P]. 1981-09-08.
[9] GONG B, HUANG W, ZHANG Q. A study on separation of molybdenum from tungsten by an adsorption process using activated carbon[J]. Int J Refract Met Hard Mater, 1996, 14(5/6): 319�C323.
[10] ZHAO Z, XIAO L, SUN F, HUO G, LI H. Study on removing Mo from tungstate solution by activated carbon loaded with copper[J]. Int J Refract Met Hard Mater, 2010, 28(4): 503-507.
[11] ����, ����÷, ����毣�����ΰ, ������, ������, ��ïʢ. ����������Һ�г������⡢�顢�ࡢ���ķ���: �й�ר��, ZL 97108113.1[P]. 1997-06-19.
LI Hong-gui, SUN Pei-mei, LI Yun-jiao, ZHAO Zhong-wei, HUO Guang-sheng, SU Peng-tuan, LIU Mao-sheng. The precipitation method for removing Mo, As, Sb and Sn from tungstate solution: China, ZL 97108113.1[P]. 1997-06-19.
[12] LI H, HUO G, SUN P, ZHAO Z, LI Y, SU P, LIU M. Developing new reagent for selectively precipitation of molybdenum from tungstate solution[J]. Trans. Nonferrous Metals Society of China, 2003, 13(1): 184-187.
[13] MINCZEWSKI J, CHWASTOWSKA J, DYBCZYNSKI R. Separation and preconcentration methods in inorganic trace analysis[M]. Chichester: Ellis Horwood Ltd, 1982: 40-61.
[14] ���ط�, ������. ������������η���������о�С��[J]. �й���ҵ, 1995, 10(8): 10-14.
GONG Bai-fan, ZHANG Qi-xiu. The research summary of tungsten-molybdenum separation based on the thiomolybdates[J]. China Tungsten Industry, 1995, 10(8): 10-14.
[15] ���ط�, ��εׯ. ��������Һ�������������������������о�[J]. ϡ�н�����Ӳ�ʺϽ�, 1987(1/2): 41-45.
GONG Bai-fan, HUANG Wei-zhuang. The research of generating thiomolybdate ions in the tungstate solution[J]. Rare Metals and Cemented Carbides, 1987(1/2): 41-45.
[16] ZHAO Z, ZHANG W, CHEN X, CAO C, LI J, LIU X. Study on removing Mo from tungstate solution using coprecipitation-adsorption method based on a novel Mo-sulfidation process[J]. Canadian Metallurgical Quarterly, 2013, 52(4): 358-363.
[17] ������, Ф����, ���ط�, ϯ����. ������������������Ʊ�����: �й�ר��, CN 1251825A[P]. 1998-10-20.
ZHANG Qi-xiu, XIAO Lian-sheng, GONG Bai-fan, XI Xiao-li. The preparation method of thiomolybdate for the separation of tungsten and molybdenum: China, CN 1251825A[P]. 1998-10-20.
[18] ������, ����Ӣ, Ф����. �������������Һ�з������õ�����������Ʊ�����: �й�ר��, CN 1413912A[P]. 2001-10-16.
ZHANG Qi-xiu, CAO Zuo-ying, XIAO Lian-sheng. The preparation method of thiomolybdate in the tungstate solution congtaining molybdenum: China, CN 1413912A[P]. 2001-10-16.
[19] ZHANG W, ZHAO Z, CHEN X. The behaviour of phosphorus impurities in the novel selective precipitation process[J]. Hydrometallurgy, 2013, 139: 111-115.
[20] SPEIGHT J. Lange��s handbook of chemistry[M]. New York: McGRAW-HILL, 2004: 1240-1261.
[21] ���ں�, ������. Sb2S3�������ѧ[J]. ����������ѧѧ��, 2000, 25(6): 49-53.
DENG Lun-hao, YANG Xian-wan. Thermodynamics for electro-slurry process of Sb2S3[J]. Journal of Kunming University of Science and Technology, 2000, 25(6): 49-53.
[22] ������, ʯ����. ��ұ��������ѧ[M]. ��ɳ: ���ϴ�ѧ������, 2006: 99-102.
ZHAO Rui-rong, SHI Xi-chang. Physical chemistry of Sb metallurgy[M]. Changsha: Central South University Press, 2006: 99-102.
[23] HELZ R, TOSSELL J. Thermodynamic model for arsenic speciation in sulfidic waters: A novel use of ab initio computations[J]. Geochimica et Cosmochimica Acta, 2008, 72(18): 4457-4468.
[24] BENSON S, BUSS J. Additivity rules for the estimation of molecular properties, thermodynamic properties[J]. J Chem Phys, 1958, 29(3): 546-572.
[25] ����ΰ, ������. Li-Mn-H2Oϵ����ѧ����[J]. �й���ɫ����ѧ��, 2004, 14(11): 1926-1933.
ZHAO Zhong-wei, HUO Guang-sheng. Thermodynamic analysis of Li-Mn-H2O system[J]. The Chinese Journal of Nonferrous Metals, 2004, 14(11): 1926-1933.
[26] ����ΰ, �����. Li-Fe-P-H2Oϵ����ѧ����[J]. �й���ɫ����ѧ��, 2006, 16(7): 1257-1263.
ZHAO Zhong-wei, LIU Xu-heng. Thermodynamic analysis of Li-Fe-P-H2O system[J]. The Chinese Journal of Nonferrous Metals, 2006, 16(7): 1257-1263.
[27] ����ΰ, ������, �����, ������, ������, ˾���, �°���. ����������ɸ±ˮ�������ѧ����[J]. �й���ɫ����ѧ��, 2013, 23(2): 559-567.
ZHAO Zhong-wei, LIANG Xin-xing, LIU Xu-heng, HE Li-hua, CHEN Xing-yu, SI Xiu-fen, CHEN Ai-liang. Thermodynamic analysis of Li-extraction from brine using FePO4 ion-sieve[J]. The Chinese Journal of Nonferrous Metals, 2013, 23(2): 559-567.
[28] ���ٷ�, ֣����, ���⸣. �����Ͻ���ϻ��չ����о�����������ѧ����[J]. �ɶ��Ƽ���ѧѧ��, 1985(2): 13-21.
PENG Shao-fang, ZHENG Chang-qiong, YIN Guang-fu. The thermodynamic analysis on eliminating phosphorus the process of the recovery of superalloy scrap[J]. Journal of Chengdu University of Science and Technology, 1985(2): 13-21.
(�༭ ������)
������Ŀ��������Ȼ��ѧ�����ص���Ŀ(51334008)
�ո����ڣ�2013-10-25�������ڣ�2014-01-05
ͨ�����ߣ�����ΰ�����ڣ���ʿ���绰��0731-88830476��E-mail��zhaozw@csu.edu.cn