加碳方式对磷酸铁锂动力学及电化学性能的影响
张 宝,彭春丽,王志兴,王云燕,李新海
(中南大学 冶金科学与工程学院,湖南 长沙,410083)
摘 要:以FeSO4?7H2O和NH4H2PO4为原料,以H2O2为氧化剂,通过液相沉淀法制得前驱体FePO4,然后通过碳热还原反应制得LiFePO4。采用2种加碳方式:方法一是先制得FePO4,然后加入乙炔黑混合后高温合成LiFePO4;方法二是先把乙炔黑分散在液相中,然后通过液相沉淀制得含碳的FePO4,再高温合成LiFePO4。研究结果表明:采用方法二合成的LiFePO4动力学及电化学性能比方法一合成的优。采用方法二所制备的LiFePO4样品以0.1C的倍率放电,其比容量达149 mA・h/g;当放电倍率为1C时,其比容量为124 mA・h/g,且循环性能良好。
关键词:锂离子电池;LiFePO4;交流阻抗;液相沉淀;碳热还原
中图分类号:TM912.9 文献标识码:A 文章编号:1672-7207(2007)05-0863-04
Effect of adding carbon modes on kinetic and electrochemical performances of LiFePO4
ZHANG Bao, PENG Chun-li, WANG Zhi-xing, WANG Yun-yan, LI Xin-hai
(School of Metallurgical Science and Engineering, Central South University, Changsha 410083, China)
Abstract: Two samples of LiFePO4 were synthesized with different adding carbon modes. In the first method, acetylene black was mixed with FePO4 which was prepared by aqueous precipitation of FePO4 from FeSO4?7H2O and NH4H2PO4 with hydrogen peroxide as oxidizing agent, then LiFePO4 was synthesized by carbothermal reduction. In the second method, acetylene black was mixed with FePO4 in liquid during the process of aqueous precipitation, and then LiFePO4 was synthesized with the same condition. The results show that the kinetic and electrochemical performances of LiFePO4 synthesized by the second method is better than those of the first one, which presents discharge capacity of 149 mA・h/g at 0.1C rate and 124 mA・h/g at 1C rate with satisfactory capacity retention.
Key words: lithium ion batteries; LiFePO4; alternating current impedance; aqueous precipitation; carbothermal reduction
橄榄石型LiFePO4作为一种新型的锂离子电池正极材料,具有资源丰富、价格便宜、无毒、对环境污染少、放电电压稳定、理论容量可达170 mA・h/g等优点,因而备受研究者的广泛关注[1-10]。然而,由于LiFePO4本身的电子导电率较低,高倍率放电时比容量降低等缺点使得其在实际应用中受到很大限制。如何提高LiFePO4的电子导电率,是改善其电化学性能特别是倍率性能的关键之一。通过研究发现,在其表面包覆碳材料[11-12]可以提高其导电性。
本文作者采用液相沉淀法制得前驱体FePO4,然后以乙炔黑作为碳源,通过碳热还原法合成表面包覆碳材料的LiFePO4。研究了2种不同的加碳方式对前驱体形貌及LiFePO4动力学性能和电化学性能的影响。
1 实 验
1.1 2种合成材料的方法
方法一:称取相同量的FeSO4?7H2O和NH4H2PO4,分别用去离子水溶解配成溶液。然后将这2种溶液混合加入反应器中,搅拌反应一段时间后加入H2O2,立即有大量的FePO4白色沉淀产生。反应完全后进行离心分离与洗涤,然后烘干。将原料按量比n(FePO4)? n(Li2CO3)?n(乙炔黑)=4?2?2.38混合研磨均匀,在Ar气保护下于560 ℃煅烧12 h,即可得到含碳的LiFePO4,记为样品S1。
方法二:称取相同量的FeSO4?7H2O和NH4H2PO4,分别用去离子水溶解配成溶液。然后将乙炔黑(按n(乙炔黑)?n(FeSO4?7H2O)=2.38?4)分散在盛有少量分散剂的反应器中,然后将FeSO4?7H2O和NH4H2PO4溶液加入反应器中,搅拌反应一段时间后加入H2O2,得到的沉淀经过离心分离与洗涤,然后烘干即可得到FePO4。将FePO4和Li2CO3按化学计量比混合均匀,在Ar气的保护下于560 ℃煅烧12 h,即可得到含碳的LiFePO4,记为样品S2。
1.2 仪器
采用美国SDT Q600型热分析,Ar气保护,升温速度为10 ℃/min,对前驱体进行热分析。采用SEM(JEOL,JSM-5600LV)在20 kV下对样品的表面形貌进行观察。采用CHI660A电化学工作站测量样品的交流阻抗。
1.3 电池组装和测试
将原料按质量比m(LiFePO4)?m(乙炔黑)? m(PVDF)=8?1?1混合均匀后涂片,经过120 ℃真空干燥10 h压片后得正极。以金属锂片作负极,1 mol/L LiPF6/(乙基纤维素EC +碳酸二甲酯DMC,体积比为1?1)为电解液,在手套箱里组装成CR2025型扣式电池。采用新威测试仪测试电池的充放电性能,在电压2.3~4.1 V范围内进行充放电实验。
2 结果与讨论
2.1 2种加碳方式对前驱体形貌的影响
图1所示为采用方法一制备的前驱体磷酸铁的热重-差热分析(TG-DTA)曲线。从DTA曲线中可以看到:在150 ℃左右出现明显的吸热峰,同时伴随着前驱体的质量损失,此峰应为前驱体失去结晶水的过程。而在580 ℃和710 ℃左右出现2个放热峰而又没有质量损失,这可能分别对应着磷酸铁从无定型转变为α晶型,及从α晶型转变为β晶型的2个过程。从TG曲线可以看到在20~400 ℃之间,前驱体质量损失率为20%,采用重铬酸钾滴定前驱体中Fe3+的含量,测得其含量为29.88%,该数据与文献[13]报道的FePO4具有2个结晶水相符合,即为FePO4?2H2O。
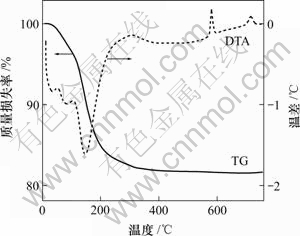
图1 方法一合成FePO4的TG-DTA曲线
Fig.1 TG- DTA curves for FePO4 synthesized by method 1
图2所示为采用不同方法合成前驱体FePO4的扫描电镜(SEM)照片。由图可见,采用方法一和二合成的前驱体颗粒均呈类球状,粒度分布均匀。采用方法二合成的颗粒更加细小(小于0.1 μm),同时也没有出现两相情况,且通过方法二合成的前驱体具有更大的比表面积,将有利于LiFePO4的合成。

(a) 方法一;(b) 方法二
图2 不同方法合成的FePO4的SEM照片
Fig.2 SEM images of FePO4 synthesized by different methods
2.2 2种加碳方式对LiFePO4交流阻抗性能的影响
图3所示为样品S1和S2在不同荷电状态下的交流阻抗图谱(其中,Z′为阻抗Z的实部;Z″为阻抗Z的虚部)。由图可见,每条曲线都由两部分组成:在高中频部分,是1个压缩的半圆,对应于发生在电解质/正极界面电荷传输反应引起的电化学阻抗;而在低频部分,是1条直线,对应于锂离子在正极界面的扩散引起的Warburg阻抗。通常电荷传输反应分为2步:锂离子在电极表面的吸附和吸附的锂离子嵌入材料的内部。随着放电的进行,材料的电化学反应阻抗逐渐变大,这可能是由于随着放电的进行,越来越多的锂离子嵌入到材料中去,锂离子之间的库仑斥力增大,电荷转移就越困难,因而阻抗增大。同时可以发现,在相同荷电条件下,样品S2比样品S1的电化学阻抗明显偏小。
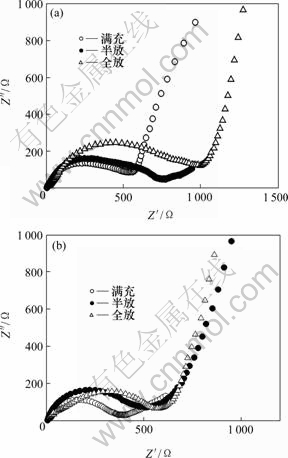
(a) 样品S1;(b) 样品S2
图3 样品S1在不同荷电状态下的交流阻抗图谱
Fig.3 Electrochemical impedance spectra of samples S1 and S2 under different depths of discharge
为了进一步观察电极在循环过程中电化学阻抗的变化情况,测试了样品S2循环3次和30次后的电极在满充态条件下的交流阻抗,结果如图4所示。可以看出,样品循环3次和30次后的阻抗变化不大,说明样品的电化学性能良好,随循环次数的增加,电化学阻抗改变比较小。

图4 样品S2循环3次和30次后的交流阻抗图谱
Fig.4 Electrochemical impedance spectra of sample S2 cycling after 3 and 30 cycles
2.3 2种加碳方式对LiFePO4电化学性能的影响
图5所示为样品S1和S2以0.1C倍率充放电时的首次充放电曲线。由图可见,其库仑效率均为100%。其中,样品S2的比容量为149 mA・h/g,而样品S1只有134 mA・h/g。当放电倍率达到1C时(见图6),样品S2的比容量为124 mA・h/g,放电平台为3.33 V,其效率为100%,而样品S1则只有91 mA・h/g,其放电电位远低于样品S2的放电电位,且无明显的放电平台,效率也仅为77.8%。从而可以看出方法二所合成的材料其大电流充放电性能比较好。
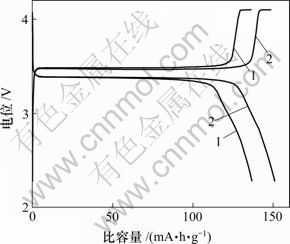
1―样品S1; 2―样品S2
图5 不同方法合成的LiFePO4在0.1C倍率下的首次充放电曲线
Fig.5 First charge-discharge curves of LiFePO4 synthesized by different methods recorded at 0.1C

1―样品S1; 2―样品S2
图6 不同方法合成的LiFePO4在1C倍率下的首次充放电曲线
Fig.6 First charge-discharge curves of LiFePO4 synthesized by different methods recorded at 1C
图7所示为采用方法二合成的LiFePO4分别以0.5C和1C倍率充放电时的循环性能图。以0.5C倍率放电时,第1次及第30次循环的比容量分别为134.8 mA・h/g和134.5 mA・h/g,而以1C倍率放电时,其比容量分别为124 mA・h/g和125.8 mA・h/g,说明所合成的材料具有良好的大电流充放电循环性能。

图7 样品S2以不同倍率放电时的循环性能曲线
Fig.7 Electrochemical cycling performance of sample S2 discharging at different rates
3 结 论
a. 通过碳热还原法,采用2种不同的加碳方式分别合成了LiFePO4。
b. 采用方法二合成的前驱体FePO4的颗粒明显比方法一合成的粒径小,其平均粒径小于0.1 μm;采用方法二合成的LiFePO4电化学阻抗小,而且循环30次后,电化学阻抗变化不大。通过方法二所合成的LiFePO4电化学性能好,以0.1C倍率放电时,比容量达149 mA・h/g,以1C倍率放电时,比容量达124 mA・h/g,且循环性能良好。
参考文献:
[1] Yang S, Zavalij P Y, Whittingham M S. Hydrothermal synthesis of lithium iron phosphate cathodes[J]. Electrochemistry Communications, 2001,148(3): 505-508.
[2] Hu H Q, Doeff M M, Kostecki R, et al. Electrochemical performance of sol-gel synthesized LiFePO4 in lithium batteries[J]. J Electrochem Soc, 2004, 151(8): A1279-A1285.
[3] Huang H, Cyin S, Nazar L F. Approaching theoretical capacity of LiFePO4 at room temperature at high rates[J]. Electrochemical and Solid State Letters, 2001, 4(10): A170-A172.
[4] Padhi A K, Nanjundaswamy K S, Goodenough J B. Phospho-olivines as positive-electrode materials for rechargeable lithium batteries[J]. J Electrochem Soc, 1997, 144(4): 1188-1194.
[5] Macneil D D, Lu Z, Chen Z, et al. A comparison of electrode/electrolyte reaction at elevated temperature for various Li-ion battery cathodes[J]. J Power Sources, 2002, 108: 8-14.
[6] Croce F, Epifanio A D, Hassoun J, et al. A novel concept for the synthesis of improved LiFePO4 lithium battery cathode[J]. Electrochemical and Solid-State Letters, 2002, 5(3): 47-50.
[7] Takahashi M, Tobishima S I, Takei K, et al. Characterization of LiFePO4 as the cathode material for rechargeable lithium batteries[J]. J Power Sources, 2001, 97-98: 508-511.
[8] 朱 伟, 樊小勇, 胡 杰, 等. LiFePO4的制备及其电化学性能研究[J]. 功能材料, 2004, 35(6): 734-736.
ZHU Wei, FAN Xiao-yong, HU Jie, et al. Preparation and electrochemical performance of LiFePO4[J]. Journal of Function Materials, 2004, 35(6): 734-736.
[9] Zhou F, Kang K, Maxisch T, et al. The electronic structure and band gap of LiFePO4 and LiMnPO4[J]. Solid State Communications, 2004, 132(3/4): 181-186.
[10] Zane D, Carewska M, Scacia S, et al. Factor affecting rate performance of undoped LiFePO4[J]. Electrochimica Acta, 2004, 49(25): 4259-4271.
[11] 朱炳权, 李新海, 张 宝, 等. 改进的碳热还原法制备正极材料LiFePO4/C[J]. 电池, 2005, 35(6): 445-447.
ZHU Bing-quan, LI Xin-hai, ZHANG Bao, et al. Synthesis of LiFePO4/C cathode material by modified carbothermal method[J]. Battery Bimonthly, 2005, 35(6): 445-447.
[12] 吕正中, 周震涛. LiFePO4/C复合正极材料的结构与性能[J]. 电池, 2003, 33(5): 269-271.
LU Zheng-zhong, ZHOU Zhen-tao. Structure and performance of LiFePO4/C composite as cathode materials[J]. Battery Bimonthly, 2003, 33(5): 269-271.
[13] Scaccia S, Carewska M, Wisniewski P, et al. Morphological investigation of sub-micron FePO4 and LiFePO4 particles for rechargeable lithium batteries[J]. Materials Research Bulletin, 2003, 38: 1155-1163.
收稿日期:2006-12-26;修回日期:2007-02-05
基金项目:国家自然科学基金资助项目(50302016)
作者简介:张 宝(1971-),男,江苏盱眙人,博士后,从事材料及电化学领域的研究
通信作者:张 宝,男,博士后;电话:0731-8836357;E-mail: zhangbaovip@163.com