采用复盐法脱除工业废水中的硫酸根
王海鹰,彭小玉,王云燕,柴立元,舒余德
(中南大学 冶金科学与工程学院,湖南 长沙,410083)
摘 要:以水合铝盐及石灰乳为脱除剂,采用实验室自行配制的模拟废水,对工业废水中高浓度硫酸根的脱除进行研究。考察溶液pH值、铝盐加入量、反应时间、 初始浓度以及反应温度等因素对硫酸根去除率的影响,并设计三因素三水平正交实验。得出单因素和正交实验确定的最佳工艺条件为:反应温度25 ℃,反应时间60 min,溶液pH值11.0,
初始浓度以及反应温度等因素对硫酸根去除率的影响,并设计三因素三水平正交实验。得出单因素和正交实验确定的最佳工艺条件为:反应温度25 ℃,反应时间60 min,溶液pH值11.0, 与Al3+的物质的量比为1.1?1.0,且各因素影响程度由大至小的顺序为:溶液pH值、铝盐加入量、反应时间;在最佳工艺条件下,硫酸根离子质量浓度由1 720 mg/L降至100 mg/L以下,达到生活饮用水卫生标准。沉淀物XRD检测结果表明:其主要物相为钙矾石(Ca6Al2(SO4)3(OH)12?26H2O)。
与Al3+的物质的量比为1.1?1.0,且各因素影响程度由大至小的顺序为:溶液pH值、铝盐加入量、反应时间;在最佳工艺条件下,硫酸根离子质量浓度由1 720 mg/L降至100 mg/L以下,达到生活饮用水卫生标准。沉淀物XRD检测结果表明:其主要物相为钙矾石(Ca6Al2(SO4)3(OH)12?26H2O)。
关键词:铝盐;复盐沉淀;工业废水;硫酸根
中图分类号:X703.1 文献标志码:A 文章编号:1672-7207(2010)02-0434-06
Removal of sulfate from industry wastewater by double salt method
WANG Hai-ying, PENG Xiao-yu, WANG Yun-yan, CHAI Li-yuan, SHU Yu-de
(School of Metallurgical Science and Engineering, Central South University, Changsha 410083, China)
Abstract: Removal of sulfate from industry wastewater containing sulfate with high concentration were studied using hydrated aluminum salt and lime milk as remover. The effects of solution pH value, aluminum salt dosage, reaction time, initial concentration of  and reaction temperature on the removal of
and reaction temperature on the removal of  were also investigated, and three factors and three levels orthogonal experiments were designed. The results determined by single factor and orthogonal experiments indicate that the optimum conditions for the removal of sulfate are as follows: reaction temperature is 25 ℃, reaction time is 60 min, pH value of solution is 11, the molar ratio of sulfate to aluminum is 1.1?1.0, and the influencing sequence of each factor from large to small is solution pH value, aluminum salt dosage, reaction time. By comparison between the wastewater and the purified water, the sulfate concentration decreased sharply from 1 720 mg/L to 100 mg/L or below under the optimum conditions, which is less than hygienic standard for drinking water. The X-ray diffraction pattern of the precipitation shows that the main composition of the solid phase is ettringite (Ca6Al2(SO4)3(OH)12?26H2O).
were also investigated, and three factors and three levels orthogonal experiments were designed. The results determined by single factor and orthogonal experiments indicate that the optimum conditions for the removal of sulfate are as follows: reaction temperature is 25 ℃, reaction time is 60 min, pH value of solution is 11, the molar ratio of sulfate to aluminum is 1.1?1.0, and the influencing sequence of each factor from large to small is solution pH value, aluminum salt dosage, reaction time. By comparison between the wastewater and the purified water, the sulfate concentration decreased sharply from 1 720 mg/L to 100 mg/L or below under the optimum conditions, which is less than hygienic standard for drinking water. The X-ray diffraction pattern of the precipitation shows that the main composition of the solid phase is ettringite (Ca6Al2(SO4)3(OH)12?26H2O).
Key words: aluminum salt; double salt precipitation; industry wastewater; sulfate ion
高浓度硫酸盐废水大量存在于矿山、冶金、食品及医药等行业中[1],这些废水不经处理直接排入水体,将会产生一系列危害[2-5],如:过量的硫酸根可使水体产生恶臭,影响水的感官性状及其使用;过量的硫酸根不利于作物生长,使土地盐渍化;含有硫酸盐的饮用水有苦涩味,并有致泻作用,如长期饮用,将引起腹泻和消化不良等症状。因此,水中硫酸根脱除研究越来越引起人们的关注。目前,比较成熟的脱除硫酸根的方法主要有BaCl2法、CaCl2法、冷冻法及生物 法[6-10]。BaCl2法是工业应用最广泛的化学除 方法,其工艺操作简单,去除效果好,但BaCl2有较强的毒性,贮存条件要求高,使用成本高[11]。采用CaCl2法时,由于硫酸钙的溶度积(9.1×10-6)较大,去除
方法,其工艺操作简单,去除效果好,但BaCl2有较强的毒性,贮存条件要求高,使用成本高[11]。采用CaCl2法时,由于硫酸钙的溶度积(9.1×10-6)较大,去除 的效果比氯化钡法差。采用冷冻法能耗相当大,目前工业上应用很少见。采用生物法处理含硫酸盐废水具有成本低、适用性强、无二次污染等优点[12],但启动时间较长、处理速度慢、效率低、有机物消耗量大[1]。近几年,人们开发出了离子交换法、膜分离法及吸附法等[10, 13],其中,离子交换法具有吸附和脱附速度快、操作方便等优点。膜分离法是由加拿大Kvaerner chenetics公司开发的一种新型脱除硫酸根离子的技术,可以有效地从盐水溶液单价阴离子Cl-中分离出
的效果比氯化钡法差。采用冷冻法能耗相当大,目前工业上应用很少见。采用生物法处理含硫酸盐废水具有成本低、适用性强、无二次污染等优点[12],但启动时间较长、处理速度慢、效率低、有机物消耗量大[1]。近几年,人们开发出了离子交换法、膜分离法及吸附法等[10, 13],其中,离子交换法具有吸附和脱附速度快、操作方便等优点。膜分离法是由加拿大Kvaerner chenetics公司开发的一种新型脱除硫酸根离子的技术,可以有效地从盐水溶液单价阴离子Cl-中分离出 ,具有硫酸根脱除率高、操作简便、成本较低等特点。目前,这些方法主要应用于氯碱生产过程中盐水中硫酸根脱除,而它们在工业废水处理领域的应用还有待进一步研究。此外,也有采用针铁矿、柱撑蒙脱石、焙烧水滑石等吸附去除水中硫酸根离子的文献报道[14-16],但此类方法受溶液pH值、操作温度等因素影响较大,且成本较高,尚处于实验研究阶段。因此,有必要开发一种有效的硫酸根脱除方法。有研究报道
,具有硫酸根脱除率高、操作简便、成本较低等特点。目前,这些方法主要应用于氯碱生产过程中盐水中硫酸根脱除,而它们在工业废水处理领域的应用还有待进一步研究。此外,也有采用针铁矿、柱撑蒙脱石、焙烧水滑石等吸附去除水中硫酸根离子的文献报道[14-16],但此类方法受溶液pH值、操作温度等因素影响较大,且成本较高,尚处于实验研究阶段。因此,有必要开发一种有效的硫酸根脱除方法。有研究报道 能与Ca2+和Al3+在一定条件下形成复合物硫酸钙铝沉淀(Al2Ca3(SO4)6)[17-18]。基于这种原理,本研究以水合硝酸铝及氢氧化钙为脱除剂,脱除重金属废水中的硫酸根。探讨铝盐加入量、溶液pH值、反应时间、反应温度及
能与Ca2+和Al3+在一定条件下形成复合物硫酸钙铝沉淀(Al2Ca3(SO4)6)[17-18]。基于这种原理,本研究以水合硝酸铝及氢氧化钙为脱除剂,脱除重金属废水中的硫酸根。探讨铝盐加入量、溶液pH值、反应时间、反应温度及 初始浓度等因素对
初始浓度等因素对 脱除效果的影响,旨在为工业废水中硫酸根的脱除开辟一条新途径。
脱除效果的影响,旨在为工业废水中硫酸根的脱除开辟一条新途径。
1 实验
1.1 主要仪器及试剂
主要仪器:PHS-3C精密pH计;AUY220型电子分析天平;HJ-6多头磁力加热搅拌器;HH-601恒温数显水浴;SHZ-CD型循环水式多用真空泵。
主要试剂:Na2SO4(分析纯);CaSO4・2H2O(分析纯);Al(NO3)3・9H2O(分析纯);Ca(OH)2(分析纯);NaOH(优级纯);盐酸联苯胺(分析纯);酚酞(指示剂);超纯水(电导率为5.47×10-4 S/m)。
1.2 实验方法
有色冶炼废水经中和水解及脱钙工序处理后,溶液中Ca2+,Na+及 的质量浓度分别为300,220,1 720 mg/L,故采用分析纯CaSO4・2H2O和无水Na2SO4,配制成
的质量浓度分别为300,220,1 720 mg/L,故采用分析纯CaSO4・2H2O和无水Na2SO4,配制成 质量浓度为1 720 mg/L的溶液,作
质量浓度为1 720 mg/L的溶液,作 脱除的实验溶液。实验时准确称取1.29 g CaSO4・2H2O和1.479 g无水Na2SO4,置入250 mL烧杯中,加入200 mL超纯水搅拌溶解,且微微加热,溶解后转入1 L 容量瓶定容以备用。每次实验取100 mL溶液置于三角瓶中,再加入一定量铝盐,用Ca(OH)2调节溶液pH值,搅拌一定时间,沉淀过滤,取滤液分析其中
脱除的实验溶液。实验时准确称取1.29 g CaSO4・2H2O和1.479 g无水Na2SO4,置入250 mL烧杯中,加入200 mL超纯水搅拌溶解,且微微加热,溶解后转入1 L 容量瓶定容以备用。每次实验取100 mL溶液置于三角瓶中,再加入一定量铝盐,用Ca(OH)2调节溶液pH值,搅拌一定时间,沉淀过滤,取滤液分析其中 残余量。
残余量。
1.3 分析方法
硫酸根离子浓度采用酸碱滴定法测定[19]。在盐酸联苯胺的冷溶液中,加入含有硫酸盐的中性溶液,生成不溶性的硫酸联苯胺沉淀,反应式如下:
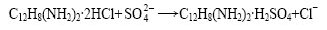
沉淀静置10~15 min后,真空过滤、洗涤,置于50 ℃以上的热水中水解为游离硫酸和联苯胺:

以酚酞为指示剂,用标定后的NaOH标准溶液滴定,反应终点为无色变为微红色。
2 结果与讨论
2.1 pH值对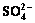 脱除的影响
脱除的影响
分别取100 mL初始质量浓度为1 720 mg/L的 溶液置于8个三角瓶中,铝盐加入量为1.4 g,反应温度为25 ℃,用石灰乳调节至不同的pH值,搅拌90 min,沉淀、过滤,取滤液分析其中
溶液置于8个三角瓶中,铝盐加入量为1.4 g,反应温度为25 ℃,用石灰乳调节至不同的pH值,搅拌90 min,沉淀、过滤,取滤液分析其中 含量。结果如图1所示。
含量。结果如图1所示。
 去除率明显依赖于溶液的pH值。当溶液pH≤10.0时,
去除率明显依赖于溶液的pH值。当溶液pH≤10.0时, 去除率小于43.4%,
去除率小于43.4%, 残留质量浓度大于970 mg/L;当pH值为10.0~10.5时,
残留质量浓度大于970 mg/L;当pH值为10.0~10.5时, 去除率随pH值升高迅速提高,从pH=10.0的43.6%提高到pH=10.5的90.5%,当pH≥10.5时,随着pH值增大,
去除率随pH值升高迅速提高,从pH=10.0的43.6%提高到pH=10.5的90.5%,当pH≥10.5时,随着pH值增大, 去除率变化不明显,维持在90%~96%,
去除率变化不明显,维持在90%~96%, 残留质量浓度低于100 mg/L。由此可见:复盐沉淀法去除
残留质量浓度低于100 mg/L。由此可见:复盐沉淀法去除 的有效pH值应大于10.5。
的有效pH值应大于10.5。
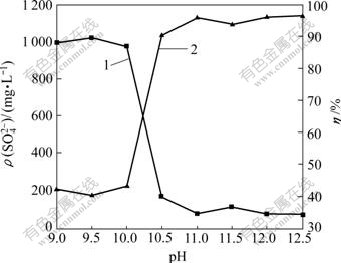
1―ρ( )与pH值的关系;2―η与pH值的关系
)与pH值的关系;2―η与pH值的关系
图1 pH值对 去除率η及其残留质量浓度ρ(
去除率η及其残留质量浓度ρ( )的影响
)的影响
Fig.1 Effects of pH values on removal ratio and residual concentration of sulfate
2.2 硝酸铝加入量对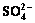 脱除的影响
脱除的影响
 初始质量浓度为1 720 mg/L,溶液体积为100 mL,反应温度为25 ℃。加入不同量的铝盐,用石灰乳调pH值至12.0,搅拌90 min,结果如图2所示。从图2可见:当铝盐加入量小于0.62 g时,
初始质量浓度为1 720 mg/L,溶液体积为100 mL,反应温度为25 ℃。加入不同量的铝盐,用石灰乳调pH值至12.0,搅拌90 min,结果如图2所示。从图2可见:当铝盐加入量小于0.62 g时, 去除率随着铝盐加入量的增大基本呈直线上升,表明此时Al3+的投加量不够,
去除率随着铝盐加入量的增大基本呈直线上升,表明此时Al3+的投加量不够, 的去除率取决于Al3+投加量,要提高
的去除率取决于Al3+投加量,要提高 的去除率,需增加Al3+投加量;当铝盐加入量增大到0.62 g时,
的去除率,需增加Al3+投加量;当铝盐加入量增大到0.62 g时, 去除率达到95.6%,
去除率达到95.6%, 残留质量浓度为 75.6 mg/L;继续增大铝盐加入量,
残留质量浓度为 75.6 mg/L;继续增大铝盐加入量, 去除率基本保持不变,维持在96%左右,说明此时Al3+投加量已基本满足沉淀
去除率基本保持不变,维持在96%左右,说明此时Al3+投加量已基本满足沉淀 的需求,再继续投加Al3+,
的需求,再继续投加Al3+, 去除率增加已不明显。由Al3+投加量0.62 g对应的残留质量浓度可计算出,27 mg Al3+可以去除99.4 mg
去除率增加已不明显。由Al3+投加量0.62 g对应的残留质量浓度可计算出,27 mg Al3+可以去除99.4 mg  ,与理论计算相比多消耗17.66 mg Al3+。这说明加入体系中的Al3+只有部分用于形成硫酸钙铝复合物沉淀。
,与理论计算相比多消耗17.66 mg Al3+。这说明加入体系中的Al3+只有部分用于形成硫酸钙铝复合物沉淀。

1―ρ( )与铝盐加入量的关系;2―η与铝盐加入量的关系
)与铝盐加入量的关系;2―η与铝盐加入量的关系
图2 铝盐加入量对 去除率及其残留质量浓度的影响
去除率及其残留质量浓度的影响
Fig.2 Effects of aluminum salt dosage on removal ratio and residual concentration of sulfate
2.3 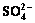 初始质量浓度对
初始质量浓度对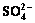 脱除的影响
脱除的影响
取100 mL浓度不同的 溶液,反应温度为25 ℃,
溶液,反应温度为25 ℃, 与Al3+物质的量为1.1?1.0,用石灰乳调pH值至12.0左右,搅拌90 min,研究
与Al3+物质的量为1.1?1.0,用石灰乳调pH值至12.0左右,搅拌90 min,研究 初始质量浓度对去除率的影响,结果如图3所示。
初始质量浓度对去除率的影响,结果如图3所示。
由图3可见:当 初始质量浓度低于1 300 mg/L时,
初始质量浓度低于1 300 mg/L时, 去除率随其初始质量浓度的增加而增大;当
去除率随其初始质量浓度的增加而增大;当 初始质量浓度高于1 300 mg/L时,对
初始质量浓度高于1 300 mg/L时,对 去除率无明显影响,保持在94%~96%之间。其原因是
去除率无明显影响,保持在94%~96%之间。其原因是 初始质量浓度高,Ca2+,Al3+和
初始质量浓度高,Ca2+,Al3+和 三者碰撞机会多,硫酸钙铝晶核容易形成,且大量硫酸钙铝在沉降过程中会吸附部分
三者碰撞机会多,硫酸钙铝晶核容易形成,且大量硫酸钙铝在沉降过程中会吸附部分 ,使
,使 去除率增大。由图3还可以看出:当溶液
去除率增大。由图3还可以看出:当溶液 初始质量浓度高于 1 300 mg/L时,经本方法处理后,出水
初始质量浓度高于 1 300 mg/L时,经本方法处理后,出水 质量浓度低于100 mg/L,达到生活饮用水卫生标准。
质量浓度低于100 mg/L,达到生活饮用水卫生标准。

图3  初始质量浓度ρ0(
初始质量浓度ρ0( )对
)对 脱除率的影响
脱除率的影响
Fig.3 Effect of initial concentration of sulfate ion on removal of sulfate
2.4 反应时间对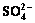 脱除的影响
脱除的影响
在6个三角瓶中,分别取100 mL初始质量浓度为1 720 mg/L的  溶液,加入0.62 g铝盐,加入1.3 g Ca(OH)2调pH值至12.0左右,反应温度为25 ℃。搅拌不同时间后,沉淀、过滤,取滤液分析
溶液,加入0.62 g铝盐,加入1.3 g Ca(OH)2调pH值至12.0左右,反应温度为25 ℃。搅拌不同时间后,沉淀、过滤,取滤液分析 含量,结果如图4所示。由图4可见:当搅拌时间小于60 min时,
含量,结果如图4所示。由图4可见:当搅拌时间小于60 min时, 去除率随着搅拌时间的增长而提高,从搅拌20 min的76.8%增至搅拌60 min的95.4%;当搅拌时间达到60 min后,再增加搅拌时间,
去除率随着搅拌时间的增长而提高,从搅拌20 min的76.8%增至搅拌60 min的95.4%;当搅拌时间达到60 min后,再增加搅拌时间, 去除率无明显变化,基本维持在96%左右,
去除率无明显变化,基本维持在96%左右, 残留质量浓度约为70 mg/L,说明搅拌时间为60 min时反应基本达到平衡。可见,复盐法脱除
残留质量浓度约为70 mg/L,说明搅拌时间为60 min时反应基本达到平衡。可见,复盐法脱除 最佳反应时间为60 min。
最佳反应时间为60 min。
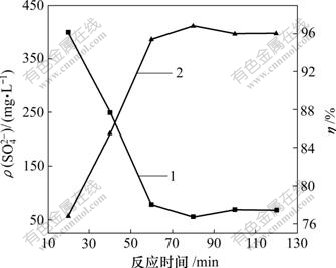
1―ρ( )与反应时间的关系;2―η与反应时间的关系
)与反应时间的关系;2―η与反应时间的关系
图4 反应时间对 去除率及其残留质量浓度的影响
去除率及其残留质量浓度的影响
Fig.4 Effects of reaction time on removal ratio and residual concentration of sulfate
2.5 反应温度对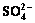 脱除的影响
脱除的影响
反应所需温度是决定本方法是否适用于实际工程的重要因素之一。取100 mL初始质量浓度为1 720 mg/L的 溶液,置入三角瓶中,加入0.62 g铝盐;用0.40 g Ca(OH)2调pH值为11.0~12.0,搅拌60 min,考察反应温度对
溶液,置入三角瓶中,加入0.62 g铝盐;用0.40 g Ca(OH)2调pH值为11.0~12.0,搅拌60 min,考察反应温度对 去除率的影响,实验结果如图5所示。
去除率的影响,实验结果如图5所示。
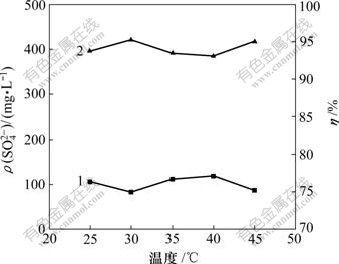
1―ρ( )与温度的关系;2―η与温度的关系
)与温度的关系;2―η与温度的关系
图5 反应温度对 去除率及其残留质量浓度的影响
去除率及其残留质量浓度的影响
Fig.5 Effects of reaction temperature on removal ratio and residual concentration of sulfate
由图5可见:在反应温度在25~45 ℃时, 去除率无明显变化,保持在93%~95%。可见:在常温条件下,用复盐沉淀法能有效地去除溶液中硫酸根离子。
去除率无明显变化,保持在93%~95%。可见:在常温条件下,用复盐沉淀法能有效地去除溶液中硫酸根离子。
2.6 正交实验
为了分清影响因素的主次,选择各因素的最优水平,根据单因素条件实验结果,采用三因素三水平正交设计表进行正交实验,并对实验结果数据进行极差分析,结果如表1所示。
表1 正交实验结果及极差分析
Table 1 Results of orthogonal experiment and range analysis
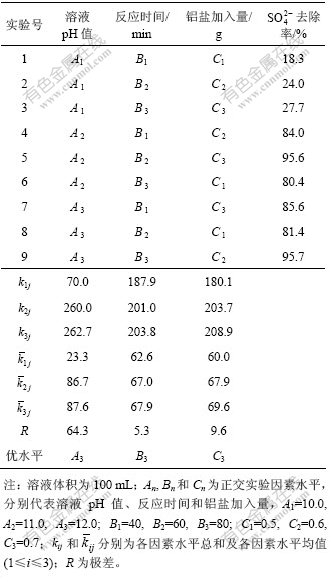
根据各因素极差的大小可以判断因素重要性顺序。表1中极差表明:pH值是影响 脱除的重要因素,当pH值大于11.0时,
脱除的重要因素,当pH值大于11.0时, 可以脱除到100 mg/L左右,但随着pH值降低,
可以脱除到100 mg/L左右,但随着pH值降低, 残余浓度增加,脱除率降低;当pH值为10.0时,
残余浓度增加,脱除率降低;当pH值为10.0时, 只能脱除到1 200 mg/L。极差表明反应时间和铝盐加入量对
只能脱除到1 200 mg/L。极差表明反应时间和铝盐加入量对 脱除未表现出明显的影响,各因素对
脱除未表现出明显的影响,各因素对 去除率影响由大至小的顺序依次为:溶液pH值、铝盐加入量、反应时间。较优水平组合为A3B3C3,即最佳工艺条件为:溶液pH值为12.0,反应时间为80 min,铝盐加入量为0.7 g。但由于溶液pH值为11.0和12.0时,
去除率影响由大至小的顺序依次为:溶液pH值、铝盐加入量、反应时间。较优水平组合为A3B3C3,即最佳工艺条件为:溶液pH值为12.0,反应时间为80 min,铝盐加入量为0.7 g。但由于溶液pH值为11.0和12.0时, 脱除率相差较小,且考虑到成本问题,确定实际工艺条件如下:溶液pH值为11.0,反应时间为60 min,硝酸铝加入量为0.6 g。
脱除率相差较小,且考虑到成本问题,确定实际工艺条件如下:溶液pH值为11.0,反应时间为60 min,硝酸铝加入量为0.6 g。
2.7 固相XRD分析
实验条件: 初始质量浓度为1 720 mg/L,溶液体积为100 mL,反应温度为25 ℃。加入铝盐的量为0.6 g,用石灰乳调pH值至11.0,搅拌60 min;过滤、沉淀烘干。固相XRD分析结果如图6所示。
初始质量浓度为1 720 mg/L,溶液体积为100 mL,反应温度为25 ℃。加入铝盐的量为0.6 g,用石灰乳调pH值至11.0,搅拌60 min;过滤、沉淀烘干。固相XRD分析结果如图6所示。

图6 固相XRD谱
Fig.6 XRD pattern of precipitation
由图6可以看出:固相沉淀的主要组成物相为钙矾石,其分子式为Ca6Al2(SO4)3(OH)12・26H2O,为一种常用的混凝土膨胀剂[20-22]。检测结果表明:在碱性条件下,溶液中的 可与Ca2+和Al3+形成复合物沉淀而得以脱除。
可与Ca2+和Al3+形成复合物沉淀而得以脱除。
3 结论
(1) 在碱性条件下,溶液中的 可与Ca2+和Al3+形成复合物沉淀而得以去除,其去除率随着
可与Ca2+和Al3+形成复合物沉淀而得以去除,其去除率随着 初始质量浓度的增大而提高。实验所用
初始质量浓度的增大而提高。实验所用 初始质量浓度为1 300~2 500 mg/L时,经本方法处理后,出水
初始质量浓度为1 300~2 500 mg/L时,经本方法处理后,出水 质量浓度可以达到100 mg/L以下。
质量浓度可以达到100 mg/L以下。
(2)  去除率依赖于溶液pH值、铝盐投加量及反应搅拌时间。当pH值为11.0,
去除率依赖于溶液pH值、铝盐投加量及反应搅拌时间。当pH值为11.0, 与Al3+的物质的量比为1.1?1.0,搅拌时间为60 min时,去除率可达到95%左右。此外,固相分析结果表明:其主要物相为Ca6Al2(SO4)3(OH)12・26H2O,这说明溶液中的
与Al3+的物质的量比为1.1?1.0,搅拌时间为60 min时,去除率可达到95%左右。此外,固相分析结果表明:其主要物相为Ca6Al2(SO4)3(OH)12・26H2O,这说明溶液中的 以复盐形式脱除。
以复盐形式脱除。
参考文献:
[1] 柴立元, 刘恢, 闵小波, 等. 改性活性污泥高效处理高浓度硫酸盐废水[J]. 中南大学学报: 自然科学版, 2005, 36(3): 431-436.
CHAI Li-yuan, LIU Hui, MIN Xiao-bo, et al. Efficient treatment of high concentration sulfate wastewater by modified aerobic activated sludge[J]. Journal of Central South University: Science and Technology, 2005, 36 (3): 431-436.
[2] 谢杰, 洪文笔, 高玉梅, 等. 液膜分离技术提取水中硫酸根的可行性分析[J]. 吉林建筑工程学院学报, 2007, 24(4): 5-8.
XIE Jie, HONG Wen-bi, GAO Yu-mei, et al. The feasibility analysis of extracting sulfate from water by liquid membrane separation technology[J]. Journal of Jilin Institute Architectural & Civil, 2007, 24(4): 5-8.
[3] Benattia C T, Tavares C R G, Lenzi E. Sulfate removal from waste chemicals by precipitation[J]. Journal of Environmental Management, 2009, 90 (1): 504-511.
[4] Lens P N L, Visser A N L, Janssen A J H, et al. Biotechnological treatment of sulfate-rich wastewaters[J]. Critical Reviews in Environmental Science and Technology, 1998, 28(1): 41-88.
[5] Ghigliazza R, Lodi A, Rovatti M. Kinetic and process considerations on biological reduction of soluble and scarcely soluble sulfates[J]. Resources, Conservation and Recycling, 2000, 29(3): 181-194.
[6] 王广兴, 郭连才. 盐水中硫酸根的脱除技术[J]. 中国氯碱, 2006(8): 5-7.
WANG Guang-xing, GUO Lian-cai. Removal technology of sulfate anion in brine system[J]. China Chlor-Alkali, 2006(8): 5-7.
[7] 苏恒熙, 王秀丽, 蔡泽坚. 无机盐复合体系脱除 的工艺研究[J]. 盐业与化工, 2006, 36(3): 1-3, 10.
的工艺研究[J]. 盐业与化工, 2006, 36(3): 1-3, 10.
SU Heng-xi, WANG Xiu-li, CAI Ze-jian. Research on the process of removing  from multi-component type solution[J]. Guangdong Chemical Industry, 2006, 36(3): 1-3, 10.
from multi-component type solution[J]. Guangdong Chemical Industry, 2006, 36(3): 1-3, 10.
[8] Kabdasli I, Tünay O, Orhon D. Sulfate removal from indigo dyeing textile wastewater[J]. Water Science and Technology, 1995, 32(12): 21-27.
[9] 金哲男, 熊雪松, 李席孟, 等. 吸附法深度除去氯化锂中硫酸根的实验研究[J]. 稀有金属, 2007, 31(3): 404-406.
JIN Zhe-nan, XIONG Xue-song, LI Xi-meng, et al. Deeply removing sulfate radical from lithium chloride in adsorption method[J]. Chinese Journal of Rare Metals, 2007, 31(3): 404-406.
[10] 曹天飚, 郭伟, 马红钦, 等. 盐卤中硫酸根脱除技术[J]. 中国井矿盐, 2006, 37(4): 19-22.
CAO Tian-biao, GUO Wei, MA Hong-qin, et al. Technology of sulfate removal from brine[J]. China Vell and Rock Salt, 2006, 37(4): 19-22.
[11] 祝清生. 卤水中硫酸根的去除方法[J]. 氯碱工业, 2004(12): 10.
ZHU Qing-sheng. Removal technology of sulfate in brine system[J]. Chlor-alkali Industry, 2004(12): 10.
[12] 常晓雷, 康勇, 冯颖. 硫酸盐还原菌与单质铁协同作用处理酸性含锌废水[J]. 中国有色金属学报, 2006, 16(9): 1647-1652.
CHANG Xiao-lei, KANG Yong, FENG Ying. Treatment of acid zinc wastewater by sulfate reducing bacteria cooperated with iron[J]. The Chinese Journal of Nonferrous Metals, 2006, 16(9): 1647-1652.
[13] 袁斌. 新法脱除硫酸根技术国内外进展[J]. 氯碱工业, 2000(11): 3-6.
YUAN Bin. Progress of new  removing technology at home and abroad[J]. Chlor-alkali Industry, 2000(11): 3-6.
removing technology at home and abroad[J]. Chlor-alkali Industry, 2000(11): 3-6.
[14] 李冬梅, 王海增, 王立秋, 等. 焙烧水滑石吸附脱除水中硫酸根离子的研究[J]. 矿物学报, 2007, 27(2): 109-114.
LI Dong-mei, WANG Hai-zeng, WANG Li-qiu, et al. Removal of sulfate from aqueous solution by adsorption of it on layered double hydroxides[J]. Acta Mineralogica Sinica, 2007, 27(2): 109-114.
[15] 刘桂荣, 廖立兵. 柱撑蒙脱石吸附水中硫酸根离子的实验研究[J]. 矿物学报, 2001, 21(3): 470-472.
LIU Gui-rong, LIAO Li-bing. Removal of sulfate from aqueous solutions by adsorption on pillared montmorillonite[J]. Acta Mineralogica Sinica, 2001, 21(3): 470-472.
[16] Rietra R P J J, Hiemstra T, van Riemsdijk W H. Sulfate adsorption on goethite[J]. Journal of Colloid and Interface Science, 1999, 218: 511-521.
[17] 胡文容. 铝盐沉淀法去除酸性矿井水中 的试验研究[J]. 煤矿环境保护, 1996, 10(5): 18-20, 32.
的试验研究[J]. 煤矿环境保护, 1996, 10(5): 18-20, 32.
HU Wen-rong. Removal of sulfate from acid mine drainage by aluminum-salt precipitation technology[J]. Energy Environmental Protection, 1996, 10(5): 18-20, 32.
[18] Schaezier D J. Precipitation of calcium aluminates and sulfoaluminates from water[J]. Journal Water Pollution Control Federation, 1978, 50(7): 1821-1826.
[19] 王建国, 王瑞斌. 盐酸联苯胺分离-酸碱滴定法测定实验室废水中硫酸根研究[J]. 科学技术与工程, 2007, 7(17): 4438-4440.
WANG Jian-guo, WANG Rui-bin. Study on the determination of sulfate in laboratory wastewater by benzidine hydrochloride separate and acid-base titration[J]. Science Technology and Engineering, 2007, 7(17): 4438-4440.
[20] 石云兴, 王泽云, 吴东, 等. 钙矾石的形成条件与稳定性[J]. 混凝土, 2000(8): 52-54.
BAI Yun-xing, WANG Ze-yun, WU Dong, et al. Forming condition and stabil ity of ettringite[J]. Concrete, 2000(8): 52-54.
[21] 彭家惠, 楼宗汉. 钙矾石形成机理的研究[J]. 硅酸盐学报, 2000, 28(6): 511-515.
PENG Jia-hui, LOU Zong-han. Study on the mechanism of ettringite formation[J]. Journal of the Chinese Ceramic Society, 2000, 28(6): 511-515.
[22] 马惠珠, 邓敏. 碱对钙矾石结晶及溶解性能的影响[J]. 南京工业大学学报, 2007, 29(5): 37-40.
MA Hui-zhu, DENG Min. Effect of alkali on ettringite crystallization and solubility[J]. Journal of Nanjing University of Technology, 2007, 29(5): 37-40.
收稿日期:2009-01-26;修回日期:2009-04-25
基金项目:国家科技支撑计划重点项目(2007BAC25B01);教育部科技重大项目(308019);湖南省自然科学基金资助项目(08JJ3020);湖南省科技计划项目(2008SK4031);湖南省节能减排科技重大专项(08SK1005);湖南省节能减排科技重大专项(08SK1002)
通信作者:王云燕(1975-),女,山西闻喜人,博士,副教授,从事工业废水处理的研究;电话:0731-88830875;E-mail: wyy@mail.csu.edu.cn
(编辑 陈爱华)