���±�ţ�1004-0609(2011)11-2971-07
����TiO2����(��)����������
��ѩ��1, ������1, ������2, �� ��1, �����1, �� ��1
(1. ������ѧ ��ѧѧԺ������ 110036��2. ����װ���� פ�������´����֣����� 110031)
ժ Ҫ��ͨ������ʵ���о�����TiO2��Cd(��)��������Ϊ��������Һ��pHֵ������ʱ����¶ȵ����ض�������Ӱ�졣�����������pHΪ 4~7��Χ�ڣ�����TiO2��Cd(��)�������ʾ�����97%������������TiO2�ϵ�Cd(��)����7.0 mL 0.1 mol/L HCl��70 �����ˮԡ�ж���ϴ�ѣ����������̷���������Ӧ����ѧģ�ͣ��䷴Ӧ�ı��ۻ��Ϊ3.16 kJ/mol�������ڲ���ɢ���������������̵����ʿ��Ʋ��裬��Һ��߽�������ӱ������ɢ������ܺ��ԣ���������������Langmuir��D-R����ģ����ϽϺá��������£�����TiO2��Cd(��)�ı�����������Ϊ6.34 mg/g��ƽ��������Ϊ11.54 kJ/mol��������Ӧ���ʱ���ر��Ϊ��ֵ��������Ϊ��ֵ��˵������������Ϊ�Է������ȹ��̡�
�ؼ��ʣ�Cd(��)������TiO2������������ѧ������ѧ
��ͼ����ţ�O 647.3 ���� ���ױ�־�룺A
Adsorption properties of nano-TiO2 for Cd(��)
LIU Xue-yan1, YANG Li-jun1, JIN Yan-li2, ZHANG Lei1, XU Tian-ci1, LI Na1
(1. College of Chemistry, Liaoning University, Shenyang 110036, China;
2. Military Representative Bureau in Shenyang, Navy Equipment Department, Shenyang 110031, China)
Abstract: The titanium dioxide nanoparticles were employed for the sorption of Cd(��) ions from aqueous solution. The process was studied by varying the pH, sorption time and temperature. The adsorption rate of Cd(II) by the sorbent is over 97% at pH of 4-7. The adsorbed Cd(��) are desorbed by 7.0 mL 0.1 mol/L HCl in constant temperature water bath at 70 ��. The kinetic experimental data properly correlate with the second-order kinetic model. The apparent activation energy is 3.16 kJ/mol. The overall rate process is mainly controlled by the intraparticle diffusion, while the boundary layer resistance cannot be ignored. The sorption data can be well interpreted by the Langmuir and D-R type sorption isotherms. At room temperature, the static saturated adsorption capacity is 6.34 mg/g, and the average sorption energy is 11.54 kJ/mol. The thermodynamic parameters: ?H����0, ?S����0 and ?G����0, which indicates a spontaneous and decalescence adsorption process.
Key words: Cd(��); nano-TiO2; adsorption; kinetics; thermodynamics
�����Ӽ��ӵĻ����ﱻ�㷺��Ӧ���ڵ�ƹ�ҵ������Ͻ����ء����ϡ�������ϩ�ȶ������˷�Ӧ�ѵ��������ռ��ȡ�������Ȼ���������ӿ����ʽ���ڣ�������п��Ǧ��ͭ���̵ȿ棬��Щ�����ľ������̶����ų������ӣ���ˣ����Թ�ҵ��ˮ����������������ʽ��Ⱦ���������Ƕ��Խ�ǿ���ؽ���Ԫ�أ���ˣ����١���Ч��ȥ���Ӿ���ʮ����Ҫ�����塣Ŀǰ�����õ�ȥ���ӵķ����й�������[1]����ѡ��[2]���ܼ���ȡ��[3]�����ӽ�����[4]��ҺĤ��[5]��������[6]�ȡ���������һ�ִ�ͳ�ķ��븻������������Һ�м������������������������Ϊ���壬��������Һ�е��ӣ����ӽ������뷨���������ӽ�����֬�������ӽ�����֬ȥ���ӣ����ø�ֲ����֬��������֬ȥ���ӵķ���Ҳ�м�������Ĥ���뷨�������ӷ�ˮ������Ⱦ��ȥ���ʸߡ����ռ��ص㣬 ��Ĥ�ڴ�����ˮʱ��ѡ���Ժ�ʹ�óɱ��ϸߣ� Ĥ��������Ҳ��һ�����⣬���ԣ�Ĥ��ȥ�ӵ�Ӧ���ܵ����ƣ������������ö���ԵĹ���������������ȥ���ӵģ������ڴ������ӷ�ˮ���������У�����̿���绯ú���ǻ�ú����¯��������ʯ���Ǿ��ǡ��ȼ��Ǿ��ǡ���������������ά�������������͵��ǵȡ����ײ����ǽ�������չ������һ�������ܲ��ϣ������бȱ��������ԭ����Ŀ����ŵ㣬���ܵ��о������ߵĹ㷺��ע���������Ӷ�����������Ӿ��к�ǿ��������������ˣ���ȥ���ж��к��ؽ�����Ⱦ�������������[7]��
�����[8]����ICP-AES�о�������TiO2��Cr(��)/Cr(��)����������,����������ˮ���и�����̬�������Ŷ���[9]��������������Ʒ����ˮ���ؽ���Ǧ���ӵ��������ܡ�MAT??��[10]����ET-AAS��ICP-OES�о�������TiO2�����������Al(��)�Ŀ����ԣ�̽��������TiO2���϶�Al(��)��������Ϊ�����ٵ�[11]����������TiO2����(��)�������ܵ��о���
�йؽ��ʯ������TiO2���ӵ����������о��ʼ����������������Խ��ʯ������TiO2Ϊ��������̽��pH��������Ӱ�켰���������������������TiO2�����ӵ�����ѧ�붯��ѧ��Ϊ���н�ϵͳ���о������о�Ϊ������������Чȥ�����ṩ���������ݡ�
1 ʵ��
1.1 ʵ���������Լ�
1.1.1 ʵ������
AAnalyst-700ԭ�����չ�����(������PE��˾)��pHS-3C�;���pH��(�Ϻ��״�)��Malvern Nano ZS�������ȼ�Zeta��λ������(������Malvern��˾)��X ���߷�ĩ������(D8 ADVACE �¹� BRUKER ��˾)��KQ-100B�ͳ�������ϴ��(��ɽ�г�����������˾)��TDL80-2B̨ʽ���Ļ�(�Ϻ���ͤ��ѧ������)��DK-98-1�͵��Ⱥ���ˮԡ��(�����̩˹����������˾)
1.1.2 ��Ҫʵ���Լ�
��Ҫ�Լ����£����ӣ����ᣬ���ᣬ�������ƣ����ʯ������-TiO2(��ɽ�������ײ�������˾)��ʵ�������Լ���Ϊ��������ˮΪ��������ˮ��
�ӱ�������Һ(�ż���)Ϊ1 mg/mL��ȷ��ȡ 1 g �������ձ��У�����20 mL HNO3(����V(HNO3):V(H2O)=1:1)��Һ�������������Һ��Ϊ��ɫ������ȴ��ת����1 000 mL����ƿ�У��Զ�������ˮ���ݣ�ҡ�ȡ�
1.1.3������������
ԭ�����շֹ��ȼơ������������£�����228.8 nm�������0.7 H����˿����4.0 mA����Ȳ����2.0 L/min����������17 L/min��
1.2 ʵ�鷽��
1.2.1 �ӵIJ�������
ȷ��ȡ0��0.10��0.25��0.50��1.00��1.50��2.00��2.50��3.00 mL���ӱ���Һ��25 mL����ƿ�У���0.5 mol/L HNO3ϡ�͡�ҡ�ȡ���AAnalyst700 ԭ�����չ����ǣ�����Ȳ-���������棬HNO3���հ���Һ���ⶨ�����A��
1.2.2 ���������ѵȵ��IJⶨ
��0.059 9 g�Ľ��ʯ�����������ѷ�����250 mLˮ��Һ�У�������ɢ�γɷ�ɢҺ����HCl��NaOH����һϵ�з�ɢҺ��pHֵ������Zeta��λ�����ǣ�������ɢҺ��Zeta��λ��Zeta��λΪ��ʱ����Ӧ��pHֵ���ǽ��ʯ�����������ѵĵȵ�㡣
1.2.3 �ӵ���������
��ȡ10 mLһ��Ũ��Cd(��)����Һ����50 mL������ƿ�У���HCl ��NaOH ��Һ����Cd(��)����Һ��pH ֵ��Ȼ�����һ����������TiO2��������ɢ3 min������5 min�����ķ���5 min (4 000 r/min)��Ȼ�����ˮ����Cd(��)��Ũ�ȣ�����1.2.1 �ⶨ�������ⶨ�����A������Cd(��)�����������ʡ�
�����ʦǵļ��㹫ʽΪ
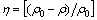 ��100% (1)
��100% (1)
ʽ�У���0Ϊԭ��Һ�������ʵ�����Ũ�ȣ�mg/L����Ϊ����ƽ��ʱ��Һ��ʣ�������ʵ�����Ũ�ȣ�mg/L��
1.2.4 ����ѧʵ��
��ȡ10 mLŨ��Ϊ20 mg/L��Cd(��)��Һ����һϵ��50 mL������ƿ�У�����ҺpHΪ6.0����80 mg����TiO2���ֱ���273��293��313 K�����£��ⶨ��ͬʱ��������Һ�������ʵ�Ũ�ȣ�ֱ�������ﵽƽ�⡣
1.2.5 ����ѧʵ��
��һϵ��50 mL������ƿ�У����벻ͬ����Ũ�ȵ�Cd(��)��Һ10 mL����HCl��NaOH����Һ��pHΪ6.0������80 mg����TiO2���ֱ���273��293��313 K�����½�������ʵ�顣
2 ���������
2.1 ����TiO2�ı���
��ƷXRD�ķ��������ͼ1��ʾ�������������Ʒ�������2��= 27.4������������壬����������Ӧ������dֵ�� JCPDS ���� 211276 �Ž��ʯ��TiO2��dֵ��ȫһ�£�˵����ƷΪ���ʯ��ṹ�����ⶨ��Ʒ��ƽ�������ߴ�ԼΪ81.9 nm���ң��Դ�������Χ(��ͼ2)��
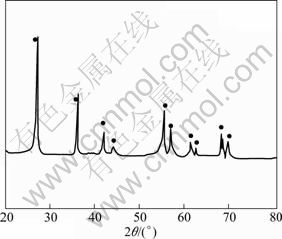
ͼ1 ���������ѵ�XRD��
Fig.1 XRD pattern of nano-TiO2
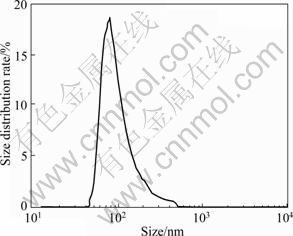
ͼ2 ����TiO2�����ȷֲ�ͼ
Fig.2 Particle diameter distributions of nano-TiO2
2.2 pH��Ӱ��
pHֵ������TiO2����Cd(��)������Ҫ�����á��ڲ�ͬpHֵ�����£�����TiO2��Cd(��)�������ʵ�Ӱ����ͼ3��ʾ����pHֵ4~7��Χ�ڣ�����TiO2��Cd(��)�������õ��������ܣ������ʿɴ�97%���ϣ������Ա�����������
Cd(��)�������Խ��ʣ����������Ժͼ��Խ����У���ˮ��Һ�У���Ҫ��Cd2+��Cd(OH)2������̬���ڡ���pH��7ʱ����Ҫ��Cd2+��̬���ڣ�pH��7ʱ����Ҫ��Cd(OH)2��̬����(��ͼ4)���ⶨ���ʯ������TiO2�ĵȵ��pHZPCΪ3.8(��ͼ4)��pH��3.8ʱ������TiO2���������ɣ�������Cd2+����������ҺpH��3.8~7֮�䣬����TiO2���������ɣ�������Cd2+�������ʱ�ʵ��ѡ��pH 6.0Ϊ���������ȡ�
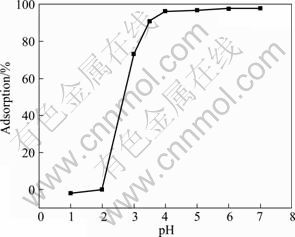
ͼ3 pHֵ������TiO2����Cd(��)��Ӱ��
Fig.3 Effect of pH on adsorption rate of Cd(��) for nano- TiO2
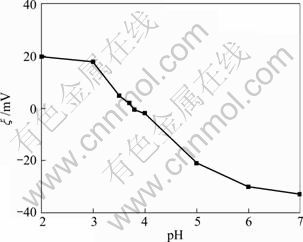
ͼ4 ��ͬpHֵ�½��ʯ������TiO2��Zeta��λ
Fig.4 Zeta potential of rutile type nano-TiO2 at different pH
��ͼ3��֪��pH��2ʱ��Cd(��)�������ʽϵͣ����о�ѡ��HCl��Һ����Cd(��)��ʵ����������7.0 mL 0.1 mol/L HCl ��Һ��70 �����ˮԡ�пɶ�������Cd(��)��������Ϊ95%��
2.3 �������Ӷ�������Ӱ��
���о�Ҳ�����˳����Ĺ������Ӷ�����TiO2�����ӵĸ��������ʵ�������������� 200 ��g/mL ��Cd2+��1 mg/ mL �� K+��1.5 mg/ mL Na+��3 mg/ mL ��Ca 2+��Mg 2+��3 mg/mL��Cl-��1.5 mg/mL��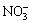 �� 1 mg/ mL ��
�� 1 mg/ mL ��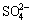 ��
��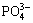 �� 0.8 mg/ mL��
�� 0.8 mg/ mL�� �Բⶨ�����������Ӱ�졣
�Բⶨ�����������Ӱ�졣
2.4 ��������ѧ�о�
ȡ10 mL 20 mg/L��Cd(��)��Һ������ҺpH 6.0������80 mg����TiO2����������qt��ʱ��t��ͼ���õ�Cd(��)����������ʱ��仯����������ѧ����(��ͼ5)����ͼ5�ɼ���qt��ʱ�����������������3 min �����ﵽƽ�⡣
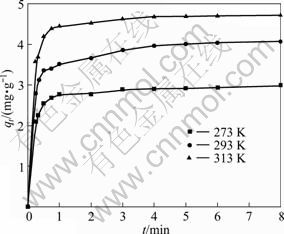
ͼ5 ��ͬ�¶�ʱ�ӵ���������ʱ��ı仯����
Fig.5 Adsorption capacity of Cd(��) on sorbent vs time at different temperature
������ʵ������������������ѧ���̣�
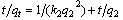 (2)
(2)
ʽ�У� k2Ϊ������Ӧ���ʳ�����g��mg-1��min-1��qtΪtʱ�̵���������mg��g-1��q2Ϊƽ����������mg��g-1����t/qt��t��ͼ�����������ݽ������Իع��������б�ʺͽؾؿɵõ���ͬ�¶�������TiO2����Cd(��)��k2��q2�Լ����ϵ��r��ʵ���������1���ӱ�1�ɿ�������3���¶��£�����ѧʵ�������������Ӧ����ѧģ���нϺõ����(r2��0.999)��
���ݲ�ͬ�¶�������������ѧʵ�����ݣ��ð���������˹(Arhenius)��ʽ��������Ӧ�Ļ����⣬�������TiO2��Cd(��)�����Ļ��EaΪ3.16 kJ/mol��
��1 ��ͬ�¶�������TiO2����Cd(��)�Ķ���ѧ����
Table 1 Kinetic parameters for Cd(��) adsorption on nano-TiO2 at different temperatures

2.5 ��ɢģ��
�����ڲ���ɢ���̣�
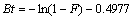 (3)
(3)
ʽ�У�F=qt /qe��qt��qe �ֱ�Ϊt ʱ�̵�����������ƽ������������mg��g-1��B=��2Di /d 2(Di Ϊ�ڲ���ɢϵ����d Ϊ���Ӱ뾶)��������ѧ������������ɢ���̽�����ϣ�����ʽ(3)����-ln(1-F)-0.497 7��t��ͼ(��ͼ6)��ͼ6��ֱ�߽���ͨ��ԭ�㣬���������ڲ���ɢ���������̵���Ҫ���Ʋ���[12]��
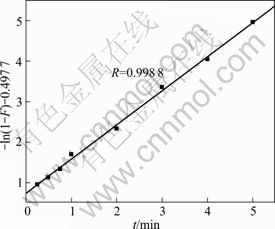
ͼ6 �����ڲ���ɢ�������
Fig.6 Fitted curve of intraparticle diffusion
Cd(��) ���������ڲ�����ɢ���̿ɽ�һ����Weber-Morris ģ��������[13]������ʽ���£�
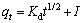 (4)
(4)
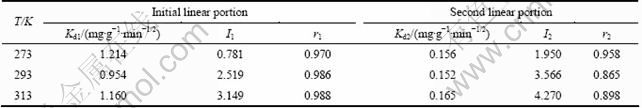
ʽ�У�KdΪ�ڲ���ɢ�ٶȳ�����mg��g-1��min-1/2��I ��ʾ��߽�����йصij�����IֵԽ�߽���������Ӱ��Խ��[14-15]����Weber-Morrisģ�����ݽ��зֶ�������ϣ����������ͼ7��ʾ����ģ�͵õ����ڲ���ɢ�ٶȳ������������ϵ��r ���2 ���С���ͼ7���Կ�����Weber-Morrisģ�����ߵ�2�������������Ϻã�˵�������ڲ���ɢ�������������̵Ŀ��Ʋ��裻����ɢģ�����ֱ�߲�������ԭ�㣬˵������TiO2����Cd(��)�����Ƚϸ��ӣ���������ΧҺ��߽�������ӱ������ɢ���̲����Ժ��ԡ�
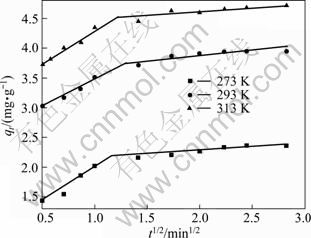
ͼ7 �ڲ�ͬ�¶���Weber-Morris ģ���������
Fig.7 Fitted curves of Weber-Morris at different temperatures
��2 ��ͬ�¶���Weber-Morrisģ�Ͷ�������������ϵ�������ϵ��
Table 2 Calculated parameters for Cd(��) adsorption on nano-TiO2 at different temperatures
2.6 ��������ѧ�о�
2.6.1 ��������ģ�ͺ���������
�ֱ��ڲ�ͬ�¶���(0��20��40 ��)������������(1.2.5)��������ʵ�飬����������ͼ8������Langmuir��������ģ�� [16]���Ԧ�e/qe��Ce��ֱ�߿ɵ�qm �� b��
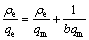 (5)
(5)
ʽ�У�qmΪ������������mg��g-1����eΪCd(��)����ƽ��ʱ������Ũ�ȣ�mg��L-1��bΪ����ƽ�ⳣ����L��mg-1��Langmuir ��������ģ����Ͻ�����3���С��ɱ�3��֪����3���¶��£�ʵ��������Langmuir �����������нϺõ����(r��0.99)�������������������¶ȵ����߶����ӣ�˵������TiO2 ��Cd(��)�����������ȹ��̡�
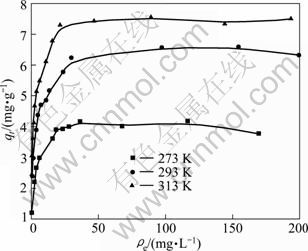
ͼ8 ��ͬ�¶��µ�����������
Fig.8 Isotherm of Cd(��) adsorption on nano-TiO2 at different temperatures
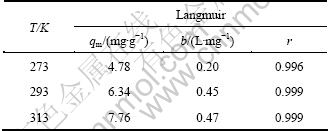
��3 ��ͬ�¶���Langmuir�����������ߵIJ���
Table 3 Langmuir isotherm constants at different temperatures
2.6.2 ���������е�����ѧ����
ʵ�鿼������273��293��313 K�²�ͬ��ʼŨ�ȵ�Cd(��)���������������ѧ�������㣬������������������������ߣ���ln �Ѷ�1/T��ͼ������Clausius-Clapeyron���̿ɵ�[17]��
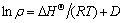 (6)
(6)
ʽ�У���Ϊ��ͬ�¶�ʱCd(��)������ƽ��Ũ��(mg��L�C1)�������Իع鷨���б�ʣ����������?H�����������¹�ϵ������������ѧ����ֵ�����������ڱ�4��
 (7)
(7)
 (8)
(8)
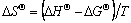 (9)
(9)
ʽ�У���Be�ͦ�Ae�ֱ���Cd(��)���������е�ƽ��Ũ��(mg��L�C1)������Һ�е�ƽ��Ũ��(mg��L �C1)��KCΪƽ�ⳣ����
�ɱ�4��֪������TiO2����Cd(��)���ӵ��������Է�����(?G����0)����?G���ľ���ֵ�����¶ȵ����߶����ӣ�������������߱��ֳ����¶����ߣ����������ӵ�ʵ����һ�£���������ӦΪ���ȹ���(?H����0)�����ر��Ϊ��ֵ(?S����0)��
2.6.3 ƽ��������
ƽ��������E ���ж��������͵���Ҫָ�꣬�����ʽΪ[18]
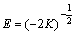 (10)
(10)
����D-Rģ�͵�������ʽ(��ʽ(11))����lnqe�Ԧ�2��ֱ��(��ͼ9)����ֱ��б�����K��
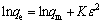 (11)
(11)
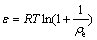 (12)
(12)
ʽ�У�EΪƽ�������ܣ�kJ/mol��KΪ���������йصij�������ΪPolanyi���ܣ�kJ������ʽ(10)����273��293��313 K�����£�����TiO2��Cd(��)��ƽ�������ֱܷ�Ϊ13.36��11.54��10.82 kJ/mol�����ӽ�����Ӧ��������ΧΪ8~16 kJ/mol���ʸ�������Ӧ�������ӽ� ��[19]��
��4 ������������TiO2������ѧ���۲���
Table 4 Thermodynamic parameters for adsorption of Cd(��) on nano-TiO2

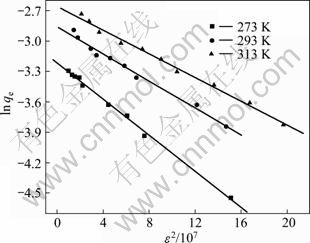
ͼ9 �ڲ�ͬ�¶��µ�D-R����������
Fig.9 D-R adsorption isotherms at different temperatures
3 ����
1) ��pH 4~7 ��Χ�ڣ�����TiO2��Cd(��)�������ʿɴ�97%���ϣ�ǿ��������������Cd(��)��������7.0 mL 0.1 mol/L HCl ��Һ�ɶ�������Cd(��)��������Ϊ95%��
2) ���������̷���������Ӧ����ѧģ�ͣ������£��䷴Ӧ���ʳ���Ϊ1.89 g��mg-1��min-1����Ӧ���Ϊ3.16 kJ/mol�����������Ƚϸ��ӣ������ڲ���ɢ���������������Ʋ��裬��Һ��߽�������ӱ������ɢ������ɺ��ԡ�
3) ����TiO2��Cd(��)����������Langmuir��D-R����ʽ����273��293 ��313 K �����£��䱥�����������ֱ�Ϊ4.78��6.34��7.76 mg��g-1��ƽ�������ֱܷ�Ϊ13.36��11.54��10.82 kJ��mol-1������������������ϵ�¶����߶�����˵����������ӦΪ���ȹ��̣�ƽ�������ܷ�ΧΪ8~16 kJ��mol-1���ʸ�������Ӧ�������ӽ������̡�
4) ����TiO2��Cd(��)����������ѧ�����ֱ�Ϊ?H����0��?G����0��?S����0������������ӦΪ�Է������ȹ��̡�
REFERENCES
[1] ¬��Ӣ, ����, Ҷ���. ���������ӹ������������о�[J].��ѧ�����﹤��, 2004, 6: 44-45.
LU Lian-ying, ZOU Guang-zhong, YE Song-di. Experiment research on concomitance deposition of cadmium and ferrite[J]. Chemistry & Bioengineering, 2004, 6: 44-45.
[2] ������, ���. ���û�-�����-�⻯��-��������B��ѡ������[J]. �ҿ����, 2007, 26(2): 126-128.
YI Xiao-ming, LI Jian-wen. Separation of Cadmium(II) with replacement -flotation[J]. Rock and Mineral Analysis, 2007, 26(2): 126-128.
[3] �� ��, �� ��. Tween80-(NH4)2SO4-H2O��ϵ��ȡ�ӵ��о�[J].ʪ��ұ��, 2007, 26(2): 92-95.
LIU Ge, ZHOU Kai. Extraction of Cd(��) in Tween80- (NH4)2SO4-H2O system[J]. Hydrometallurgy of China, 2007, 26(2): 92-95.
[4] ������, ������, �� ��, �ŵ�ǿ. ���ӽ�����֬�����ӵĶ���ѧ�о�[J]. ���ӽ���������, 2004, 20(2): 138-143.
YANG Li-li, KANG Hai-yan, LI Na, ZHANG De-qiang. Study on the kinetics of adsorption of cadmium by ion-exchange resin[J]. Ion Exchange and Adsorption, 2004, 20(2): 138-143.
[5] ���·�, ������, �ζ�ʤ. ���ҺĤ������п�Ķ���ѧ����[J]. �����Ϳ��, 2009, 28(6): 44-47.
LIU Xin-fang, ZHANG Xiao-yu, HE Ding-sheng. Dynamic analysis on the separation of cadmium and zinc with hybrid liquid membrane[J]. Electroplating & Finishing, 2009, 28(6): 44-47.
[6] �� ��, �����. ��֦�Ǿ��Ƕ�Ǧ, ��������Ϊ�о���Ӧ��[J].����������, 2006, 25(10): 1-6.
HOU Ming, LIU Zhen-guo. Study on adsorption properties of carboxyl-containing grafted chitosan polymer toward Pb(II) and Cd(��) and its application[J]. Chinese Journal of Analysis Laboratory, 2006, 25(10): 1-6.
[7] ����̫, ��Ԫ��, ������, �ſ�Ӣ. ���ײ��ϼ��似����Ӧ��ǰ��[J]. ���Ϲ���, 2000, 3: 42-48.
ZHANG Zhong-tai, LIN Yuan-hua, TANG Zi-long, ZHANG Jun-ying. Nanometer materials & nanotechnology and their application prospect[J]. Materials Engineering, 2000, 3: 42-48.
[8] �� ��, ���, ������, �� ��, �����. ���������ѷ��븻����ICP-AES �ⶨˮ����Cr(VI)/ Cr(III)[J]. ������ѧѧ��, 2000, 16(4): 300-303.
LIANG Pei, LI Chun-xiang, QIN Yong-chao, HU Bin, JIANG Zu-cheng. Selective adsorption on nanometer size TiO2 powders for the chromium speciation using ICP-AES[J]. Journal of Analytical Science, 2000, 16(4): 300-303.
[9] �� ��, �� ƽ. ��������Ʒ�����Ʊ������ˮ��Ǧ���ӵ�������Ϊ[J]. ��ѧѧ��, 2009, 12(67): 1336-1342.
ZHANG Dong, HOU Ping. Preparation of nano-calcium titanate powder and its adsorption behavior for lead ion and cadmium ion in water[J]. Acta Chimica Sinica, 2009, 12(67): 1336-1342.
[10] MAT?? P, HAGAROV? I, BUJDO? M, DIVI? P, KUBOV? J. Determination of trace amounts of total dissolved cationic aluminium species in environmental samples by solid phase extraction using nanometer-sized titanium dioxide and atomic spectrometry techniques[J]. Journal of Inorganic Biochemistry, 2009, 103: 1473-1479.
[11] �� ��, ��ѩ��, ������, �� �, ��ƽ��. ����TiO2����(��)����������[J]. �й���ɫ����ѧ��, 2010, 20(2): 301-307.
ZHANG Lei, LIU Xue-yan, JIANG Xiao-qing, LI Qi, KANG Ping-li. Adsorption properties of nano-TiO2 for Mo(��) [J]. The Chinese Journal of Nonferrous Metals, 2010, 20(2): 301-307.
[12] AKSU Z. Application of biosorption for the removal of organic pollutants: A review[J]. Process Biochemistry, 2005, 40(3/4): 997-1026.
[13] SHAUHA M S, SARWAR M I, QADEER R. Adsorption of strontium ions from aqueous solution on Pakistani coal[J]. Journal of Radioanalytical and Nuclear Chemistry, 2005, 265(1): 73-79.
[14] ?ZER A, AKKAYA G, TURABIK M. The biosorption of acid red 337 and acid blue 324 on enteromorpha prolifera: The application of nonlinear regression analysis to dye biosorption[J]. Chemical Engineering Journal, 2005, 112(1/3): 181-190.
[15] MALL I D, SRIVASTAVA V C, AGARWAL N K, MISHRA I M. Removal of congo red from aqueous solution by bagasse fly ash and activated carbon: Kinetic study and equilibrium isotherm analyses[J]. Chemosphere, 2005, 61(4): 492-501.
[16] ������, �����, ����ƽ, л ˪, ʯ ��. ��������/ʯӢɰ (MOCS)��ͭ��Ǧ���ӵ������о�[J]. ������ѧѧ��, 2005, 25(6): 779-784.
ZOU Wei-hua, CHEN Zong-zhang, HAN Run-ping, XIE Shuang, SHI Jie. Removal of copper cation and lead cation from aqueous solution by manganese-oxide-coated-sand [J]. Acta Scientiae Circumstantiae, 2005, 25(6): 779-784.
[17] BEREKET G, AROGUZ A Z, ?ZEL M Z. Removal of Pb(��), Cd(��), Cu(��) and Zn(��) from aqueous solutions by adsorption on bentonite [J]. Journal of Colloid and Interface Science, 1997, 187: 338-343.
[18] KILISLIOGLB A, BILGIN B. Thermodynamic and kinetic investigations of uranium adsorption on amberlite IR-118H resin[J]. Applied Radiation and Isotopes, 2003, 58(2): 155-160.
[19] EL-SHAHAWI M S, NASSIF H A. Retention and thermodynamic characteristics of mercury(��) complexes onto polyurethane foams[J]. Analytica Chimica Acta, 2003, 481(1): 29-39.
(�༭ ����)
������Ŀ������ʡ���������д����Ŷ���Ŀ(2007T053)������ʡ����ǧ���˲Ź��̡�������Ŀ; ����ʡ�ߵ�ѧУ�����˲�֧�ּƻ�(2009R30)
�ո����ڣ�2010-11-01�������ڣ�2011-05-23
ͨ�����ߣ����٣����ڣ���ʿ���绰��024-62207809�����棺024-62202380; E-mail: zhanglei63@126.com