ϡ�н��� 2012,36(01),149-153
������ѹ������ͭ��������
������ �Ż�Ȼ ������ ����
����������ѧ�����뻯ѧ����ѧԺ
ժ Ҫ��
���������ǻ���Ŀ������백�γ�������ӽ�����Һ,ʵ��Ŀ������벿�����ʵķ���,��˽������̾���ѡ���ԡ����ܡ�ͭ�백����ϻ��Ƽ��������ƻ�ԭ���ܵ�Ӱ�����ؽ����˷������������:���cNH3/cMe�������γ��ȶ��Ըߵ��ܡ�ͭ���������;����cSO42-/cSO32-,�����ϵpH�ɽ��ͻ�ԭ����ԭ��λ��ʵ����̲��ü�ѹ��������,��NH3-NH4+-H2O��ϵ�н�����ͭ�������е��ܺ�ͭ,�о����ܰ�Ũ�ȡ���隣ȡ�Һ�̱ȡ������¶ȡ���ԭ�����������������ܺ�ͭ�����ʵ�Ӱ�졣�������,���ܰ�Ũ��7 mol.L-1����隣�2��1��Һ�̱�6��1�������¶�100�桢��ԭ��������������Ϊ�����ܺ���(Ħ����)4��������������,�ܽ����ʿɴﵽ95.2%,ͭ�����ʿɴﵽ95.8%������Һ�����������ռ�,������ο�ʵ�ֱ�·ѭ��,�Ի����Ѻá�
�ؼ��ʣ�
NH3-NH4+-H2O��ϵ;��ͭ������;������;
��ͼ����ţ� TF803.21
����飺������(1954-),��,����������,������;�о�����:ʪ��ұ��(E-mail:Ljh1781@163.com);
�ո����ڣ�2011-05-06
����������Ȼ��ѧ������Ŀ(51164011)����;
Process of Ammonium Leaching Oxidation Ore of Cobalt and Copper at High Pressure
Abstract��
Ammonium leaching was a selective process,the principle was that goal metal formed complex ions with ammonia so as to be separated from impurities.The coordination reaction mechanism of ammonia with cobalt and copper and the affective factors of sodium sulfite reduction were analyzed.It showed that increasing the ratio of ammonia was in favor of the stability of complexes,and low reduction potential was available while decreasing the cSO2-4/cSO2-3 and improving the pH value.Cobalt and copper were leached with NH3-NH4+-H2O system at high pressure from cobalt and copper oxide ore.The influence of total concentration,ratio of ammonia to ammonium,ratio of liquid to solid,temperature and amount of reductant on leach rate were studied.The results showed that the leach rate of cobalt and copper was 95.2% and 95.8% respectively under the optimal conditions that total ammonia concentration was 7 mol �� L-1,NH3/NH4+ was 2�� 1,the ratio of liquid to solid was 6�� 1,leaching temperature was 100 ��,the amount of the reductant sodium sulfite was 4 times to the amount of trivalent cobalt(mol ratio).Processes after leaching was simple,ammonia and ammonium was recycled and this process benefited environment protection.
Keyword��
NH3-NH4+-H2O system;cobalt and copper oxide ore;leaching rate;
Received�� 2011-05-06
�ҹ�����Դƶ��,������ұ����ҵ��ԭ����������[1,2]�������ŵ�ء�Ӳ�ʺϽ𡢹�ҵ��[3,4,5]����ҵ�ķ�չ,�ҹ����������������ӡ��ڴ�ͳ�ᷨ�����ܿ�Ĺ�����,�������ʽ������Һ,�������̸���,���Ӽ������������������ͭ�����ϸ�,���½���Һ��ͭ����һ���;��Ŀ���,��Ϊ���ӡ��ڰ�����ϵ��,��������ѡ����,����Ч���ٸơ�þ���������ӽ������Һ,������������̼�[6,7,8]������Һ����ͭ��,�������õ����Ƚϸߵ��ܻ�����,�������ð�����η��ؽ������봫ͳ�ᷨ�����ܿ�������,�ܻ�����ĺ����������̿����Լ��ٷ�ˮ���ŷ�����
���ڰ���ұ����,������ѧ�߽����˴������о������������������ƽ��͵��ƽ���˫ƽ�ⷨ������ϵ��Ni,Mg,Zn,Cd�����ƽ��������о�[9,10];�������[11]�����˽������İ�������;Yachenko��[12]�о���ͭ������������Ȼ����ϵ�еĽ�������;������[13]���ó��³�ѹ����������ͭ����,Cu,Cd,Zn�����ʽϸ�;���ڵ�[14]����̼什�ȡ-�û���������Դ�����������շ���ͭ,ȡ�����þ���Ч��ͻ���Ч���,��Ŀǰ���ڶ����ı�����Ҫ�Ǵ��������ȶ�����Դ,���ð�������ԭ��ı������١������Ըչ�ij��ͭ������Ϊԭ��,���ü�ѹ����������NH3-NH4+-H2O��ϵ�н����ܡ�ͭ,�����˸����ض��ܡ�ͭ�����ʵ�Ӱ�졣
1ʵ��
1.1ԭ�ϼ��Լ�
ʵ������ԭ��Ϊ�չ�������ͭ��,��XRD����,ԭ����Co,Cu��Ҫ��Co3O4,CoxCuyOz,CowCuxNiyOz��ʽ����,Fe,Mn�����ʽ�����Ҫ�Ը��Ϲ�������ʽ����,�仯ѧ�ɷ����1��ԭ����ĥ��90%����С��0.075 mm��
��1 ��������ѧ�ɷ�(%)Table 1 Component of cobalt oxide minerals(%) ����ԭͼ

��1 ��������ѧ�ɷ�(%)Table 1 Component of cobalt oxide minerals(%)
������Ҫ�Լ���25%Ũ��ˮ������李��������ơ�����ˮ�ȡ�
1.2ʵ��װ�ü�����
����������GCF-2ʵ����ѹ��Ӧ���н��С�
��ԭ������李���ˮ���������ƺ�ˮ����Ƶ����鷽�������ѹ����,�ܱ�������Ԥ���¶�,��ʼ��ʱ,��Ӧʱ��4 h�������б��ֽ����ٶ�400 r��min-1,�����¶�����2�档��Ӧ������ͨ����ȴˮ��������ȴ��60�������,��������Ƭʽ��ձù��˷��롣��������10%��ˮϴ�ӡ����,��¼����,����Һ�ͽ������ֱ��ͷ�����������Co,Cu������������ʡ�
1.3ʵ��ԭ��
1.3.1���������ܡ�ͭԭ��
����������ͭ�������,Co,Cu�백�γ������[M(NH3)z]2+������Һ,��Ca,Fe,Si�Ȳ���NH3��Ӧ,�Ӷ�ʵ�ֽ�������������Ԫ�ط����Ŀ�ġ��䷴ӦʽΪ: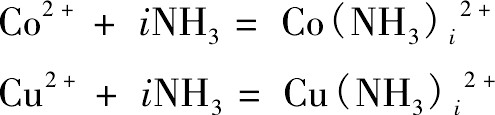
��Ӧ��ϵ��,����Ҫ��[Co(NH3)1-6]2+��ʽ����,��cNH3/cCo��Сʱ,���백�γ�Ũ�Ƚϵ͵�[Co(NH3)1-3]2+�����,��cNH3/cCo�ϴ�ʱ,���백������[Co(NH3)4-6]2+�����,���������ȶ������,��ͭ�ڰ�����ϵ����Ҫ����ƽ�������νṹ��Cu(NH3)42+�����ܺ�ͭ�İ�������������ȶ�����[15]�ֱ����2,3��ʾ��
�ɱ�(2,3)��֪:��ͬcNH3/cMe����������Co,Cu�������ӵ��ȶ��Բ�ͬ,ʵ��������Ű�Ũ��,��������Co,Cu�����ʵ���ߡ�
1.3.2��ԭ������ԭ����Ӱ�����ط���
���ǵ�������ϵ�л�ԭ�����ܵIJ��,��ʵ���������������Ϊ��ԭ����
������Һ���������ƵĻ�ԭ��Ӧ��������(��*)��ʽ(1)

����˹�ط���
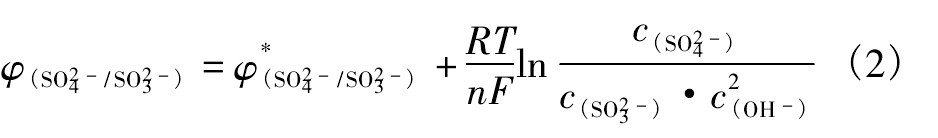
����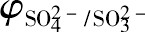 Ϊʵ�ʵ���;RΪ8.314 J��K-1��mol-1;FΪ�����ڳ���,ȡ96485 C��mol-1;nΪ�缫��Ӧ��ת�Ƶĵ�����Ŀ;TΪ����ѧ�¶�,K��
Ϊʵ�ʵ���;RΪ8.314 J��K-1��mol-1;FΪ�����ڳ���,ȡ96485 C��mol-1;nΪ�缫��Ӧ��ת�Ƶĵ�����Ŀ;TΪ����ѧ�¶�,K��
��ʽ(2)���Կ������¶�һ����������,�յĴ�Сȡ����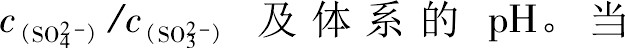
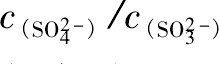 ��Сʱ,��ֵ��С,�������ƵĻ�ԭ������ǿ;��
��Сʱ,��ֵ��С,�������ƵĻ�ԭ������ǿ;��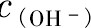 ���ʱ,��ֵ��С,�������ƻ�ԭ������ߡ����ʵ���п��ƻ�ԭ�������������ϵ��p HΪ����ʱ,�������ܵĻ�ԭ������
���ʱ,��ֵ��С,�������ƻ�ԭ������ߡ����ʵ���п��ƻ�ԭ�������������ϵ��p HΪ����ʱ,�������ܵĻ�ԭ������
2���������
2.1�ܰ�Ũ�ȶԽ����ʵ�Ӱ��
�ڽ����¶�Ϊ100�桢��隣�Ϊ2��1��Һ�̱�Ϊ6����ԭ������Ϊ3���ܺ���4�����������ܰ�Ũ�ȶ��ܡ�ͭ��������ͼ1��ʾ��
��2 �ܰ�������ȶ�����(T=298 K)Table 2 Stability constant level of cobalt-ammonia complexation ion ����ԭͼ
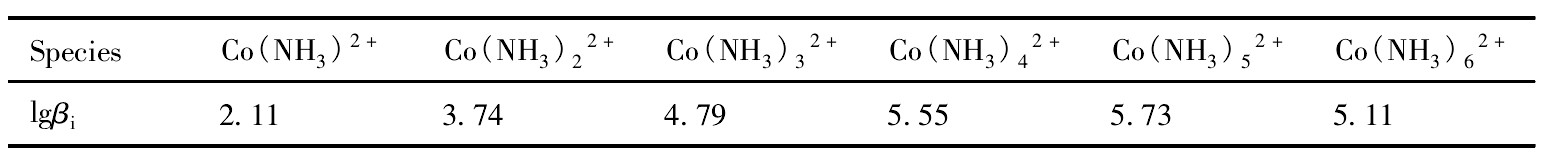
��2 �ܰ�������ȶ�����(T=298 K)Table 2 Stability constant level of cobalt-ammonia complexation ion
��3 ͭ��������ȶ�����(T=298 K)Table 3 Stability constant level of copper-ammonia complexation ion ����ԭͼ

��3 ͭ��������ȶ�����(T=298 K)Table 3 Stability constant level of copper-ammonia complexation ion
��ͼ1���Կ���,���ܰ�Ũ��Ϊ5 mol��L-1ʱ,ͭ�����ʽӽ�96%,�ܵĽ����ʽ�Ϊ88%,�����ܰ�Ũ��,ͭ�Ľ����ʻ�������,���ܵĽ�������߽Ͽ졣���ܰ�Ũ�ȴ���7 mol��L-1ʱ,�ܽ���������ٶȱ仺�����ǵ�����������ѹ������,��˽��ܰ�Ũ�ȶ�Ϊ7 mol��L-1��
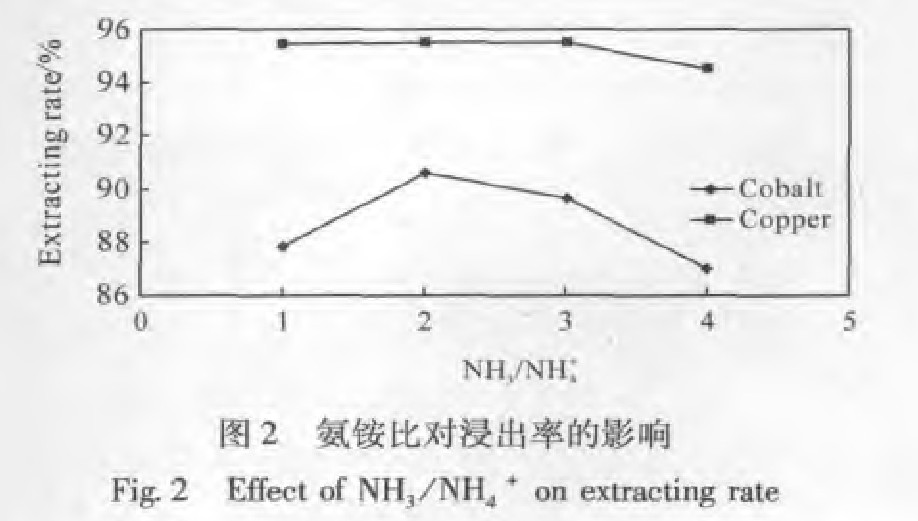
2.2��隣�(NH3/NH4+)�Խ����ʵ�Ӱ��
�ڽ����¶�Ϊ100�桢�ܰ�Ũ��Ϊ7 mol��L-1��Һ�̱�Ϊ6����ԭ������Ϊ�����ܺ���4���������°�隣ȶԽ����ʵ�Ӱ����ͼ2��ʾ����ͼ�п��Կ���,��隣ȶ�ͭ������Ӱ�첻��,����隣���1��1��3��1֮��ʱ,ͭ������û�����Ա仯;����隣ȴ���3��1ʱ,ͭ���������н��͡���隣ȶ��ܽ�����Ӱ����ֳ���������,����隣�С��2��1ʱ,������백�����������ܵĽ���;����隣�Ϊ2��1ʱ,�ܽ����ʴﵽ����ֵ,�ɴﵽ91%;����隣ȴ���2��1ʱ,�ܽ����ʷ������½�����,������Ϊ��隣������������Һ��p Hֵ,��ԭ����ԭ��λ����,�ܱ���ԭ��Ϊ�����ܽ������С���Co2+/Co�缫����С��Cu(NH3)2+/Cu�缫����,����ͭ������ﱻ�û���ͭ�������е���ͭ���������½��������Ѱ�隣�Ϊ2��1��

ͼ1 �ܰ�Ũ�ȶԽ����ʵ�Ӱ��Fig.1 Effect of total ammonia concentration on extracting rate
2.3Һ�̱ȶԽ����ʵ�Ӱ��
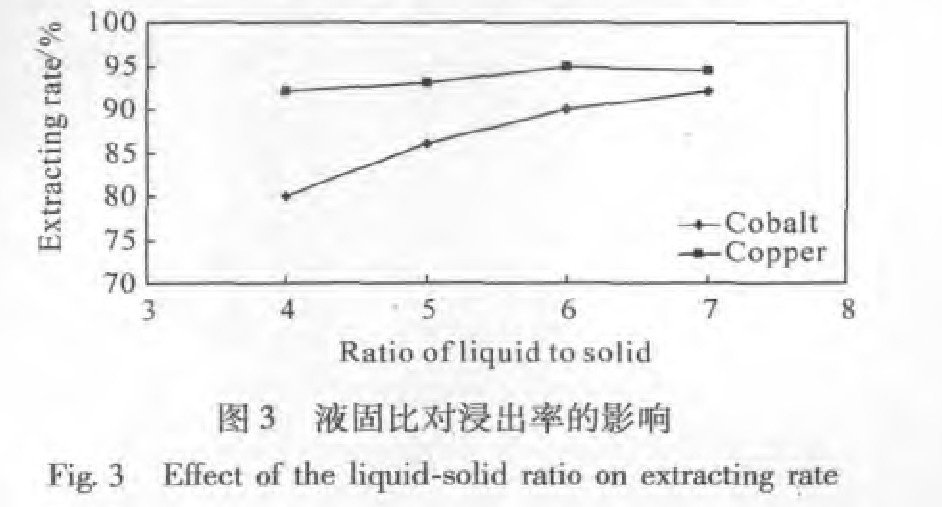
�ڽ����¶�Ϊ100�桢��隣�Ϊ2��1���ܰ�Ũ��Ϊ7 mol��L-1����ԭ������Ϊ�����ܺ���4����������Һ�̱ȶԽ����ʵ�Ӱ����ͼ3��ʾ����ͼ�ɼ�:����Һ�̱�����,ͭ�Ľ��������ӻ���,�ܵĽ������������ԡ���Һ�̱ȴ���6ʱ,����������ٶȱ仺,��Һ�̱ȹ�����ɽ���ҺŨ�ȵ�,�������δ�������,���,����Һ�̱�Ϊ6��
2.4�¶ȶԽ����ʵ�Ӱ��
�ڰ�隣�Ϊ2��1���ܰ�Ũ��Ϊ7 mol��L-1��Һ�̱�Ϊ6����ԭ������Ϊ�����ܺ���4�����������¶ȶԽ����ʵ�Ӱ����ͼ4��ʾ����ͼ�п��Կ���,���¶�С��120��ʱ,ͭ�Ľ����������¶ȵ����������,���¶ȴ���120��ʱ,ͭ�Ľ����ʱ仯�����ԡ��������¶�����,����ѹ������,����������ȶ��Խ���,�ɱ�2,3��֪,ͭ���������ȶ�����ԶԶ�����ܰ��������ȶ�����,������ͭ�Ľ���������,���ܵĽ����ʼ�С��ѡ�������¶�Ϊ100�档
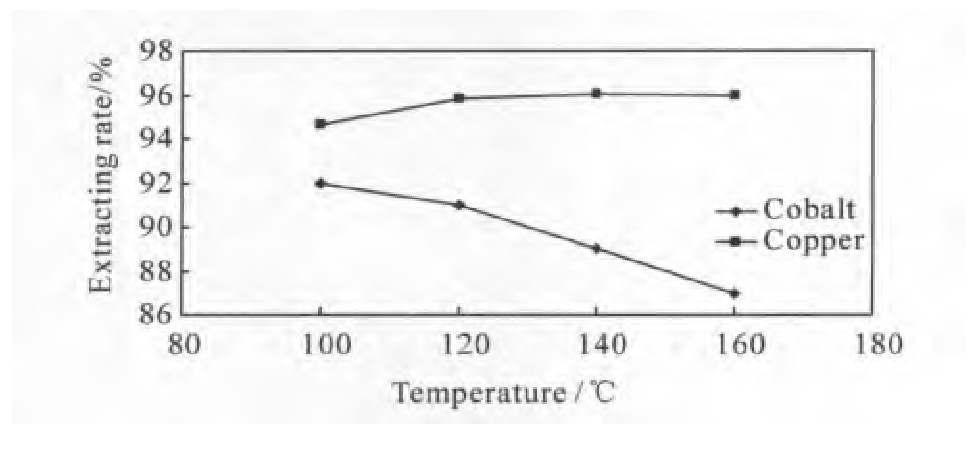
ͼ4 �¶ȶԽ����ʵ�Ӱ��Fig.4 Effect of the temperature on extracting rate
2.5��ԭ�������Խ����ʵ�Ӱ��
�ڽ����¶�Ϊ100�桢��隣�Ϊ2��1���ܰ�Ũ��Ϊ7 mol��L-1��Һ�̱�Ϊ6�������»�ԭ���������ܡ�ͭ��������ͼ5��ʾ:��ԭ��������ͭ������Ӱ���С;���ܽ�����Ӱ��ϴ���ԭ������С��4��ʱ,�����Ż�ԭ������������,�ܽ���������,���������������Χ��,��ԭ��λ����,�������ܵĻ�ԭ����;����ԭ��������һ������ʱ,�ܵĽ����ʼ����½�,�����ܱ���ԭ�ɽ����ܵ���������,�������γ��ܰ�������ӽ�����Һ�����,��ԭ�������������ܺ���4������Ϊ��ѡ�
2.6��֤ʵ��
�������������ضԽ�����Ӱ��,ȡ�����������ֵ,���ܰ�Ũ��Ϊ7 mol��L-1����隣�Ϊ2��1��Һ�̱�Ϊ6��1�������¶�Ϊ100�桢��ԭ������Ϊ�����ܺ�����4��,������֤��ʵ�顣���:�ܽ�����Ϊ95.2%,ͭ������Ϊ95.8%,˵��ʵ�������ԽϺá�
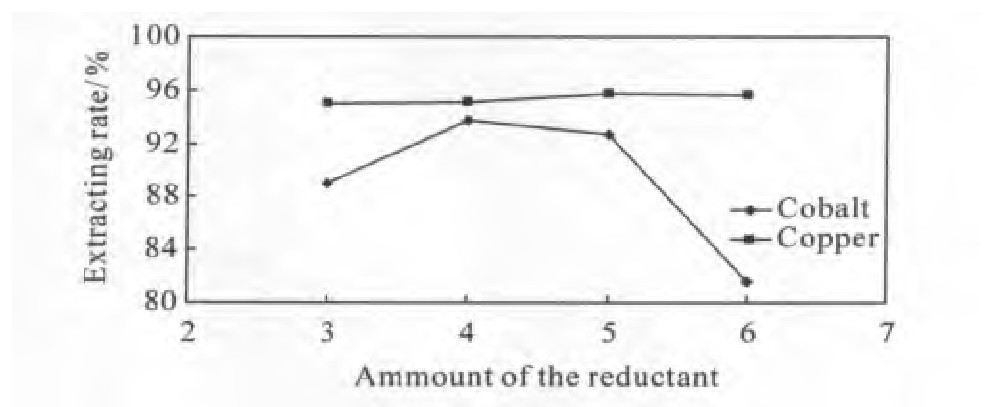
ͼ5 ��ԭ�����Խ����ʵ�Ӱ��Fig.5 Effect of amount of reductant on extracting rate
3����
1.��ͭ�������ѹ��������ѽ���������:�ܰ�Ũ�ȶ�Ϊ7 mol��L-1����隣�Ϊ2��1��Һ�̱�Ϊ6�������¶�Ϊ100�桢��ԭ����Ϊ�����ܺ�����4����
2.��ѽ����������ܡ�ͭ�����ʾ��ﵽ95%����,��ʵ���ȶ��Խϸߡ�
3.����Һ�м�����Ca,Fe������Ԫ��,ʹ�������ռ�,���ᷨ����нϴ�Ľ�����
4.�������ܱջ����н���,���ӷ���ʧ��,�Ի����Ѻá�
5.����Һ����ͭ��,�������õ����Ƚϸߵ��ܻ�����,�������ð�����η��ؽ������봫ͳ�ᷨ�����ܿ�������,�ܻ�����ĺ����������̿����Լ��ٷ�ˮ���ŷ�����
�����
[1] Wu W,Zhang H L.Recovery of Ni,Co,Rare Earth from wasteMH-Ni battery[J].Chinese Journal of Rare Metals,2010,34(1):79.(��Ρ,�ź���.���������������ܺ�ϡ���������չ����о�[J].ϡ�н���,2010,34(1):79.)
[2] Zhou Y H,Jiang S Q.Situation of copper-cobalt mine develop-ment in Congo(DRC)[J].Geology and Exploration,2010,46(3):525.(��Ӧ��,������.�չ�(��)ͭ�ܿ�ҵ��������[J].�����뿱̽,2010,46(3):525.)
[3] Wang L M,Zhang G C,Ma F.Theoretical and experimentalstudy on acid decomposition of waste diamond tools for recyclingof valuable metals[J].Chinese Journal of Rare Metals,2010,34(6):919.(������,�Ź���,����.�Ͼɽ��ʯ������ֽ�����м۽��������ۼ�ʵ���о�[J].ϡ�н���,2010,34(6):919.)
[4] Fu X M,Fan J,Liu Z W.Coarse-grained CoO prepared with co-balt oxalate through circulatory oxidization-reduction method[J].China Powder Science and Technology,2011,17(2):32.(��С��,����,������.������ѭ��������ԭ���Ʊ��ֿ�CoO[J].�й����弼��,2011,17(1):32.)
[5] Zheng Y J,Teng H,Yan H Q.Nitric acid oxidation leaching ofcobalt from refractory high-arsenic cobalt ores[J].Chinese Jour-nal of Nonferrous Metals,2010,20(7):1418.(֣�Ž�,����,�ƺ�Ȫ.��������������ұ�������ܿ�[J].�й���ɫ����ѧ��,2010,20(7):1418.)
[6] Zhang Y M,Li J,Chen Q Y,Ding H Q.Influence of ultrasonicirradiation on ammonial leaching of zinc from low-grade oxide zincore[J].Chinese Journal of Nonferrous Metals,2009,19(5):960.(����÷,���,����Ԫ,������.����������Ե�Ʒλ����п����Ϊ��Ӱ��[J].�й���ɫ����ѧ��,2009,19(5):960.)
[7] Gao B S,Wang H J,Wu A X,Zhang Y,Jin Z C.Experimentalstudy on influencing factors of ammonia leaching for a copper tail-ing[J].Metal Mine,2009,(11):169.(�߱�ʤ,���齭,�Ⱞ��,����,������.ijͭ��β��Ӱ������ʵ���о�[J].������ɽ,2009,(11):169.)
[8] Fang J J,Li Y F,Lu X L,Zhang W B.Effects and industry ap-plication of ammonia leaching of low copper oxide ore under nor-mal temperature and pressure[J].Ming and Metallurgical Engi-neering,2008,28(3):81.(������,���շ�,³����,���ı�.��Ʒλ����ͭ��ʯ���³�ѹ��������Ӱ�������о��빤ҵӦ�ý��[J].��ҵ����,2008,28(3):81.)
[9] Wang R X,Tang M T,Ju S H,Yang S H,Zhang W H,Tang CB,He J,Yang J G.Thermodynamics of Ni(��)complex equi-librium in system of Ni(��)-NH3-Cl--H2O[J].Journal ofCentral South University of Technology,2008,39(5):891.(������,������,���ٻ�,������,���ĺ�,�Ƴ���,�ξ�,���.Ni(��)-NH3-Cl--H2O��ϵ��Ni(��)���ƽ������ѧ[J].���ϴ�ѧѧ��(��Ȼ��ѧ��),2008,39(5):891.)
[10] Wang R X,Tang M T,Zeng J.Thermodynamics of Mg(��)complex equilibrium in Mg(��)-NH3-NH3Cl-H2O system[J].China Nonferrous Metallurgy,2010,(1):69.(������,������,���.Mg(��)-NH3-NH3Cl-H2O��ϵ��Mg(��)���ƽ������ѧ[J].�й���ɫұ��,2010,(1):69.)
[11] Wang K Y,Cai C L,Qian D,Li T,Chen X Y,Lai D Y.Studyon process for ammonia leaching of cobalt dregs[J].ChineseJournal of Rare Metals,2001,25(4):312.(������,�̴���,Ǯ��,����,��С��,������.�����������յ��о�[J].ϡ�н���,2001,25(4):312.)
[12] D'yachenko A N,Kraidenko R l.Processing oxide-sulfide copperores using ammonium chloride[J].Metallurgy of NonefrrousMetals,2010,51(5):377.
[13] Liu H Y,Yan W B,Shi A H,Gao F.Researching on leachingprocess of copper,zinc and cadmium from copper-cadmium slag[J].Journal of Jishou University(Natural Science Edition),2010,31(2):97.(������,���ı�,ʯ����,�߷�.��ͭ����������ͭп�ӵ�������������[J].���״�ѧѧ��,2010,31(2):97.)
[14] Zhu L,Duan X C,Liu Y L,Ding X,Zhang Z J.Ammoniumleaching and cementation method for recycling waste copper[J].Journal of Kunming University of Science and Technology(Scienceand Technology),2010,35(4):25.(����,��ѧ��,������,����,���ǽ�.�����û�����Դ������ͭ���о�[J].����������ѧѧ��(������),2010,35(4):25.)
[15] Dean A J.Langes Handbook of Chemistry(13th Ed)[M].NewYork:Plenum Press,1991.