DOI: 10.11817/j.ysxb.1004.0609.2020-37691
ZnSO4-FeSO4��Һ��ϵ����ǿ������������۶���ѧ�о�
���ij�����㣬�������������裬�Ƴ�������ΰ־�����곿
(���ϴ�ѧ ұ���뻷��ѧԺ����ɳ 410083)
ժ Ҫ�����л��߷����黯��ɢ�������ļ��л�����ʪ��ұ������������������̣���ZnSO4-FeSO4��Һ��ϵ��������Ϊ�о�����չ����ǿ�������������̵ĺ�۶���ѧ�о������õ��������鷨������������¶ȡ�pH������ǿ����ʽ���������ʡ�����Ũ�ȶԳ������ʵ�Ӱ�졣����������¶ȡ�pH������ǿ����ʽ���������ʡ�����Ũ�ȶԳ�������Ӱ���������ڴ˻����Ͽ�չ�Ķ���ѧ�о�������������������ܴ��ʹ��̿��ƣ�����ǿ��������������һ����Ӧ������Fe2+���������ı�����Ӧ����Ϊ��������Ӧ���ۻ��ԼΪ27.85 kJ/mol��
�ؼ��ʣ����У�����ǿ��������ѧ��������
���±�ţ�1004-0609(2020)-12-2971-09���� ��ͼ����ţ�TF813���� ���ױ�־�룺A
п��һ���ڶ���������Ҫ��;���ؽ��������������Ż�е���졢�������ϵ���ҵ�ķ�չ������п��������������[1-4]��п��ұ����ʽ��Ϊ����ʪ����ʪ����п��Ŀǰ����Ҫ����п��ʽ�������ռ�����ܲ�п��85%����[5]��ʪ����п����Ҫԭ������п�������п��������ͨ��Ϊп������-����-����-��������ս�����ʽ�IJ�ͬҲ�ɷ�Ϊ����������������������ֱ�ӽ����ȡ�п����ͨ������[6]��������п��������뵽пҺ���Ժ�������������Ӱ�죬���͵���Ч�ʣ������ھ��������ȥпҺ�е�����ʪ����п����������Ҫ[7]��
�����ij����������������Ƽ���������������[8]�����������ھ��г�����ȫ�������������ܺá������ڻ��������ࡢ����ϡɢ�������ŵ㣬��Ŀǰʪ����п����Һ�����ij��÷������ɱ���ʱ��ɽ��˾(Vieille Montagne)��1965~1969��ǰ���о��ɹ�������1971���ڰ���(Balen)������Ͷ��[9]���������������ж��ʪ����п�������Ӧ����������ϵͳ������������������Bartlesville��������ʱ��Overpolt�����������SAMIM��˾�Լ�������Onsan����[10]���ҹ����͵�ʪ����п��ҵ����ұ���š������н����ϵ�ϼұ������Ҳ��2007~2009��ǰ����̲�������������Һ������
�ѿ�չ���о�������������������һϵ�и��ӵ�������ѧ��Ӧ���̣�������������������������������ˮ���Լ��кͷ�Ӧ�ȡ���Щ��ѧ��Ӧ�������¶ȡ����֡��������ʡ����̶ȡ����Ũ���Լ�pHֵ������Ӱ�졣��Ԫ������Һ�еĻ�ԭ���������ᾧ�����漰һϵ������Һ�����������ϵĻ�ѧ��������Ӧ����Ӧ�����dz����ӡ�������ר��ѧ�߶Դ˽����˴����о�����[11-14]���������������Ӧ�����Ż�������װ���Ľ��ȷ�������ϵ���о��ɹ�������ʵ�������У�������Һ���������������Һ�в�ͬλ�ô�Fe2+/Fe3+Ũ�ȡ�pHֵ���¶ȳʷ����ԡ�ʱ����ص㣬�������е���Ա������ط�ʽ������ʵ�ֶ���Һ���ʵ�ʵʱ���أ��������ͳ��������ȶ����ƣ���������������Ʒλ�͡�п�����ߣ�����ʵ��������Դ��ȫ���������á�Ŀǰ�о��Ľ����������Ч���Ƴ���������Һ��ϵ�ṹ�����ľ�һ�ԡ�
������һ��ͨ���̶����ӣ�������תת�Ӳ������������ҽ�����Һ����ϵ�������и���Һ�ķ�Ӧǿ���ֶΡ����ټ��в����������پ�һ��Һ�ɷ֣�Ϊ��Ӧ��ϵ���������������ٽ���Һ�з�Ӧ�ķ���[15]����������������ѧ�߶Լ���������Ӧ�������о������磬�����[16]���ü��������յ�ipp���½ᾧ����˶��[17]ģ��������������о�Һ���������ײ��Ϊ�ȡ�ǰ�ڣ��ڹ����ص��з�ר�����������£��������齫�����Ʊ����л��߷����黯��ɢ�������õļ�������ǿ����ʽ����ʪ����п��������������ȡ���˽Ϻõ�Ч����������Ҫ������ZnSO4-FeSO4��Һ��ϵ������������Ϊ�о�����չ�ĸ�������ǿ�������������̺�۶���ѧ�о����������Ϊ�о�ͬ���ṩ�ο���
1 ԭ���뷽��
1.1 �����Լ�
����ѧ�о�������Һ��Ϊ�ο��н����ϵ�ϼұ��������ǰҺ��Ҫ��ѧ�ɷ��������õ�ZnSO4-FeSO4�����Һ����Ҫ��ѧ�ɷ����1���С�
��1 ZnSO4-FeSO4�����Һ��Ҫ��ѧ�ɷ�
Table 1 Main chemical components of ZnSO4-FeSO4mixed solution

�����Լ�����ˮ��������(FeSO4��7H2O��AR����ҩ���Ż�ѧ�Լ�����˾����)����ˮ������п(ZnSO4��7H2O��AR����ҩ���Ż�ѧ�Լ�����˾����)����ˮ������ͭ(CuSO4��5H2O��AR����ҩ���Ż�ѧ�Լ�����˾����)������п(ZnO��AR����ҩ���Ż�ѧ�Լ�����˾����)�Ⱦ�Ϊ���������ܼ�ˮΪȥ����ˮ��
1.2 �����豸�벽��
�����豸����ʾ��ͼ��ͼ1��ʾ��
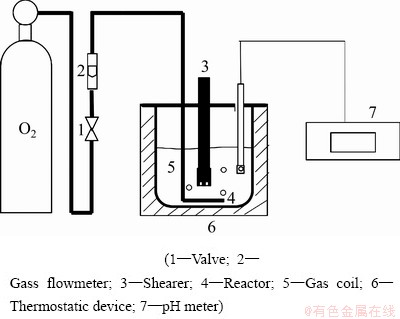
ͼ1 ����ǿ������������Ӧװ������ʾ��ͼ
Fig. 1 Schematic diagram of reaction devices of iron removal by goethite method enhanced by high shear
��Ͳ��ȡ����ZnSO4-FeSO4�����Һ��������¼���װ���У����ú���Ҫ���¶ȡ������������������ʵȲ�����ʼ��ʱ��Ӧ��pHͨ��ʵʱ��������пȫ�̵�������������̶�ֵ��ÿ��һ��ʱ������Һ����ȡ1 mL��ӦҺ�����û�ѧ�ζ����ⶨFe2+Ũ�Ⱥ�����
���õ��������鷨�ֱ첻ͬ�¶ȡ�pH������Ũ�ȡ�����ǿ����ʽ�ͼ������ʵ������£���������ʱ��ı仯���������˫Ĥ���۽���ģ��ͨ������������Ͽ�չ����ǿ�������������̵Ķ���ѧ�о���
1.3 ��������
���û�ѧ�ζ����ⶨ��Һ��Fe2+Ũ�ȣ����岽��Ϊ���������1:1��������Ԥ��������Һ�������������������Ϊָʾ�����ö����ζ�ϵ��Ϊ0.002000 g/mL���ظ���ر��ζ�Һ�ζ�Fe2+Ũ�ȡ�
����XRD�������������࣬����SEM�۲����������ò��
2 ���������
2.1 �¶ȶԳ������ʵ�Ӱ��
��ͬ�¶��³�������ʱ��ı仯��������ͼ2��ʾ����ͼ2���Կ�����������Ӧ������������Ϊǰ�ڳ������ʿ죬���ڳ����������½���������Ϊ��Ӧǰ��Fe2+Ũ�Ƚϸߣ���Һ��Fe2+�������Ӵ��ļ��ʽϸߣ�Fe2+���������������ŷ�Ӧ���У�Fe2+�����ģ�Fe2+�����������ͣ���������Ҳ�Ż���
ͬʱ��ʵ�������������¶�����ϵ�������ʳ�����ء����ڸ���ǿ�������������̣��¶�������������ϵ�������������Һ�л������ӵı�������������������ײ���ʣ�ʹ�õ�λʱ��Fe2+�������ӷ�����Ч��ײ�Ļ������࣬Fe2+�������ʸ��죬�Ӷ�����˳������ʡ�
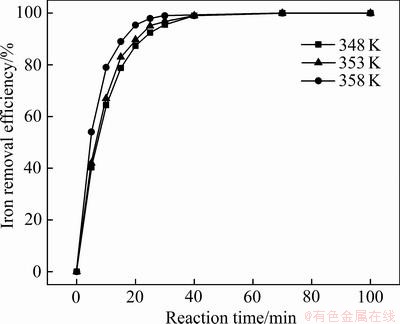
ͼ2 ��ͬ�¶��³�������ʱ��ı仯��ϵ
Fig. 2 Relationship between temperature and iron removal efficiency with time
2.2 pHֵ�Գ������ʵ�Ӱ��
��ҺpHֵ�Գ�����Ӧ��Ӱ�������ͼ3��ʾ����ͼ3���Կ�������ϵpHֵԽ�ߣ���������Խ�죬���鷶Χ��pHֵ4.0Ϊ����������pHֵ�Ը���ǿ�������������̵�Ӱ����Ҫ�����ڸı�������Ũ�ȡ��������dz�����Ӧ����֮һ����Ũ�Ƚϸ����Ʒ�Ӧ����(����)���е����ƣ��Ӷ����ͷ�Ӧ���ʡ���֮��������Ũ�Ƚϵ�ʱ���ٽ�Fe2+��������ת�䣬��߷�Ӧ���ʡ��ڸ������������£������ٶȴ��ӿ죬��Һ��H+Ũ�ȷֲ����Ӿ��ȣ������ڳ�������pHֵ�Ŀ��ơ����ǣ�������͵�pHֵ�Է�Ӧ���в���Ӱ�죬pHֵ����ʹ����Һ��п���ӳ�����pHֵ��������������������������ʹ�������ܡ�
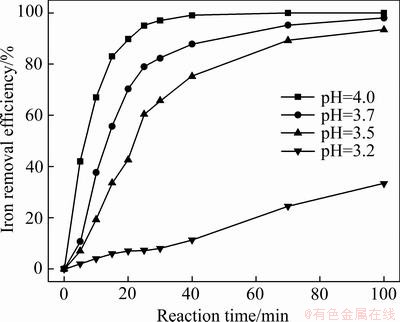
ͼ3 ��ͬpH�³�������ʱ��ı仯
Fig. 3 Relationship between pH value and iron removal efficiency with time
2.3 ����Ũ�ȶԳ������ʵ�Ӱ��
�Ժ���100%(�������)�Ĵ����뺬��21%(�������)�Ŀ����ֱ���Ϊ��������ͨ�������������٣�ʹ���������嵥λʱ��ͨ�뷴Ӧ��ϵ�����������ͬ������ͨ�����������ͬ������Ũ�Ȳ�ͬʱ��������ʱ��ı仯��ʵ������ͼ4��ʾ����ͼ4���Կ�������ͬ����Ũ�Ȼ�ı������������̷�Ӧ���ʣ�����Ũ��Խ�ߣ���Ӧ����Խ�졣�������������ԭ��һ���棬�������(����������)��������������Ȼһ�£���������Ũ�Ƚϵ͵Ŀ������ҪԶ���ڴ����ģ�Ҳ���ǿ�������Ҫ���ڴ������٣�ʹ����������Һ�еĶ���ʱ������٣�����������Һ��Fe2+�ĽӴ�ʱ���̣�Fe2+���������Ŀ����Խ��͡���һ���棬ͬ�������µ�λ����ڿ�����������Ũ�ȵ��ڴ����������Ũ�ȣ�Ҳʹ���Կ���Ϊ������ʱ�ij������ʵ���ͬ��������������Ϊ������ʱ�ij������ʡ�
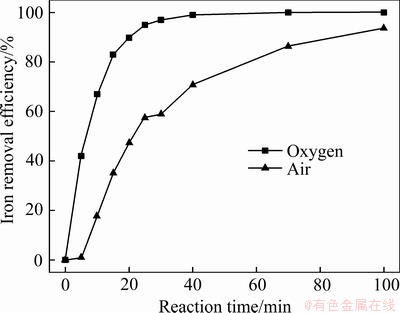
ͼ4 ��ͬ�������³�������ʱ��ı仯
Fig. 4 Relationship between oxygen concentration and iron removal efficiency with time
2.4 ����ǿ����ʽ�Գ������ʵ�Ӱ��
���������봫ͳ����������ȣ��������鷴Ӧ��Ͳ������������Ӧ�����ϸ�������������������������״ﵽ��Һ���ʾ�һ�ȶ�����ơ�ѡȡ�����豸�ɿ��ȶ�����5000 r/min�봫ͳ�������������豸�ɴ�ת��800 r/min���Աȿ�����ټ��������(��Լ��еĸ��ٶ���)����������ʽ�Գ������ʵ�Ӱ�죬�������ͼ5��ʾ������������ټ��жԷ�Ӧ���ʵ���������ͳ���跽ʽ��ʵ����Һ���ʣ��ӿ���Һ��Fe2+������Ӵ��������ӿ췴Ӧ���̣������ټ���������ʵ�ָ����ٵľ��ʣ��������߷�Ӧ��֮��ĽӴ����ᣬͬʱ����������Ϊ����������Ӧ�����ṩ�����������������ڿ�Խ���ݣ��ٽ�������Ӧ���С�
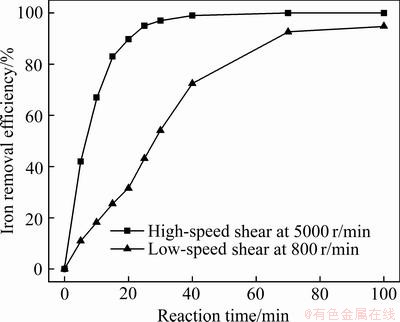
ͼ5 ��ͬǿ����ʽ�³�������ʱ��ı仯
Fig. 5 Relationship between strengthening way and iron removal efficiency with time
2.5 �������ʶԳ������ʵ�Ӱ��
��������Ҳ��Ӱ�췴Ӧ���ʵ���Ҫ���أ��������ʵIJ���ɻ����������л�����ϵ����ǿ�ȵIJ��죬����������ʶԳ�����Ӱ��ʵ�����ǿ������ǿ�ȵ�Ӱ�졣��ͬ���������³�������ʱ��ı仯��ϵ����ͼ6��ʾ����ͼ6���Կ��������ż������ʵ���������Ӧ����Ѹ����ߣ�3000 r/minʱFe2+��2 h���������20%������ת�ٴﵽ5000 r/min��Ӧ��40 min���Ҽ�����Ӧ��ȫ�����˺��������ת�ٶԳ�������Ӱ�첻���ԡ���Ȼ���ڵ�ת���£����л�����Һ�������ޣ�����ǿ�Ƚϵͣ�����ʱ��־�һ��Һ��Fe2+���ܼ�ʱ�������Ӵ�ʹ�ó������ʽϵͣ������Ƿ�Ӧ��Ҫ�������ء�����ת������£����ټ���ʹ�������ӷ���������ײ����ײ����������ϵ�������ܲ�ʹ�ø������ӻ�����ӿ��˷�Ӧ���̡���ʱ�����ڼ���������������ϵ���ʺ��ܵ�Ҫ��Fe���ӱ���Ũ�ȶԷ�Ӧ���̳�Ϊ��ҪӰ�����أ����������������ʲ����������ӿ������Ӧ���̡�
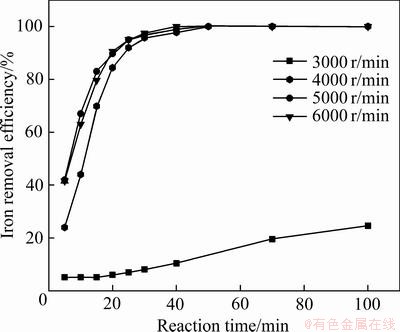
ͼ6 ��ͬ���������³�������ʱ��ı仯
Fig. 6 Relationship between shear velocity and iron removal efficiency with time
2.6 ��Ӧ����Ŀ���ѧ����
������Ӧ����������ֽ�Գ�����Һ����Һ�̷��룬�����������¸��������X���������ɨ��羵��⡣����ֱ���ͼ7��ͼ8��ʾ��
ͼ7����������ʽ��������������л���״�ṹ����ò��������ͨ��ˮ�ȷ���ͳ���跽ʽ�Ʊ���������һ��[18]������ò���д����ԡ�������ò��������ͨ�����нϴ�ıȱ���������нϺõ��������ܡ���������ټ��в��������������Ҳ�����в��ϻ����õļ�ֵ�������˸��ټ����������պ���������о������塣

ͼ7 ���������������õ���������SEM��
Fig. 7 SEM image of goethite residue produced by goethite process enhanced by high shear
ͼ8��ʾΪˮ�ȷ�����ǿ���ϳɵ�������XRD�ס���ͼ8���Կ������������ɵ��������X���������������������(PDF#29-0731)�Ǻϣ���������ø�����Һ����ǿ������ʵ�ֺ�����Һ����������
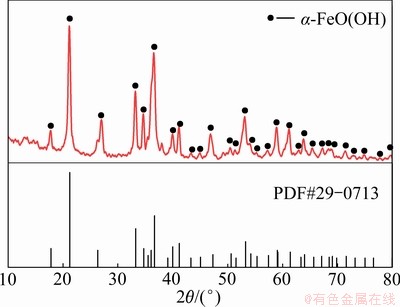
ͼ8 ���������������õ���������XRD��
Fig. 8 XRD pattern of goethite residue produced by goethite process enhanced by high shear
3 �������۶���ѧ
������Ϊһ��ǿ���ֶζ���ϵ������һ�������ṩ�����������ӿ촫�ʴٽ���Ӧ����һ������ͨ����ϵ������ײ�o��Ӧ�����ṩ����(�������������;����γɹ�����Ϊ��Ӧ�����ṩ���������ͷ�Ӧ������ֵ)�����ڴ�ͳ������������ý�����ʽ������������ǿ��������ϵ��ָ��ܣ��䶯��ѧ�����봫ͳ��ʽ���в��
�����������Ӧ���ڶ��෴Ӧ���漰������Һ��Ĵ��ʺ���صĻ�ѧ��Ӧ����Ӧ�����У���Ӧ���ײ��̹ܲ��Ϲ���������������������ʽ����Һ�ж���ͣ��������ÿ�����ݲ�����������ֱ����ײ����˫Ĥ����[19-20]����������ɢ�Ĺ��̣������������ӦҪ�������²��衣
1) ������������������Һ�������ɢ��
2) ������Fe2+������淢����Ӧ��֮��һ����ҺĤ����ɢһ����Fe2+��Ӧ����Ӧʽ��ʽ(1)��ʾ��
Fe2++O2+H+=Fe3++H2O (1)
3) ��Ӧ���ɵ�Fe3+��ˮ����γ��������ͷ������ӣ��ɱ�ʾΪʽ(2)��
Fe3++H2O=FeOOH+H+ (2)
4) �кͼ��������ɵ�H+����Ӧʽ��дΪʽ(3)��
ZnO+2H+=Zn2++H2O (3)
���У�����1)���ڴ��ʲ��裬����2)�漰���ʺͻ�ѧ��Ӧ������3)���ڻ�ѧ��Ӧ���裬ʽ(2)���ڲ��漰�����ഫ�ʣ�����Ϊ��˲ʱ��Ӧ��
�ۺ�ʽ(1)��(2)����д���ܰ���Ӧʽ(4)��
Fe2+(Һ��B)+O2(����A)+H2O=FeOOH+H+ (4)
����Fe2+��ˮ�������ķ�Ӧ�Dz�������Һ�෴Ӧ����Ӧ��������Fe2+�ļ����ֱ�Ϊm��n����ô����Һ��䴫�����ʷ��̿���ʽ(5)��ʾ��
NA=kG(pA-pAi)=EkL(cAi-cAL) (5)
ʽ�У�NA��ʾ�������ʣ�kGΪ�����ܴ���ϵ����kLΪҺ���ܴ���ϵ����pA��ʾ���������౾��ķ�ѹ��Pa��pAi��ʾ�����������ķ�ѹ��Pa��cAiΪ������������Ũ�ȣ�mol/L��cALΪ������Һ�౾���Ũ�ȣ�mol/L��EΪ��ǿ����[21]��
 (6)
(6)
ʽ�У�HaΪ���ﳣ��[22]�������ʽΪ
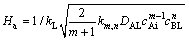 (7)
(7)
ʽ�У�mΪ������Ӧ������nΪFe2+��Ӧ������km,nΪm��n��������Ӧ���ʳ�����DAL��ʾ������ɢϵ����cm2/s��cBL��ʾҺ��������Fe2+Ũ�ȣ�mol/L��
�����������ݣ���Ϊ����������Ӧ���ڿ��ٷ�Ӧ����Կ��ٷ�Ӧ[23]����Ӧ������ͼ9��ʾ��ͼ�У�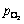 Ϊ����ռ���౾��ķ�ѹ��Pa��
Ϊ����ռ���౾��ķ�ѹ��Pa�� Ϊ�����������Ũ�ȣ�mol/L��
Ϊ�����������Ũ�ȣ�mol/L��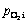 Ϊ�����������ķ�ѹ��Pa��
Ϊ�����������ķ�ѹ��Pa��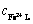 ΪFe2+��Һ�౾���Ũ�ȣ�mol/L��
ΪFe2+��Һ�౾���Ũ�ȣ�mol/L��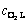 ΪO2��Һ�౾���Ũ�ȣ�mol/L��
ΪO2��Һ�౾���Ũ�ȣ�mol/L��
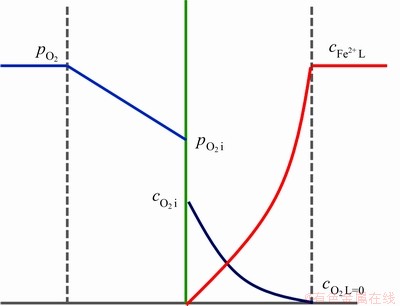
ͼ9 ���ٷ�Ӧ��Ӧ����
Fig. 9 Process of rapid reaction
��Һ����洦ƽ������cAi=HApAi��Һ��������cAL=0���ó�Fe2+�ķ�Ӧ���ʣ�
 (8)
(8)
ʽ�У�HA��ʾ�����ĺ���ϵ����mol/(L��Pa)��cB��ʾFe2+Ũ�ȣ�mol/L��t��ʾ��Ӧʱ�䣬s��a��ʾ���ݱȱ������m2/m3��
���ٷ�ӦΪ���ʹ��̿��ƣ�����ȫ��������ҺĤ�ڽ��У���ʱHa��3���ó�E=Ha���Ӷ���

 (9)
(9)
ʽ�У�kΪ���ʳ�����
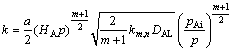 (10)
(10)
��348~358 K�¶������µ��������ݷֱ���һ����Ӧ�Ͷ�����Ӧ���ص������ϣ������ͼ10��11��ʾ����Ȼ��������Ӧ������һ����Ӧ������
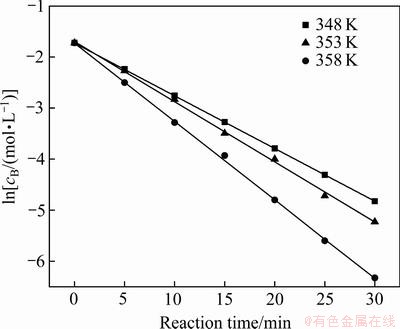
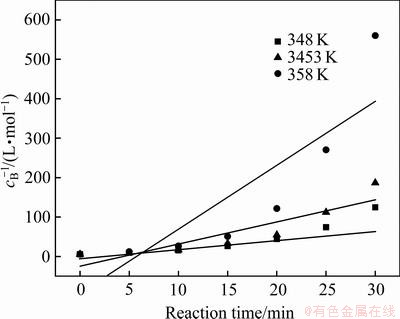
ͼ10 ��ͬ�¶���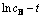 �������ͼ
�������ͼ
Fig. 10 Linear relationship between 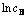 and reaction time at various temperatures
and reaction time at various temperatures
ͼ11 ��ͬ�¶��� �������ͼ
�������ͼ
Fig. 11 Linear relationship between 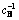 and reaction time at various temperatures
and reaction time at various temperatures
����һ����Ӧ���������������������õ����������ݶ�ʱ����д������Բ�ͬ������Fe2+Ũ�ȵ���Ȼ������ʱ����ͼ������������ϣ������ͼ12~15��ʾ���������ֱ���㲻ͬ�¶�������Ӧ�������ʳ������������ϵ������ֵ���2����(���У�k1��ʾ�������ʳ�����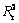 ��ʾ�������ϵ��)��
��ʾ�������ϵ��)��
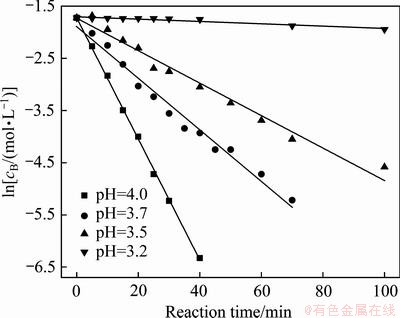
ͼ12 ��ͬpH��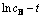 �������ͼ
�������ͼ
Fig. 12 Linear relationship between 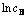 and reaction time at various pH values
and reaction time at various pH values

ͼ13 ��ͬ����Ũ����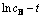 �������ͼ
�������ͼ
Fig. 13 Linear relationship between 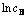 and reaction time at various oxygen concentrations
and reaction time at various oxygen concentrations
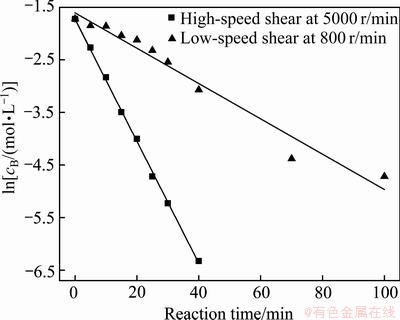
ͼ14 ��ͬ����ǿ����ʽ��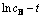 �������ͼ
�������ͼ
Fig. 14 Linear relationship between 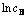 and reaction time in different strengthening ways by flow field
and reaction time in different strengthening ways by flow field
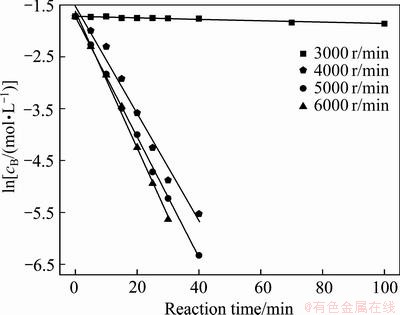
ͼ15 ��ͬ����������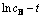 �������ͼ
�������ͼ
Fig. 15 Linear relationship between 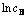 and reaction time at various shear-velocity
and reaction time at various shear-velocity
��2 ��ͬ�¶�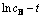 ͼ����
ͼ����
Table 2 Parameters of 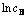 versus time at various temperatures
versus time at various temperatures
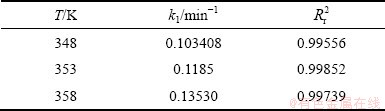
��ͬ�������������ݾ��ܽϺõ���һ����Ӧ��ϣ���Ԥ������ϣ�����Ϊ���������������̷���һ����Ӧ����ѧ������
���ݰ��������ȹ�ʽ��
 (11)
(11)
ʽ�У�AΪָǰ���ӣ�EaΪ��ܣ�kJ/mol��RΪĦ�����峣����R=8.314 J/(mol��K)��ȡ��ͬ�¶��·�Ӧ���ʳ����Ķ������¶ȵĵ�����ͼ����ͼ16��ʾ��
�������ۻ����ָǰ���ӷֱ��ǣ�Ea=27.85 kJ/mol��A=1.57��103��������ʳ�����ʾΪ
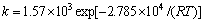 (12)
(12)
���ڻ�ѧ�ζ�����Fe2+Ũ�Ⱥܵ�ʱ���ϴ�δ����Fe2+Ũ�ȵ���0.01 mol/Lʱ�IJ������ݡ����������ⷴӦ��Ũ�ȷ�Χ�ڣ������������Ӧ���Ϻõķ�����һ����Ӧģ�ͣ����ʽ(9)���ó�n=2������Ϊ����������Ӧ����Fe2+���ӵı�����Ӧ����Ϊ������
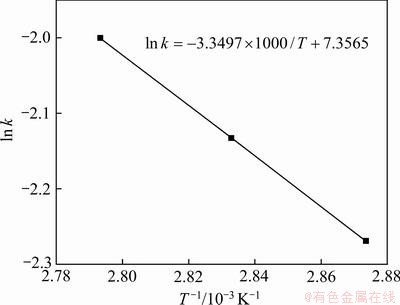
ͼ16 ln k-T-1�������ͼ
Fig. 16 Linear relationship between arrhenius plot of ln k and T-1
4 ����
1) ������Һ���з�ʽ������ǿ��������������ѧ���̣��ӿ������Ӧ���ʣ����ɵ���������ϴ�ͳ������ṹ����ò������
2) �¶ȡ�pH��ǿ����ʽ���������ʡ�����Ũ�ȵ����ضԸ���ǿ��������������Ӱ��������
3) ����ǿ������������Ӧ���̿�����˫Ĥ����ģ�ͽ��ͣ���Ӧ��ҺĤ�ڽ��У��ܴ��ʹ��̿��ơ��䶯��ѧ���̶���Fe2+����һ����Ӧ��������Fe2+�ı�����Ӧ����Ϊ��������Ӧ���Ϊ27.85 kJ/mol��
REFERENCES
[1] MURALI A, SOHN H Y. Photocatalytic properties of plasma-synthesized zinc oxide and tin-doped zinc oxide (TZO) nanopowders and their applications as transparent conducting films[J]. Journal of Materials Science: Materials in Electronics, 2018, 29(17): 14945-14959.
[2] MARIKKANNAN M, DINESH A, MAYANDI J, VISHNUKANTHAN V, PEARCE J M. Properties of Al-doped zinc oxide and In-doped zinc oxide bilayer transparent conducting oxides for solar cell applications[J]. Materials Letters, 2018, 222: 50-53.
[3] XIAO Zhen-yu, SUN Ya-yong, BAO Yu-xiang, SUN Yue-xin, ZHOU Ru-jie, WANG Lei. Two new inorganic-organic hybrid zinc phosphate frameworks and their application in fluorescence sensor and photocatalytic hydrogen evolution[J]. Journal of Solid State Chemistry, 2019, 269: 575-579.
[4] ��ï��. ���п��п�Ͻ�չ��״[J]. �����Ϳ��, 2003, 22(6): 40-45.
AN Mao-zhong. Current development of zinc and zinc alloy electroplating[J]. Clectroplating & Finishing. 2003, 22(6): 40-45.
[5] ���. ������пұ���������½�չ[J]. �й���ɫұ��, 2004, 6(3): 5-8.
SUN De-kun. New progress of zinc metallurgical technology at home and abroad[J]. China Nonferrous Metallurgy, 2004, 6(3): 5-8.
[6] �����, �����, �� ��. ʪ����п�����г������յĽ�չ[J]. ����ۺ�����, 2014(6): 11-14.
WU Ke-ming, SUN Da-lin, HU Jie. Progress of technology optimization of precipitation of iron in zinc hydrometallurgy[J]. Multipurpose Utilization of Mineral Resources, 2014(6): 11-14.
[7] �� ��, �� ��, ������, ������. ��ɫұ�����̽�ģ���Ż���������̽��[J]. �Զ���ѧ��, 2017, 43(6): 880-892.
ZHANG Bei, SUN Bin, YANG Chun-hua, GUI Wei-hua. Discussion on modeling and optimal control of nonferrous metallurgical purification process[J]. Acta Automatica Sinica, 2017, 43(6): 880-892.
[8] Ԭ����, �����, ��ٻٻ. ʪ����п�������յ���״��չ��[J]. ����ۺ�����, 2011(2): 32-34.
YUAN Fan-qin, WU Ke-ming, DING Qian-qian. Status and prospect of technology for iron removal in zinc hydrometallurgy[J]. Multipurpose Utilization of Mineral Resources, 2011(2): 32-34.
[9] �� ɯ. ֱ�ӽ�����п����������������Fe2+Ũ���ݶ��Ż�[D]. ��ɳ: ���ϴ�ѧ, 2012.
WANG Sha. Fe2+ concentration gradient optimization in the process of iron removal by goethite method during direct leaching of zinc[D]. Changsha: Central South University, 2012.
[10] ������. ʪ����п���������������������[J]. ����������о�, 1998(1): 12-16.
HU Peng-fei. Hot acid leaching process of zinc hydrometallurgy: A review[J]. Engineering Design & Research, 1998(1): 12-16.
[11] CHOI H B, CHUN M P, CHUN S Y, H J A. Synthesis and shape control of goethite nano particles[J]. Journal of the Korean Institute of Electrical and Electronic Material Engineers, 2016, 29(9): 552-558.
[12] CLAASSEN J O, MEYER E H O, RENNIE J, SANDENBERGH R F. Iron precipitation from zinc-rich solutions: Defining the zincor process[J]. Hydrometallurgy, 2002, 67(1): 87-108.
[13] LOAN M, NEWMAN O M G, COOPER R M G, FARROW J B, PARKINSON G M. Defining the paragoethite process for iron removal in zinc hydrometallurgy[J]. Hydrometallurgy, 2005, 81(2): 104-129.
[14] ֣����. ������������ʵ��[J]. ���̼��������(Ӣ��), 2017(3): 242-243.
ZHRNG Li-li. The industrial practice of iron removal by goethite method[J]. Engineering Technology & Management, 2017(3): 242-243.
[15] ף��ˮ, ������. ������������������Ļ���̽��[J]. ������Ⱦ�����, 2007(3): 178-203.
ZHU Chun-shui, SUN Zhen-ya. Adsorption of chromium on biomineralized goethite[J]. Environmental Pollution & Control, 2007(3): 178-203.
[16] �� ��, ��ع��, ֣ ǿ. ���������յ�iPP���½ᾧ��Ϊ���о�[J]. �߷���ѧ��, 2007(5): 70-74.
CHEN Qing, FAN Yu-run, ZHEN Qiang. Shear induced crystallization of isotactic polypropylene[J]. Acta Polymerica Sinica, 2007(5): 70-74.
[17] �� ˶, �� ��. ������������Һ���������ײģ��[J]. ����������ѧ��, 2007, 28(1): 189-192.
CHEN Shuo, SHANG Zhi. Simulating the breakup and collision of drops in simple shear flow[J]. Journal of Engineering Thermophysics, 2007, 28(1): 189-192.
[18] ���콾. ������Ի�״��������Ʊ�����ˮ��Һ��ȥ��U(��)��ʵ���о�[D]. ����: �ϻ���ѧ, 2018.
JIANG Tian-jiao. Preparation of a phosphate-modified flower-like ��-FeOOH composite and its application for aqueous U(��) removal[D]. Hengyang: University of South China, 2018.
[19] WANG J. Flow reactor models for fluid-fluid systems, based on the two-film theory[J]. Chemical Engineering Journal & the Biochemical Engineering Journal, 1995, 60(1/3): 105-110.
[20] HANSEN E, MOLLERUP J. Application of the two-film theory to the determination of mass transfer coefficients for bovine serum albumin on anion-exchange columns[J]. Journal of Chromatography A, 1998, 827(2): 259-267.
[21] KUMAR P S, HOGENDOORN J A, FERON P H M. Approximate solution to predict the enhancement factor for the reactive absorption of a gas in a liquid flowing through a microporous membrane hollow fiber[J]. Journal of Membrane Science, 2003, 213(1/2): 231-245.
[22] ALAGY J, TRAMBOUZE P, van LANDEGHEM H. Designing a cyclohexane oxidation reactor[J]. Industrial & Engineering Chemistry Process Design and Development, 1974, 13(4): 317-323.
[23] �����, ��ϣ��, ������, �����. ���������������ͪ���ٷ�Ӧ����ѧ[J]. ������ѧѧ��, 1993(5): 692-697.
LI Da-zhen, DENG Xi-xian, WANG Yu-wen, HOU En-jian. Studies on kinetics of the fast reaction between potassium permanganate and acetylacetone[J]. Acta Physico-chimica Sinica, 1993(5): 692-697.
Study of macro-kinetic of iron removal by goethite process enhanced by high shear on ZnSO4-FeSO4 solution system
WANG Wen-chao, YANG Jian-guang, YAN Wan-peng, NAN Tian-xiang, TANG Chao-bo, ZENG Wei-zhi, LI Ling-chen
(School of Metallurgy and Environment, Central South University, Changsha 410083, China)
Abstract: Shear used commonly in polymer emulsification and dispersion was introduced into the process of iron removal by goethite method in the field of hydrometallurgy. In order to study the macro-kinetic of iron removal by goethite process enhanced by high shear, ZnSO4-FeSO4 solution system was taken as research object. The effects of temperature, pH, strengthening way by flow field, shear-velocity and oxygen concentration on the velocity of iron removal were investigated by single factor test method. The results show that temperature, pH, strengthening way by flow field, shear-velocity and oxygen concentration have significant effects on the velocity of iron removal. Kinetic data based on the results show that the process of iron removal by goethite method is controlled by mass transfer process, and the reaction is in line with the characteristics of first-order reaction. The reaction of iron removal by goethite method by high shear is second-order with respect to Fe2+ with activation energy of 27.85 kJ/mol.
Key words: shear; strengthening way by flow field; kinetic; goethite
Foundation item: Project(2018YFC1900403) supported by The National Key Research and Development Program of China
Received date: 2019-07-09; Accepted date: 2020-06-11
Corresponding author: YANG Jian-guang; Tel: +86-731-88830470; E-mail: jianguang_y@163.com
(�༭ �� ��)
������Ŀ�������ص��з�ר�����������Ŀ(2018YFC1900403)
�ո����ڣ�2019-07-09�������ڣ�2020-06-11
ͨ�����ߣ���㣬���ڣ���ʿ���绰��0731-88830470��E-mail��jianguang_y@163.com