文章编号:1004-0609(2014)06-1678-07
浸矿微生物共培养体系的耐氟特性及其在氟胁迫下的群落动态分析
李 乾1, 2,丁德馨1, 2,王清良1,胡鄂明1,史文革1,马丽媛3,刘学端3
(1. 南华大学 核资源工程学院,衡阳 421001;
2. 南华大学 铀矿冶生物技术国防重点学科实验室,衡阳 421001;
3. 中南大学 资源加工与生物工程学院,长沙 410083)
摘 要:为了探明混合浸矿微生物的耐氟特性及其群落动态,构建5株浸矿细菌(Acidithiobacillus ferrooxidans ATCC 23270, Leptospirillum ferriphilum YSK, Sulfobacillus thermosulfidooxidans ST, Acidithiobacills thiooxidans A01, Acidithiobacills caldus S1)的共培养体系。结果表明:氟胁迫在一定程度上抑制了该共培养体系的生长繁殖,对于高浓度的氟胁迫,共培养体系也保持较为平稳的生长延滞状态;氟胁迫对共培养体系硫氧化活性的影响并不明显。采用实时荧光定量PCR技术对其培养体系的群落动态进行分析。结果表明,不论是氟胁迫下还是无氟胁迫下,L. ferriphilum YSK和A. caldus S1,都是群落中的优势种群;而A. ferrooxidans ATCC 23270、S. thermosulfidooxidans ST和A. thiooxidans A01为劣势种群。共培养体系中受氟胁迫影响最大的是S. thermosulfidooxidans ST,菌体密度急剧下降;其次是A. caldus S1、A. thiooxidans A01和A. ferrooxidans ATCC 23270,氟胁迫在一定程度上也抑制了对它们的生长;而L. ferriphilum YSK在氟胁迫下的生长非常稳定。
关键词:浸矿微生物;共培养体系;氟耐受性;群落动态
中图分类号:Q819 文献标志码:A
Fluoride tolerance of co-culture of bioleaching microorganisms and community dynamics under fluoride stress
LI Qian1, 2, DING De-xin1, 2, WANG Qing-liang1, HU E-ming1, SHI Wen-ge1, MA Li-yuan3, LIU Xue-duan3
(1. School of Nuclear Resources Engineering, University of South China, Hengyang 421001, China;
2. Key Discipline Laboratory for National Defence of Biotechnology in Uranium Mining and Hydrometallurgy,
University of South China, Hengyang 421001, China;
3. School of Minerals Processing and Bioengineering, Central South University, Changsha 410083, China)
Abstract: In order to explore the fluoride tolerance and the community dynamics of mixed bioleaching microorganisms, a co-culture including five typical bioleaching strains (Acidithiobacillus ferrooxidans ATCC 23270, Leptospirillum ferriphilum YSK, Sulfobacillus thermosulfidooxidans ST, Acidithiobacills thiooxidans A01, Acidithiobacills caldus S1) was constructed. The results show that the growth of the co-culture is inhibited by fluoride stress, and the co-culture keeps the stable cell density at high fluoride stress. The sulfur activity of the co-culture is not affected by fluoride stress. Microbial community dynamics of the co-culture was analyzed by real-time fluorescent quantitative PCR technology. The results show that L. ferriphilum YSK and A. caldus S1 are always the dominant species at fluoride stress or non-stress, while the minor is A. ferrooxidans ATCC 23270, S. thermosulfidooxidans ST and A. thiooxidans A01. Besides, S. thermosulfidooxidans ST is inhibited most obviously in the co-culture at fluoride stress, secondly A. caldus S1, A. thiooxidans A01 and A. ferrooxidans ATCC 23270, while the L. ferriphilum YSK still maintains a very stable growth.
Key words: bioleaching microorganisms; co-culture; fluoride tolerance; community dynamics
生物冶金技术适用于处理低品位铀矿及其尾矿,然而氟对微生物的生长具有很强的抑制或杀死作用,高氟铀矿石的微生物浸出一直是一个难题。据报道,高氟铀矿石的微生物堆浸尾液中的氟浓度达到2~4 g/L[1],这对浸矿微生物的耐氟能力是一个严峻的挑战,因此,研究微生物对氟的耐受性机制具有极其重要的理论和实践意义。
浸矿微生物主要是一些嗜酸性微生物,在这些微生物中,既有一些利用铁、硫的氧化代谢来获得生长发育所需能量的自养菌,又包括一些能够利用有机物质的异养菌,这些微生物在浸矿系统中相互作用,共同维持着体系的碳、氮、铁和硫的物质循环[2-3]。大量研究[4-10]表明,在生物浸矿过程中,嗜酸硫氧化细菌与铁氧化细菌的混合培养物在硫化矿的浸出过程中浸出速率比单独使用某种细菌时的浸出速率显著提高。DOPSON等[9]通过将Acidithiobacillus caldus与Sulfobacillus thermosulfidooxidans在含砷黄铁矿中混合浸矿,发现其浸矿速率比单独使用其中一种时明显提高,并推测其机理为Acidithiobacillus caldus能利用附着在矿物表明的固体硫,从而浸矿细菌能接触到矿物并起作用。OKIBE等[10]研究了7种细菌和1种古菌种的组合,最有效的浸出系统是 A. caldus、Leptospirllum sp. MT6和Ferroplasma sp. MT17的组合。大量研究[4-11]表明,当多种不同特性的酸性浸矿菌株混合使用时,各菌株对铁离子、硫元素及其他金属离子的不同作用方式使混合菌株具有优势互补作用。
另一方面,微生物在浸矿过程中常会遭遇高浓度重金属离子、阴离子等不利环境,但迄今为止,很少有关于混合浸矿微生物在不同环境胁迫下的耐受能力和生存维持能力的相关研究报道,大部分关于浸矿微生物耐受性的报道还停留在对单一浸矿细菌的研究上,研究表明[12-16],微生物耐受性优劣除了与微生物生长环境的化学因素有关外,更重要的是由微生物本身的生理结构与遗传特性决定的。然而,混合浸矿微生物应对环境胁迫的耐受能力还有待进一步研究。
为了研究混合浸矿微生物的耐氟特性,本文作者有效地构建一个浸矿微生物共培养体系,并考虑到其多样性和稳定性,选取如下3类典型的浸矿微生物:1) 嗜酸氧化亚铁硫杆菌(Acidithiobacills ferrooxidans)和嗜热硫氧化硫化杆菌(Sulfobacillus thermosulfidooxidans),既有硫氧化能力又有铁氧化能力,最适生长温度分别为30和45 ℃;2) 嗜铁钩端螺旋菌(Leptospirillum ferriphilum),该类细菌是铁氧化菌,只能氧化亚铁,铁离子耐受度高,最适生长温度为40 ℃;3) 嗜酸氧化硫硫杆菌(Acidithiobacills thiooxidans)和喜温嗜酸硫杆菌(Acidithiobacills caldus),该类细菌为硫氧化菌,能以单质硫和还原性硫化合物(硫化物、亚硫酸盐、硫代硫酸盐及各种连多硫酸盐等)作为能源物质进行专性或兼性化能自养生长。为了研究混合浸矿微生物的耐氟特性,本文作者构建了上述5株铁硫氧化细菌的共培养体系,并研究该共培养体系在不同氟胁迫下的生长速率及铁、硫氧化速率,进一步应用实时荧光定量PCR技术检测该共培养体系在氟胁迫下的群落动态规律。
实时荧光定量PCR(Real time fluorescent quantitative PCR,FQ-PCR)技术是在PCR 技术基础上发展起来的一种高度灵敏的核酸定量技术。它是在PCR 反应体系中加入荧光基团,利用荧光信号来实时监测整个PCR 进程,最后通过所测基因的标准曲线对未知模板浓度进行定量分析,可通过微生物的16S rDNA、gyrB等管家基因作为分子标尺来精确定量微生物种群数量[17-18]。
1 实验
1.1 共培养体系的构成与培养条件
本研究中所用的5株浸矿细菌(Acidithiobacillus ferrooxidans ATCC 23270, Leptospirillum ferriphilum YSK, Sulfobacillus thermosulfidooxidans ST, Acidithiobacills thiooxidans A01, Acidithiobacills caldus S1)的分离与培养参照文献[19]。将上述浸矿细菌等量混合组成,每株细菌的接种量为6×105 cell/mL。培养基为9K基本盐,加入44.7 g/L FeSO4・7H2O和10.0 g/L单质硫作为能源物质,培养温度为40 ℃,培养基pH值为1.8,摇床转速为175 r/min。
1.2 共培养体系的氟胁迫处理
细菌总量到对数生长前期时,用20 g/L NaF溶液来胁迫处理细菌,调节菌液的氟浓度分别为2.4、4.8、7.2、9.6和12 mmol/L,分别测定生长曲线;氟胁迫处理的时间为共培养体系总菌量的生长对数期(30 h)。
1.3 细菌生长测定与铁、硫氧化速率检测
应用血细胞计数板计数来检测共培养体系的总菌量变化,进而通过Real-time PCR技术来定量各个菌株的生长变化。铁氧化速率通过重铬酸钾滴定Fe2+浓度来测定,硫氧化速率通过测定pH值来间接反映。根据不同细菌的生长周期合理取样,检测细胞个数与铁、硫氧化速率。应用数据制图分析软件Origin 8.0分析数据,得到共培养体系的总生长曲线与铁、硫氧化速率曲线。
1.4 细菌收集与基因组DNA的提取和纯化
根据细菌浓度取30~200 mL菌液,用滤纸过滤,12000 g离心收集菌体后,用pH值2.0的稀硫酸洗涤菌体。后续的DNA提取与纯化采用TIANamp细菌基因组DNA提取试剂盒,按照其说明进行操作。提取的基因组DNA采用1%的琼脂糖凝胶电泳检测其质量,并采用NanoDrop ND-1000微量分光光度计检测其浓度及纯度。
ND-1000微量分光光度计检测其浓度及纯度。
1.5 特异性引物的设计与检测
采用“Primer Premier 5.0”软件针对所用的5株浸矿细菌设计gyrB基因的特异性引物,然后由上海生工生物公司合成。各株细菌的特异性引物序列及相关信息如表1所列。
每对引物都要通过严格的检测来验证其特异性。以5株纯菌的基因组DNA依次作为模板,将所设计的每一对特异性引物来PCR扩增的gyrB特异性片段,用溴乙锭染色的2%琼脂糖凝胶电泳,观察片段的大小以及特异性情况,保证对应的引物扩增对应的模板得到准确的目标产物。并切取凝胶上的特异性片段,经克隆后,送上海生工生物公司进行序列分析,并将测得的序列与目的片段进行比对,保证目的gyrB片段的准确性。
1.6 Real-time PCR检测
1.6.1 建立标准曲线
每株菌的gyrB基因PCR产物经2%琼脂糖凝胶电泳分离,切胶回收,经DNA凝胶回收试剂盒(E.Z.N.A.TM Gel Extraction Kit, Omega)纯化,根据每株菌的gyrB基因PCR产物长度及其浓度初步计算其拷贝数。将获得的PCR产物按10倍梯度稀释,作为阳性定量标准模板,用于Real-time PCR反应条件的优化、标准曲线的建立和样品的检测。同时,将DNA样品稀释成100 ng/μL左右,Real-time PCR检测待用,因为浓度过高会减低其精确度。
1.6.2 配置反应体系
准备Real-time PCR专用的96孔板,加入反应物(25 μL):iQ SYBR Green Supermix (Toyobo Co., LTD., Osaka, Japan) 12.5 μL、正反向引物各0.5 μL、待测DNA 5 μL,补充ddH2O 6.5 μL。每个样品检测3次,同时设置3个阴性对照样。
1.6.3 设置程序,收集数据
Real-time PCR所用仪器为iCycler iQ detection system (Bio-Rad Laboratories Inc., Hercules, USA)。其反应程序如下:95 ℃预变性3 min;然后95 ℃解链15 s,在退火温度(见表1)下引物退火15 s,72 ℃延伸20 s,共40个循环;在循环结束后,95 ℃ 1 min,55 ℃ 1 min,最后进行PCR产物溶解曲线的检测,反应温度从55 ℃逐渐上升到PCR products95 ℃,每增加0.5 ℃保持10 s。由溶解曲线判别PCR扩增产物的特异性情况,根据荧光曲线的Ct值(荧光信号达到设定阈值所需循环数)以及标准曲线计算种群数量。然后应用数据制图分析软件Origin 8.0绘制曲线,得到细菌种群的动态变化曲线。
表1 所用5株浸矿细菌的特异性引物信息
Table 1 Primers information specified for five bioleaching strains

2 结果与讨论
2.1 引物特异性检测分析
采用将所设计的每对特异性引物来对所用5株纯菌的基因组DNA依次进行PCR扩增,PCR产物经2%的琼脂糖凝胶电泳检测,发现对应的引物恰好能扩增对应的模板DNA,并且PCR产物均是一条片段,片段的长度也与所设计的相一致,再将测序结果与待扩增的DNA片段序列进行比对,结果表明,获得了准确的目标基因片段,而且具有良好的特异性。
Real-time PCR扩增反应完成后,通过逐步增加温度同时监测每一步的荧光信号来产生溶解曲线,随着反应中双链DNA变性,荧光染料又回复到游离状态,导致荧光信号降低。因此,以荧光信号改变的负的一次导数(纵坐标,-dRfu)对反应温度(横坐标,t)作图,得图1。由图1可见,在扩增产物的溶解温度上有一特征峰(tm,DNA双链解链50%的温度),且均呈单峰带,表明无非特异性产物或引物二聚体区产生,从而再次验证了引物的特异性。
2.2 共培养体系的耐氟性状分析
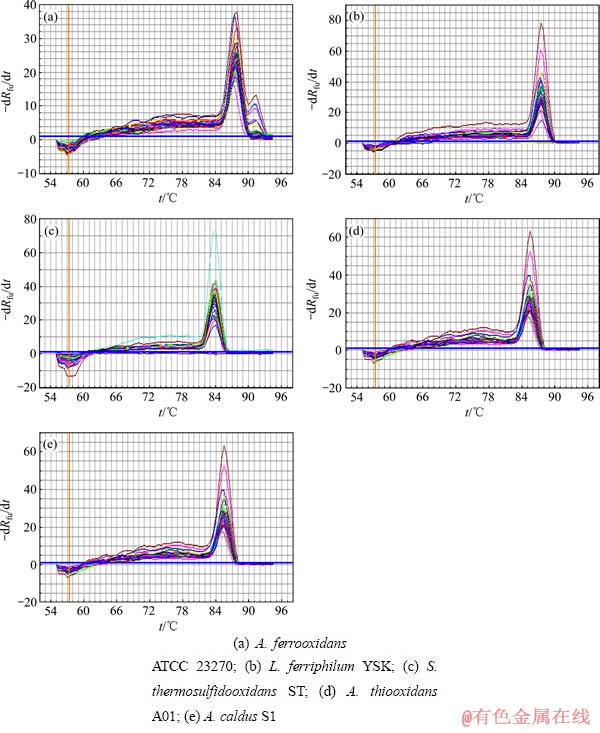
图1 所用5株浸矿细菌的Real-time PCR产物溶解曲线
Fig. 1 Melt curves of Real-time PCR products of five strains in this study
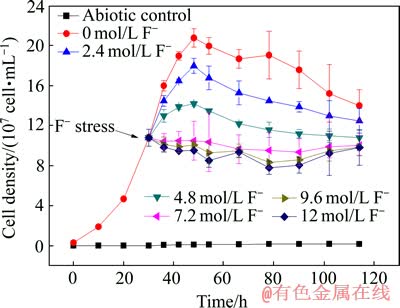
图2 所构建的共培养体系在不同浓度氟胁迫下的生长曲线
Fig. 2 Growth curves of co-culture at different fluoride stresses
图2所示为所构建的共培养体系在不同浓度氟胁迫下的生长曲线。由图2可知,在不同浓度氟的胁迫下,该共培养体系的生长繁殖也受到了不同程度的抑制。当培养环境的氟浓度为2.4 mmol/L时,共培养体系的菌体密度出现了较为明显的下降,最大菌体密度比无胁迫条件下的低2.0×107 cell/mL左右;当4.8 mmol/L的氟胁迫时与2.4 mmol/L氟胁迫时的情况比较相似,只是菌体密度抑制得更明显一些,其最大菌体密度比无胁迫条件下的低5.8×107 cell/mL左右;当培养基中氟浓度升高到7.2~12 mmol/L时,共培养体系出现了明显的生长延滞,但是并没发现菌体密度明显下降的现象,处于较为平稳的生长状态,这也是共培养体系相比纯培养细菌体现出的一些优势,因为纯培养细菌在氟浓度较高的情况下都出现了一定程度的细胞裂解的现象。上述结果说明,氟胁迫在一定程度上抑制了该共培养体系的生长繁殖,但对于高浓度的氟胁迫共培养体系表现出了较为稳定的生长(见图2)。
但是,该共培养体系在高浓度的氟胁迫下铁氧化速率抑制较为明显(见图3)。如图3所示,在2.4 mmol/L氟胁迫下,其铁氧化速率有所减缓,铁完全氧化时间延长了18 h左右;当4.8 mmol/L氟胁迫时,其铁氧化速率减缓很明显,铁完全氧化时间延长了30 h左右;当7.2 mmol/L氟胁迫时,亚铁已难以被完全氧化,当氟胁迫浓度高于9.6 mmol/L时,其铁氧化速率几乎停滞。单从铁氧化速率来说,共培养体系不如单一的铁氧化细菌[19],这可能是因为共培养体系的能源选择更多,不只有亚铁,还有硫作为能源,也许更多的细菌在利用硫来生长。
研究表明,单一的硫氧化细菌在氟的胁迫下培养基pH值的下降速率明显减慢甚至停滞[19],而共培养体系不同,如图4所示,共培养体系在不同浓度的氟胁迫下,pH值下降的趋势与无胁迫时的基本一致,因为pH值的下降主要是硫被氧化为硫酸导致的,因此共培养体系的硫氧化速率并没有受到明显的抑制。需说明的是,在加氟的瞬间,pH值有稍许的增大,但这是NaF溶液部分水解呈弱碱性所造成的,并不是因为硫氧化活性被抑制了,更加说明共培养对硫氧化能力保持的稳定性。
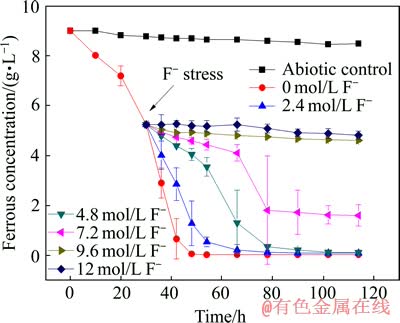
图3 所构建的共培养体系在不同浓度氟胁迫下的铁氧化速率
Fig. 3 Iron oxidation rate of co-culture at different fluoride stresses
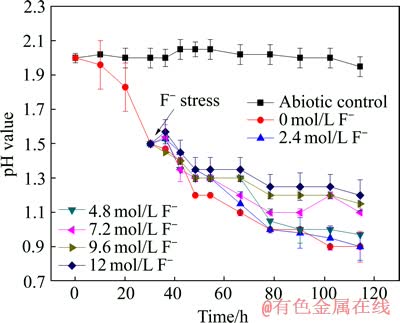
图4 所构建的共培养体系在不同浓度氟胁迫下的pH值变化
Fig. 4 Variation of pH value of co-culture at different fluoride stresses
综上所述,该共培养体系能耐受更高浓度的氟胁迫,虽然其铁氧化速率不如单一的铁氧化细菌,但是其硫氧化速率的保持能力得到明显增强。
2.3 氟胁迫前后共培养体系的群落动态变化
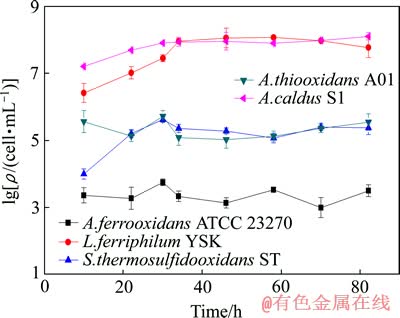
图5 所构建的共培养体系在无氟胁迫下的群落动态
Fig. 5 Microbial community dynamics of co-culture at non-fluoride stress (ρ is bacteria density)
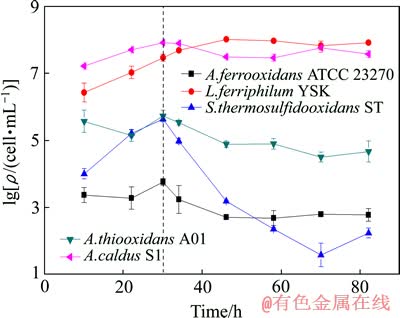
图6 所构建的共培养体系在4.8 mmol/L氟胁迫后的群落动态
Fig. 6 Microbial community dynamics of co-culture at 4.8 mmol/L fluoride stress
为了探明氟胁迫对该共培养体系种群结构及其动态的影响,对比分析了无氟胁迫和4.8 mmol/L氟胁迫下该共培养体系的群落动态(见图5和6)。由图5和6可知,不管是无氟胁迫下还是4.8 mmol/L氟胁迫下,L. ferriphilum YSK和A. caldus S1,都是群落中的优势种群;而A. ferrooxidans ATCC 23270、S. thermosulfidooxidans ST和A. thiooxidans A01也都是群落中的劣势种群,且A. ferrooxidans ATCC 23270的菌体密度最低。产生这种现象的主要原因可能是培养温度40 ℃最为接近L. ferriphilum YSK和A. caldus S1的最适生长温度,单一的培养条件不利于保持群落的多样性。
比较分析无氟胁迫和4.8 mmol/L氟胁迫的群落动态,发现共培养体系中受氟胁迫影响最大的是S. thermosulfidooxidans ST,菌体密度直线下降,58 h时无氟胁迫条件下菌体密度为1.16×105 cell/mL,而同期氟胁迫条件下为2.24×102 cell/mL,下降了516.8倍;到70 h时,无氟胁迫条件下菌体密度为2.5×105 cell/mL,而同期氟胁迫条件下菌体密度为3.78×101 cell/mL,下降到原菌密度的1/6613。其次是A. caldus S1、A. thiooxidans A01、A. ferrooxidans ATCC 23270,氟胁迫在一定程度上也抑制了它们的生长。58 h时,A. caldus S1在无氟胁迫条件下的菌体密度为7.87×107 cell/mL,而同期氟胁迫条件下为4.05×107 cell/mL,下降到原菌密度的1/1.94;同时A. thiooxidans A01的菌体密度下降到原菌密度的1/1.72,A. ferrooxidans ATCC 23270的下降到原菌密度的1/1.6。有意思的是,L. ferriphilum YSK生长基本保持稳定,并没有受到氟胁迫的影响。
3 结论
1) 氟胁迫在一定程度上抑制了该共培养体系的生长繁殖,对于高浓度的氟胁迫共培养体系也保持较为平稳的生长延滞状态。单就铁氧化活性来说,共培养体系不如单一的铁氧化细菌。对于硫氧化活性来说,单一的硫氧化细菌在氟胁迫时硫氧化活性基本消失,而共培养体系硫氧化活性受到的影响并不明显。
2) 群落动态分析表明,不论是氟胁迫下还是无氟胁迫下,L. ferriphilum YSK和A. caldus S1都是群落中的优势种群;而A. ferrooxidans ATCC 23270、S. thermosulfidooxidans ST和A. thiooxidans A01为劣势种群。共培养体系中受氟胁迫影响最大的是S. thermosulfidooxidans ST,菌体密度急剧下降;其次是A. caldus S1、A. thiooxidans A01和A. ferrooxidans ATCC 23270,氟胁迫在一定程度上也抑制了它们的生长;然而,L. ferriphilum YSK在氟胁迫下保持非常稳定的生长。
REFERENCES
[1] 李 江, 饶 军, 刘亚洁, 孙占学, 李学礼, 史维浚. 高氟铀矿石微生物堆浸工业试验[J]. 有色金属: 冶炼部分, 2011(7): 26-29.
LI Jiang, RAO Jun, LIU Ya-jie, SUN Zhan-xue, LI Xue-li, SHI Wei-jun. Industrial bio-heap leaching of uranium ores rich in fluorite[J]. Nonferrous Metals: Extractive Metallurgy, 2011(7): 26-29.
[2] RAWLINGS D E. Characteristics and adaptability of iron- and sulfur-oxidizing microorganisms used for the recovery of metals from minerals and their concentrates[J]. Microbial Cell Factories, 2005, 4: 13.
[3] RAWLINGS D E, JOHNSON D B. The microbiology of biomining: Development and optimization of mineral-oxidizing microbial consortia[J]. Microbiology, 2007, 153: 315-324.
[4] FU Bo, ZHOU Hong-bo, ZHANG Ru-bin, QIU Guan-zhou. Bioleaching of chalcopyrite by pure and mixed cultures of Acidithiobacillus spp. and Leptospirillum ferriphilum[J]. International Biodeterioration and Biodegradation, 2008, 62: 109-115.
[5] RAWLINGS D E, JOHNSON D B. The microbiology of biomining: Development and optimization of mineral-oxidizing microbial consortia[J]. Microbiology, 2007, 153: 315-324.
[6] AKCIL A, CIFTCI H, DEVECI H. Role and contribution of pure and mixed cultures of mesophiles in bioleaching of a pyritic chalcopyrite concentrate[J]. Minerals Engineering, 2007, 20: 310-318.
[7] ZHANG Ru-bin, WEI Man-man, JI Hou-guo, CHEN Xin-hua, QIU Guan-zhou, ZHOU Hong-bo. Application of real-time PCR to monitor population dynamics of defined mixed cultures of moderate thermophiles involved in bioleaching of chalcopyrite[J]. Applied Microbiology and Biotechnology, 2009, 81: 1161-1168.
[8] PLUMB J J, MCSWEENEY N J, FRANZMANN P D. Growth and activity of pure and mixed bioleaching strains on low grade chalcopyrite ore[J]. Minerals Engineering, 2008, 21: 93-99.
[9] DOPSON M,  E B. Potential role of Thiobacillus caldus in arsenopyrite bioleaching[J]. Applied and Environmental Microbiology, 1999, 65(1): 36-40.
E B. Potential role of Thiobacillus caldus in arsenopyrite bioleaching[J]. Applied and Environmental Microbiology, 1999, 65(1): 36-40.
[10] OKIBE N, JOHNSON D B. Biooxidation of pyrite by defined mixed cultures of moderately thermophilic acidophiles in pH-controlled bioreactors: Significance of microbial interactions[J]. Biotechnology and Bioengineering, 2004, 87(5): 574-583.
[11] XIA Le-xian, TANG Lu, XIA Jin-lan, YIN Chu, CAI Li-yuan, ZHAO Xiao-juan, NIE Zhen-yuan, LIU Jian-she, QIN Guan-zhou. Relationships among bioleaching performance, additional elemental sulfur, microbial population dynamics and its energy metabolism in bioleaching of chalcopyrite[J]. Transactions of Nonferrous Metal Society of China, 2012, 22: 192-198.
[12] 高 健, 丁建南, 康 健, 吴学玲, 邱冠周. 分离于酸性矿坑水的疑似钩端螺旋菌的鉴定及重金属对其铁氧化能力影响的评估[J]. 中国有色金属学报, 2011, 21(1): 220-226.
GAO Jian, DING Jian-nan, KANG Jian, WU Xue-ling, QIU Guan-zhou. Identification and heavy metal toxicity assessment upon Fe2+-oxidizing ability of Leptospirillum-like bacterium isolated from acid mine drainage[J]. The Chinese Journal of Nonferrous Metals, 2011, 21(1): 220-226.
[13] 吴学玲, 张云静, 刘代刚, 段 红, 范宏伟, 刘学端. 嗜酸氧化亚铁硫杆菌中金属转运基因的克隆与差异表达[J]. 中国有色金属学报, 2013, 23(2): 577-584.
WU Xue-ling, ZHANG Yun-jing, LIU Dai-gang, DUAN Hong, FAN Hong-wei, LIU Xue-duan. Clone and differential expression of metal transport genes in Acidithiobacillus ferrooxidans[J]. The Chinese Journal of Nonferrous Metals, 2013, 23(2): 577-584.
[14] KIM S, BAE J, PARK H, CHA D. Bioleaching of cadmium and nickel from synthetic sediments by Acidithiobacillus ferrooxidans[J]. Environmental Geochemistry and Health, 2005, 27(3): 229-235.
[15] CABRERA G, GOMEZ J M, CANTERO D. Kinetic study of ferrous sulphate oxidation of Acidithiobacillus ferrooxidans in the presence of heavy metal ions[J]. Enzyme and Microbial Technology, 2005, 36(2/3): 301-306.
[16] van der MERWE J A, DEANE S M, RAWLINGS D E. The chromosomal arsenic resistance genes of Sulfobacillus thermosulfidooxidans[J]. Hydrometallurgy, 2010, 104(3/4): 477-482.
[17] YIN Hua-qun, CAO Lin-hui, QIU Guan-zhou, WANG Dian-zuo, KELLOGG L, ZHOU Ji-zhong, LIU Xin-xin, DAI Zhi-min, DING Jian-nan, LIU Xue-duan. Molecular diversity of 16S rRNA and gyrB genes in copper mines[J]. Archives of Microbiology, 2008, 189: 101-110.
[18] YIN Hua-qun, CAO Lin-hui, XIE Ming, CHEN Qi-qiong, QIU Guan-zhou, ZHOU Ji-zhong, WU Li-you, WANG Dian-zuo, LIU Xue-duan. Bacterial diversity based on 16S rRNA and gyrB genes at Yinshan Mine, China[J]. Systematic and Applied Microbiology, 2008, 31: 302-311.
[19] 李 乾, 丁德馨, 王清良, 史文革, 胡鄂明, 李会娟, 马丽媛, 肖云花, 曹 杨, 刘学端. 五种典型浸矿微生物的耐氟性状对比研究[J]. 南华大学学报: 自然科学版, 2013, 27(2): 16-22.
LI Qian, DING De-xin, WANG Qing-liang, SHI Wen-ge, HU E-ming, LI Hui-juan, MA Li-yuan, XIAO Yun-hua, CAO Yang, LIU Xue-duan. Comparative study of fluoride-tolerance of five typical bioleaching microorganisms[J]. Journal of University of South China: Science and Technology, 2013, 27(2): 16-22.
(编辑 陈卫萍)
基金项目:国家重点基础研究发展计划资助项目(2010CB630901);湖南省自然科学基金(14JJ6024);湖南省教育厅科研基金(13C821);南华大学博士科研启动基金(2012XQD05)
收稿日期:2013-06-24;修订日期:2014-04-21
通信作者:刘学端,教授,博士;电话:0731-88830546;E-mail: xueduanliu@yahoo.com