ӫ���ǵ�Ҷ�����οǾ���������������
���Σ������£�����ΰ�������������, ����������
(���ϴ�ѧ �������ε�������о����ģ����� ��ɳ 410008)
ժ Ҫ���Ʊ�ӫ���ǵ�Ҷ��ż���Ǿ�����������Ϊ������ҩ���ҩϵͳ�ṩ������ϡ�ͨ��Ҷ���������Ǿ����ϵİ�����Ӧ��ʹҶ����Ǿ���ż�������������ӫ������Ҷ��ż���Ǿ��ǽ��л�ѧ�ӣ������ӽ������Ƴɾ���ӫ���Ҷ��ż���Ǿ���������������ΰ�HepG2ϸ����������ϸ��ʵ�顣ʵ����������Ҷ������������ͷ�Ӧ�¶ȼ��Լ��μ��ٶ���Ӱ��ż���ȵ���Ҫ���أ���Ҷ���������Ǿ�������������Ϊ1?1����Ӧ�¶�Ϊ30 �棬�μ��ٶ�Ϊ2 mL/min����Ӧʱ��Ϊ12 h�������¿ɵõ�ż���ȶ���Ҷ��ż���Ǿ��ǣ����Ƶõ�����������Ϊ290 nm����̬����ϸ��ӫ��Ч�����ԣ��˷����������Ʊ�ӫ���ǵ�Ҷ�����οǾ������������塣
�ؼ��ʣ�Ҷ��Ǿ��ǣ����������������ӫ����
��ͼ����ţ�R979.1; TQ460.6 ���ױ�־�룺A ���±�ţ�1672-7207(2010)01-0161-05
Preparation and characterization of fluorimetric folate-coupled chitosan nano-carrier
JIN Xin, ZHANG Yang-de, WANG Ji-wei, ZHANG Li-hua, YANG Pu, ZHANG Xu, HU Yu, YU Li
(National Hepatobiliary and Enteric Surgery Research Center, Central South University, Changsha 410008, China)
Abstract: Folate-coupled chitosan was prepared as a delivery system material for anticancer drug by the reaction of the activated folate ester with the amine group on the chitosan. The compound of folate-coupled chitosan grafted on fluorescein isothiocyanate (FITC) by chemical bond was prepared. Then FITC-labelled nanoparticles were prepared by ionically cross-linking method, and reaction with HepG2 and cells in vitro experiments. The results show that the amount of the activated folate ester, the speed of adding agent and the reaction temperature are the main factors affecting the coupling ratio. Folate-coupled chitosan is stably coupled when the ratio of the mass of the active folate ester to chitosan used is 1?1, the speed of adding agent is 2 mL/min, the reaction temperature is 30 �� and the reaction time is 12 h. The average nanoparticles size is 290 nm. The forms of the folate-coupled chitosan nanoparticles are regular, fluorescent cells results are good. Fluorimetric folate-coupled chitosan nano-carrier can be prepared successfully by this method.
Key words: folate; chitosan; nanoparticles; fluorescein isothiocyanate
������Ϊ��в���ཡ�����ش������������ǵĸ߶ȹ�ע�����ֿ�����ҩ����Ʒ���������������ҩ������ѡ���Բ��ߣ���ɱ������ϸ����ͬʱҲ����ɱ����������ϸ�����������ô����ߴ��������ʹ�ࡣ���ԣ������߿�����ҩ��İ����ԺͰ�ȫ�Գ�Ϊ�������Ƶ��������⡣Ҷ������[1]�����ǽ�����һ�ֱ��ܹ�ע�����Ϳ��������ƣ���Ҷ���Ҷ��������и߶ȵ����ԣ����ԣ���������һ���Խ�Ҷ����Ϊ������ҩ��İ������壬����Ҷ��������ijЩ������λ�Ĺ��ȱ������������֯��ˮƽ���������ʵ��Ҷ��ż��ҩ��İ�������[2-3]����ż�������Դ��������Ϊ�����������ӳ����ڱ���ʱ�䣬�����Ч���Ǿ���[4]��һ�ּ����á��������Ρ��������������Ժò�����һ�����������Ե��������ӣ��㷺����ҩ���������塣���⣬�Ǿ��ǽ������㷺Ӧ�õ���ҩ�����е��������ɽ�һ�����ҩ����ȶ��ԣ���ʵ�ֻ��ͺͿ���ҩ�����ԣ�������Ҷ������ԺͿǾ��ǻ��ͺͿ���ҩ���ص㣬ѡ��Ǿ���Ϊ�������Ʊ�Ҷ������������壬�����������ӫ����[5]��ӫ���ǣ�Ϊ��һ������ʵ������[6-7]��
1 �������Լ�
����Ϊ��AUW120D������ƽ(�����ձ�)��79-1�������Ƚ�����(����ʡ��̳��������������˾)������䶳�����(LABCONCO������)��TGL16M�����䶳���Ļ�(Ӣ̩����˾����ɳ)��TENSOR27����Ҷ���������(BRUKER���¹�)��1000HSA�������ȷ�����(�����ģ�Ӣ��)��MFP-3Dԭ��������(ASYLUM RESEARCH������)��LB2ӫ�������(LEICA���¹�)��
�Լ�Ϊ���Ǿ���(�Ϻ���������Ƽ�����˾���������ȣ�90%)�����������(TPP����ҩ���Ż�ѧ�Լ�����˾)��SePHadexG-50�Ͼ�������(��ҩ�����Ϻ���ѧ�Լ���˾)����������(DMSO����ҩ���Ż�ѧ�Լ�����˾)��N-�ǻ��������ǰ�(NHS����ҩ���Ż�ѧ�Լ�����˾)����������̼���ǰ�(DCC��J&K Chemical Ltd)��Ҷ��(FA����ҩ���Ż�ѧ�Լ�����˾)�������Լ�����Ϊ������������
2 ʵ�鷽��
2.1 Ҷ����������Ʊ�
��ȡ2.6 gҶ�ᣬ����50 mL��ˮ��������(DMSO)�У��ټ���2.38 g��������̼���ǰ�(DCC)��1.35 g N-�ǻ��������ǰ�(NHS)��1.25 mL���Ұ�����30 �淴Ӧ����ҹ�����˳�ȥ��Ӧ��������������壬��ѹ�����ȥ�����ܼ����ڽ�������ε��뺬30%��ͪ����ˮ������Һ�У��õ���ɫ�����Ȼ������ˮ����ϴ�����������ո���õ�Ҷ�������[8]�������±��汸�á�
2.2 Ҷ��ż���Ǿ��ǵ��Ʊ������������
��ȡ�Ǿ���160 mg������40 mL����-�����ƻ���Һ(pH 4.6)�У��ڴ���������������2 mL/min���ٶȻ�������8 mLҶ���������DMSO��Һ(20 mg/mL)����30 �淴Ӧ12 h��Ȼ����10 moL/L NaOH��pHֵ��9�����ģ�������ˮϴ���������������2%����ˮ��Һ���õ�Ҷ��ż���Ǿ�����Һ[9]��
ȡҶ����������Ǿ��Ǻ�Ҷ��ż���Ǿ������������ú�������Ǽ��ż�������
2.3 ӫ���ǵ�Ҷ��-�Ǿ������������Ʊ�
��ȡ10 mg��������ӫ����(FITC)������10 mL��ˮ�Ҵ��У��ڴ���������������μ��뵽20 mLҶ��-�Ǿ��ǵĴ�����Һ�У��ܹⷴӦ4 h��ʹFITC�ϵ�̼ԭ����Ǿ����ϵİ�����Ӧ�Ա���б��[10]����10 mol/L NaOH ����pHֵ��9�����ģ�������ˮϴ�ӣ�ֱ����Һ�������ɫΪֹ��������������2%������Һ�ܽ⣬��10 mol/L NaOH ����pHֵ��5���ڴ���������������μ���10 mL TPP��Һ(2 g/L)����Ӧ20 min��õ�ӫ���ǵ�Ҷ��-�Ǿ���������[11]��
2.4 Ҷ��ż���Ǿ�������������̬�۲�
ȡ����Ҷ��ż���Ǿ�������������Һ�μ�����ĸƬ�ϣ���ԭ���������۲�����̬���ü������ȷ����Dzⶨ��������������
2.5 ����ϸ��ʵ��
ȡ�ΰ�HepG2ϸ�����ں���10%��СţѪ���1640��������������������������Ϊ��5%(�������)CO2��37 �档ȡ����������ϸ������ø���������������еĸDz�Ƭ�Ͻ��֣�����������������24 h��
���������е�ϸ��������������ȥ����������PBS��ϴ3�Ρ�����ӫ���ǵ�Ҷ��ż���Ǿ�������������Һ�ͿǾ�������������Һ����37 ������24 h����PBS��ϴϸ��3�Σ���С����ȡ���Dz�Ƭ������Ԥ��ϴ�����ز�Ƭ�ϣ��ÿ��������Ƭ����ӫ���������й۲졣
3 ���������
3.1 Ҷ��-�Ǿ������������Ʊ�
���������ӵ���ҩ�������ϵķ�����ԭ����ȡ����ż������������װǰ��������װ����С���������װ��ɺ��������壬�����ʵĻ��Թ��ܻ�������������ijһ�ɷֵ�ĩ�ˡ����Թ��ܻ��ű������������װ����Ӧ�����ҿ�����Ч�غ��������ӡ���һ���������ڴ������絥��¡��������ӡ�����������װǰ���������ӵ�������������ף������ַ�����ȱ�����������������װ��ɺ�һ���ֽ�ϵ�����ᱻ���������ڲ����Ӷ������������ϡ��������ӽ�����Ӧ�����Ʊ�Ҷ��-�Ǿ����������������ö��������(TPP)��Ҷ��-�Ǿ��ǽ��������յ�������������һ���������Ʊ���Ҷ��-�Ǿ�������ҩ�����塣�����£��ڽ�������У���pHֵΪ7~9��TPP��Һ���뵽pHֵΪ4~6��Ҷ��-�Ǿ��Ǵ�����Һ�У�ͨ��������������������Ǿ��Ƿ������ϴ���������ӻ��������������ںͷ��Ӽ�Ľ�������������Ѹ���γ���������[12]��
3.2 ���������
���ú�������Ƿ���Ҷ����Ǿ��ǵ�ż�������ͼ1~3��ʾ�ֱ�Ϊ�Ǿ��ǡ�Ҷ�����֬��Ҷ��ż���Ǿ��ǵĺ�����ס���Ҷ��ż���Ǿ��ǵĺ�������Կ���(ͼ3)����NH2��1 640 cm-1�������շ�(��ͼ1)�͡�COOH��1 692 cm-1�������շ�(��ͼ2)��ʧ����1 562 cm-1���������µ�ǿ���շ壬˵���Ǿ����ϵİ�����Ҷ���ϵ��Ȼ��γ���������[13]�����߳ɹ�ż����
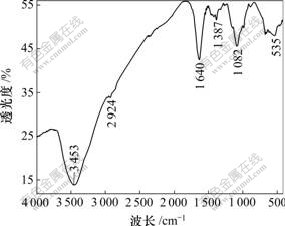
ͼ1 �Ǿ��ǵĺ������
Fig.1 Infrared spectra of chitosan

ͼ2 Ҷ��������ĺ������
Fig.2 Infrared spectra of folic acid
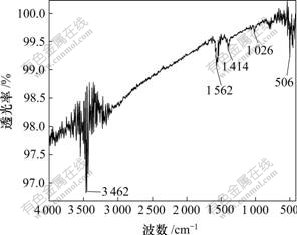
ͼ3 Ҷ��ż���Ǿ��ǵĺ������
Fig.3 Infrared spectra of Folate-conjugated chitosan
3.3 �������������ͱ�����̬
ͼ4��ʾΪӫ���ǵ�Ҷ��-�Ǿ������������������ߡ��ɼ���ӫ���ǵ�Ҷ��-�Ǿ����������Ŀ��������Ƚϼ��У������ž�����ƽ������ԼΪ290 nm��ӫ���ǵ�Ҷ��-�Ǿ�����������ԭ��������ɨ�����ͼ5���ɼ����������̬��������С�ȽϾ��ȣ������ž�����[14]��
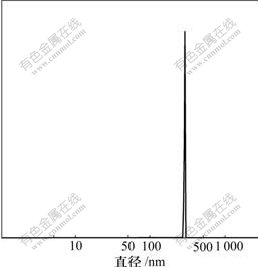
ͼ4 ӫ���ǵ�Ҷ��-�Ǿ�������������������
Fig.4 Measurement of particle size map of Fluorimetrc Folate-coupled Chitosan nanoparticles
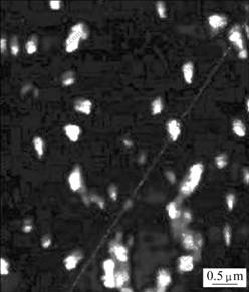
ͼ5 ӫ���ǵ�Ҷ��-�Ǿ�����������ԭ��������ɨ����
Fig.5 Atomic force microscope scanning image of fluorimetrc folate-coupled chitosan nanoparticles
3.4 ����ϸ��ʵ����
ʹ�õ���ӫ�������۲�Ҷ��-�Ǿ����������塢�Ǿ����������������Ҷ�������ϸ��֮�������ã������ͼ6��ͼ7�����Է��֣�ϸ��ӫ��Ч�����ԣ���ӫ��ǿ����������ͬϸ�������ʱ������ȡ�
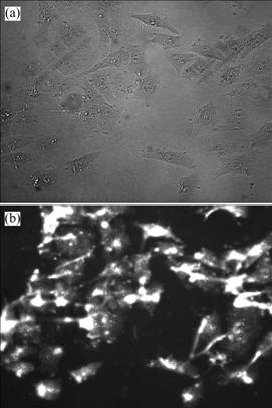
(a) ��Ȼ�⣻(b) ��Ȼ��+ӫ��
ͼ6 ӫ���ǵ�Ҷ��-�Ǿ�����������HepG2ϸ������õĵ���ӫ��������
Fig.6 Inverted fluorescence microscope images of fluorimetrc folate-coupled chitosan nanoparticles interaction with HepG2 cells

ͼ 7 ӫ���ǵĿǾ�����������HepG2ϸ������õĵ���ӫ��������
Fig.7 Inverted fluorescence microscope image of fluorimetrc chitosan nanoparticles interaction with HepG2 cells
4 ����
(1) �Ǿ����ϵ�2�����Ի��ſ����ڻ�ѧ���Σ�һ������ȥ��̪����λ���ϵ����백������һ������ȥ��̪����λ���ϵ��ǻ���
(2) ͨ���Ǿ��������ϵ����백����Ҷ���ϵ��Ȼ��γ�̪�������ﵽ�Ǿ��ǻ�ѧ���ε�Ŀ�ġ�
(3) ���ڿǾ��ǵĸ߷������ԣ���ˮ���Բֻ��������ˮ��Һ���ܽ⣬Ҷ��������������ˮ��Һ�����ԣ������Ƚ��Ǿ�����DMSO�е�Ҷ��ż���������ӫ���Ǽ��������ӽ�����Ӧ���Ʊ��������ķ������Ʊ��˾���ӫ���ǵ�Ҷ��Ǿ���������������������ӫ���ر�ǿǾ��Ǻ�Ҷ��ż���Ǿ��ǣ��Ա��������Ҷ�������HepG2ϸ��Ϊģ��ϸ��������ϸ����ȡ�����о���
(4) ��HeLaϸ��������ʱϸ��ӫ��Ч�����ԣ���ӫ��ǿ��ͬ��������ϸ�������ʱ������ȡ�
(5) ������������Ҷ�����οǾ�������������Ʊ����գ�Ϊ���������������Ƽ��������ṩ�˼��� �ֶΡ�
�ο����ף�
[1] Shia J, Klimstra D S, Nitzkorski J R, et al. Immunohistochemical expression of folate receptor a in colorectal carcinoma[J]. Patterns and Biological Significance Human Pathology, 2008, 39(4): 498-505.
[2] ������, ������, ë����. Ҷ��ż�������������Ʊ������о�[J]. ����ҽѧ����ѧ��־, 2004, 21(2): 255-258.
ZHANG Liang-ke, HOU Shi-xiang, MAO Sheng-jun. Study on the preparation of folate-conjugated albumin nanoparticles[J]. Journal of Biomedical Engineering, 2004, 21(2): 255-258.
[3] Lee R J, Low P S. Delvery of liposomes into cultured KB cells via folate receptor-mediated endocytosis[J]. Biol Chem, 1994, 269(5): 3198-3199.
[4] WANG San-lang, LIN Hue-tin, LIANG Tzu-wen, et al. Reclamation of chitinous materials by bromelain for the preparation of antitumor and antifungal materials[J]. Bioresour Technol, 2008, 99(10): 4386-4393.
[5] ̷���, �Ʒ�ӭ. FITC����Ͼ���ճ�������ⶨ������֯Ѫ���ܶ�[J]. ����ҽѧԺѧ��, 2007, 13(5): 409-413.
TANG Guang-hong, HUANG Feng-ying. Quantitative determination of relative tumor vascularity by FITC-dextran adsorption[J]. Journal of Hainan Medical College, 2007, 13(5): 409-413.
[6] ������, ������. Ҷ�����弰���ڽ鵼ҩ���������ϸ�������е�Ӧ��[J]. �й�ʵ��ѪҺѧ��־, 2005, 13(5): 911-914.
GAO Xiao-ning, TAN Suo-qing. Folate receptor and its application in the selective receptor-mediated targeting therapy of tumor cells��Review[J]. Journal of Experimental Hematology, 2005, 13(5): 911-914.
[7] �ַ���, ���վ�. Ҷ������鵼�İ����ҩ�о���չ[J]. �й�ҽԺҩѧ��־, 2006, 26(10): 1281-1284.
LIN Feng-yun, ZHU Zhao-jin. The progress of folate receptor in the selective receptor-mediated targeting therapy[J]. Chinese Journal of Hospital Pharmacy, 2006, 26(10): 1281-1284.
[8] Guo W J, George H, Hinkle, et al. 99mTc-HYNIC-Folate: a novel receptor-based targeted radiopharmaceutical for tumor imaging[J]. Nucl Med, 1999, 40(9): 1563-1569.
[9] Ѧ����, ͯ����, Ф��Ң. ŵ��ɳ��-�Ǿ�������Ʊ�����ҩ����[J]. ���ϴ�ѧѧ��: ��Ȼ��ѧ��, 2008, 39(3): 480-485.
XUE Chang-gang, TONG Chun-yi, XIAO Su-yao. Preparation of norfloxacin-chitosan microsphere and its drug release property[J]. Journal of Central South University: Science and Technology, 2008, 39(3): 480-485.
[10] �ζ���, ���䶴, ��С��. ӫ���ǿǾ��ǵķ�Ӧ����ѧ�о�[J]. ���ܲ���, 2004, 35: 2463-2465.
REN Dong-wen, LIU You-dong, MA Xiao-jun. A kinetics study of labeling reaction of chitosan with a fluorescent dye[J]. Journal of Funcyional of Materials Contents, 2004, 35: 2463-2465.
[11] ������, �ܴ�ɽ, �ſ�ɽ. Ӧ������������Ϊ�������Ʊ���ҩ�����������о�[J]. �й��ִ�ҽѧ��־, 2003, 13(22): 69-71.
JIANG Xin-yu, ZHOU Chun-shan, ZHANG Jun-shan. Study on the preparation of nanoparticles using sodium tripolyphosphate as cross-linking agent[J]. China Journal of Modern Medicine, 2003, 13(22): 69-71.
[12] Aronov O. Folate-targeted PEG as a potential carrier for Carboplatin analogs: Synthesis and in vitro studies[J]. Bioconjugate Chemistry, 2003, 14(3): 563-574.
[13] ��ͦ��. ����[M]. ����: ��ѧ��ҵ������, 2004: 1-649.
JIANG Ting-da. Chintin[M]. Beijing: Chemical Industry Press, 2004: 1-649.
[14] �ű�, ����. ż����������HAP/HDPE��������������ϵ���ѧ���ܺ��۽ṹ[J]. ���ܲ���, 2007, 38(11): 1912-1915.
ZHANG Bin, ZHU Wu. Mechanical properties and microstructure of nano HAP/HDPE extrusion bio-composite modified by silane-coupling agents[J]. Journal of Functional Materials, 2007, 38(11): 1912-1915.
�ո����ڣ�2008-10-16�������ڣ�2008-12-06
������Ŀ�����ҡ�ʮ�塱�Ƽ����ؼƻ���Ŀ(2004BA310A54)
ͨ�����ߣ�������(1955-)���У����ϳ�ɳ�ˣ����ڣ���ʿ����ʦ�����°��������������Ƽ����о����绰��0731-84327931��E-mail: zyd@2118.cn
(�༭ �°���)