文章编号:1004-0609(2010)04-0756-09
新型外科植入用钛合金TZNT的生物相容性
李 军1,李佐臣2,陈杜娟2
(1. 上海工程技术大学 材料工程学院,上海 201620;
2. 西北有色金属研究院,西安 710016)
摘 要:制备一种新型外科植入用钛合金Ti12.5Zr2.5Nb2.5Ta(TZNT),通过溶血试验、细胞毒性试验和皮下埋植试验系统评价该合金的生物相容性,并与3种标准外科植入用钛合金Ti6Al4V、Ti6Al7Nb以及TA2进行对比。该合金经完全退火工艺处理后(700 ℃,45 min,AC),主要由大量位向不同的片层状α相簇和少量位于α片间的β相组成。溶血试验结果表明:TZNT的溶血率为0.683%(远低于5%),因此不会引起急性溶血。细胞毒性试验结果表明:TZNT、Ti6Al4V和Ti6Al7Nb在3个时间组(2、4和6 d)的相对细胞增殖率均不低于100%,细胞毒性等级评定为0级,即对细胞不产生毒性。皮下埋植试验结果表明:与Ti6Al4V和Ti6Al7Nb相比,TZNT和TA2植入白鼠体内4周和8周后,无论是炎细胞密度还是植入物周围的纤维膜厚度均有所降低,TZNT合金植入4周后,组织良好,包绕材料的纤维膜较疏松且与组织间的界限不清;随着植入时间延长至8周,炎细胞密度进一步减少,纤维膜也变得更薄,更致密。综合评价结果表明该新型合金具有良好的生物相容性。
关键词:生物材料;钛合金;医用钛合金;生物相容性;溶血;细胞毒性;皮下埋植
中图分类号:R318.08 文献标志码:A
Biocompatibility of new titanium alloy TZNT for
surgical implant application
LI Jun1, LI Zuo-chen2, CHEN Du-juan2
(1. School of Materials Engineering, Shanghai University of Engineering Science, Shanghai 201620, China;
2. Northwest Institute for Nonferrous Metal Research, Xi’an 710016, China)
Abstract: The biocompatibility of a new titanium alloy Ti12.5Zr2.5Nb2.5Ta (TZNT) for surgical implant application was investigated by hematolysis test, cytotoxic test and subcutaneous implantation test. The three standard titanium alloys Ti6Al4V, Ti6Al7Nb and TA2 for surgical implant application were taken as contrast materials. TZNT subjected to the full annealing treatment (700 ℃, 45 min, AC) is composed of a large number of lamellar α-phase clusters with different orientations and a small amount of β-phase between lamellar α-phase. The hematolysis test result shows that the hematolysis rate of TZNT is 0.683% (less than 5%), which indicates that the acute hematolysis cannot be induced by TZNT. The cytotoxic test result shows that the relative cell proliferation rates of TZNT, Ti6Al4V and Ti6Al7Nb are more than or equal to 100% at different cultivation periods (2, 4 and 6 d), the cytotoxicity is ranked as 0 grade, which indicates that three titanium alloys cannot induce the cytotoxic effect. The subcutaneous implantation test result shows that the density of inflammation cells and the thickness of fibrous membrane decrease in the TZNT and TA2 groups at different implantation periods (4 weeks and 8 weeks) to white mice when compared with those in the Ti6Al4V and Ti6Al7Nb groups. For TZNT implanted for 4 weeks, the tissues surrounding TZNT are good, the fibrous membrane is very loose and the interface between the fibrous membrane and the tissues is very obscure. When the implantation period increases to 8 weeks, the density of inflammation cells further decreases. Other than that, the fibrous membrane also gets compacter and thinner. The comprehensive evaluation results show that the new titanium alloy TZNT possesses good biocompatibility and is an ideal biomedical material.
Key words: biomaterial; titanium alloy; medical titanium alloy; biocompatibility; hematolysis test; cytotoxic test; subcutaneous implantation
当前在医学界广泛使用生物相容性良好和耐蚀性能优良的钛合金作为硬组织修复替代材料[1]。Ti6Al4V是第一代用作生物材料的钛合金[2],然而,研究发现该合金中的元素V在人体使用过程中会少量释放,从而引起细胞毒性反应和生理紊乱[3-4]。随后Ti6Al7Nb作为第二代医用钛合金在瑞士被开发,该合金用无毒元素Nb取代V,因而具有更好的生物相容性。但这两种α+β型合金具有较高的弹性模量(大约120 GPa)[5],以及人体骨骼的弹性模量严重不匹配(大约28 GPa)。研究表明:如果合金的弹性模量比骨骼的高,承受应力的金属和骨骼将产生不同的应变,在金属与骨的接触界面处会出现相对位移,从而造成界面处松动。另外,由于应力不能完全从人体关节传递到其临近的自然骨组织,可能导致骨的吸收和功能的退化,产生应力-屏蔽现象[6]。β型合金由于具有低弹性模量的特点而成 为人们开发的第三代医用钛合金,其弹性模量比α+β型钛合金的降低30%~50%,然而其容许应变(屈服强度和弹性模量的比值)达到1.337%,远高于皮质骨的0.67%[7]。STEINEMANN等[8]指出,仅仅考虑骨骼和植入物弹性模量的差异是片面的,自然骨和人工植入物之间另一个很重要的差异是容许应变,该指标可以用来衡量植入物的生物力学相容性。由此可知,开发一种新的医用材料,不仅要考虑骨和植入物弹性模量的匹配,还要考虑容许应变的匹配问题。
针对以上三代钛合金存在的问题,本文作者采用d-电子合金设计理论设计并制备一种近α型新型医用钛合金Ti12.5Zr2.5Nb2.5Ta(TZNT)。研究表明:该合金具有比Ti6Al4V和Ti6Al7Nb更低的弹性模量以及与骨骼更匹配的容许应变[9],因而具有更优异的生物力学相容性。作为一种新型医用钛合金,评价其生物相容性是非常必要的。生物相容性是生物医学材料区别于其它功能材料所必须具备的特性。本研究根据国际标准化组织7406技术报告(ISO/TR7406)推荐的试验项目,采用溶血试验、细胞毒性试验和皮下埋植试验,对该合金生物安全性进行初步评价。
1 实验
1.1 材料制备
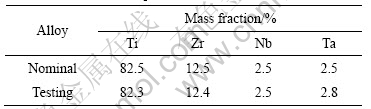
试验合金的名义化学成分为Ti-12.5Zr-2.5Nb- 2.5Ta (简称TZNT,质量分数,%),采用真空自耗电弧炉熔炼,二次重熔而成。原材料选用1级海绵钛、海绵锆、高纯钽以及Ti53.5Nb中间合金。按名义成分投料5 kg,在300 t油压机上制备出6根d 30 mm×270 mm电极,3根电极头尾相接焊成d 30 mm×900 mm的电极棒,作为熔炼一次锭的原材料。熔炼成2根d 60 mm的一次锭再焊接成电极棒,然后熔炼出d 90 mm的二次锭。二次锭经过削去冒口、扒皮再取样分析,其成分如表1所列。由表1可以看出,合金的名义化学成分和实际检测结果非常接近。将该合金锭高温锻造成d 18 mm的棒,并采用完全退火工艺进行热处理,具体工艺通过α+β/β相变点的测定来确定。对比材料Ti6Al4V、Ti6Al7Nb和TA2均为退火态,由西北有色金属研究院提供。
表1 TZNT合金的化学成分
Table 1 Chemical composition of TZNT
1.2 α+β/β相变点的测定
钛合金的α+β/β相变点是确定热处理工艺的重要基本参数。本试验采用热膨胀法在NETZSCH型热膨胀仪上进行测试,试样尺寸为5 cm×5 cm×40 cm。
1.3 组织表征
采用Rigaku D/mas 2550V 型X射线衍射仪(XRD)对合金TZNT物相组成进行分析。采用Cu靶(波长 λ=0.154 06 nm),管电压40 kV,管电流100 mA,扫描速度2.5 (?)/min。金相试样在Buehler Phoenix 4000型金相试样制备仪上制备,然后将试样用酒精和丙酮浸洗,经冷风吹干后用10%HF+60%HNO3+30%H2O (体积分数)进行侵蚀,最后采用PMG3型光学显微镜(OM)对合金组织进行观察。
1.4 溶血试验
取1 mm厚的TZNT棒材,表面磨光后将其切割成5 mm×3 mm的方片状,共计15 g。用丙酮洗净材料表面油污后,以酒精超声洗涤20 min,用蒸馏水冲洗3遍,于70 ℃烘干备用。抗凝剂采用质量分数为2%的草酸钾溶液。试验步骤如下。
1) 采用心脏穿刺法抽取兔血10 mL,立即注入有0.5 mL草酸钾抗凝试的试管中,从中取4 mL加入含5 mL生理盐水的试管,制成新鲜抗凝稀释兔血。
2) 取已准备好的试验材料5 g,浸泡在10 mL生理盐水的试管中。阳性对照组:在每个试管中加10 mL蒸馏水;阴性对照组:在每个试管中加10 mL生理盐水。试验组以及阳性、阴性对照组均需3支试管。将此9支试管放在37 ℃恒温水浴箱30 min后取出,每个试管加0.2 mL稀释兔血,缓慢混合,再放入37 ℃恒温水浴箱中维持60 min。
3)、将所有试管置入离心机中离心5 min (2 500 r/min),分别吸取各试管上清液,用分光光度计测定光密度(OD)值,所选波长为545 nm,每组3支试管的均值为该组的吸光度。
4) 根据下式计算溶血率η:

式中:Dt为试验样品的吸光度;Dnc为阴性对照的吸光度;Dpc为阳性对照的吸光度。
若材料的溶血率小于5%,说明材料符合医用材料的溶血要求;若溶血率大于5%,则预示材料有溶血作用。
1.5 细胞毒性试验
将试验材料TZNT、Ti6Al4V和Ti6Al7Nb制备成9 mm×9 mm×1 mm的薄片,并抛光成镜面,用丙酮洗净材料表面油污后,用蒸馏水冲洗3遍。以三氯乙烯超声洗涤10 min,然后用酒精超声洗涤10 min,再用蒸馏水冲洗3次,于60 ℃烘干备用。试验前经 121 ℃高压灭菌20 min。试验步骤如下。
1) 浸提液的制备。浸提液采用含体积分数为10%的小牛血清的DMEM培养液,浸提时试件表面积(cm2)与浸提介质体积(mL)之比为R1=1.5,R2=3,R3=6。浸提时使用无菌操作技术,浸提后将浸提液置于37 ℃培养箱内24 h,使金属离子尽可能多地析出,然后采用0.22 μm微孔滤膜过滤除菌,制备出材料浸提液。阳性对照组浸提液是铝浓度为300 mg/mL的培养液;阴性对照组浸提液是未放试样的空白培养液。
2) 细胞接种和培养。将传代一次的原代培养家兔的成骨细胞用细胞培养液配制1×105/mL的细胞悬液,分注于96孔塑料培养皿内,每孔300 μL,共种3板,每观察期每种材料接种8孔。然后置于细胞培养箱中((37±2) ℃、CO2的体积分数为5%)培养24 h后,弃去原培养液,用磷酸盐缓冲液洗涤两次,试验组分别加入100 μL的浸提液,对照组分别加入100 μL相应的对照液,放入上述培养环境中继续培养2、4和6 d。
3) 活细胞观察和吸光度值测定。取一块R1=1.5且培养4 d的培养板,在倒置相差显微镜下观察活细胞形态并摄影。在2、4和6 d各取一块培养板,每孔加入20 μL MTT液(Sigma, USA,使用浓度为5 mg/mL,溶解于磷酸盐缓冲液),继续培养6 h。然后吸取原液,每孔加150 μL二甲基亚砜(Amresco, USA),置震荡器上震荡10 min,使结晶物充分溶解,用酶联免疫检测仪测定各孔吸收值,所选波长为500 nm。
4) 用下式计算细胞的相对增殖率(R):
R=Ds/Dnc×100% (2)
式中:R为相对增殖率;Ds为试验组(包括试验样品、阳性对照组及阴性对照组)平均吸光度;Dnc为阴性对照组吸光度。
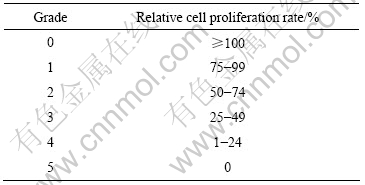
5) 根据表2所示,将相对增殖率转换成6级材料毒性评级。试验结果为0级或1级,反应为合格;试验结果为2级,应结合细胞形态来综合评价;试验结果为3~5级,反应为不合格。
表2 细胞毒性等级的评级标准
Table 2 Grade evaluation of standard cell cytotoxic
1.6 皮下埋植试验
选用健康、卫生情况良好的雄性SD大白鼠,共20只,按4周和8周两个时间组,每组10只。试验用材料为TZNT、Ti6Al4V、Ti6Al7Nb和TA2,将材料加工成长2 mm,直径为1 mm的圆柱体,圆柱两端用400#金相砂纸磨光,手术前对试验材料进行严格消毒处理。用丙酮洗净材料表面油污后,用蒸馏水冲洗3遍,用酒精超声洗涤20 min,再用蒸馏水冲洗3次,于37 ℃烘干备用。试验前于121 ℃高压灭菌20 min。按试验步骤如下。
1) 固定动物,暴露背部,手术区用脱毛剂脱鼠毛,常规消毒皮肤,铺无菌小洞巾。然后按每千克大白鼠40~50 mg的剂量,将质量分数为1%的戊巴比妥钠采用腹腔注射麻醉大白鼠。
2) 皮下埋植在无菌条件下沿脊柱长轴作左右各2点的长切口,深至皮下,钝性分离皮下组织,按A(TZNT)、B(Ti6Al4V)、C(Ti6Al7Nb)和D(TA2)顺序(见图1)分别将试样平行于脊柱植入,缝合皮肤。
3) 手术24和48 h后,观察动物活动状况,创口有无渗血、红肿、化脓和材料有无排出等迹象。
4) 术后4周和8周分别麻醉动物,首先观察种植体有无移位,然后切开皮肤,肉眼观察种植体周围组织情况。
5) 切取种植材料及周围组织,用中性福尔马林液固定,从试样中心垂直试样将组织切成二等份,去除试样,常规石蜡包埋,沿试样长轴进行切片,伊红-苏木精染色。光学显微镜下检查试样与结缔组织界面区域,观察是否存在炎症、炎症的密度和范围、组织坏死形成与否等。
6) 用显微镜的C5型0.5网形目镜尺和C7型0.1坐标目镜尺,在放大倍数为400倍条件下,分别对4周和8周组进行炎细胞记数和膜厚度测量。在材料两端区域内,任意记3次整个网尺的炎细胞数,取每个试样2端共6次记数的均值为该试样的炎细胞密度,测每个试样的两端中心点及附近2点的膜厚,取6次测量值的均数作为该试样的膜厚度。

图1 皮下埋植试验示意图
Fig.1 Schematic diagram of subcutaneous implanting test: (a) Shape of sample; (b) Implanting position
2 结果与讨论
2.1 α+β/β相变点的测定
图2所示为合金TZNT的线膨胀率和热膨胀系数随温度的变化。由图2可见,在室温到753 ℃的温度范围内,该合金基本呈线形膨胀,热膨胀系数随温度变化维持在一个相对稳定的数值,大约为1.1×10-5 ℃-1。这说明合金的热膨胀特性在这个温度区间保持不变,即物相组成没有发生改变。当温度大于753 ℃时,热膨胀系数随着温度的升高急剧增加,这是开始发生相变α→β的缘故,晶体结构的变化,导致热膨胀特性的改变。由图2可看出,在整个温度区间热膨胀系数会出现一个峰值,对应的温度816 ℃就是α+β/β的相变点,该温度低于纯钛的同素异晶转变温度882.5 ℃,这是因为所添加的元素中Nb和Ta为β相稳定化元素,降低Ti的同素异晶转变温度所致。Zr为中性元素,对纯Ti的同素异晶转变温度影响较小。根据相变发生的温度范围,采用完全退火工艺进行处理,以获得稳定的、塑性好的或对应一定综合性能的显微组织。近α型钛合金在退火中除发生再结晶外,还有α相和β相在组成、数量及形态上的变化,确定退火工艺比较复杂,一般选择在α+β/β相变点以下120~200 ℃进行,冷却方式也采用空冷。该合金的α+β/β相变点为816 ℃,故采用的完全退火工艺为(700 ℃,45 min,AC)。
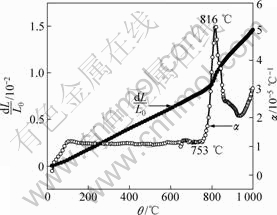
图2 钛合金TZNT线膨胀率和热膨胀系数随温度的变化
Fig.2 Change of linear expansion rate and thermal expansion coefficient of alloy TZNT with temperature
2.2 组织观察
图3所示为经完全退火处理后合金TZNT的XRD谱。根据所有衍射峰的标定结果,可知合金主要由大量密排六方结构的α相和少量体心立方结构的β相组成。物相组成和各相含量的差异主要与合金的化学成分有关。Nb和Ta是两种β相稳定化元素,可以使β相区向较低温度移动,有利于β相的稳定存在,但这两种元素含量较低,因此合金中β相的含量也较低。根据式(3)和(4)可以计算该合金的β稳定化元素质量分数weq(Mo)和α稳定化元素质量分数weq(Al)[10],计算结果表明weq(Mo)和weq(Al)分别为1.25%和2.08%。根据文献[11]对钛合金的分类标准,可知TZNT为低铝含量近α型合金。

完全退火处理后的合金组织如图4所示。由图4可看出,组织呈片层状,主要由大量不同位向的片层状α相簇和分布于片层状α相间的少量β相组成。原始的β相晶界已经被破坏,且被多个α相簇分割,在每一簇中,各α相片是平行的,有相同的结晶学取向。各α片由β相中间层分开。α相和β相点阵有以下取向关系:{110}β-Ti∥{011}α-Ti、á111?β-Ti∥á100?α-Ti,这个关系决定在同一β晶粒中,α相可能存在12个独立取向。
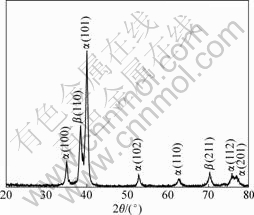
图3 完全退火(700 ℃,45 min,AC)后TZNT合金的XRD谱
Fig.3 XRD pattern of TZNT alloy after full annealing (700 ℃, 45 min, AC)

图4 完全退火(700 ℃,45 min,AC)后TZNT合金的OM像
Fig.4 OM image of TZNT alloy after full annealing (700 ℃, 45 min, AC)
2.3 溶血试验
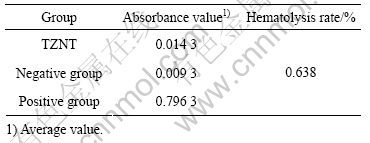
溶血是红细胞溶解导致血红蛋白释放入血浆的现象。造成溶血的因素除红细胞本身疾病如红细胞膜异常,血红蛋白异常以及机体存在异常抗体,单核吞噬细胞系统破坏红细胞过多等外,还一些外源性因素,如进入生物体内的某些药物,与生物组织接触的材料以及一些物理因素等。它们可引起红细胞的细胞毒性或对红细胞的机械损伤以及使血浆渗透压改变等。FDI和ISO文件指出,种植体、修复用合金和义齿基托材料等应用于机体与生物组织接触的生物医用材料需要进行此项测试。表3所列为各组吸光度值和TZNT合金的溶血率。FDI标准要求试验中阳性对照组吸光度值应在0.8±0.05范围内,阴性对照组吸光度值应小于0.03,否则试验不可进行。本试验阳性和阴性对照组的测试值均符合要求,因此试验结果有效。表3所列为TZNT的溶血率为0.683%,一般认为超过5%才会发生溶血,所以该合金不会引起急性溶血。
表3 各组别材料吸光度和TZNT合金溶血率
Table 3 Absorbance values of different groups and hematolysis rate of TZNT group
2.4 细胞毒性试验
细胞毒性是生物医用材料对特定细胞造成毒性作用的能力或趋势,可对细胞造成损伤或使细胞死亡。通过体外细胞毒性试验可检测材料的细胞毒性作用。
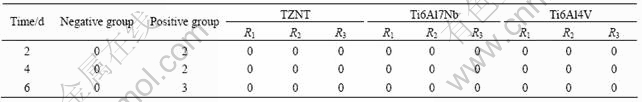
细胞毒性试验结果如表4、5和6所列。由表4可见,阳性对照组(纯铅组)的吸光度值明显低于其他组别的。培养2 d时,吸光度值为0.187 75;随着时间延长到4 d,该值增加到0.285 75;但当时间进一步延长至6 d时,该值减少至0.235 13,表明随时间的进一步延长,细胞生长受到抑制。由表5和6可见,该组在不同培养时间的相对增殖率明显低于100%,培养2和4 d的毒性等级为2级,培养6 d后毒性等级进一步增加到3级,毒性等级较高,表明阳性对照组具有潜在的毒性,在人体中的长期毒性作用较大。相对而言,阴性对照组和TZNT、Ti6Al4V和Ti6Al7Nb组在相同培养时间的吸光度值相差不大,并且随时间延长呈增加趋势,提示细胞在这4个组别生长良好(见表5和6),以上3个钛合金组的细胞相对增殖率均大于或等于100%,毒性等为0级,表明这3种合金不具有细胞毒性,符合国家标准中的要求。
图5所示为阴性对照组、阳性对照组和TZNT合金组3个组别细胞培养4 d的OM像。由图5可见,阳性对照组中细胞的数量比TZNT合金组、阴性对照组的细胞数量明显减少,大量细胞变圆缩小、核固缩并聚集成团,在胞浆内可见大量中毒颗粒,处于中毒状态,少量细胞已死亡,其余细胞形态正常。另外两组的细胞形态正常,呈密集规则排列,细胞多为长梭形,可见少量的分裂状态细胞,未见含有中毒颗粒的细胞浆。相比而言,合金TZNT组的细胞数量要多于阴性对照组。细胞形态的分析结果和毒性等级测量结果相吻合。
表4 各组材料的吸光度值
Table 4 Absorbance values of different groups
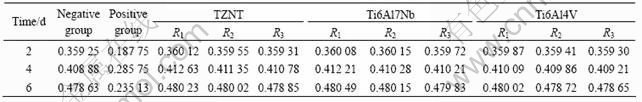
表5 各组别材料的细胞相对增殖率
Table 5 Relative cell proliferation rates of different groups
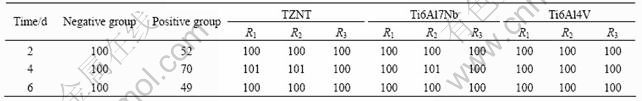
表6 各组别材料的细胞毒性等级
Table 6 Toxicity grades of different groups
2.5 皮下埋植试验
动物体内的植入试验是研究生物材料与机体反应的主要手段,其中最常用的方法是将样品埋植在皮下、肌肉、骨骼系统内一段时间后,取周围组织做成切片进行组织学观察。本试验经24和48 h后,各组动物饮食和活动良好,创口轻度充血、无肿胀、渗血、化脓和无材料被排出现象。试验过程中无动物死亡。取样时肉眼观察发现,各组种植体无移位,周围有纤维包膜包绕,贴近材料的组织未见腐蚀产物沉积和结节等恶变现象。
表7所列为不同材料植入4周和8周后的炎细胞密度和纤维膜厚度。由表7可知,TZNT和TA2组在4周和8周的炎细胞密度和纤维膜厚度相近,8周的炎细胞密度较4周组的炎细胞密度有所减少,纤维膜的厚度也显著减低,且均低于相同时间的Ti6Al4V和Ti6Al7Nb组的炎细胞密度和纤维膜厚度,这表明TZNT和TA2比Ti6Al4V和Ti6Al7Nb引起的组织反应要轻,具有更优异的组织相容性。
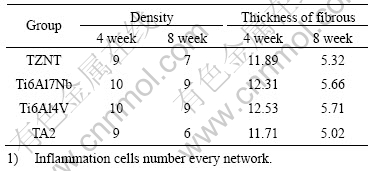
表7 不同材料植入4周和8周后的炎细胞密度和纤维膜厚度
Table 7 Densities of inflammation cells and thickness of fibrous membranes of different groups implanted different materials for 4 and 8 weeks
TZNT合金植入4周和8周后的组织形貌如图6所示。由图6(a)和(b)可看出,组织结构良好,未见坏死区,包绕材料的纤维包膜较疏松且与组织间的界限不清,包膜组织主要由大量的成纤维细胞组成,可见少量炎细胞,主要为中性粒细胞、淋巴细胞、单核细胞和浆细胞,炎症反应轻。由图6(c)和(d)可看出,包膜较8周组变得更薄且更致密,膜内细胞成分进一步单一化,形成以排列有序的成纤维细胞为主体的结缔组织,包膜与构件不易分离,呈现材料与膜组织的粘结现象。炎细胞较4周组更少见,主要为单核细胞和淋巴细胞。综合评价该材料植入4周和8周引起组织反应程度均为轻度。
影响组织与材料反应的因素尚不清楚,但可能包括材料的物理和化学性质、材料的表面结构、手术创伤和材料被污染等。本试验过程中已注意减少组织创伤,也未发现术后伤口感染,所以不同的组织反应主要与材料本身的性质有关。材料性质不同,材料在使用环境中的耐蚀性能就存在差异,进而影响到其生物相容性。因此,材料的生物相容性和其耐蚀性有着密切的关系,这是因为材料的使用环境为人体体液,约含1%氯化钠(质量分数)及少量其他盐类和有机物,温度保持在37 ℃左右。这种环境极易对金属材料产生腐蚀,析出的金属离子和腐蚀产物与临近的组织接触,甚至渗入正常的组织或整个生物系统,对正常组织产生影响和刺激,引起包括组织非正常生长、畸变或炎症、感染等不良生物反应,甚至诱发癌变。STERNEMANN和PERREN[12]提出金属和组织相互反应的判据:对于一种金属,如果生成腐蚀产物的pk(-lgk)(k为腐蚀产物的溶解度)值大于14,那么该产物可以稳定存在,且避免金属络合物的生成,进而阻止金属和组织相互反应;反之,腐蚀产物就发生溶解,以离子形式进入人体,由于植入材料和组织或体液的充分接触,使得离子可以通过体液被传送到不同器官,这些离子在某一器官就有可能发生反应形成毒性的络合物,当离子的积蓄量超过器官的忍受极限时,一些不希望的细胞毒性反应就可能出现。表8所列为钛合金组成元素基本腐蚀产物的化学数据[13-15]。由表8可

图5 培养4 d时不同组别细胞的OM像
Fig.5 OM images of cells in different groups cultivated for 4 d at R1=1.5: (a) Negative group; (b) TZNT alloy group; (c) Positive group
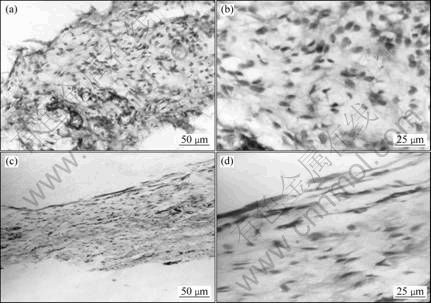
图6 TZNT合金植入4周和8周的组织形貌
Fig.6 Morphologies of tissues of group implanted TZNT for 4 and 8 weeks: (a), (b) 4 weeks; (c), (d) 8 weeks
表8 合金化元素基本腐蚀产物的化学性质[13-15]
Table 8 Chemical properties of some principle corrosion products associated with corresponding alloying elements[13-15]
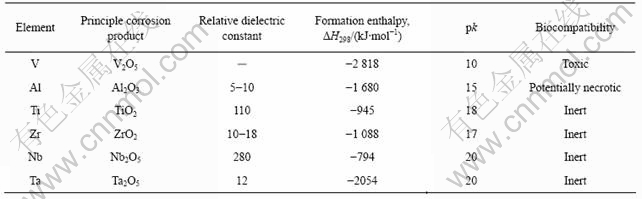
看出,根据金属和组织反应的判据可知,元素V的基本腐蚀产物V2O5的pk值小于14,不稳定。这说明该元素的氧化物较不稳定,易发生水解作用,离子容易进入体液,且该元素本身还具有毒性,那么很容易对组织造成伤害。即使对于本身不具有毒性的元素,如果在人体中的含量超过人体所能承受的极限,也能引起正常生理过程的紊乱。元素Al的基本腐蚀产物Al2O3的pk值大于14,表明该产物可以稳定存在,但该元素的存在引起骨疽的潜在危险。而Ti、Zr、Nb和Ta这4种元素基本腐蚀产物的pk值都大于14,这说明这些腐蚀产物比较稳定,不易发生水解,在人体中具有很好的耐蚀性,且这4种元素本身呈惰性,对组织不产生毒性。基于以上分析,不难得出如下结论,即以Zr、Nb和Ta作为强化元素的新型医用钛合金TZNT应比Ti6Al7Nb和Ti6Al4V具有更好的生物相容性,这和前面的试验结果是相吻合的。
3 结论
1) TZNT的溶血率为0.683%,远小于5%,不会引起急性溶血。
2) TZNT、Ti6Al7Nb和Ti6Al4V 3个时间组(2、4和6 d)的相对增殖率不小于100,毒性等级为0级,对细胞没有毒性;TZNT合金4 d组的细胞多为长梭形,可见少量分裂状态的圆形细胞,未见含有大量中毒颗粒的细胞浆。
3) TZNT植入4周和8周引起的组织反应均为轻度。4周组的中性粒细胞很少,只有少量的淋巴细胞和单核细胞,未见多核巨细胞和异物巨细胞,包饶植入体的纤维膜厚度为11.89 μm,纤维膜较疏松与组织间的界限不清楚;植入体内8周组的炎细胞密度进一步减少,纤维膜较致密,且变薄。TZNT和TA2植入后的纤维膜厚度和炎细胞密度均小于Ti6Al7Nb和Ti6Al4V的。
4) TZNT比Ti6Al7Nb和Ti6Al4V具有更好的生物相容性,有望成为一种理想的硬组织修复替代材料。
REFERENCES
[1] GORDINA D M, GLORIANTA T, NEMTOIB G H, CHELARIUC R, AELANEID N, GUILLOUA A, ARSELA D. Synthesis, structure and electrochemical behavior of a beta Ti-12Mo-5Ta alloy as new biomaterial[J]. Materials Letters, 2005, 59(23): 2959-2964.
[2] GEETHA M, SINGH A K, MURALEEDHARAN K, GOGIA A K, ASOKAMANI R. Effect of thermomechanical processing on microstructure of a Ti-13Nb-13Zr alloy[J]. Journal of Alloys and Compounds, 2001, 329(1/2): 264-271.
[3] GEETHA M, KAMACHI MUDALI U, GOGIA A K, ASOKAMANI R, RAJ B. Influence of microstructure and alloying elements on corrosion behavior of Ti-13Nb-13Zr alloy[J]. Corrosion Science, 2004, 46(4): 877-892.
[4] NILSON T C, OLIVEIRA G A, CARAMB R, ANTONIO C G. Development of Ti-Mo alloys for biomedical applications: Microstructure and electrochemical characterization[J]. Mater Sci Eng A, 2007, 452/453(15): 727-731.
[5] STEINEMANN S G, MAUSLI P A, SZMUKLERMONCLER S, SEMLITSCH M, POHLER O, HINTERMANN H E, PERREN S M. Beta-titanium alloy for surgical implants[C]//FROEA F H, CAPLAN I. Proceedings of Titanium’92 Science and Technology. Warrendale: TMS. 1993: 2689-2694.
[6] 李 军, 周 廉, 李佐臣, 陈杜娟. 新型医用钛合金Ti-12.5Zr-2.5Nb-2.5Ta的研究[J]. 稀有金属材料与工程, 2003, 32(5): 398-400.
LI Jun, ZHOU Lian, LI Zuo-chen, CHEN Du-juan. Study of a new titanium alloy for surgical implant application[J]. Rare Metal Materials and Engineering, 2003, 32(5): 398-400.
[7] 王金友, 葛志明, 周彦邦. 航空α用钛合金[M]. 上海: 上海科学技术出版社, 1985: 60.
WANG Jin-you, GE Zhi-ming, ZHOU Yan-bang. α titanium alloys for aviation applications[M]. Shanghai: Shanghai Science and Technology Press, 1985: 60.
[8] БОРИСОВА E A. 钛合金金相学[M]. 陈石卿, 译. 北京: 国防工业出版社, 1986: 4-7.
БОРИСОВА E A. Titanium alloy metallography[M]. CHEN Shi-qing, transl. Beijing: National Defence and Industry Press, 1986: 4-7.
[9] STEINEMANN S G, PERREN S M. Titanium alloys as metallic biomaterials[C]//L?TJERING G, ZWICKER V, BUNK W. Proceeding of the 5th International Conference on Titanium. Münich: FRG, 1985: 1327-1334.
[10] 梁英教. 物理化学[M]. 北京: 冶金工业出版社, 1995: 369-373.
LIANG Ying-jiao. Physical chemistry[M]. Beijing: Metallurgical Industry Press, 1995: 369-373.
[11] HELSEN J A, BREME J. Metals as biomaterials[M]. New York: Wiley, 1998: 30-40.
[12] JONSSON A K, NIKLASSON G A, VESZELEI M. Electrical properties of ZrO2 thin films[J]. Thin Solid Films, 2002, 402(11): 242-247.
(编辑 李艳红)
基金项目:上海市青年科技启明星计划(A类)资助项目(08QA14035)
收稿日期:2009-06-09;修订日期:2009-11-26
通信作者:李 军,副教授,博士;电话:021-67791203;E-mail:jacob_lijun@sina.com