文章编号:1004-0609(2016)-06-1264-08
氧化石墨烯/二氧化硅复合材料对铀(Ⅵ)的吸附性能
王 亮,谢水波,杨金辉,曾涛涛,刘金香
(南华大学 城市建设学院污染控制与资源化技术湖南省重点实验室,衡阳 421001)
摘 要:以氧化石墨烯(GO)、正硅酸乙酯(TEOS)为原料,聚氧乙烯-聚氧丙烯-聚氧乙烯(P123)为表面活性剂,利用TEOS水解成SiO2合成了氧化石墨烯/二氧化硅复合材料(GOS)。通过静态实验,探讨pH、GOS投加量、吸附时间和U(Ⅵ)初始浓度对GOS吸附U(Ⅵ)的影响,采用傅里叶变换红外光谱(FTIR)、X-射线衍射(XRD)、扫描电子显微镜(SEM)和能谱分析(EDS)对GOS进行表征,并探讨其吸附U(Ⅵ)的机理。结果表明:当溶液pH为6,投加量为0.2 g/L,吸附时间为120 min时,GOS吸附U(Ⅵ)效果最佳;吸附过程较好地拟合准二级动力学模型(R2≈1)和Freundlich等温模型(R2≈1);SiO2成功与GO复合,GOS对U(Ⅵ)具有很好的吸附性能,其吸附U(Ⅵ)前后自身结构并未发生变化,其对U(Ⅵ)的吸附机理以―COOH、―OH的离子交换作用为主,Si―OH的络合反应并存。
关键词:氧化石墨烯;二氧化硅;复合材料;铀(Ⅵ);吸附
中图分类号:O647.3;X591 文献标志码:A
铀矿冶生产中的低浓度含铀废水如果直接进入水体,将对人体健康和生态环境构成严重危害。高效处理含铀废水并回收铀成为亟待解决的核环境问题[1-2]。传统的离子交换、化学沉淀、植物修复、溶剂萃取等含铀废水处理方法存在处理成本高、效率较低、回收利用率低等不足[3],因而高效廉价、重复利用率好等的新型铀吸附材料备受关注。其中,石墨烯[4-5]以其优异特性而被广泛应用,其比表面积巨大,含有丰富的羟基、羧基等含氧官能团,为废水中铀的吸附提供了大量结合位点[6]。李琰[7]利用氧化石墨烯吸附U(Ⅵ)、Th(Ⅳ)、Eu(Ⅲ),均取得了很好的吸附效果。KUMAR等[8]利用氧化石墨烯对Cr(Ⅵ)进行去除,均取得很好的效果。SiO2价廉、无毒害、化学稳定强,是具有生物相容性的多功能材料,与氧化石墨烯进行材料修饰可克服氧化石墨烯本身易聚集的问题,有助于其比表面积的增加以及结合位点数目的增加,提高吸附效果[9-10]。
本课题采用聚氧乙烯-聚氧丙烯-聚氧乙烯(P123)为表面活性剂,二氧化硅前驱体―正硅酸乙酯(TEOS)为原料与氧化石墨烯(GO)复合,制备了氧化石墨烯/二氧化硅复合材料(GOS)。通过试验探讨了GOS对U(Ⅵ)的吸附特性,利用动力学、热力学模型分析了GOS吸附U(Ⅵ)的过程,利用FTIR、XRD、SEM和EDS等手段探讨了其相关机制,以期为含铀废水的处理提供理论参考。
1 实验
1.1 主要试剂与仪器
主要试剂:石墨(25 μm)、NaNO3、浓硫酸、KMnO4、双氧水、正硅酸乙酯、聚氧乙烯-聚氧丙烯-聚氧乙烯等,均为市售分析纯;含铀废水采用U3O8(基准纯GBW04201[11])配制而成;试验用水为双重蒸馏水。
主要仪器:T6分光光度计(北京普析通用仪器有限责任公司生产);傅里叶变换红外光谱仪(NICOLET6700型,美国Thermo Fisher公司生产);X射线衍射(ULTIMA IV型,日本Rigku公司生产);扫描电子显微镜(JSM-7500F型,日本JEOL公司生产);X射线能谱仪(X-Max型,英国OXFORD公司生产)。
1.2 GO的制备
以石墨为原料,采用Hummers法制备氧化石墨[12],干燥储存以备用。
1.3 吸附剂GOS的制备
称取0.03 g氧化石墨置于100 mL双重蒸馏水中,通过对其进行超声(100 W,2 h)得到氧化石墨烯(GO),加入0.35 g P123[13]于溶液中,将其pH调为3,常温下磁力搅拌1 h,量取0.8 mL TEOS[14]加入混合液中,继续磁力搅拌12 h。将所得产物离心洗涤3次,以去除残留的P123和其他杂质。将离心产物置于60 ℃真空干燥箱中,得到GOS,干燥储存以备用。
1.4 GOS吸附试验
量取适当浓度铀溶液30 mL置于100 mL锥形瓶中,用0.1 mol/L、0.01 mol/L HCl和NaOH调节其pH值。称取0.01 g GOS,配置成悬浮液20 mL。将30 mL铀溶液与20 mL悬浮液混合,于恒温摇床内以以130 r/min的转度震荡相应时间,反应后过滤取10 mL上清液,用紫外可见分光光度计(T6)测定其吸光度,重复两次,取平均值计算剩余U(Ⅵ)浓度,并按式(1)、(2)计算GOS对U(Ⅵ)的吸附量及U(Ⅵ)的吸附率。
 (1)
(1)
 (2)
(2)
式中:q为GOS对U(Ⅵ)的吸附量,mg/g;R为U(Ⅵ)的吸附率,%;ρ0为吸附前溶液中U(Ⅵ)浓度,mg/L;ρe为吸附后溶液中U(Ⅵ)浓度,mg/L;V为溶液体积,L;m为GOS质量,g。
1.5 GOS解吸附试验
称取0.01 g吸附铀后的GOS投入50 mL HCl (0.1 mol/L)溶液中,30 ℃恒温震荡解吸90 min,过滤取10 mL上清液,测定上清液铀离子浓度。将解吸后的吸附剂用去离子水洗涤3次,然后放置60 ℃真空干燥箱干燥至恒重,再进行吸附-解吸试验,循环4次。铀解吸率由(3)式计算:
 (3)
(3)
式中:d为U(Ⅵ)的解吸量,mg/g;q为GOS对U(Ⅵ)的吸附量,mg/g;D为U(Ⅵ)的解吸率,%。
2 结果与讨论
2.1 pH值对GOS吸附U(Ⅵ)的影响
在U(Ⅵ)初始浓度为10 mg/L,GOS投加量为0.1 g/L,温度为30 ℃的条件下,将pH值调为2.0~8.0内,吸附120 min,过滤取上清液测定溶液中残余U(Ⅵ)浓度,探讨pH值对GOS吸附U(Ⅵ)的影响,试验结果如图1所示。

图1 pH值对GOS吸附U(Ⅵ)的影响
由图1表明,pH值对GOS吸附U(Ⅵ)的影响较大。吸附反应后,各组溶液的pH值出现不同程度的升高,这表明H+参与了吸附过程。当pH=2时,吸附率仅为46.5%,这是因为pH较低时,以UO22+形式存在的铀与溶液中大量存在的H+发生竞争吸附,并且大量的H+附着在GOS表面使其质子化,增加吸附剂与UO22+之间的静电斥力,阻碍U(Ⅵ)被吸附,吸附率较低;当2.0<pH<6.0时,随着pH值的升高,竞争吸附减少,同时GOS质子化变弱,U(Ⅵ)吸附率增加[15];当pH=6.0时,铀主要以[UO2(OH)]+离子形式存在,此时吸附效果最好(达98.7%)[16]。当pH>6.0时,吸附率缓慢下降,这是因为此时铀以[UO2-(CO3)3]4-[17]形式存在,在碱性环境下,U(Ⅵ)水解形成难于吸附的沉淀,U(Ⅵ)吸附率降低。因此,本试验条件下GOS吸附U(Ⅵ)最佳pH值为6。
2.2 GOS投加量对GOS吸附U(Ⅵ)的影响
吸附剂GOS投加量直接影响GOS与U(Ⅵ)的结合位点数目,进而直接影响U(Ⅵ)的吸附率[18]。在温度为30 ℃,U(Ⅵ)初始浓度为10 mg/L,pH=6,吸附时间为120 min的条件下,考察不同GOS投加量(0.05、0.1、0.15、0.2、0.25、0.3、0.35 g/L)对GOS吸附U(Ⅵ)的影响,结果如图2所示。
由图2可以看出,GOS投加量为0.05 g/L时,U(Ⅵ)吸附量最大(达162 mg/g),但U(Ⅵ)吸附率仅81%。随着GOS投加量的增加,U(Ⅵ)吸附率逐渐上升,吸附容量逐渐降低。这是由于随着GOS用量的增加,GOS与U(Ⅵ)结合位点数目增多,从而使U(Ⅵ)的吸附率上升。但GOS投加量的增加一方面导致GOS片层之间相互团聚概率增大,降低有效结合位点数目,比表面积减少,另一方面导致单位质量吸附剂吸附U(Ⅵ)的结合位点数目减少,所以吸附容量随之降低[19]。当GOS投加量达到0.2 g/L时,U(Ⅵ)吸附率达到97.60%;继续增加投加量至0.25 g/L,GOS对U(Ⅵ)的吸附率基本没变化。因此,本试验条件下GOS吸附U(Ⅵ)最佳投加量为0.2 g/L。
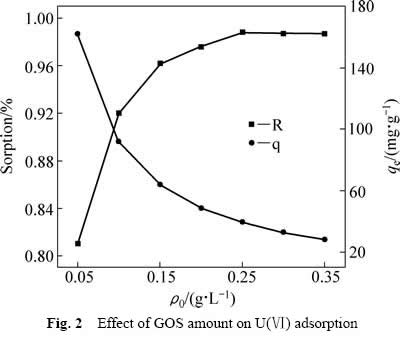
图2 GOS投加量对吸附效果的影响
2.3 GOS对U(Ⅵ)的吸附动力学
在温度为30 ℃,溶液pH值为6,U(Ⅵ)初始浓度分别为5、10和15 mg/L的条件下,探讨吸附时间对GOS吸附U(Ⅵ)的影响,试验结果如图3所示。
图3表明,GOS对U(Ⅵ)的吸附经历了快速吸附(0~20 min)、慢速吸附(20~60 min)、吸附平衡(60~120 min)3个阶段[20]。在20 min时,GOS对不同U(Ⅵ)浓度的吸附量分别达平衡吸附量的92.68%(5 mg/L)、92.69%(10 mg/L)和92.71%(15 mg/L);120 min时,3个不同U(Ⅵ)初始浓度的吸附都基本趋于平衡。因此,本试验条件下GOS吸附U(Ⅵ)最佳吸附时间选为120 min。
为进一步研究GOS吸附U(Ⅵ)的动力学特征,采用常用的3种动力学模型(准一级动力学模型、准二级动力学模型和颗粒内扩散模型)对GOS吸附U(Ⅵ)过程进行拟合,拟合参数见表1。
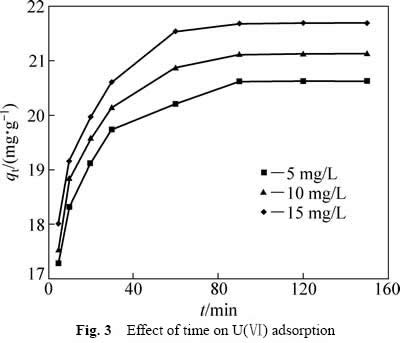
图3 吸附时间对吸附U(Ⅵ)的影响
从表1可以看出,准二级动力学方程的拟合度较准一级动力学方程高,且其理论平衡吸附量qe,cal与实际平衡吸附量qe,exp很接近,因此,准二级动力学方程能更好地描述GOS对U(Ⅵ)的吸附动力学过程。这表明GOS吸附U(Ⅵ)的过程以化学吸附为速控步骤[21]。由表1中数据得知,颗粒内扩散模型的拟合曲线未经过原点,说明颗粒内扩散不是GOS吸附U(Ⅵ)的速率控制步骤,吸附过程是由多种吸附机理共同控制[22]。
2.4 GOS对铀的等温吸附研究
在温度为30 ℃,pH为6,t=120 min,GOS投加量为0.2 g/L的条件下,探讨U(Ⅵ)初始浓度对GOS吸附U(Ⅵ)的影响,其结果如图4所示。由图4可见,随着U(Ⅵ)初始浓度的升高,GOS的吸附量逐渐增大,而吸附率却呈现下降趋势。这是由于U(Ⅵ)初始浓度较高时,其浓度梯度(?ρ=ρ0-ρe)较大,促进U(Ⅵ)向GOS表面和内部扩散,使U(Ⅵ)与GOS中结合位点结合的几率增加,从而吸附量增大[1];而吸附率降低是因为单位质量的吸附剂与U(Ⅵ)结合位点是有限的[18]。因此,在实际含铀废水处理中,为达到较好的处理效果,废水中U(Ⅵ)浓度以10~20 mg/L为宜。
表1 吸附动力学拟合参数

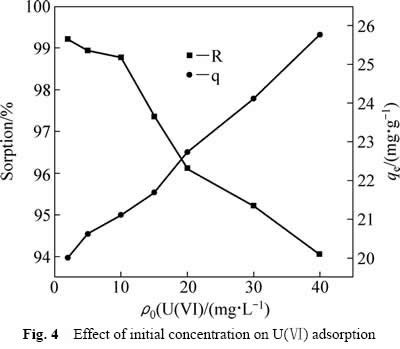
图4 U(Ⅵ)初始浓度对吸附的影响
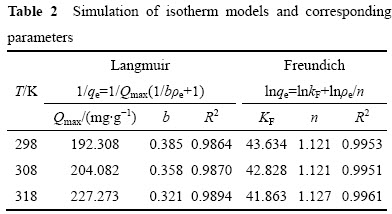
吸附剂对金属离子的吸附机理可用吸附等温线阐述[23]。本试验采用Freundlich和Langmuir等温吸附模型对GOS吸附U(Ⅵ)的过程进行拟合,以描述吸附体系达到吸附平衡时,GOS内吸附量与此时溶液中残余U(Ⅵ)浓度之间关系[22]。其拟合参数见表2,从表2中相关系数R2可以看出,Freundlich方程拟合得更好,这表明GOS对U(Ⅵ)的吸附为多层吸附;当T=308 K时,相应的特征常数n为1.121,一般认为n值大于1时易于吸附[24]。理论饱和吸附容量Qmax为204.082 mg/g。
表2 等温吸附模型拟合参数
2.5 GOS吸附铀前后的红外光谱分析
图5中曲线(a)、(b)分别为GOS吸附铀前后的红外光谱图(FTIR)。按文献[25-26]对吸收谱带进行分析,在曲线(a)中,3409 cm-1处是羟基―OH对应的伸缩振动吸收峰;2904 cm-1、2853 cm-1处分别是样品的―CH3、―CH2―基团的伸缩振动吸收峰;1717 cm-1处是羧基中的C=O基团的伸缩振动吸收峰;1634 cm-1处的吸收峰对应样品中水分子的弯曲振动吸收峰;1520 cm-1处是样品中―CH3、―CH2―基团的弯曲振动吸收峰;1402 cm-1处是羧酸中―OH基团的弯曲振动吸收峰;1259 cm-1处是甲基硅烷Si―CH3弯曲振动吸收峰;1076 cm-1处是硅氧烷Si―O―Si伸缩振动吸收峰;940 cm-1处是Si―OH的弯曲振动吸收峰;833 cm-1处是C―Si的伸缩振动吸收峰。
对比曲线(b)可见,吸附U(Ⅵ)后,―OH、―COOH、Si―CH3、Si―OH均出现偏移,表明―OH、―COOH、Si―CH3、Si―O―Si为主要吸附位点。但吸附前后的红外光谱变化不大,表明GOS吸附U(Ⅵ)后自身结构并未发生改变[15]。在3410 cm-1左右,在吸附前后均存在一个较宽的―OH吸收谱带,而吸附后峰型的移动和增宽,说明GOS所含的羟基可能与U(Ⅵ)发生了离子交换;在1374 cm-1处出现强度增大的谱峰,表示―COO―的对称伸缩峰和反对称伸缩峰,说明GOS与U(Ⅵ)发生了离子交换。在937 cm-1处出现峰强增加和峰型的移动,说明GOS可能与U(Ⅵ)发生了络合反应。

图5 GOS吸附U(Ⅵ)前后的红外光谱
2.6 GO、GOS的X射线衍射(XRD)分析
在对产物官能团分析的基础上,利用X-射线衍射(XRD)对其晶体结构进行了表征,如图6所示。
由图6可见,GO在2θ=9.8°附近出现很强的衍射峰,对应(002)面[27]。而在GOS的衍射谱上,2θ=9.8°的GO特征峰消失,在2θ=19.88°附近出现一个较强的衍射峰,这说明GO与SiO2复合过程中,晶体结构发生了变化,复合材料中GO分散很好,无较明显团聚,与SiO2复合后,根据特征衍射峰的位置,对照PDF标准卡片数据库,可以得出结论:氧化石墨烯表面、层间的SiO2是某种特殊的晶象。这是因为GO片层上存在大量的羟基、羧基等含氧基团,使得SiO2能够成功负载于GO中。
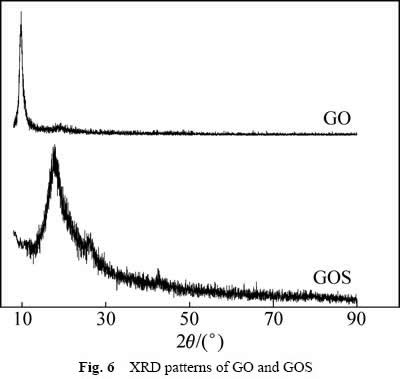
图6 GO和GOS的XRD谱
2.7 GOS吸附U(VI)前后扫描电镜及能谱分析
图7所示为GOS吸附铀前后的SEM像。由图7(a)可见,GOS吸附铀之前呈不规则片状结构,表面较光滑。片层之间存在一定间距且堆积较少,这就增加GOS的有效比表面积,同时使更多的结合位点暴露出来。对比图7(a)、(b)可知,吸附铀后,GOS表面较吸附前平整,表面及片层之间已被吸附的铀填充了[27],这说明GOS对U(Ⅵ)具有很好的吸附效果。图8所示为吸附铀前后的X射线能谱(EDS)分析图。从图8(a)可以看出,吸附前,GOS主要由C、O、Si元素构成,没有U(Ⅵ)元素的存在;吸附后,GOS中U(Ⅵ)的质量含量高达14.37%,表明GOS对U(Ⅵ)具有较强的吸附能力[1]。其对U(Ⅵ)吸附可能是羟基、羧基的离子交换,或者与Si―OH的络合反应。
2.8 GOS对U(Ⅵ)的解吸附试验
解吸是吸附的逆过程,解吸率是判断吸附剂性能好坏的重要指标之一。以0.1 mol/L的HCl溶液对吸附U(Ⅵ)(ρ0=10 mg/L)后的GOS进行解吸试验[28],其结果如图9所示。
解吸主要是利用H+破坏GOS上官能团与UO22+所形成的化合物,从而使UO22+从GOS中解析出来。

图7 GOS吸附U(Ⅵ)前后的SEM像

图8 GOS吸附铀前和吸附铀后的EDS谱
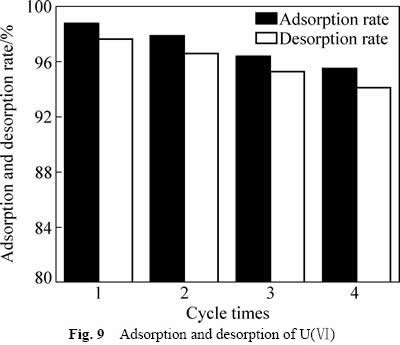
图9 U(Ⅵ)的吸附与解吸
从图9可以看出,初次解吸率高达97.62%,经过吸附-解吸-吸附4轮循环后,解吸率仍然高达94%以上,说明GOS具有重复使用的性能,具有应用于废水中铀的回收利用的潜力。
3 结论
1) 根据静态吸附试验,pH对GOS吸附U(Ⅵ)影响较大,其吸附U(Ⅵ)最佳pH值为6;GOS吸附U(Ⅵ)的最佳投加量为0.2 g/L;在GOS吸附U(Ⅵ)的过程中,主要表现为快速的表面吸附,20 min的吸附量达平衡吸附量的92.69%,吸附在120 min趋于平衡;吸附过程符合准二级动力学模型(R2≈1)和Freundlich等温吸附模型(R2≈1)。
2) FTIR、SEM、EDS分析结果表明:U(Ⅵ)能够很好地吸附在GOS上,其反应主要是与羟基、羧基的离子交换,以及与GOS中Si―OH的络合作用。
3) 以0.1 mol/L的HCl溶液为解吸液,对吸附U(Ⅵ)后的GOS解吸,经过吸附-解吸-吸附循环4次后解吸率仍然达94%以上,说明吸附剂GOS具有较高的重复利用价值和应用于放射性含铀废水处理的可能。
REFERENCES
[1] 陈华柏, 谢水波, 刘金香, 肖拾红, 曾涛涛, 凌 辉, 王劲松. 厌氧颗粒污泥吸附铀(Ⅵ)的特性与机理[J]. 中国有色金属学报, 2014, 24(9): 2418-2425.
CHEN Hua-bai, XIE Shui-bo, LIU Jin-xiang, XIAO Shi-hong, ZENG Tao-tao, LING Hui, WANG Jin-song. Characteristics and mechanism of uranium(Ⅵ) absorbed by anaerobic granular sludge[J]. The Chinese Journal of Nonferrous Metals, 2014, 24(9): 2418-2425.
[2] 谢水波, 陈 胜, 马华龙, 唐振平, 曾涛涛, 凌 辉, 吴宇琦. 硫酸盐还原菌颗粒污泥去除U(Ⅵ)的影响因素及稳定性[J]. 中国有色金属学报, 2015, 25(6): 1713-1720.
XIE Shui-bo, CHEN Sheng, MA Hua-long, TANG Zhen-ping, ZENG Tao-tao, LING Hui, WU Yu-qi. Influence factors and stability of U(Ⅵ) removal by sulfate reducing bacteria granular sludge[J]. The Chinese Journal of Nonferrous Metals, 2015, 25(6): 1713-1720.
[3] 彭国文, 丁德馨, 胡 南, 杨雨山, 王晓亮. 纳米Fe3O4负载啤酒酵母菌对铀的吸附性能与机理[J]. 中国有色金属学报, 2012, 22(2): 604-610.
PENG Guo-wen, DING De-xin, HU Nan, YANG Yu-shan, WANG Xiao-liang. Adsorption properties and mechanism of Saccharomyces cerevisiae loaded by nano-Fe3O4 on uranium[J]. The Chinese Journal of Nonferrous Metals, 2012, 22(2): 604-610.
[4] GEIM A K, NOVOSELOV K S. The rise of graphene[J]. Nature Materials, 2007, 6(3): 183-191.
[5] KATSNELSON M I. Graphene: Carbon in two dimensions[J]. Materials Today, 2007, 10(1): 20-27.
[6] NAM S W,JUNG C,LI H,YU M,FLORA J R V,BOATENG L K, HER N, ZOH K D, YOON Y. Adsorption characteristics of diclofenac and sulfamethoxazole to graphene oxide in aqueous solution[J]. Chemosphere, 2015, 136: 20-26.
[7] 李 琰. 氧化石墨烯的合成、表征及其对U(Ⅵ)、Th(Ⅳ)、Eu(Ⅲ)的吸附研究[D]. 兰州: 兰州大学, 2012.
LI Yan. The synthesis, characterization of graphene oxide and its sorption to U(Ⅵ),Th(Ⅳ), Eu(Ⅲ)[D]. Lanzhou: Lanzhou University, 2012.
[8] KUMAR A S K, KAKAN S S, RAJESH N. A novel amine impregnated graphene oxide adsorbent for the removal of hexavalent chromium[J]. Chemical Engineering Journal, 2013, 230: 328-337.
[9] CAO Y, LI X. Adsorption of graphene for the removal of inorganic pollutants in water purification: A review[J]. Adsorption, 2014, 20(5/6): 713-727.
[10] LUO L L, GU X X, WU J, ZHONG S X, CHEN J R. Advances in graphene for adsorption of heavy metals in wastewater[J]. Advanced Materials Research, 2012, 550: 2121-2124.
[11] 中国标准物质委员会. QBW 04201. 八氧化三铀成分分析标准物质[S].
China Standards Committee. QBW 04201. The certified reference material for composition analysis of triuranium octoxide[S].
[12] 张佳利. 化学还原氧化石墨烯及其衍生物的制备、性质和应用研究[D]. 上海: 上海交通大学, 2011.
ZHANG Jia-li. Preparations, properties and applications of chemically reduced grapheme oxide and its derivatives[D]. Shanghai: Shanghai Jiao Tong University, 2011.
[13] 林翠英, 邱 羽, 江琳沁, 赵剑曦. Pluronic F127和P123嵌段共聚物胶束结构[J]. 福州大学学报(自然科学版), 2000, 6: 77-81.
LIN Cui-yin, QIU Yu, JIANG Lin-qin, ZHAO Jian-xi. Micellar structure of Pluronic F127 and P123 triblock copolymers[J]. Journal of Fuzhou University, 2000, 6: 77-81.
[14] YANG Shu-bin, FENG Xin-liang, WANG Long, TANG Kun, JOACHIM M, KLAUS M. Graphene-based nanosheets with a sandwich structure[J]. Angewandte Chemie International Edition, 2010, 49(28): 4795-4799.
[15] 谢水波, 罗景阳, 刘 清, 凌 辉, 段 毅, 王劲松. 羟乙基纤维素/海藻酸钠复合膜对六价铀的吸附性能及吸附机制[J]. 复合材料学报, 2015, 1: 268-275.
XIE Shui-bo, LUO Jing-yang, LIU Qing, LIN Hui, DUAN Yi, WANG Jin-song. Adsorption characteristics and mechanism of hydroxyethyl cellulose/sodium alginate blend films for uranium(Ⅵ)[J]. Acta Materiae Compositae Sinica, 2015, 1: 268-275.
[16] 郑伟娜, 夏良树, 王 晓, 谭凯旋. 谷壳对铀(Ⅵ)的吸附性能及机理研究[J]. 原子能科学技术, 2011, 45(5): 534-540.
ZHENG Wei-na, XIA Liang-shu, WANG Xiao, TAN Kai-xuan. Adsorption behavior and mechanism of uranium by chaff[J]. Atomic Energy Science and Technology, 2011, 45(5): 534-540.
[17] KILINCARSLAN A, AKYIL S. Uranium adsorption characteristic and thermodynamic behavior of clinoptilolite zeolite[J]. Journal of Radioanalytical and Nuclear Chemistry, 2005, 263(3): 541-548.
[18] WANG Hou, YUAN Xing-zhong, WU Yan, HUANG Hua-jun, ZENG Guang-ming, LIU Yan, WANG Xue-li, LIN Ning-bo, QI Yu. Adsorption characteristics and behaviors of graphene oxide for Zn (Ⅱ) removal from aqueous solution[J]. Applied Surface Science, 2013, 279: 432-440.
[19] LI Zi-jie, CHEN Fei, YUAN Li-yong, LIU Ya-lan, ZHAO Yu-liang, CHAI Zhi-fang, SHI Wei-qun. Uranium (Ⅵ) adsorption on graphene oxide nanosheets from aqueous solutions[J]. Chemical Engineering Journal, 2012, 210: 539-546.
[20] MISHRA S, MAITY S, BHALKE S, PANDIT G G, PURANIK V D, KUSHWAHA H S. Thermodynamic and kinetic investigations of uranium adsorption on soil[J]. Radioanal Nucl Chem, 2012, 294: 97-102.
[21] SOLGY M, TAGHIZADEH M, GHODDOCYNEJAD D. Adsorption of uranium (Ⅵ) from sulphate solutions using Amberlite IRA-402 resin: Equilibrium, kinetics and thermodynamics study[J]. Annals of Nuclear Energy, 2015, 75: 132-138.
[22] ANIRUDHAN T S, JALAJAMONY S. Ethyl thiosemicarbazide intercalated organophilic calcined hydrotalcite as a potential sorbent for the removal of uranium (Ⅵ) and thorium (Ⅳ) ions from aqueous solutions[J]. Journal of Environmental Sciences, 2013, 25(4): 717-725.
[23] WANG Xiao-liang, PENG Guo-wen, YANG Yan, WANG Yan-fei, HE Ting-ting. Uranium adsorption by dry and wet immobilized Saccharomyces cerevisiae[J]. Radioanal Nucl Chem, 2012, 291: 825-830.
[24] 李小燕, 刘义保, 花 明, 李金轩, 高 柏. 改性玉米芯吸附溶液中U(Ⅵ)的热力学特证[J]. 中国有色金属学报, 2013, 23(4): 1168-1172.
LI Xiao-yan, LIU Yi-bao, HUA Ming, LI Jin-xuan, GAO Bai. Adsorption thermodynamic characteristics of U(Ⅵ) on modified corncob in aqueous solution[J]. The Chinese Journal of Nonferrous Metals, 2013, 23(4): 1168-1172.
[25] LIU Ya-lan, YUAN Li-yong, YUAN Ya-li, LAN Jian-hui, LI Zi-jie, FENG Yi-xiao, ZHAO Yu-liang, CHAI Zhi-fang, SHI Wei-qun. A high efficient sorption of U(Ⅵ) from aqueous solution using amino-functionalized SBA-15[J]. Journal of Radioanalytical and Nuclear Chemistry, 2012, 292(2): 803-810.
[26] WANG Xiao, XIA Liang-shu, TAN Kai-xuan, ZHENG Wei-na. Studies on adsorption of uranium(Ⅵ) from aqueous solution by wheat straw[J]. Environmental Progress & Sustainable Energy, 2012, 31(4): 566-576.
[27] 范艳煌, 邹正光, 龙 飞, 吴 一, 高 洁, 孔令奇. 以氧化石墨烯为氧化介质制备石墨烯/聚苯胺导电复合材料[J]. 复合材料学报, 2013, 1: 27-31.
FAN Yan-huang, ZHOU Zheng-guang, LONG Fei, WU Yi, GAO Jie, KONG Ling-qi. Preparation of graphene/polyaniline conducting composite by grapheme oxide for oxidant[J]. Acta Materiae Compositae Sinica, 2013, 1: 27-31.
[28] 冯 媛, 易发成. 稻壳对铀吸附性能的研究[J]. 原子能科学技术, 2011, 2: 161-167.
FENG Yuan, YI Fa-cheng. Adsorptive property of rice husk for uranium[J]. Atomic Energy Science and Technology, 2011, 2: 161-167.
Adsorption properties of graphene oxide/silica composite materials for uranium (Ⅵ)
WANG Liang, XIE Shui-bo, YANG Jin-hui, ZENG Tao-tao, LIU Jin-xiang
(Hunan Province Key Laboratory of Pollution Control and Resources Reuse Technology,
University of South China, Hengyang 421001, China)
Abstract: The graphene oxide/silica composite (GOS) was fabricated using graphene oxide (GO), ethylsilicate (TEOS) as the raw material, oxygen polyoxyethylene-polypropylene-polyoxyethylene (P123) as the surfactant. Through a static test, different experimental parameters, such as solution pH, dosing, initial concentration and contact time, were examined to investigate their effects on adsorption of uranium by GOS. The composite was investigated by FTIR, XRD, SEM and EDS. The results show that the optimal pH, addition, adsorption time are 6, 0.2 g/L and 120 min, respectively. The equilibrium data fit well with the pseudo-second-order model (R2≈1) and Freundlich model (R2≈1). Silicon dioxide has been successfully combined with GO. GOS has good adsorption effect on U(Ⅵ), and the GOS structure itself keeps unchanged during the adsorption. It is shown that both ion exchanges of ―COOH and ―OH play a major role, with the assistant of complexation reaction of Si―OH in the adsorption.
Key words: graphene oxide; silica; composite; uranium (Ⅵ); adsorption
Foundation item: Projects (11175081, 51408293) supported by the National Natural Science Foundation of China; Project (CX2015B405) supported by the Hunan Provincial Innovation Foundation of Postgraduate, China; Project (20134324110003) supported by the Specialized Research Fund for the Doctoral Program of Higher Education, China; Project (13K085) supported by Key Laboratory of Innovation Fund in Hunan Provincial, China
Received date: 2015-08-25; Accepted date: 2015-11-03
Corresponding author: XIE Shui-bo; Tel: +86-734-8281603; E-mail: xiesbmr@263.net
(编辑 王 超)
基金项目:国家自然科学基金资助项目(11175081,51408293);湖南省研究生科研创新项目(CX2015B405);高等学校博士点基金资助项目(20134324110003);湖南省高校重点实验室创新基金资助项目(13K085)
收稿日期:2015-08-25;修订日期:2015-11-03
通信作者:谢水波,教授,博士;电话:0734-8281603;E-mail:xiesbmr@263.net