文章编号:1004-0609(2008)S1-0236-06
超声波作用下用氧化锌和硫化钠反应合成纳米硫化锌
丘克强,曾恒志,龙桂花
(中南大学 化学化工学院,长沙 410083)
摘 要:以氧化锌和硫化钠为原料,采用固液化学反应,在超声波的作用下,制备纳米硫化锌。实验得出最佳反应条件为:反应温度80 ℃,Na2S浓度2.0 mol/L,反应时间2 h,反应前超声分散15 min。对最佳条件下得到的纳米硫化锌颗粒进行X射线衍射、扫描电镜、红外光谱及热重-微分热重分析。结果表明:该颗粒为结晶完全的闪锌矿,平均粒度为50 nm,且颗粒在400~4 000 cm-1具有红外透光性,在纯氧气氛围中具有良好的热稳定性。
关键词:超声波;氧化锌;纳米硫化锌;晶体
中图分类号:O 614.24 文献标识码:A
Preparation of nanoparticles ZnS by solid-liquid chemical reaction with ZnO and Na2S under ultrasonic
QIU Ke-qiang, ZENG Heng-zhi, LONG Gui-hua
(School of Chemistry and Chemical Engineering, Central South University, Changsha 410083, China)
Abstract: Nanoparticles ZnS were prepared with ZnO and Na2S by solid-liquid chemical reaction under ultrasonic condition. The optimum conditions gained from experiment are as follows: reacting temperature 80 ℃, Na2S concentration 2.0 mol/L, reacting time 2 h, and dispersing with ultrasonic 15 min before reaction. The nanoparticles ZnS obtained by the optimum conditions were characterized by X-ray diffractometry (XRD), scan electron microscopy (SEM), infrared(IR) and thermogravimetry-differential thermogravimetry (TG-DTG). The results show that these particles are good crystal zinc blende with average size of 50 nm, and these particles also possess good IR transmittance in the range from 400 to 4 000 cm-1 and good thermal stability in oxygen.
Key words: ultrasonic; ZnO; nano-ZnS; crystal
纳米科技是20世纪80年代末期以来迅速崛起的新科技,纳米结构的微粒以其独特的物理性质,例如量子尺寸效应、异常的发光现象引起国内外广大学者的关注[1-3]。作为一种过渡族金属硫化物,纳米硫化锌显示出许多特异的光电性能,它的电致发光和光致发光效率较高[4-5],在光致发光、电致发光、磷光体、传感器、红外窗口材料、光催化等许多领域具有广泛的用途[6-7]。ZnS具有闪锌矿型(立方晶型)和纤锌矿型(六面体型) 2种结构,常用于发光材料的ZnS为闪锌矿 型[8]。
制备纳米ZnS的方法可分为物理法和化学法2大类[9-13],其中,物理方法主要有:气相沉积法、溅射沉积法、低温等离子法和蒸汽冷凝法等,这类方法仪器设备复杂,成本高;化学法主要有水热溶剂热法、化学沉淀法、微乳液法、溶胶-凝胶法和LB膜法等,这些方法原料较贵,并使用大量有机溶剂,过程控制复杂,或颗粒均匀性差,粒子易粘结或团聚等[14-17]。XU等[18-19]发明了一种制备纳米硫化锌的方法:即先利用气相蒸发技术制备出平均粒径为80 nm的锌粉粒子,高活性的锌粉粒子在接触空气时表面会有一部分被氧化,即为Zn/ZnO纳米粉末。将适量的Zn/ZnO粉末置于一定浓度的Na2S溶液中,形成悬浮液,在50 ℃下超声振荡,反应体系的颜色由黑转白,形成ZnS沉淀,过滤、洗涤,得到平均粒径为40 nm的球状ZnS微粒,过程如下:

从上述方法可知:1) 该方法本质是反应(2),因此不需要用纳米锌作为原料。因为制备纳米氧化锌比制备纳米锌粉更简单,成本也更低,所以可直接用氧化锌做原料。2) 正如该研究者的实验结果表明,所得产品容易残留金属锌,纯度不高。在此,本文作者首次直接以普通氧化锌粉和硫化钠为原料,利用超声波预分散作用,制备出性能优良的纳米硫化锌。
1 实验
1.1 试剂和仪器
DF-101S集热式恒温加热磁力搅拌器、B3200S-T型超声波仪、SHZ-3型水循环真空泵、TCE-I温度控制器、XMZ数显指示仪、自制环绕电阻丝电炉。
ZnO 分析纯;Na2S.9H2O分析纯;无水CuSO4 分析纯;均是市售。
1.2 纳米ZnS粉末的制备
室温下,用蒸馏水配制2.0 mol/L的Na2S,0.01 mol/L CuSO4溶液。将40 mL Na2S(2.0 mol/L)溶液与2 g普通分析纯的ZnO固体粉末混于200 mL烧杯中,超声波振荡分散一段时间,然后立即倒入100 mL的三颈瓶中,连接好直型冷凝管及冷却水,用氩气排除氧气,三颈瓶2/3没入90 ℃的水浴中,磁力搅拌2 h,反应完成后立即用蒸馏水将三口瓶中的产物冲至200 mL烧杯中,置于冷水中急冷,抽滤并用蒸馏水洗涤直至滤夜滴加CuSO4不变色,再用无水乙醇洗涤3次,最后真空干燥,研碎即得纳米ZnS粉末。
1.3 纳米ZnS颗粒的测试和表征
所制备的ZnS颗粒采用Rigaku D/max-2550V型X射线衍射仪进行物相分析,石墨单色器,Cu Kα (0.154 056 nm),扫描速率为2 (?)/min,以粒径为28 μm的SiO2标样对仪器宽化进行校正,并按照样品特征峰强度、宽化信息和晶面间距来测量样品的结构;采用KYKY 2800型扫描电镜(SEM)观察和测量样品的形貌和粒度。在纯O2气氛下,采用TGA/SDTA 851e热重差热同步分析仪(美国仪器厂)进行热重(TG-DTG)分析,升温速率为10 ℃/min,流速为70 mL/min;用BrukerFT-IRIFS-48型红外光谱仪进行红外分析,用日立F-2500荧光分光光度计测定光致发光光谱。
1.4 实验原理
对于反应:

若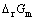 <0,则反应可以正向进行;反之,反应不能正向进行。如果
<0,则反应可以正向进行;反之,反应不能正向进行。如果 的绝对值很大,则
的绝对值很大,则 的正负号基本上就决定了
的正负号基本上就决定了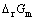 的符号。因此,若
的符号。因此,若 有很大的负值,则在一般情况下,
有很大的负值,则在一般情况下,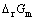 大致也为负值。
大致也为负值。
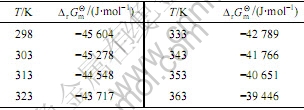
表1所示为不同温度下反应(3)的标准吉布斯自由能 。由表1可判断,将ZnO 和 Na2S 溶液反应制备ZnS 是可能的。
。由表1可判断,将ZnO 和 Na2S 溶液反应制备ZnS 是可能的。
表1 不同温度反应时的标准吉布斯自由能变化
Table 1 Standard free energy change for reaction at different temperatures
在室温下,ZnO、ZnS在水中的溶度积分别为3×10-18和1×10-24,ZnS比ZnO更难溶于水,因而有利于反应正向进行。
2 结果与讨论
2.1 产物纯度
2.1.1 反应温度对ZnS纯度的影响
不同反应温度下得到的纳米ZnS的质量分数如图1所示。由图1可知,随温度升高,产物中ZnS质量分数逐渐增大,且在80 ℃以下,其增幅较大;在80 ℃以上,其增幅缓慢,反应趋于平衡。由于此反应是一个吸热反应,随着温度的升高,促进反应向正方向进行,使ZnO进一步转化成ZnS,提高了ZnS在产物中的质量分数;但当温度超过80 ℃时,反应趋于平衡,故ZnS质量分数增幅缓慢。
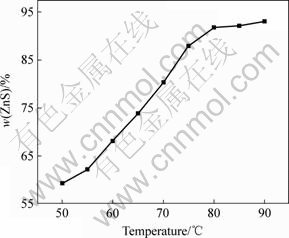
图1 不同温度下ZnS的质量分数
Fig.1 Mass fraction of ZnS at different temperatures
2.1.2 Na2S浓度对ZnS纯度的影响
不同Na2S浓度下得到的纳米ZnS的质量分数如图2所示。由图2可见,随Na2S浓度升高,产物中ZnS质量分数逐渐增大,且Na2S浓度在2.0 mol/L以下时,增幅较大;当Na2S浓度达到2.0 mol/L后,ZnS质量分数增幅缓慢,反应趋于平衡。
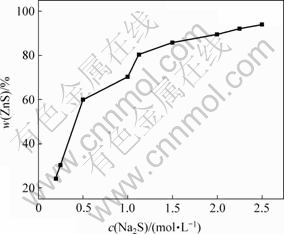
图2 不同Na2S浓度下ZnS的质量分数
Fig.2 Mass fraction of ZnS with different Na2S concentrations
2.1.3 反应搅拌时间对ZnS纯度的影响
不同反应时间下得到的纳米ZnS的质量分数如图3所示。由图3可见,随搅拌反应时间延长,产物中ZnS质量分数逐渐增大,特别是在2 h以内,其增幅明显;但当搅拌反应时间超过2 h后,其增幅趋缓慢。
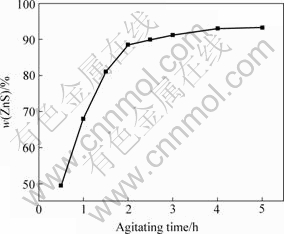
图3 不同搅拌时间下ZnS的质量分数
Fig.3 Mass fraction of ZnS with different agitating time
2.2 产物粒度
在反应温度为80 ℃,Na2S浓度为2.0 mol/L,反应时间为2 h的条件下,反应前超声波分散时间对产物平均粒度的影响如图4所示。由图4可见,超声波分散后反应得到的ZnS颗粒均达到了纳米级。
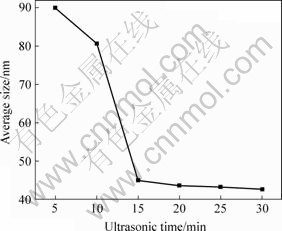
图4 超声波对ZnS颗粒平均粒度的影响
Fig.4 Effect of ultrasonic condition on average particle size of ZnS
由图4可见,反应前加入超声波分散,能促进小颗粒的形成和稳定,且随着超声波分散时间的延长,颗粒粒度进一步减小,但减小的幅度缓慢。这是由于超声波具有声空化作用,当在液体内施加超声场时,会使液体产生成群的气泡,这些气泡同时受到超声的作用,在经历超声的稀疏相和压缩相时,气泡生长、收缩、再生长、再收缩,经多次周期性振荡,最终以高速崩裂,在液固表面达到了良好的冲击作用,从而形成小颗粒的前驱反应物,所以能加速无机过饱和溶液中晶体形成过程,增加成核速率,抑制晶体生长而得到细晶粒。没有加入超声波作用所形成的ZnS颗粒均达不到纳米级别,大多是微米级别。
2.3 产物形貌
图5所示为反应温度 80 ℃,Na2S摩尔浓度2 mol/L,ZnO 2 g,搅拌时间2 h,液固比(L/S)为1.2?1,水浴搅拌前超声分散15 min时得到的ZnS粉末的SEM照片。由图5可以看出,在最佳条件下制备的ZnS粒度小,分布均匀;产物ZnS颗粒的边界光滑、明显,生长完好,能很清楚地看出单个颗粒的形状呈棱柱体形,平均粒径为50 nm左右。此外,本文所用的方法不需要将粉末煅烧,在低温下就制备出结晶完全、平均粒径小和分布均匀的棱柱体形纳米ZnS颗粒,不但降低制备过程的能耗,而且避免了ZnS粉末的氧化及团聚。

图5 纳米ZnS产物的SEM像
Fig.5 SEM image of ZnS sample
2.4 产物性能
2.4.1 XRD分析
将Na2S浓度分别为1.125 mol/L及2.0 mol/L反应得到的ZnS进行XRD分析,得到的结果如图6所示。
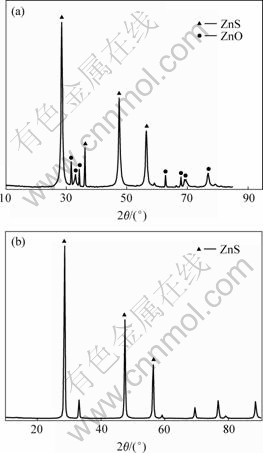
图6 ZnS粉末的XRD谱
Fig.6 XRD patterns of ZnS: (a) 1.125 mol/L; (b) 2.0 mol/L
由图6可见,Na2S反应浓度为1.125 mol/L时得到的ZnS不纯,还杂有少量未反应的ZnO,XRD谱上有ZnS的特征峰(111)、(220)、(311),为立方晶型的闪锌矿结构,同时还显示了ZnO的特征峰(100)、(002)、(101)、(110);Na2S反应浓度为2.0 mol/L得到的ZnS纯度较高,基本没有其他杂质峰。进一步比较图6(a)和图6(b)的XRD衍射峰。Scherrer公式为:
Dhkl=kλ/βcosθhkl
式中 Dhkl是垂直于晶面(hkl)方向上晶粒的粒度,k是常数,λ为X射线波长,β是(hkl)晶面衍射峰的半高宽,θhkl是(hkl)晶面的Bragg衍射角。由Scherrer公式可以估算出样品(a)和(b)的平均粒度分别为17.0 nm和27.0 nm。峰的宽化对应着晶粒粒度的减小,图6(a)比图6(b)的衍射峰宽化更明显,图6(a)条件下生成的产物颗粒粒度更小;图6(b)比图6(a)的衍射峰要尖锐,图6(b)条件下生成的产物颗粒结晶性更完全。
将图6的ZnS粉末的XRD谱与其他研究者用液相反应制备的ZnS粉末的XRD谱比较,发现本研究制备的ZnS衍射峰更尖锐,为结晶更好的立方晶型晶体。
2.4.2 红外光谱分析
为了了解所获硫化锌纳米微粒的光谱性质,对样品进行红外光谱分析,ZnS样品的红外光谱图如图7所示。

图7 ZnS样品的红外光谱图
Fig.7 UV pattern of ZnS
由图7可见,所得ZnS样品在420~460 cm-1处看不到对应的Zn―O拉伸振动的吸收峰,表明样品没有或基本上没有被氧化为ZnO,说明反应体系中充入惰性气体Ar排除氧气,再结合水浴回流装置能有效地防止纳米ZnS的氧化;在2 900~3 600 cm-1也看不到水的―OH基团的吸收峰,表明真空干燥能有效地去除吸附在颗粒上的水分;在400~4 000 cm-1处基本无吸收峰,表明该纳米ZnS呈现良好的红外透明性,是一种优良的红外透光材料。
2.4.3 热分析
对2.5 mol/L Na2S反应得到的ZnS粉末于纯氧气气氛中进行TG-DTG分析,结果如图8所示。由图8可知,在50 ℃时,样品质量稍微增加,由于ZnS强烈地吸附水[17],因而能吸附氧气中的部分水分,从而使质量稍有增加;当温度超过50 ℃,达到100 ℃左右时,样品质量又稍微减少,这是因为ZnS失去吸附水而表现出质量损失,其后在温度较低时,在氧气中质量基本上保持不变,直到570 ℃有1个快速质量损失阶段,质量损失约14%。据此可推断,当温度达到570 ℃时,ZnS在氧气中才被氧化成ZnO[18]。最终质量损失约16%,说明ZnS在氧气中具有良好的热稳定。

图8 硫化锌的热重曲线
Fig.8 TG-DTG curves of ZnS
2.4.4 荧光发射光谱分析
将纳米ZnS粉体进行荧光发射光谱分析,以考察其光学性能,结果如图9所示。
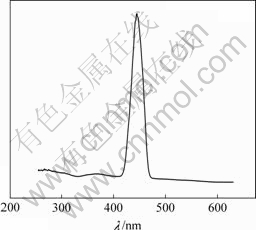
图9 纳米ZnS粉体的发射光谱
Fig.9 PL emission spectrum of ZnS sample
图9表明,本实验条件下制得的纳米ZnS粉体在440 nm左右只有1个发射峰;发射峰的强度大且发射谱带范围较窄,这进一步说明实验所得纳米ZnS粉体具有良好的结晶性。
3 结论
1) 运用固液化学反应法,在超声波的作用下,首次直接用氧化锌制备出稳定的纳米硫化锌,制备纳米硫化锌的最佳条件为:反应温度80 ℃,反应液浓度2.0 mol/L,反应时间2 h。
2) 实验获得ZnS属于闪锌矿型构型,粒度分布均匀,分散性好,平均粒径约为50 nm;纯度高,XRD谱上基本没有其他任何杂质峰;具有良好的结晶性、红外透明性和良好的热稳定性,是一种优良的红外透光材料。
3) 产品纳米ZnS制备过程不需要添加任何表面活性剂,具有工艺简单、产率高、原料便宜、制备周期短的优点,并且有很好的产业化前景。
REFERENCES
[1] 张立德. 纳米材料[M]. 北京: 化学工业出版社, 2000.
ZHANG Li-de. Nanocrystal materials[M]. Beijing: Chemical Industry Press, 2000.
[2] SCHMIDT H M, WELLER H. Quantum size effects in semiconductor crystallites: Calculation of the energy spectrum for the confined exciton[J]. Chemical Physics Letters, 1986, 129(6): 615-618.
[3] RAMA K M V, FRIESNER R A. Quantum confinement effects in semiconductor clusters[J]. Journal Chemical Physics, 1991, 67: 629-632.
[4] HUANG J M, YANG Y, XUE S H, YANG B, LIU S Y, SHEN J C. Photoluminescence and electroluminescence of ZnS?Cu nanocrystals in polymeric networks[J]. Appl Phys Lett, 1997, 70(18): 2335-2337.
[5] YANG Y, HNANG J M, LIU S Y, SHEN J C. Preparation, characterization and electroluminescence of ZnS nanocrystals in a polymer matrix[J]. J Mat Chem, 1997, 7(1): 131-133.
[6] 杨 桦, 王子忱, 宋利珠, 张厚玉, 窦 凯. 发光材料硫化锌纳米晶的合成与结构表征[J]. 功能材料, 1996, 27(4): 302-306.
YANG Hua, WANG Zi-chen, SONG Li-zhu, ZHANG Hou-yu, DOU Kai. Study of preparation and structure on ZnS nanocrystal doped with manganese[J]. Journal of Functional Materials, 1996, 27(4): 302-306.
[7] 舒 磊, 俞书宏, 钱逸泰. 半导体硫化物纳米微粒的制备[J]. 无机化学学报, 1999, 15(1): 1-7.
SHU Lei, YU Shu-hong, QIAN Yi-tai. Synthesis of metal sulfide semiconductor nanoparticles[J]. Chin J Inorg Chem, 1999, 15(1): 1-7.
[8] 赵 康, 刘正堂, 鄢君辉, 郑修麟. CVD法制备ZnS的生长率均匀性研究[J]. 功能材料, 1998, 29(1): 58-60.
ZHAO Kang, LIU Zheng-tang, YAN Jun-hui, ZHENG Xiu-lin. Study on the growth rate uniformity for preparing ZnS by CVD[J]. Journal of Functional Materials, 1998, 29(1): 58-60.
[9] DIMOS K, KOUTSELAS I B, KARAKASSIDES M A. Synthesis and characterization of ZnS nanosized semiconductor particles within mesoporous solids[J]. J Phys Chem B, 2006, 110(45), 22339-22345.
[10] DHAS N A, ZABAN A, GEDANKEN A. Surface synthesis of zinc sulfide nanoparticles on silica microspheres: Sonochemical preparation, characterization and optical properties[J]. Chem Mater, 1999, 11(3): 806-813.
[11] WANG L P, HONG G Y. A new preparation of zinc sulfide nanoparticles by solid state method at low temperature[J]. Mater Res Bull, 2000, 35(5): 695-701.
[12] ZHAO Z G, GENG F X, CONG H T, BAI J B, CHENG H M. A simple solution route to controlled synthesis of ZnS submicrospheres, nanosheets and nanorods[J]. Nanotechnology, 2006, 17(8): 4731-4735.
[13] CHAI L L, ZHU Y C, DU J, ZOU G F, XIONG K, QIAN Y T. One-step hydrothermal method to synthesize self-encapsulated ZnS micron core-shell spheres on a large scale[J]. Chem Lett, 2005, 34(10): 1324-1325.
[14] KOLB D M, ULLMANN R, ZIEGLER J C. Electrochemical nanostructuring[J]. Electrochimica Acta, 1998, 43(19/20): 2751-2760.
[15] WONG E W, MAYNOR B W, LIEBER C M. Growth of metal carbide nanotubes and nanorods[J]. Chemistry of Materials, 1996, 8(8): 2041-2043.
[16] 程丽娅, 陈 云, 吴庆生. 单分散ZnS纳米球与纳米梭之间的形貌转换及光学性能研究[J]. 化学学报, 2007, 65(17): 1851-1854.
CHENG Li-ya, CHEN Yun, WU Qing-sheng. Morphology exchange and optical properties of monodispersed ZnS nanospheres and nanoshuttles[J]. Acta Chimica Sinica, 2007, 65(17): 1851-1854.
[17] 孙 伟, 钟江华, 张灿英, 江 宏, 焦 奎. 巯基乙酸修饰ZnS纳米颗粒的水相合成及表征[J]. 过程学报, 2007, 7(5): 984-988.
SUN Wei, ZHONG Jiang-hua, ZHANG Can-ying, JIANG Hong, JIAO Kui. Synthesis and characterization of ZnS nanoparticles modified with mercaptoacetic acid in aqueous solution[J]. The Chinese Journal of Process Engineering, 2007, 7(5): 984-988.
[18] XU J F, JI W, LIN J Y, TANG S H, DU Y W. Preparation of ZnS nanoparticles by ultrasonic radiation method[J]. Appl Phys A, 1998, 66(6): 639-641.
[19] XU J F, JI W. J Characterization of ZnS nanoparticles prepared by new route[J]. Mater Sci Lett, 1999, 18(2): 115-117.
通讯作者:丘克强,教授,博士生导师;电话:0731-8877364;E-mail: qiuwhs@sohu.com
(编辑 赵 俊)