�Ǿ���-L-���Ḵ�ϲ��Գ�Ĥ���Ʊ������
�캣��1, 2������1������1��������1
(1. �人������ѧ ��������빤���о����ģ����� �人��430070��
2. �人������ѧ ����ѧԺ������ �人��430070)
ժ Ҫ���Բ�ʹ���κλ�ѧ�������������ʹ�Ǿ�����L-�����֦���۽����о����������䶳���﹤���Ʊ�һ��������Χ�������ĸ��ϲ��Գ�Ĥ���ϡ���ȫ���丵��Ҷ������ס�ɨ��羵����ʾɨ�����ȷ����ǵȽ��б������о����ϲ��Գ�Ĥ�����Ỻ����Һ(pH=7.4)�е��������ܲ�������ѧ���ܽ��вⶨ���о�������������ϲ��Գ�Ĥ���нϺõĽ�֦Ч���������ڲ����ܣ�������ɡ���������Ķ�ṹ����Լ100 ��m�����ϲ��Գ�Ĥ�IJ���ת���¶�Ϊ192.982 �棻������Ϊ��֦ǰ��1/2��1/6�����ϲ��Գ�Ĥ����ѧ������L-������Ǿ��ǵ������ȱ仯���仯������ǿ�ȡ�����ģ���������쳤�ʵ���������L-������Ǿ��ǵ�������Ϊ2ʱ���������ֵ��
�ؼ��ʣ��Ǿ��ǣ�L-������ϲ��Գ�Ĥ
��ͼ����ţ�TQ316.6+2 ���ױ�ʶ�룺A ���±�ţ�1672-7207(2007)03-0433-06
Preparation and characterization of chitosan-L- lactic acid
composite asymmetric membrane
XU Hai-xing1, 2, YAN Yu-hua1, WAN Tao1, LI Shi-pu1
(1. Biomedical Materials and Engineering Research Center, Wuhan University of Technology, Wuhan 430070, China;
2. Department of Pharmaceutical Engineering, School of Chemical Engineering,
Wuhan University of Technology, Wuhan 430070, China)
Abstract: Chitosan-L-lactic acid composite asymmetric membrane for the regeneration of peripheral nerve was obtained by grafting L-lactic acid onto the amino groups in chitosan without any chemical initiator combined vacuum freezer drier. The composite asymmetric membranes were characterized by ATR-FTIR, DSC and SEM. The swelling property in phosphate buffer solution (PBS, pH=7.4) and the mechanical properties were also investigated. The composite asymmetric membrane has a better graft efficiency. The membrane has a dense inner layer and a loose outer layer with porous structure and the pore size is about 100 ��m. The glass transition temperature is 192.982 ��. The swelling degree is about 1/2-1/6 of chitosan and the mechanical properties change with the mass ratio of LA to CS. First, the tensile strength, modulus of elasticity and breaking elongation become strong and then they become weak. It has the maximum values when the mass ratio of LA to CS is 2.
Key words: chitosan; L-lactic acid; composite asymmetric membrane
���������Ǿ���(chitosan, CS)�;�����(PLA)��Ϊ2�־����������������Ե�����ҽ�ò����ܵ��˹㷺�Ĺ�ע[1-7]���Ǿ��Ƿ��ӽṹ�к��д����ǻ�����������������������������Ի��ţ������ڼ����Ӽ���ڴ����������ṹ��һЩ������ϸ������ʵ���Ҫ�ɷְ����Ͼ��Ƿdz����ƣ������õ����������ԡ��ɽ����ԡ��̼��ԡ�������ԭ�Ժ�����Դ��Ӧ��������ѧ�ӹ����ܽϲ�[8-9]��������Ҳ��һ�ֳ����ɽ����������ϣ��������õ����������ԺͿɼӹ����ܣ�������������ȱ��[10-15]��
a. ��������е����´�ЧӦ��ʹ����λ�����Բ�������֯������������
b. ��ˮ����ʶ��ͽ����������ϸ��ȱ����Ч��ճ�ϣ�
c. ������ɡ�û�пɷ�Ӧ���ţ��������κ��ԡ�
�������Χ������֧�ܲ��ϲ���Ҫ�������õ���ѧ���ܺ��������ά�༶�ṹ������Ҫ�������õ�ϸ�����ԣ���ֲ��ʱ���յ�ϸ�����ٵ�𤸽���� ��[16-18]����ˣ�������ͿǾ�����Ϊ��Χ������֧�ܲ��϶�������һ���ľ����ԡ�
�ԿǾ�����L-�����֧�����Ʊ��ʺ���Χ�������IJ��Գ�Ĥ֧�ܲ���δ���������ڴˣ����������ÿǾ�����L-�����ڲ����κλ�ѧ��������������ͨ����շ�Ӧ������䶳���﹤�����Ʊ�һ�ֲ��Գ�Ĥ�����ÿǾ��Ƿḻ��������Ի����Լ����������õ���ѧ���ܣ�����һ�־���������ѧ���ܡ�ϸ�����Ժ�������ά�༶�ṹ��������֧�ܲ��ϡ�
1 ʵ ��
1.1 ҩƷ���Լ�������
ҩƷ���Լ����Ǿ���(��������90%����Է�������Ϊ80���ൺҩ���о��� ʳƷ��)��L-���� (88%������������Լ��� AR)��1-ethyl-3- (3-dimethylaminopropyl)carbodiimide(EDAC��Aldrich)������ҩƷ���Լ�����Ϊ��������
����: Nexus����Ҷ�任��������ǣ�JSM-��5610LVɨ�����������STA499C TG-DSC�ۺ��ȷ����ǣ�FD-1-B-80�䶳�������KY8000�����������
1.2 �Ǿ���-L-���Ḵ�ϲ��Գ�Ĥ���Ʊ�
��LA��CS������Ϊ1?1��2?1��3?1��4?1�����ƿǾ���-L-����ˮ��Һ��ˮԡʹ֮��Ĥ����85 �澭��ո����γɽ�֦������ĵ�Ĥ����ȡ���ƺõ���Ӧ�����ĿǾ���-������Һ���������ֱ���붨����ϸ�����ǣ���Ϊ�¿���������ܽ�ֱ�������Ӧ�Ǿ��ǣ���������ĵ�Ĥ�ϣ������䶳��ҹ����85 ������䶳�������ո���ȷ¡��״��ֱ������ȡ24 h������䶳����ÿǾ���-L-���Ḵ�ϲ��Գ�Ĥ����LA��CS ������Ϊ1?1��2?1��3?1��4?1���ø��ϲ��Գ�Ĥ�ֱ��ΪCL-1��CL-2��CL-3��CL-4��
1.3 �ṹ����ò����
��Nexus����Ҷ�任����������Ͻ���ȫ���������ײ���(AFT-FT-IR)����TG-DSC�ۺ��ȷ����ǽ��в��ȷ�������JSM-5610LVɨ������������б�����ò���ԡ�
1.4 ���ܲ���
1.4.1 ������
������õĸ���Ĥ���ɳ�����(0.5 cm��1.5 cm)���������úõ����Ỻ����Һ(pH 7.4��37 ��)�У�����12 h��ȡ������������������������w��
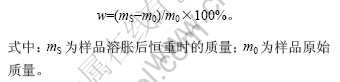
1.4.2 ��ѧ����
����Ʒ�гɳ�Լ6 cm����1 cm����״�������ض�װ���й�ҹ��ʹ����ʪ�Ⱥ㶨���ò��ϲ��Ի��ⶨ����ǿ�ȡ�����ģ���������쳤�ʣ�ȡ5��ƽ��ֵ��
2 ���������
2.1 ��֦����
ͼ1��ʾΪ�Ǿ���-L-�����֦���۷�Ӧ�������ɼ������Ǿ�������L-������Һ��ʱ���Ǿ����а������ӻ����������Ȼ�������Ӧ�γ�������Σ��ٽ��Ǿ��ǵ��ܽ⣬��������Һʱ��L-����ͿǾ����γɵ���λᷢ����ˮ��Ӧ�Ӷ��γ����������۽�ϣ��γɿǾ���������Ľ�֦�����ͬʱ�����Ʊ������У�L-���ᵥ�巢���ۺϷ�Ӧ���γɾ����ͨ���ȷ¡��״�������δ��Ӧ��L-���ᵥ������������С���ӿ���ͨ���ܽ���ɢ����ȥ�������ԣ�����ǰ�����������Է�ӳ��L-���ᵥ����Ǿ��Ƿ�����֦�Ľ�֦�ʡ�����ǰ����������ʧ�ʿ������й�ʽ���㣺
?w=(m0-m)/m0��100%��
ʽ�У�m0Ϊ����ǰ�������������mΪ�����������������
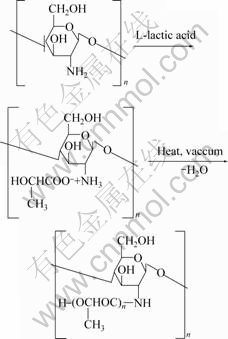
ͼ1 �Ǿ���-L-�����֦���۵ķ�Ӧ����
Fig.1 Scheme of graft copolymerization of chitosan and L-lactic acid
ͼ2��ʾΪL-������Ǿ���Ͷ�ϱ����Բ�ͬ��ȵ�Ĥ(0.07��0.15 mm)������ʧ��Ӱ�졣��ͼ2��֪����LA��CS�����ȵ���3.0ʱ��������ʧ������L-�����������Ӷ����ߣ��������ȴﵽ3.0��������ƽ����˵������ո�������У��Ǿ��Ǻ�L-��������������γɺ�L-���ᵥ��֮����������γ���ͬʱ�����ģ���L-����ļ���������ʱ��δ��Ӧ��L-���ᵥ��;�������Ӧ���ӣ���LA��CS�����ȴ���3.0ʱ����֦�ʲ������ӣ�������ķ�������ʹ��֦�IJ����䳤����������ʧ�ʵ�Ӱ����С�����⣬Ĥ�ĺ�����ӣ�ʹ��֦��Ӧ���ѽ��У���֦��Ҳ�½���������ʧ���ӡ�
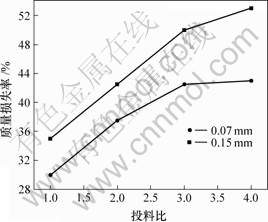
ͼ2 L-������Ǿ���Ͷ�ϱȶ�������ʧ�ʵ�Ӱ��
Fig.2 Influence of ratios of chitosan and L-lactic acid on mass loss
2.2 ȫ���丵��Ҷ���������(ATR-FT-IR)
ͼ3��ʾΪ�Ǿ��ǡ����ἰ�乲�����ȫ��������ף�����CSΪ���Ǿ��ǵĺ���ͼ�ף�PLLAΪ�ۡ�����ĺ���ͼ�ף�CSLA0 Ϊδ����������ĺ���ͼ�ף�CSLA1Ϊ�Ǿ���-L-���Ṳ����ĺ���ͼ�ף�OLLAΪ���������ĺ���ͼ�ס�CSLA0��CSLA1��CS�������Ƶķ��Σ�������������̼����C��C��������C��O������������894 cm-1 �γɵ������壬��1 582 cm-1������������������γ�һ��ǿ���շ壬���Աȴ��Ǿ��ǣ�CSLA1��CSLAO��1 726 cm-1���ҳ���һ���µ����շ壬������L-�����֦�γɵIJ����;�����OLLA�е��Ȼ������������Ų����ģ��������ĺ���ͼ�Աȷ��֣������Ե���Ͳ������������ƣ�����OLLA�е�������Ǿ����а������ǻ�ǿ���������ɵġ�CSLA1��CSLAO��ȣ�����1 726 cm-1�������շ�������������˵���������ᴦ����L-����ĵ����OLLA�Ѿ���ϴ������CSͼ�Աȣ�������������Ժ������ӣ�CSLA1��1 582 cm-1�������շ�������ǿ����Щ��֤���Ǿ��Ǻ�L-��������������˹��۽�ϣ�������������
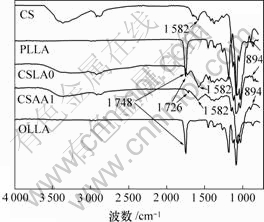
ͼ3 �Ǿ��ǡ����ἰ�乲�����ȫ���������
Fig.3 ATR-FT-IR spectrum of chitosan, L-lactic acid and their copolymer
2.3 ��ʾɨ�����ȷ���(DSC)
��ͼ4��ʾ�����Ǿ�����Ʒ������ˮ������76.648 �����1�����ȷ壬ֱ��300 �棬δ�������ڡ���֦������IJ�����ת���¶�Ϊ192.982 �棬˵���Ǿ�����L-���ᷢ����֦���ۺ��γɵĽ�֧������Ľᾧ�Ƚ��͡�
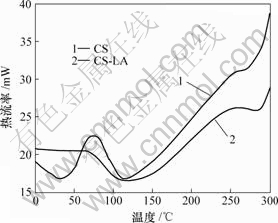
ͼ4 �Ǿ��Ǽ��Ǿ���-L-�������ɨ��ͼ
Fig.4 DSC of CS and CS-LA
2.4 ɨ��羵(SEM)
Ϊ�����������������������ʺ���Ϣ�����������������������������ܵ�������[18-19]��������ϵĿṹ(ȫͨ�ԡ���ͨ�ԡ�����)������λ�Ĺ��ָܻ����Žϴ��Ӱ�졣һ����Ϊ��ͨ��Ϊ��ѡ�����ԭ��ȫͨ�ԵIJ����������������ܰ���֯������άϸ�������гɷ�ͨ�������������Է�Ӧ�;ֲ���ά��֯������������������������������ͨ�Բ����������κ�Ӫ�����ʽ��룬��������������ʽ�����ʹ���������ܻ�����õ���������ͨ�Բ�����˷����������㣬��������ϸ����������С����Ӫ������ͨ��������˲����ɷֽ��룬��ֲ�����������������������ͼ5(a)��ʾΪ�Ǿ���-L-���Ḵ��Ĥ���ϵĺ����ͼ����ͼ��֪���ֲ�����һ�ֲ��ԳƲ��ϣ����зdz����ԵĽṹ�ݶȲ��죬���ڲ���һ�����ܵ��ṹͼ(5(c))�����������һ�����ɵ���������Ķ�ṹ(ͼ5(b))����ԼΪ50 ��m���ҿ����֮�以����ͨ���������¿����Ǻṹ������������Եı仯���γ��˻��ཻ��ᴩ�IJ�״����ṹ�ҿ�(Լ100 ��m)����(ͼ5(d))�����ֲ��Գƽṹ���������ͨ�����ã�ʹ�������������������������ʺ���Ϣ���������һ�����Ч����ֹ�ܰ���֯������άϸ���ij��룬�ܺõ��������ã���һ�ֽ��������Χ������֧�ܲ���[20]��
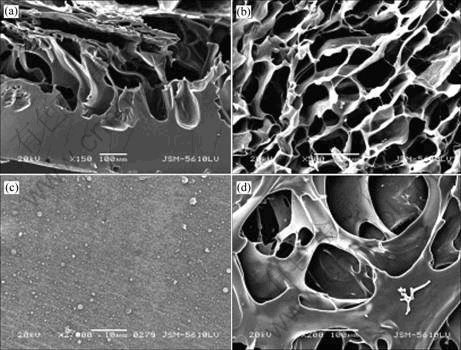
(a) ����棻(b) ��Ĥ��(c) ��Ĥ��(d) 1%������Ĥ
ͼ5 ���ϲ��Գ�Ĥ�ı���ṹ
Fig.5 Surface structures of composite asymmetric membrane
2.5 ���ܲ���
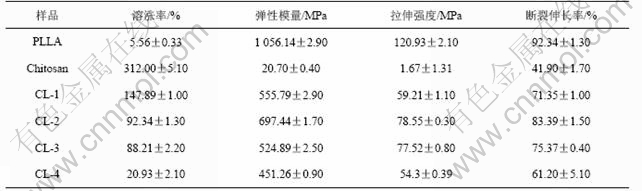
�ɱ�1��֪��������(PLLA)��������Զ���ڿǾ��ǣ�������ǿ�ȡ�����ģ���������쳤�ʾ�Զ�ȿǾ���(chistosan)�ĸߡ��Ǿ��Ǿ���L-�����֦���ۺ������ʼ���ѧ���ܵõ������Ե���ߡ�������ֻ�н�֧ǰ��1/2��1/6����L-������Ǿ�������С��2ʱ�������������ǿ�ȡ�����ģ���������쳤����L-�������������ǿ������������2ʱ�������½��������ȿǾ��ǵĸߡ�
��1 ��ͬ��Ʒ�������ʺ���ѧ����
Table 1 Swelling and mechanical properties of different samples (n=5)
������֧�ܲ���Ҫ����нϸߵ������ʼ��Ϻõ���ѧ���ܡ�������̫�ͣ����ϵı�ˮ�����͵ͣ�������������������̫�ߣ������ڲ��ϵ�ֲ�롣���о����õIJ��Գ�Ĥ�����ʶȵ��������ܣ���������Ч�ر�ˮ����������ֲ�����������õ���ѧ������������ͬ������ʮ����Ҫ�����ã�����Ϊ�����������ṩͨ������Ҫ�ֿ�����ļ�ѹ�����ֹ��Σ��ϸߵĸ��Ժ�ǿ�ȱ�֤����Щ���ܵ�ʵ�֡���֦���۸���Ĥ����ѧ������Ⱦ�����ĵͣ�����������������������Ҫ��
3 �� ��
a. ͨ���Ǿ�����L-����������½�֦���۽������䶳���﹤���Ʊ�һ�ָ��ϲ��Գ�Ĥ��
b. �Ǿ��Ǻ�L-���ᷢ���˹��۽�ϣ��γɽ�֧�������֧������Ϊ����̬���ʣ���Ǿ�����ȣ��߽ᾧ��������ߡ�
c. �Ʊ��ĸ��ϲ��Գ�Ĥ���зdz����ԵĽṹ�ݶȣ����ڲ���һ�����ܵ��ṹ�����������һ�����ɵ���������Ķ�ṹ���ҿ����֮�以����ͨ���ṹ������¿�������ͱ����ɵ���
d. ���ϲ��Գ�Ĥ�������ʺ���ѧ������Ǿ�����Ⱦ��õ����Ե���ߡ�������Ϊ��֦ǰ��1/2��1/6����ѧ������Ǿ�����L-����������ȱ仯���仯������ǿ�ȡ�����ģ���������쳤�ʵ��������������ȵ���2ʱ���������ֵ����һ�ֽ�Ϊ�������Χ������֧�ܲ��ϡ�
�ο����ף�
[1] R��cker M, Laschke M W, Junke D. Angiogenic and inflammatory response to biodegradable scaffolds in dorsal skinfold chambers of mice[J]. Biomaterials, 2006, 27(29): 5027-5038.
[2] Tao J, Abdel-Fattah W I, Laurencin C T. In vitro evaluation of chitosan/poly (lactic acid-glycolic acid) sintered microsphere scaffolds for bone tissue engineering[J]. Biomaterials, 2006, 27(28): 4894-4903.
[3] Duan B, Yuan X Y, Zhu Y. A nanofibrous composite membrane of PLGA-chitosan/PVA prepared by electrospinning[J]. European Polymer Journal, 2006, 42(9): 2013-2022.
[4] Guo T, Zhao J N, Chang J B. Porous chitosan-gelatin scaffold containing plasmid DNA encoding transforming growth factor-��1 for chondrocytes proliferation[J]. Biomaterials, 2006, 27(7): 1095-1103.
[5] Liu X H, Won Y J, Ma P X. Progeny-induced surface modification of nano-fibrous poly (l-lactic acid) scaffolds for tissue engineering[J]. Biomaterials, 2006, 27(21): 3980-3987.
[6] Sarazin P, Roy X, Basil D. Controlled preparation and properties of porous poly (L-lactide) obtained from a co-continuous blend of two biodegradable polymers[J]. Biomaterials, 2004, 25(28): 5965-5978.
[7] Yang F, Murugan R, Ramakrishna S. Fabrication of nano-structured porous PLLA scaffold intended for nerve tissue engineering[J]. Biomaterials, 2004, 25(10): 1891-1900.
[8] Suh J K, Matthew H W. Application of chitosan-based polysaccharide biomaterials in cartilage tissue engineering: A review[J]. Biomaterials, 2000, 21(24): 2589-2598.
[9] Shanmugasundaram N, Ravichandran P, Reddy P N. Collagen-chitosan polymeric scaffolds for the in vitro culture of human epidermoid carcinoma cells[J]. Biomaterials, 2001, 22(14): 1943-1951.
[10] Zhu H G, Ji J, Shen J C. Osteoblast growth promotion by protein electrostatic self-assembly on biodegradable poly (lactide)[J]. J Biomater Sci Polymer Edn, 2005, 16(6): 761-774.
[11] Fu J H, Jian Ji, Yuan W Y, et al. Construction of anti-adhesive and antibacterial multilayer films via layer-by-layer assembly of heparin and chitosan[J]. Biomaterials, 2005, 26: 6684-6692.
[12] Zhu Y B, Zhang C Y, Liu Y X, et al. LBL self-assembly of chondroitin sulfate and collagen onto poly (L-lactic acid)for improving its cytocompatibility with endothelial cells[J]. Chem J Chinese University, 2004(25): 1347-1350.
[13] Zhu H G, Ji J, Shen J C. Surface engineering of poly (DL-lactic acid) by entrapment of biomacromolecules[J]. Macromol Rapid Commun, 2003(23): 819-823.
[14] Agrawal C M, Athannasion K A. Technique to control pH in vicinity of biodegrading PLA-PGA implants[J]. J Apple Biomater, 1997, 38(2): 105-114.
[15] Suganuma J, Alexander H. Biological response of intramedullary bone to poly L-lactic acid[J]. J Appl Biomater, 1993, 4(1): 13-27.
[16] Chen P R, Chen M H, Lin F H, et al. Release characteristics and bioactivity of gelatin-tricalcium phosphate membranes covalently immobilized with nerve growth factors[J]. Biomaterials, 2005, 26(33): 6579-6587.
[17] ������, ������, �Ƽ̷�, ��. ������/���������ӻ��͵�������Χ��ȱ��ʵ���о�[J]. �й��ٴ�����ѧ��־, 2003, 21(5): 482-485.
DONG Hong-ruang, XU Yong-nian, HUANG Ji-feng, et al. Experimental study of bridging peripheral nerve defect with biodegradable PDLLA/NGF controlled release conduit[J]. Chinese Journal of Clinical Anatomy, 2003, 21(5): 482-485.
[18] Wan Y, Wen D J. Preparation and characterization of porous conducting poly (dl-lactide) composite membranes[J]. Journal of Membrane Science, 2005, 246(2): 193-201.
[19] ������, �ΰ, ������, ��. ��d, l-���ἰ���20����ȱ���յ������о�[J]. ����ͨѶ, 2000, 8: 15-18.
WANG Sheng-guo, HOU Jian-wei, BEI Jian-zhong, et al. Study on 20 mm of nerve gap recovered bypoly-d, l-lactide guide[J]. High Technology Communication, 2000, 8: 15-18.
[20] �����, ������, �� ������. ��ͬͨ�ԿǾ�������Ĥ���ϵ�������Χ��ȱ���ʵ���о�[J]. �Ϻ�ҽѧ, 2000, 23(7): 390-392.
LI Qing-feng, XU Jing-hong, LUO Min, et al. Experimental study on peripheral nerve regeneration through composite biomembrane-chitosan conduits with different permeabilities[J]. Shanghai Medicine, 2000, 23(7): 390-392.
�ո����ڣ�2007-01-29
������Ŀ�������ص�����о���չ�ƻ�������Ŀ(2005CB623905)
����飺�캣��(1973-)���У����������ˣ���ʦ����ʿ�о�������������ҽ�á�ҩ�ò����о�
ͨѶ���ߣ��������ڣ���ʿ����ʦ���绰��027-87651853(O); E-mail: yanyuhua8@126.com