Zn(Ⅱ)-(NH4)2SO4-H2O体系浸出锌烟尘
唐谟堂,张 鹏,何 静,原 霞,陈永明
(中南大学 冶金科学与工程学院,湖南 长沙,410083)
摘 要:提出硫酸铵浸出法处理锌烟尘的新工艺。该工艺利用不同温度下锌在硫酸铵溶液中的溶解度的差别,先在高温下将锌浸入溶液然后降温冷却,使锌呈含F和Cl很低的复盐析出,然后回收。以株冶集团锌烟尘为试料,对浸出过程进行研究。研究结果表明:浸出温度和硫酸铵浓度显著影响锌的浸出率;最佳浸出条件是:液固比为16?1,硫酸铵浓度为4.0 mol/L,pH值为5.5,浸出温度为90 ℃,浸出时间为4 h,在该条件下,按渣含锌计算的浸出率达到85.16%。
关键词:锌烟尘; 硫酸铵; 浸出; 湿法炼锌
中图分类号:TF813 文献标识码:A 文章编号:1672-7207(2007)05-0867-06
Leaching zinc dust in system of Zn(Ⅱ)-(NH4)2SO4-H2O
TANG Mo-tang, ZHANG Peng, HE Jing, YUAN Xia, CHEN Yong-ming
(School of Metallurgical Science and Engineering, Central South University, Changsha 410083, China)
Abstract: A new ammonium sulfate leaching process for extracting zinc from fuming furnace dust was proposed. Using fuming furnace dust from Zhuzhou Smelter Group Co. Ltd. as raw material, zinc leaching by an ammonium sulfate solution was investigated. The experimental results show that the temperature and ammonium sulfate concentration have remarkable influence on the leaching rate of zinc. The optimum conditions obtained are as follows: the ratio of liquid to solid of 16?1, concentration of ammonium sulfate of 4.0 mol/L, pH value of 5.5, leaching temperature of 90 ℃ and leaching time of 4 h. Under the optimum conditions, the leaching rate of zinc, calculated based on the zinc content in leached residue, can reach 85.16%.
Key words: zinc dust; ammonium sulfate; leaching; hydrometallurgy of zinc
传统湿法炼锌[1-2]都采用ZnSO4-H2SO4-H2O体系,从氧化锌或锌焙砂中浸出锌,经沉铁除杂净化后再电积,而氟、氯对电积过程危害很大。对于含氟、氯较高的锌物料需经水溶液洗涤或多膛炉挥发脱氯处理后[3-5]方可进入主体流程,设备投资和生产成本大为增加。而氟、氯含量太高的锌物料不能用于生产电锌,只能作生产锌的化工产品的原料。在此,本文作者提出了硫酸铵溶液浸出[6-9]-复盐结晶法处理高氟、氯锌烟尘的新工艺。该工艺利用不同温度下锌在硫酸铵溶液中溶解度差别大的特点,先在高温下将锌浸入溶液然后冷却结晶,使锌以氟、氯含量很低的复盐析出,然后回收,将母液除去氟、氯后返回浸出过程。因此,本工艺闭路循环,属清洁生产工艺,对开发利用各类复杂的锌资源,实现锌业的可持续发展具有重要意义,同时,对改造传统湿法炼锌工艺也具有潜在优势。
1 理论基础
1.1 浸出过程热力学原理
烟尘中的Zn主要以ZnO形式存在。在硫酸铵浸出过程[10-12]中,烟尘中的锌将以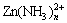 的形式进入浸出液,其反应方程式为:
的形式进入浸出液,其反应方程式为:
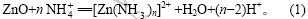
常温(25 ℃)下,硫酸铵浓度对锌平衡浓度的影响如图1[12]所示。
由图1可知,在氨浓度一定的条件下,锌平衡浓度开始随氨浓度的增加而急剧上升;继续增加氨的浓度,锌平衡浓度的增加开始变缓。图1中的曲线1表示氨浓度为0 mol/L时,纯硫酸铵溶液中锌浓度随硫酸铵浓度变化而变化的情况。可以看出,在硫酸铵浓度≥4 mol/L时,锌的平衡浓度≥50 g/L。这是在常温(25 ℃)下的情况。若提高温度,锌浓度将会更高,这就是硫酸铵浓溶液从氧化锌类物料中浸出锌的理论依据。
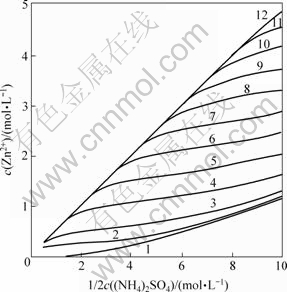
c(NH3)/(mol・L-1): 1―0; 2―0.5; 3―1.0; 4―2.0; 5―3.0; 6―4.0; 7―5.0; 8―6.0; 9―7.0; 10―8.0; 11―9.0; 12―10.0
图1 硫酸铵浓度对锌平衡浓度的影响
Fig.1 Influence of ammonium sulfate concentration on zinc equilibrium concentration
溶液中的Pb将形成PbSO4沉淀进入浸出渣:
Pb2++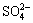 =PbSO4↓。 (2)
=PbSO4↓。 (2)
而As,Sb和In不溶于硫酸铵溶液,也进入浸出渣,从而使主元素Zn与其他杂质元素分离,烟尘中的F和Cl等阴离子随主元素Zn进入浸出液,将在浸出液冷却结晶的过程中分离除去,析出的锌复盐再经过酸化溶解,净化电积等过程得到产品电锌[13-15]。
1.2 浸出过程机理
浸出过程是由含锌物料与溶液所组成的多相反 应[16-19]。本研究体系中,浸出过程机理和步骤可以分解为以下3个步骤(见图2):
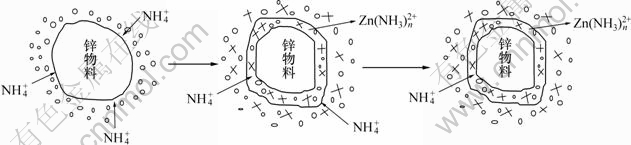
图2 浸出过程机理示意图
Fig.2 Sketch map of leaching mechanism
a. 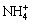 由本体向反应面扩散;
由本体向反应面扩散;
b. 在二者接触的表面上,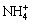 与固体进行化学反应,生成
与固体进行化学反应,生成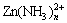 ,并在固体表面形成一层扩
,并在固体表面形成一层扩 散层;
c. 生成的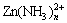 向溶液中扩散。
向溶液中扩散。
2 原料及实验方法
2.1 实验原料
本实验采用的原料为株洲冶炼厂多膛炉电收尘烟尘,烟尘中F,As和Sb含量较高,锌主要呈ZnO形态存在,其主要化学组成见表1。
表1 锌烟尘主要化学组成
Table 1 Chemical composition of zinc dust w/%

2.2 实验及分析方法
浸出实验分单因素条件实验和综合条件实验二部分进行。单因素条件实验规模为锌烟尘30 g/次,考察的因素有时间、温度、硫酸铵溶液浓度及pH值;在最佳单因素条件下进行综合条件试验。
实验步骤为:将配置好的一定浓度的(NH4)2SO4溶液480 mL装入平底烧瓶,在恒温磁力搅拌器上加热搅拌至指定温度后,将30 g锌烟尘缓缓加入其中,并开始计时,至规定时间,浆料抽滤,滤渣烘干称重,然后,用EDTA容量法测定滤液和滤渣中的Zn含量。
3 实验结果及讨论
3.1 条件实验
3.1.1 浸出时间对锌浸出率的影响
在温度为80 ℃,硫酸铵浓度为3 mol/L,液固比为16?1及pH=5.5时,考察时间对锌浸出率的影响,结果如图3所示。
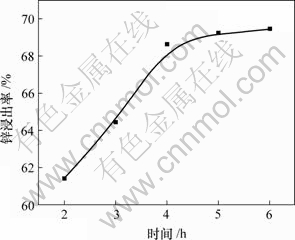
图3 浸出时间对锌浸出率的影响
Fig.3 Influence of leaching time on leaching rate of zinc
由图3可以看出,随着浸出时间的延长,锌浸出率不断增大,且在4 h后趋于平稳,故选择4 h作为最佳浸出时间。同时,由于锌浸出率还不足70%,因此,在以后的实验中将提高硫酸铵浓度进行实验。
3.1.2 浸出温度对锌浸出率的影响
在时间为4 h,硫酸铵浓度为3.5 mol/L,液固比为16?1及pH=5.5时,考察温度对锌浸出率的影响,结果如图4所示。
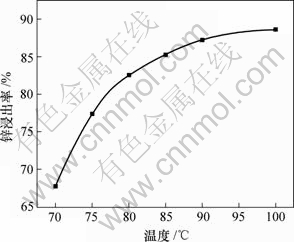
图4 浸出温度对锌浸出率的影响
Fig.4 Influence of leaching temperature on leaching rate of zinc
由图4可以看出,随着温度的升高,锌浸出率不断增大,当温度大于90 ℃ 后趋于平缓,同时,考虑到当温度高于90 ℃以后,水的蒸发加剧,会给实验带来一定误差。因此,选取90 ℃作为最佳浸出温度。
3.1.3 硫酸铵浓度对锌浸出率的影响
在时间为4 h,温度为90 ℃,液固比为16?1及pH=5.5时,考察硫酸铵溶液浓度对锌浸出率的影响,结果如图5所示。
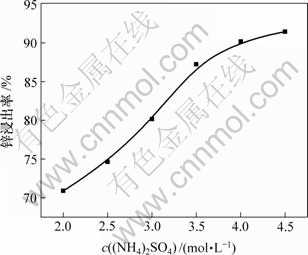
图5 硫酸铵溶液浓度对锌浸出率的影响
Fig.5 Influence of ammonium sulfate concentration on leaching rate of zinc
由图5可以看出,随着硫酸铵溶液浓度的增加,锌浸出率逐渐增大,当硫酸铵溶液浓度达到4.0 mol/L时,锌浸出率为90.18%,继续提高硫酸铵溶液浓度势必造成硫酸铵用量的增加,故选取硫酸铵溶液浓度 4.0 mol/L作为最佳条件。
3.1.4 硫酸铵溶液pH值的影响
在时间为4 h,温度为90 ℃,硫酸铵浓度为 4 mol/L,液固比为16?1时,考察pH值对锌浸出率的影响,结果如图6所示。
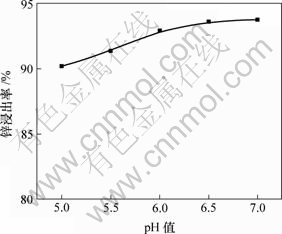
图6 硫酸铵溶液pH值对锌浸出率的影响
Fig.6 Influence of pH value of ammonium sulfate on leaching rate of zinc
由图6可以看出,随着pH值的增大,锌浸出率略有提高,考虑到增大溶液pH值将增加氨水的消耗量,同时在后续工艺中得出锌复盐的最佳冷却析出pH值应小于2.0,因此,选取pH=5.5作为最佳 条件。
3.2 综合条件实验
在最佳条件下,进行3次综合条件实验,锌的液计浸出率分别为89.95%,89.29%和89.31%,平均值为89.52%;渣计浸出率分别为85.21%,84.96%和85.31%,平均值为85.16%,浸出过程中锌的平衡见表2。
表 2 锌烟尘浸出过程中锌的平衡
Table 2 Balance of zinc in leaching process of zinc dust
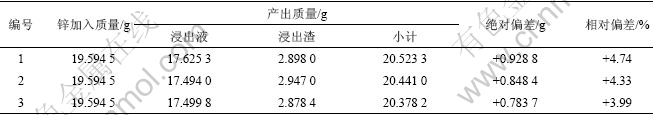
由表2可以看出,锌的平衡情况较好,平衡率可达到95.65%,而产生正偏差的原因是溶液分析锌含量 偏高。
在最佳条件下进行了200 g/次的扩大试验,试验结果良好,并对其中的杂质元素去向进行分析,其结果见表3。
表 3 锌烟尘浸出过程中杂质元素的平衡
Table 3 Balance of impurity elements in leaching process of zinc dust
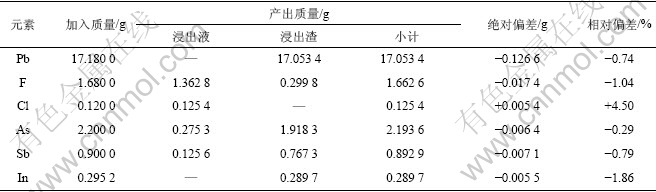
由表3可以看出,在浸出过程中杂质元素Pb,As,Sb和In主要进入浸出渣中,从而很好地与主元素Zn分离,F和Cl进入浸出液,将在后续工序中除去,各杂质元素平衡情况良好,但Cl的正偏差较大,其主要原因是在浸出过程中采用了自来水,从而使溶液中Cl含量分析结果偏高。
上述实验得到的浸出液在沉复盐过程中采取的工艺条件是:温度为25 ℃,溶液pH值≤2.0,机械搅拌1 h。沉复盐过程中主元素Zn及杂质元素F和Cl的平衡情况如表4所示。
表4 沉复盐过程中Zn, F和Cl的平衡
Table 4 Balance of Zn, F and Cl in double salt precipitation process
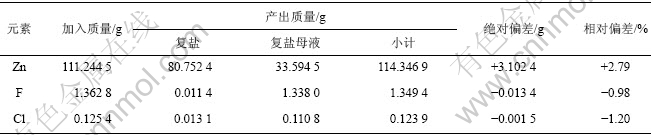
由表4可以看出,在沉复盐过程中达到了很好地去除F和Cl的效果,其中金属Zn的复盐析出率可达72.59%。
4 结 论
a. 硫酸铵溶液浸出法处理复杂的含锌烟尘,是由F和Cl含量高的锌烟尘制以电锌的一种有效的新 途径。
b. 研究了复杂的含锌烟尘硫酸铵浸出工艺,确定了最佳浸出条件:浸出温度为90 ℃,浸出时间为4 h,硫酸铵浓度为4.0 mol/L,硫酸铵溶液pH值为5.5。在最佳条件下,锌的渣计浸出率可达到85.16%,锌金属平衡率为95.65%。
参考文献:
[1] 梅光贵, 王得顺, 周敬元, 等. 湿法炼锌学[M]. 长沙: 中南大学出版社, 2001: 93-189.
MEI Guang-gui, WANG De-shun, ZHOU Jing-yuan, et al. Hydrometallurgy of zinc[M]. Changsha: Central South University Press, 2001: 93-189.
[2] 彭容秋. 有色金属提取冶金手册(锌镉铅铋卷)[M]. 北京: 冶金工业出版社, 1992: 119-130.
PENG Rong-qiu. A handbook for extractive metallurgy of nonferrous metals (Vol. Zn, Cd, Pb, Bi)[M]. Beijing: Metallurgical Industry Press, 1992: 119-130.
[3] 付一鸣, 顾立民, 王德全. 铅烟化炉氧化锌烟尘选择性氯化焙烧脱氟、氯的研究[J]. 有色矿冶, 1998(3): 22-25.
FU Yi-ming, GU Li-min, WANG De-quan. Studies on selectivity chlorination roasting the lead fuming furnace zinc oxide dust to remove fluorin and chlorin[J]. Nonferrous Mine Smelting, 1998(3): 22-25.
[4] 张元福, 陈家蓉, 黄光裕, 等. 针铁矿法从氧化锌烟尘浸出液中除氟氯的研究[J]. 湿法冶金, 1999(2): 36-40.
ZHANG Yuan-Fu, CHEN Jia-rong, HUANG Guang-yu, et al. Studies on removing fluorin and chlorin from zinc oxide dust lixivium by goethite method[J]. Hydrometallurgy of China, 1992(2): 36-40.
[5] 赵廷凯, 唐谟堂. 湿法炼锌净化钴渣新处理工艺[J]. 中南工业大学学报: 自然科学版, 2001, 32(4): 371-375.
ZHAO Ting-kai, TANG Mo-tang. A new process for treating cobalt residue in the purifying process of hydrometallurgy of zinc[J]. Journal of Central South University of Technology: Natural Science, 2001, 32(4): 371-375.
[6] 唐谟堂, 欧阳民. 硫铵法制取等级氧化锌[J]. 中国有色金属学报, 1998, 8(1): 118-121.
TANG Mo-tang, OUYANG Min. Using ammonium sulfate and ammonia-complex leaching process to produce zinc oxide of the grade[J]. The Chinese Journal of Nonferrous Metals, 1998, 8(1): 118-121.
[7] 杨声海, 唐谟堂, 邓昌雄, 等. 由氧化锌烟灰氨法制取高纯锌[J]. 中国有色金属学报, 2001, 11(6): 1110-1113.
YANG Sheng-hai, TANG Mo-tang, DENG Chang-xiong, et al. Making high-purity zinc from zinc oxide fume dusts[J]. The Chinese Journal of Nonferrous Metals, 2001, 11(6): 1110-1113.
[8] 杨声海. Zn(Ⅱ)-NH3-NH4Cl-H2O体系制备高纯锌理论及应用[D]. 长沙: 中南大学冶金科学与工程学院, 2003.
YANG Sheng-hai. Theory and application studies on preparing high purity zinc in the system of Zn(Ⅱ)-NH3-NH4Cl-H2O[D]. Changsha: School of Metallurgical Science and Engineering, Central South University, 2003.
[9] 张保平, 唐谟堂. NH4Cl-NH3-H2O体系浸出氧化锌矿[J]. 中南工业大学学报: 自然科学版, 2001, 32(5): 483-486.
ZHANG Bao-ping, TANG Mo-tang. Leaching zinc oxide ores in the system of NH4Cl-NH3-H2O[J]. Journal of Central South University of Technology: Natural Science, 2001, 32(5): 483-486.
[10] 石西昌, 赵瑞荣, 蒋汉瀛. Zn2+-Cl--NH3-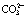 -H2O系的热力学分析[J]. 中南工业大学学报: 自然科学版, 1997, 29(2): 193-196.
-H2O系的热力学分析[J]. 中南工业大学学报: 自然科学版, 1997, 29(2): 193-196.
SHI Xi-chang, ZHAO Rui-rong, JIANG Han-ying. Thermo dynamic analysis on system of Zn-Cl--NH3-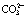 -H2O[J]. Journal of Central South University of Technology: Natural Science, 1997, 29(2): 193-196.
-H2O[J]. Journal of Central South University of Technology: Natural Science, 1997, 29(2): 193-196.
[11] 慕思国, 彭长宏, 黄 虹, 等. 298 K时三元体系MeSO4-(NH4)2SO4-H2O的相平衡[J]. 过程工程学报, 2006, 6(1): 32-36.
MU Si-guo, PENG Chang-hong, HUANG Hong, et al. Equilibrium solubility in ternary system of MeSO4-(NH4)2SO4- H2O at 298 K[J]. The Chinese Journal of Process Engineering, 2006, 6(1): 32-36.
[12] 唐谟堂, 鲁君乐, 袁延胜, 等. Zn(Ⅱ)-NH3-(NH4)2SO4-H2O系的氨络合平衡[J]. 中南矿冶学院学报, 1994, 25(6): 701-705.
TANG Mo-tang, LU Jun-le, YUAN Yan-sheng, et al. On the ammoniation-complex equilibrium in the system of Zn(Ⅱ)-NH3-(NH4)2SO4-H2O[J]. Journal of Central South Institute of Mine and Metallurgy, 1994, 25(6): 701-705.
[13] 唐谟堂, 杨声海. Zn(Ⅱ)-NH3-NH4Cl-H2O体系电积锌工艺及阳极反应机理[J]. 中南工业大学学报: 自然科学版, 1999, 30(2): 153-156.
TANG Mo-tang, YANG Sheng-hai. Electrowinning zinc in the system of Zn(Ⅱ)-NH3-NH4Cl-H2O and mechanism of anodic reaction[J]. Journal of Central South University of Technology: Natural Science, 1999, 30(2): 153-156.
[14] 赵廷凯, 唐谟堂, 梁 晶. 制取活性锌粉的Zn(Ⅱ)-NH3?H2O- (NH4)2SO4体系电解法[J]. 中国有色金属学报, 2003, 13(3): 774-777.
ZHAO Ting-kai, TANG Mo-tang, Liang Jing. Preparation of active zinc powder by electrowinning in system of Zn(Ⅱ)- NH3?H2O-(NH4)2SO4[J]. The Chinese Journal of Nonferrous Metals, 2003, 13(3): 774-777.
[15] Kim M S, Lee J C, Kim B S, et al. Electrochemical recovery of zinc from NH4Cl leaching solution of ZnO[C]//Park J T. REWAS’04-Global Symposium on Recycling, Waste Treatment and Clean Technology-Proceedings. Warrendale: Minerals, Metals and Materials Society, 2005: 1893-1899.
[16] 刘晓丹, 张元福. 铵盐浸出氧化锌矿动力学的研究[J]. 贵州工业大学学报: 自然科学版, 2004, 33(2): 82-85.
LIU Xiao-dan, ZHANG Yuan-fu. Study on kinetics of ammonium salt leaching on znicite[J]. Journal of Guizhou University of Technology: Natural Science, 2004, 33(2): 82-85.
[17] Kazinczy B, Kotai L, Gacs I, et al. Study on ammoniacal leaching of zinc from sludges containing iron and zinc hydroxides[J]. Hungarian Journal of Industrial Chemistry, 2000, 28(3): 207-210.
[18] Harvey T G. The hydrometallurgical extraction of zinc by ammonium carbonate: A review of the Schnabel Process[J]. Mineral Processing and Extractive Metallurgy Review, 2006, 27(4): 231-279.
[19] MENG Xing-hui, Han K N. Principles and applications of ammonia leaching of metals: A review[J]. Mineral Processing and Extractive Metallurgy Review, 1996, 16(1): 23-61.
收稿日期:2006-12-11;修回日期:2007-01-26
基金项目:国家“863”计划资助项目(2004AA649080);国家自然科学基金资助项目(50674104)
作者简介:唐谟堂(1942-),男,湖南武冈人,教授,从事有色重金属冶金工艺研究
通信作者:唐谟堂,男,教授;电话:0731-8830470;E-mail: mttang@mail.csu.edu.cn