
DOI: 10.11817/j.issn.1672-7207.2021.04.004
熔盐电脱氧含钛废渣制备金属钛
盖家萱1, 2,陈朝轶1, 2,李军旗1, 2,王林珠1, 2,申园园1, 2
(1. 贵州大学 材料与冶金学院,贵州 贵阳,550025;
2. 贵州省冶金工程与过程节能重点实验室,贵州 贵阳,550025)
摘要:在CaCl2熔盐电解质中,以含钛废渣为阴极,碳棒为阳极,采用熔盐电脱氧法制备金属钛。结合循环伏安法与SEM-EDS、XRD等分析手段,考查电解时间、槽电压对电脱氧效果的影响,并分析杂质行为。研究结果表明:延长电解时间,产物氧含量明显降低;电解初期,脱氧反应较为剧烈,电流急剧下降;电解3.5 h时开始析出金属Ti,6 h后产物颗粒粒度明显增大;电解12 h时,金属Ti质量分数达到94.23%,产物为金属Ti和微量TiO;当槽电压低于2.0 V时,电流较小,电脱氧效果不明显,产物主要为CaTiO3和钛的低价氧化物;当槽电压升至2.8 V时,电流明显增加,电解4 h时开始析出金属Ti,电解15 h时,产物呈海绵形态,Ti质量分数达到97.79%,O质量分数降至0.71%,残留微量的Fe,Al和Si等杂质;电脱氧历程为:CaTiO3→Ti2O3→TiO→Ti,部分杂质进入熔盐和生成氯化物挥发。
关键词:含钛废渣;电脱氧法;脱氧历程;金属钛;杂质
中图分类号:TF823 文献标志码:A
文章编号:1672-7207(2021)04-1076-07
Preparation metal titanium from molten salt electrodeoxidized titanium-containing waste residue
GAI Jiaxuan1, 2, CHEN Chaoyi1, 2, LI Junqi1, 2, WANG Linzhu1, 2, SHEN Yuanyuan1, 2
(1. School of Materials and Metallurgy, Guizhou University, Guiyang 550025, China;
2. Guizhou Province Key Laboratory of Metallurgical Engineering and Process Energy Saving, Guiyang 550025, China)
Abstract: Titanium was prepared using electro-deoxidation method in CaCl2 molten salt electrolytes. Titanium-containing waste residue acted as the cathode, while carbon rod as the anode. The effect of duration of electrolysis and bath voltage on the electro-deoxidation was investigated, and behavior of impurity was analyzed by cyclic voltammetry method, SEM-EDS and XRD detections. The results show that the oxygen content is decreased significantly with the increase of the duration of electrolysis time. In the early stage of electrolyis, the deoxidation reaction is enhanced and the current decreases sharply. Ti precipitated after electrolyzing for 3.5 h and the particle size increase after electrolyzing for 6 h. The electrolysate is composed of Ti and TiO in which Ti mass fraction reaches 94.23% after electrolyzing for 12 h. The electric current is 2.0 V, electro-deoxidation is bad and the electrolysate is mainly CaTiO3 and low valence titanium oxide at low bath voltage. When the bath voltage is 2.8 V, the current significantly increases, and the metal Ti is precipitated after electrolyzing for 4 h. The electrolysate is sponge shaped with trace of Fe, Al and Si, in which Ti mass fraction reaches 97.79% and the O mass fraction decreases to 0.71% after electrolyzing for 15 h. The electrodeoxidation process is as follows: CaTiO3→Ti2O3→TiO→Ti. Some impurities enter into the molten salt and chloride volatilization is generated.
Key words: slag containing titanium; electro-deoxidization; deoxidization process; titanium; impurity
钛具有比强度高、密度小、耐热性及耐腐蚀性强的特点,应用广泛[1-2]。工业上采用Kroll法生产海绵钛,需经过氯化与镁热还原等过程[3],工艺复杂,生产周期长,导致金属钛的价格高昂。TiCl4制备过程中会产生大量的含钛废渣[4],由于颗粒粒度小,返回冶炼炉熔炼易于产生堵塞,其添加量不能超过15%,使得回收利用率较低,这些含钛废渣中钛含量较高,具有回收价值,若直接堆弃,则会造成资源浪费,并环境污染[5-6]。因此,寻求绿色环保、高效回收利用新途径显得尤为重要。
陈林等[7]等采用酸法处理含钛烟尘,将TiO2质量分数从38.3%提高到58.5%,起到一定的富集效果;赵海涛[8]对TiCl4生产过程中产生的各种废渣提出了处理方案,但未能提供具体实验结果,回收效果有待验证。WANG等[9]采用电解脱氧工艺,以不同质量比例的TiO2和GeO2混合物为前驱体,在电压为3.0 V、温度为800 °C的电解条件下,制备Ti-Ge(TixGey)金属间化合物。刘美凤等[10]提出CaCl2熔盐中TiO2电极直接电解还原过程中,首先被还原成钛的低价氧化物,再还原生成金属钛,由高价到低价再到金属逐渐进行。WENG等[11]以NaCl-KCl-TiClx为电解质,以海绵钛为原料进行熔盐电解提纯制取高纯钛粉。由于熔盐电脱氧法(FFC法)具有流程短、操作简便等优点,近年来研究广泛,学者们选择以纯的金属氧化物以及一些复合矿与高炉渣[12]为原料,利用熔盐电脱氧法制备金属钛[13]、钛合金及电解其他稀有难熔金属与合金[14]等呈现出较好的效果。
本文作者以某钛厂氯化过程产生的含钛废渣为原料,采用FFC法对其进行电还原制备金属钛,重点考察电解时间和槽电压对电解效果的影响,并利用SEM-EDS,XRD以及循环伏安法分析产物元素分布与杂质的电还原行为。
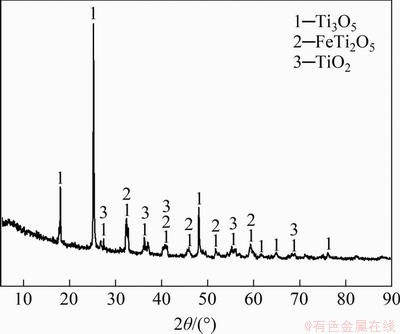
图1 含钛废渣的XRD谱
Fig. 1 XRD pattern of titanium slag
1 实验
1.1 实验原料
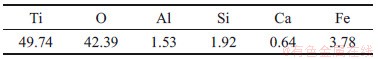
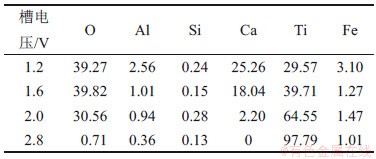
实验采用的含钛废渣取自贵州某钛厂,主要元素质量分数见表1。从表1可知:Ti质量分数为49.74%,杂质主要为Al,Si,Ca和Fe等。其XRD谱如图1所示,杂质与钛以类质同晶形态存在。
表1 含钛废渣的元素质量分数
Table 1 Element mass fraction of titanium containing slag %
1.2 实验方法
采用液体石蜡为黏结剂,将含钛废渣压制成片,经XD-1200N马弗炉在1 050 ℃烧结后制成阴极,碳棒作为阳极,铁铬铝丝为电极引线,以CaCl2熔盐作为电解质,在氩气保护下进行电脱氧。电解结束后,持续氩气保护降至室温,取出电解产物,用蒸馏水和体积分数为1%的稀盐酸对其进行冲洗,干燥后待检测。利用德国XEPOSX荧光分析仪对含钛废渣进行元素分析,烘干后对阴极产物进行XRD分析(岛津XRD-7000,Cu Kα靶,扫描速率为10 (°)/min,2θ为10°~85°),利用SEM-EDS (JSM-6700F)分析其阴极表面形貌以及元素分布。利用High Score plus(荷兰飞利浦)对含钛废渣样品进行XRD图谱分析。
2 结果与讨论
2.1 电解时间对电脱氧效果的影响
在温度为900 ℃,槽电压为3.1 V,电解时间为0.5,1,6,9和12 h条件下,阴极产物的SEM形貌如图2所示,对应的元素分布如表2所示。由图2和表2可知:随着电解时间延长,阴极产物中Ti质量分数明显增加,O质量分数明显降低;当电解时间为0.5 h和1 h时,颗粒粒度较小;当电解时间达到6 h时,阴极颗粒粒度明显增大,呈海绵形态;继续延长电解时间,颗粒粒度增加不明显,但产生烧结作用,出现聚集现象,孔隙率增大,金属化率提高。

图2 不同电解时间的阴极产物SEM形貌
Fig. 2 SEM morphologies of cathode products for different electrolysis time
表2 不同电解时间的阴极产物元素质量分数
Table 2 Element mass fraction of cathode products at different electrolysis time %
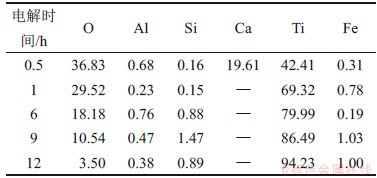
在上述电脱氧条件下阴极产物的XRD谱如图3所示。由图3和表2可知:当电解时间为0.5 h时,产物主要为CaTiO3和Ti2O3,这与表2中Ca质量分数较高的结果相吻合,说明经CaCl2熔盐浸泡及电解初期主要生成CaTiO3;随着电解时间延长,CaTiO3被电解为Ti的低价氧化物;电解1 h后,CaTiO3的衍射峰消失,经EDS分析Ca质量分数为0;当电解时间超过6 h时,出现金属Ti的衍射峰,且衍射峰的强度随时间延长而增加;当电解时间达到12 h时,产物主要为金属Ti和微量TiO,其中金属Ti质量分数为94.23%,O质量分数降至3.50%。
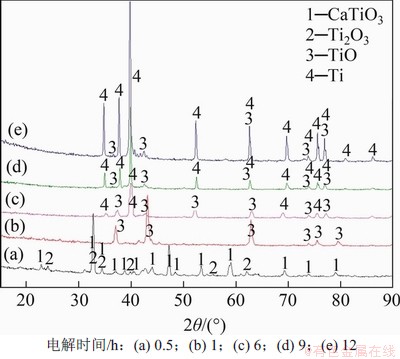
图3 不同电解时间的阴极产物XRD谱
Fig. 3 XRD patterns of cathode products for different electrolysis time
电解电流-时间曲线如图4所示。由图4可知:电解1 h以内,电流急剧下降,产物由CaTiO3向Ti2O3转变;电解1.5 h后,电流趋于平缓,产物以Ti的低价氧化物为主;电解3.5 h后,电流略为增加,经分析认为,金属Ti开始析出,增加了导电性;当电解时间达到9 h后,产物以金属Ti为主;电解后期,电流出现增大趋势,这是由于碳棒阳极发生了粉化现象,碳粉浮在电解质表面,产生了部分电子导电作用。结合图4与XRD分析结果,获得电脱氧历程为:CaTiO3→Ti2O3→TiO→Ti。
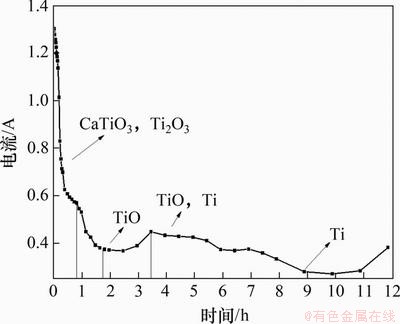
图4 电流-时间曲线
Fig. 4 Curve of current with time
电解过程中发生的主要反应方程为:
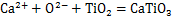 (1)
(1)
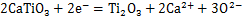 (2)
(2)
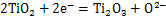 (3)
(3)
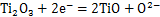 (4)
(4)
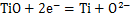 (5)
(5)
2.2 槽电压对电脱氧的影响
在温度为900 ℃时阴极的循环伏安曲线如图5所示。由图5可知:在槽电压低于1.5 V时,未出现还原峰,说明阴极未发生电脱氧反应;当槽电压高于1.5 V时,开始出现还原峰,但不明显,这是导致电还原速率慢、电流低的原因。实际开始发生还原的槽电压应该高于1.5 V。
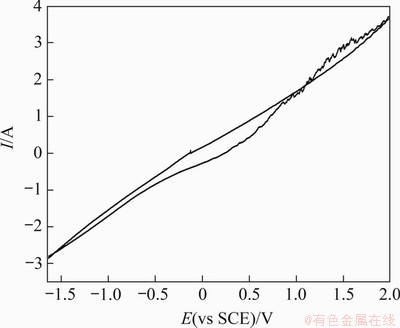
图5 阴极的循环伏安曲线图
Fig. 5 Cyclic voltampere of cathode
在温度为900 ℃,电解时间为15 h,槽电压分别为1.2,1.6,2.0和2.8 V条件下的阴极产物SEM形貌如图6所示,对应的元素分析如表3所示。由表3可知:当槽电压低于1.6 V时,Ca和O质量分数高,还原程度低;随槽电压升高至2.0 V,颗粒粒径开始增加,Ti质量分数明显增加,而Ca质量分数明显降低,但O质量分数较高,电还原程度仍然不明显;当槽电压升高至2.8 V时,颗粒的粒径明显增大,呈典型海绵形态,金属Ti质量分数达到97.79%,Ca质量分数为0,O质量分数降至0.71%,还原程度较为彻底,其他杂质元素含量也大幅降低。
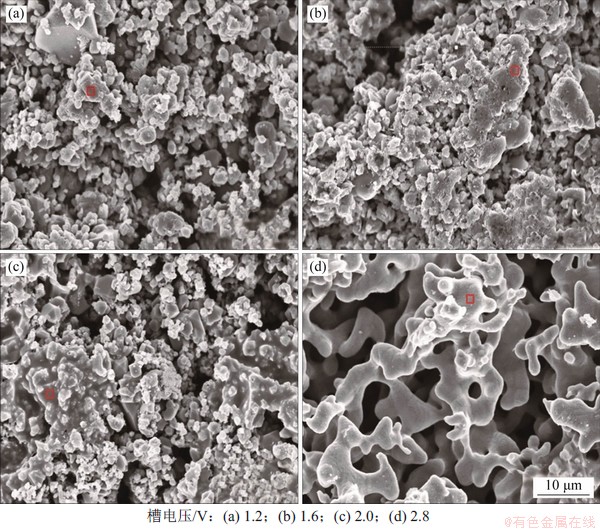
图6 不同槽电压的阴极产物微观形貌
Fig. 6 SEM morphology of cathodes at different voltages electrolysis
表3 不同槽电压的阴极产物元素质量分数
Table 3 Element mass fraction of cathode products at different cell voltages %
在上述电脱氧条件下阴极产物的XRD谱如图7所示。从图7可知:当槽电压为1.2 V时,该电压未达到CaTiO3的分解电压,阴极产物主要为CaTiO3;当槽电压升高至1.6 V时,部分CaTiO3发生分解生成钛的氧化物,Ca质量分数降低;当槽电压升高至2.0 V时,Ca质量分数明显降低,仅为2.20%,CaTiO3的衍射峰消失,钛的氧化物发生脱氧,降至更低价态,产物主要为TiO;当槽电压升至2.8 V时,只有金属Ti的衍射峰。
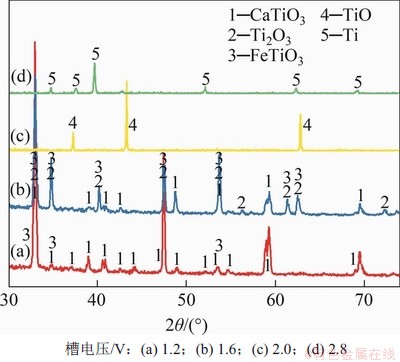
图7 不同槽电压的阴极产物XRD谱
Fig.7 XRD patterns of cathode products at different bath voltages
不同槽电压条件下阴极电流-时间曲线如图8所示。从图8可知:电流随槽电压升高而升高;电解时间在1~20 min时,电流急剧下降;当槽电压为1.2 V和1.6V时,由于电压较低导致整体电流较小;当槽电压为2.0 V时,电解时间在20~50 min时,出现电流平台,之后电流迅速降低,经分析认为,这是CaTiO3发生分解所致;而当槽电压低于1.6 V时,CaTiO3较为稳定,几乎不发生分解,没有出现电流平台现象;当槽电压升至2.8 V时,脱氧速率较快,电流明显增加,电流趋于稳定后,出现3个电流平台。经分析认为:在第一和第二电流平台,CaTiO3发生分解,并还原为Ti低价氧化物;第三平台电流略有增加,是析出金属Ti、伴随碳棒阳极粉化现象所致。
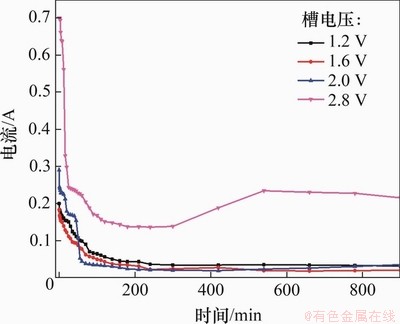
图8 不同槽电压阴极电流-时间曲线
Fig. 8 Current-time curve of cathode under different electrolytic voltage
3 杂质元素分析
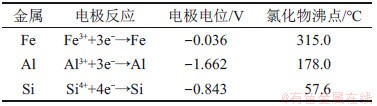
含钛废渣中主要杂质为Fe,Si和Al等元素,杂质与金属钛的分离主要是由于析出电位差不同,电位差越大,精炼效果越好。在电解过程中,相比于TiO2,电极电位更低的杂质优先在阴极析出。表4所示为杂质元素的物理化学特性。由表4可知:Fe,Al和Si的氯化物沸点均小于900 ℃。化学方程式(6)~(8)计算所得标准吉布斯自由能△GΘ如图9所示。在900 ℃生成FeCl3,AlCl3和SiCl4的△G均远大于零,不能自发进行。
表4 金属的物理化学特性
Table 4 Physical and chemical properties of metals
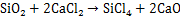 (6)
(6)
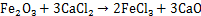 (7)
(7)
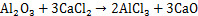 (8)
(8)
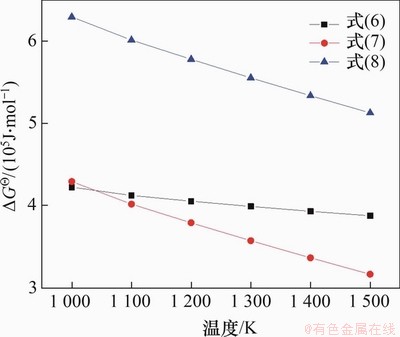
图9 标准吉布斯自由能随温度变化曲线
Fig.9 Standard Gibbs free energy with temperature curve
CaO在CaCl2熔盐电解质中具有一定溶解度[15],使得废渣中Ca全部进入熔盐,Fe,Al和Si等杂质被还原为单质,大部分起到热还原作用,最终进入熔盐,小部分与电解产生的少量氯气生成氯化物挥发,反应方程见式(9)~(11)。AlCl3的沸点低,更易于挥发,随着电解时间及槽电压的增加,产物中铝的含量大幅下降。而产物中铁含量变化不大,1.6 V电解过程中出现FeTiO3,Fe和Ti产生类质同晶现象,有形成TiFe合金的倾向[16-19],由于产物中其含量不高,未能发现对应的衍射峰。由于废渣中Si含量较低,电解过程主要在阴极孔隙中进行,产物中含量变化的规律性不强。
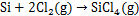 (9)
(9)
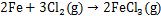 (10)
(10)
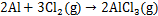 (11)
(11)
4 结论
1) 在温度为900 ℃和槽电压为3.1 V条件下,随着电解时间延长,Ti质量分数增加;电解3.5 h开始析出金属Ti,电解6 h后,阴极颗粒粒度明显增大,呈海绵形态;电解12 h时,金属Ti质量分数达到94.23%,产物为金属Ti和微量TiO;电脱氧历程为:CaTiO3→Ti2O3→TiO→Ti。
2) 在900 ℃下电解15 h,槽电压为2.0 V时,CaTiO3发生分解,产物主要为TiO;当槽电压升高至2.8 V时,Ti质量分数达到97.79%,O质量分数降至0.71%。
3) 电极电位更低的杂质优先被还原为单质,大部分起热还原作用,在阴极孔隙中进行扩散与迁移过程较复杂,使得产物中残留微量的Fe,Al和Si等杂质,而Ca全部进入熔盐。
参考文献:
[1] CHEN G Z, FRAY D J, FARTHING T W. Cathodic deoxygenation of the alpha case on titanium and alloys in molten calcium chloride[J]. Metallurgical and Materials Transactions B, 2001, 32(6): 1041-1052.
[2] FRAY D J. Anodic and cathodic reactions in molten calcium chloride[J]. Canadian Metallurgical Quarterly, 2002, 41(4): 433-439.
[3] FRAY D J. Emerging molten salt technologies for metals production[J]. JOM, 2001, 53(10): 27-31.
[4] CHEN G Z, FRAY D J, FARTHING T W. Direct electrochemical reduction of titanium dioxide to titanium in molten calcium chloride[J]. Nature, 2000, 407(6802): 361-364.
[5] 熊英禹. 浅谈海绵钛工业污染防治对策[J]. 轻金属, 2014(5): 59-62.
XIONG Yingyu. A brief analysis on pollution prevention and control countermeasures for the sponge titanium industry[J]. Light Metals, 2014(5): 59-62.
[6] 余代权. 四氯化钛生产中废渣的回收利用实践[J]. 钛工业进展, 2002, 19(1): 42-46.
YU Daiquan. Recycling practice of waste residue in titanium tetrachloride production[J]. Titanium Industry Progress, 2002, 19(1): 42-46.
[7] 陈林, 雷霆, 李楠. 酸浸富集钛渣烟尘中TiO2工艺研究[J]. 钛工业进展, 2013, 30(6): 34-37.
CHEN Lin, LEI Ting, LI Nan. Research on enriching titanium dioxide from titanium slag smoke dust by acid leaching[J]. Titanium Industry Progress, 2013, 30(6): 34-37.
[8] 赵海涛. 沸腾氯化法四氯化钛生产中固体废物的综合利用[J]. 有色金属工程, 2015, 5(1): 94-96.
ZHAO Haitao. Comprehensive utilization of solid waste from titanium tetrachloride production by fluidized bed chlorination process[J]. Nonferrous Metals Engineering, 2015, 5(1): 94-96.
[9] WANG Yinshuai, ZOU Xingli, LU Xionggang, et al. Electrolytic production of Ti-Ge intermetallics from oxides in molten CaCl2-NaCl[J]. Transactions of Nonferrous Metals Society of China, 2018, 28(11): 2351-2359.
[10] 刘美凤, 郭占成, 卢维昌. TiO2直接电解还原过程的研究[J]. 中国有色金属学报, 2004, 14(10): 1752-1758.
LIU Meifeng, GUO Zhancheng, LU Weichang. Process of direct electrochemical reduction of TiO2[J]. The Chinese Journal of Nonferrous Metals, 2004, 14(10): 1752-1758.
[11] WENG Qigang, LI Ruidi, YUAN Tiechui, et al. Valence states, impurities and electrocrystallization behaviors during molten salt electrorefining for preparation of high-purity titanium powder from sponge titanium[J]. Transactions of Nonferrous Metals Society of China, 2014, 24(2): 553-560.
[12] 冯聪, 储满生, 唐珏, 等. 不同类型含钛高炉渣主要冶金性能及物相[J]. 中南大学学报(自然科学版), 2016, 47(8): 2556-2562.
FENG Cong, CHU Mansheng, TANG Jue, et al. Main metallurgical performance and phases for different types of titanium-bearing blast furnace slags[J]. Journal of Central South University(Science and Technology), 2016, 47(8): 2556-2562.
[13] 胡小锋, 许茜, 李海滨, 等. 熔盐电脱氧法制备金属Ti的最新研究进展[J]. 材料导报, 2006, 20(8): 101-103.
HU Xiaofeng, XU Qian, LI Haibin, et al. New development of the FFC Cambridge process for preparation of titanium[J]. Materials Review, 2006, 20(8): 101-103.
[14] HUANG Youguo, WANG Yi, ZHANG Xiaohui, et al. Preparation of wettable TiB2-TiB/Ti cathode by electrolytic boronizing for aluminum electrolytic[J]. Journal of Central South University, 2019, 26(10): 2681-2687.
[15] 江洪林, 胡志方, 吴延科, 等. CaCl2-CaF2熔盐的CaO溶解度及吸水性能研究[J]. 有色金属(冶炼部分), 2018(5): 17-20.
JIANG Honglin, HU Zhifang, WU Yanke, et al. CaO solubility and water absorption property of CaCl2-CaF2 molten salt[J]. Nonferrous Metals (Extractive Metallurgy), 2018(5): 17-20.
[16] 戴玮, 秦博, 颜恒维, 等. 钛铁合金制备研究现状[J]. 有色金属(冶炼部分), 2019(5): 50-55.
DAI Wei, QIN Bo, YAN Hengwei, et al. Current research status of preparation of Ti-Fe alloy[J]. Nonferrous Metals(Extractive Metallurgy), 2019(5): 50-55.
[17] 艾刚华, 华一新, 徐存英, 等. SiO2对CaCl2熔盐电解还原钛铁矿精矿制备FeTi合金的影响[J]. 过程工程学报, 2018, 18(3): 537-543.
AI Ganghua, HUA Yixin, XU Cunying, et al. Effect of SiO2 on preparation of ferrotitanium alloy from ilmenite concentrate by electroreduction in CaCl2 molten salt[J]. The Chinese Journal of Process Engineering, 2018, 18(3): 537-543.
[18] ZHOU Zhongren, ZHANG Yingjie, HUA Yixin, et al. Preparation of ferrotitanium alloys by electrolysis-assisted calciothermic reduction of ilmenite in equimolar CaCl2-NaCl electrolyte: effect of calcium oxide[J]. JOM, 2018, 70(4): 575-580.
[19] SHI Ruimeng, BAO Longfei, ZHANG Bo. Preparation of Ti-Fe alloy from titanium concentrate by electro-deoxidization in CaCl2[J]. Advanced Materials Research, 2014, 3187: 1195-1200.
(编辑 杨幼平)
收稿日期: 2020 -06 -29; 修回日期: 2020 -08 -13
基金项目(Foundation item):国家自然科学基金资助项目(51664005,51774102);贵州省科技平台及人才团队建设计划项目([2017]5626,[2017]5788,黔教合KY字(2015)334号) (Projects(51664005, 51774102) supported by the National Natural Science Foundation of China; Projects([2017]5626, [2017]5788, KY[2015]334) supported by Talents of Science and Technology Cooperation Platform of Guizhou Province)
通信作者:陈朝轶,博士,教授,从事冶金资源综合利用研究;E-mail:ccy197715@126.com
引用格式: 盖家萱, 陈朝轶, 李军旗, 等. 熔盐电脱氧含钛废渣制备金属钛[J]. 中南大学学报(自然科学版), 2021, 52(4): 1076-1082.
Citation: GAI Jiaxuan, CHEN Chaoyi, LI Junqi, et al. Preparation metal titanium from molten salt electrodeoxidized titanium-containing waste residue[J]. Journal of Central South University(Science and Technology), 2021, 52(4): 1076-1082.