DOI: 10.11817/j.ysxb.1004.0609.2020-37633
���ƹ�������ս���̿���ת����Ϊ
������1, 2���ὡ��1���� ��1���ں���1, 2
(1. ������ѧ ұ��ѧԺ������ 110819��
2. ������ѧ �������������̬��ұ��������ص�ʵ���ң����� 110819)
ժ Ҫ��Ϊ�˲����սᷨ���������������м�Թ�������ս���Ϊ��Ӱ�죬��������-���ȷ�����X�������䡢����Ҷ������ס�ɨ����������ȷ����о�Na2O�����²�ͬ�ս��ƶȶԹ������(C2S)�ս�����е�����ת�䡢����ṹ���ȶ��Ե�Ӱ�죬�Ӷ�Ϊ����ʯ���սᷨ�ṩ�������ݡ������������CaO-SiO2��Ԫϵ�У��ս������Ҫ����Ϊ��-C2S����CaO-SiO2-Na2O��ϵ�У���Ĵ���ʹCaCO3�ֽ��¶Ƚ��ͣ��ս������Ҫ����Ϊ��-C2S��Na2O�����ۼ��ı�C2S���͵����á���Na2O���ڵ������£��ս�����Ц�-C2S�ͦ�-C2S�������������ֱ�Ϊ845 cm-1��930 cm-1������ս��¶Ⱥ��ӳ�����ʱ�䣬�ٽ��˿�״��-C2S��ʿ���״��-C2Sת������-C2S�������٣���-C2S���������࣬ʹ���ս����ᾧ�����ߣ�ͬʱʹ�ս�����ڼ���Һ�е��ȶ�����ߣ���-C2S������Ȧ�-C2S��������ȶ���
�ؼ��ʣ�������ƣ��ս���̣�����ת�䣻����ṹ���ȶ���
���±�ţ�1004-0609(2020)-09-2136-08���� ��ͼ����ţ�TF821���� ���ױ�־�룺A
�������Ϊ�����ε���Ҫ�ɷ�֮һ�����������մ�[1-2]��ˮ��[3-5]���������[6-7]�������й㷺��Ӧ�ã���Ϊ�˹�������й����ߵ��о��ȵ㡣���������(C2S)���սᷨ���������������й����Ҫ�������࣬�������������L������H���ºͦ����־���[8-10]��ʹ�������������ж�C2S�ľ��Ϳ��ƽϸ��ӡ����������в�ͬ���͵�C2S�����������������ܳ�����һ����Ӱ�죬Ϊ�ˣ������о��߶�C2S�ȶ��Ե��о������˴���������ʹ�ö�C2S�ṹ���о�ȡ����һ���Ľ�չ[11-15]���ڴ�����Ʒλ������(n(Al2O3)/n(SiO2)��4)�Ĺ����У�����ʯ���սᷨ���������ȶ��Ħ�-C2S�������ܺĸߡ��������ü�ʯ���սᷨ����Ȼ������Լ��ս��¶Ƚϵͣ������������ʸߣ�����Ŀǰ�ձ����ʪ���罬��Ҥ���ܺĸߣ���������������Na+��ʹ�ù�����ƾ�����ҪΪ�Է��Բ�Ħ�-C2S�Լ������Է������õĦ�-C2S��������ĥ����̵�������ģ�����-C2S�����Ͻ���������������������Һ�������η�Ӧ[16]�������������ܳ��ʵ͡�
������������������ҵ��ѧ�����߽����˴�����̽�����о�����ͼʵ�ָɷ����ϡ��ɷ��սᣬ����δ�ɹ����Դˣ���������˵���ʯ���սᷨ[17]����ӷ����⣬����ʵ��Ҥβ����Ԥ�ȡ��ɷ��ս������ƣ�n(CaO)/n(Al2O3)��1.4�����������������ܳ��ʿ��Դﵽ90%[18]������Na2O�Ĵ��ڻ���ֹ��-C2S���-C2Sת���������������ܳ��ʡ���ˣ�����ͨ��ģ�����ʯ���սᷨ���ϣ�����TG-DSC��XRD��FT-IR��SEM�ȼ���ֶΣ��о��˲�ͬ�ս��ƶȶ�C2S�ս�����е�����ת�䡢����ṹ���ȶ����ܵ�Ӱ�죬�Ӷ��õ����ȶ���C2S��Ϊ����ʯ���սᷨ�ṩ�������ݡ�
1 ʵ��
���Ȳ��÷������Լ�CaCO3��SiO2��Na2CO3Ϊ�ս����ϣ�CaCO3��SiO2Ħ����ΪC/S��Na2O(��Na2CO3��ʽ����)��SiO2Ħ����ΪN/S����C/SΪ2����ͬN/S������ԭ�ϰ������Ϊ3:1װ�����Ϲ��ڻ��ϻ��ϻ��2 h��ʹ��ѹ����ѹ��Ϊd 20 mm��25 mm������װ��ʯī����������ʽMoSi2����¯����10 ��/min���������������趨���ս��¶Ⱥ���һ����ʱ�䣬���ս������������¯��ȴ������ȡ�����о��䷴Ӧ������
�ս�����ȶ������鲽��Ϊ������Բ����ƿ�̶��ں���ˮԡ���У���װ����װ�ü���������װ�ã��������������Һ�̱Ƚ��ս����ͱ���Һ��������������ƿ�У�����װ�á�һ��ʱ��������Ӧ���ò���©������Һ�̷��룬���õζ�������Һ�����������������Ƽ����������Ũ�ȡ�
TG-DSC���������õ¹�NETZSCH- STA449F1�����ǣ����Է�Χ���½�Ϊ30~1450 �棬�����ٶ�Ϊ10 ��/min�����½�Ϊ1450~300 �棬�����ٶ�Ϊ20 ��/min��XRD���������ú���Philips X`Pert PW3040-60��X������������ǣ�Cu K�����ܵ�ѹΪ40 kV���ܵ���Ϊ40 mA��ɨ�跶ΧΪ5��~90�㡣���ս�����л���10%��������)MgO��Ϊ�ڱ꣬ͨ���붨���������ս��������ຬ��������ṹ�����������ߴ硢�ᾧ�Ƚ�����ϼ��㣬�������С��10%��FT-IR�������������ձ�����SHIMADZU IRPrestige-21����Ҷ�任��������ǣ���Ʒ����KBrѹƬ�������Ʊ���ɨ�跶ΧΪ4000~400 cm-1��SEM����ò�������õ¹���˾��˾ULTRA PLUS-43-13��ɨ�����������������ѹΪ15 kV��
2 ���������
2.1 �ս�����TG-DSC�ȷ���
ͼ1��ʾΪN/S=0��N/S=0.2��Ʒ��TG-DSC�������ߡ���ͼ1(a)��֪����N/SΪ0�������£����¹�����785 �洦����һ�������ȷ壬������������ڸ��¶ȴ���33.87%��������ʧ������790 ��ʱ������ʧ����������ô����ȷ�ΪCaCO3�ֽ������ͬʱ�����߷��õ��÷�Ӧ����715 �濪ʼ��������785 ��ʱ��Ӧ������죬��DTG��ֵ�����Ǻϡ�963~1400 ����½����ƣ�963 �洦����һ��С���ȷ岢����������δ�����仯���е��¶�Ϊ952 �棬����CaO��SiO2�ڸ��¶��¿�ʼ������Ӧ������C2Sǰ���壬�ù���Ϊ���ȹ��̣���963 ��ʱ��Ӧ������졣��ͼ1(b)��֪��CaCO3�ֽⷴӦ������702 �棬��764 ��ʱ��Ӧ������죬ͬʱDTG��ֵ782 ��Ϊ������ʧ�������ĵ㣬��DSC��ֵ���нϺõ��Ǻϣ�����N/SΪ0.2ʱCaCO3�ֽ��¶ȵ���N/SΪ0ʱ�ķֽ��¶ȣ�˵��Na2O�����ۼ������ã�������CaCO3�ķֽ��¶ȡ���865 �洦����һ��С���ȷ岢����һ����������ʧ�������߷��õ��÷�Ӧ����856 ���¿�ʼ����������Na2CO3�۵�Ϊ851 �棬��ˣ���Ϊ�˴��仯ΪNa2CO3����������865~1270 ����������ƣ���N/SΪ0ʱ����������������������Ҫ������Na+�Բ����û�����϶��ʽ����C2S����ṹ��������������ն��иı���C2S���͵��µģ�˵������Na2O���˸ı�C2S���͵����á�
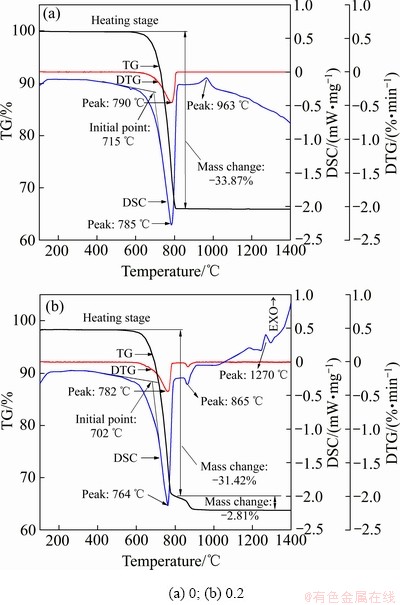
ͼ1 ��ͬN/S�ȵ�CaO-SiO2��ϵTG-DSC�������
Fig. 1 TG-DSC results of CaO-SiO2 system with different N/S ratios
2.2 �ս��¶ȶ�C2S����ת����Ϊ��Ӱ��
ͼ2��ʾΪC/SΪ2��N/SΪ0.1������ʱ��Ϊ1 hʱ��ͬ�ս��¶����ս�����XRD�ף�ͬʱ���ս�����и�������а붨���������������1���С����ͼ2�ͱ�1��֪�����ս��¶�Ϊ1300 ��ʱ���ս��������Ҫ����Ϊ��-C2S���Լ�����δ��Ӧ������CaO������C2S���γɹ���������Ƶ��γɹ��̽Ͻӽ�����Ҫ����ɢ����Ӱ��[19]�����¶Ƚϵ�ʱ������������ɢ����Ӧ���бȽϻ�������Ӧ����ȫ�����¶����ߵ�1350 ��ʱ��CaO����ʧ����-C2S�������ͣ������֦�-C2S�����������¶ȵ�1400 �棬��-C2S������12%���ߵ�32%����-C2S������51%�½���36%��ͬʱ�������¶ȵ����ߣ���-C2S�������ǿ�ȼ�������-C2S�������ǿ����ǿ�����������¶ȴٽ��ս�����Ц�-C2S���-C2S��ת������������C2S�Ĺ����屻��Ϊ��һ�ֹ�ȡ������ȱ�ݹ����壬��������C2S����Ϊ��һ����ijЩȱ�ݵĸ������ʣ���Щȱ������˻�ѧ���ȶ�״̬�����²���Ӧ����۵�˫������ʹ��-C2S����ȴ���������ɦ�-C2S����������Na2O���ڵ������£�Na+�Բ����û�Ca2+����϶��ʽ����C2S����ṹ��������������ն��иı���C2S���ͣ�Na+���ܽ�C2S�����У�������Ӧ�-C2S���ȶ��ԣ���-C2S�ľ����ǿ����ǿ��ʹC2Sʼ�ճɦ�-C2S���ڡ������¶ȵ����ߣ�Na2CO3������״̬�Ӿ磬��ӷ�����Na+���ܽ�C2S�����е��������٣����¾��������С��ʹ�æ�-C2S�ľ����ǿ�Ƚ��ͣ��ٽ������-C2S�ľ���ת�䡣

ͼ2 ��ͬ�ս��¶����ս����XRD��
Fig. 2 XRD patterns of sintered products at different temperatures
��1 ��ͬ�ս��¶����ս�����еĸ����ຬ��
Table 1 Content of sintered products at different sintering temperatures
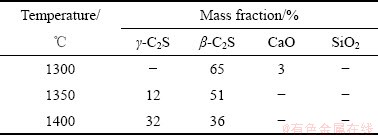
Ϊ�˽�һ����֤�������ۣ�ͨ��JADE��XRD���з������Ƚ���ƽ����Theta Calibration������Ȼ�����Rietveldȫ����Ϸ����������������徧��ָ�������������ͽᾧ�ȡ��ᾧ��Ϊ��Խᾧ�ȣ�����Ϊ�Ǿ���;���ǿ��֮��Ϊ100%������ռ��ǿ�ȵı���Ϊ��Խᾧ�ȡ���л�ֹ�ʽ[20]���㾧���ߴ磬��ʽ(1)����-C2S����-C2S��CaO��SiO2��Ӧ��������Ϊ(130)�� ��(200)��(200)�����������2�ͱ�3��ʾ��
��(200)��(200)�����������2�ͱ�3��ʾ��
 (1)
(1)
ʽ�У�D�Ǿ���ߴ磬nm��K��л�ֳ�����ͨ��Ϊ0.89������X�������䲨����nm��B�ǰ�߿�FWHM��rad����Ϊ����ǣ�rad��
�ɱ�2���Կ��������ս��¶ȵ����ߣ���-C2S�����ߴ���1350 ���43.7 nm���ӵ�1400 ���76.1 nm����߿��ʽ������ƣ���-C2S������С����߿����������ƣ���߿��뾧���ߴ�ɷ��ȡ����������¶ȴٽ���-C2S�����ߴ�ij��������˦�-C2S�����ߴ硣�ɱ�3��֪�����ս��¶���1300 �����ߵ�1400 �棬��-C2S����������½����ܽᾧ�����ߣ���������Na2O���ӵ����ս������C2S���ͱ仯��������ͬ�̶ȵľ�������Լ����ַǾ�������ɵģ�����Na+�Ĺ�������ʹ���ܽᾧ�Ƚ��ͣ������¶ȵ����ߣ�������Na+���������٣��Ǿ������������٣���-C2S���-C2Sת���������ӣ��ܽᾧ�����ߡ�
��2 ��ͬ�¶����ս�����и������߿��;�����С
Table 2 FWHM and grain size of phases in sintered products at different temperatures
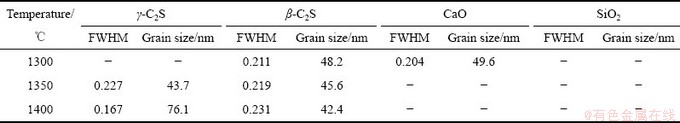
��3 ��ͬ�¶����ս�������ྦྷ������
Table 3 Lattice parameters of sintered products at different sintering temperatures


ͼ3 ��ͬ�ս��¶����ս����FT-IR����ͼ��
Fig. 3 FT-IR spectra of sintered products at different sintering temperatures
ͼ3��ʾΪ��ͬ�ս��¶����ս����ĺ�����ס��ں�������Ц�-C2S������λΪ931 cm-1��820 cm-1��555 cm-1��440 cm-1����-C2S������λ��890 cm-1��845 cm-1��520 cm-1����ͼ4���Կ����������¶���1300 ��������1400 �棬997 cm-1��Si��O���ķ��Գ�������������845 cm-1��Ϊ��-C2S��������ʶ�״��������շ�ǿ�ȼ�����˵���¶����ߦ�-C2S�������ͣ�930 cm-1Ϊ��-C2S������ʶ�״��������¶ȵ����ߣ���ǿ��������ǿ��˵���¶����ߦ�-C2S�������ӡ�845~877 cm-1����ΪSi��O�����Գ��������շ壬845 cm-1���η�λ���Ƶƫ�ƣ�516 cm-1��490 cm-1ΪO��Si��O���Գ��������������¶����ߣ��巶Χ��խ������������շ���Ŀ���ࡣ�������ڼ���������Ca2+С�����ӶԦ�-C2S�����ȶ�����[21]��Na+������������Ca2+�ģ�Na+���ܽ���-C2S�����ʹ��Na+�ڦ�-C2S��ȱ���ϸ�����ʹȱ�ݵ������ܽ��ͣ�Na+�����ྦྷ�˵ľ����Ͻ���;���Ǩ���ʣ������������Գ��Ԧ�-C2S�ɺ����谭���á��������¶ȵ����ߣ���ӷ���������Na+���������٣�C2S����ȱ�����������ߣ���-C2S���-C2Sת�����������ü���������XRD�������һ�¡�
ͼ4��ʾΪ��ͬ�ս��¶����ս���������ò����ͼ4��֪�����¶�Ϊ1300 ��ʱ���ս������Ҫ�ʿ�״�����������ֺܶ�����С��϶�����������¶ȣ���״������ַ�ɢ�Ŀ���״�����������¶ȵ���������Խ��Խ�ࡣ����������1300 ��ʱ���ս������Ҫ���Է��Բ�Ŀ�״��-C2S���������¶����ߣ���ӷ���������Na+���������٣��Է��Բ�Ħ�-C2S�����Է������õĿ���״��-C2Sת������һ��֤�������¶������ڦ�-C2S�����ɡ�

ͼ4 ��ͬ�ս��¶����ս��������ò
Fig. 4 Micromorphologies of sintered products at different sintering temperatures
2.3 ����ʱ���C2S����ת����Ϊ��Ӱ��
ͼ5��ʾΪC/SΪ2��N/SΪ0.1���ս��¶�Ϊ1350 ��ʱ��ͬ����ʱ�����ս�����XRD�ס���ͼ5���Կ������ս��������ɷ���ҪΪ��-C2S����-C2S��CaO�����ű���ʱ����0 min���ӵ�90 min��XRD�צ�-C2S������ǿ������ǿ�����������ʱ����30 min���ڣ��ս�������Ҫ����Ϊ��-C2S�����Ҽ�һ����������CaO��˵������ʱ��϶̣�������ɢ�������ս�ԭ��δ��Ӧ��ȫ��ͬʱNa2O�����ڦ�-C2S�У����Ʀ�-C2S���-C2Sת�������ŷ�Ӧʱ��Ľ�һ���ӳ����ս������е�CaO��ʧ����-C2S���࣬���ҳ������������-C2S��������������ʱ����ӳ�����-C2S�ĺ������࣬ͬʱ��ӷ���������Na+���������٣�ʹ��Na2O���ȶ����ü��������¹����в��֦�-C2Sת���ɦ�-C2S��������ʱ��Ϊ90 minʱ����-C2S������ǿ�ȼ�����ԭ��Ϊ������Na+��������һ�����٣���-C2Sת���ɦ�-C2S�϶ࡣ˵���ӳ�����ʱ��������Ca2+����ɢ���ӿ��սᷴӦ���̣��ٽ����෴Ӧ�ķ�����ͬʱҲ�ٽ���-C2S�����ɡ�

ͼ5 ��ͬ����ʱ�����ս����XRD��
Fig. 5 XRD patterns of sintered products for different durations
����XRD���ݴ�������JADE�еľ������ް����㱣��ʱ�䷶ΧΪ0~90 min�ս���������ľ�����������Ц�-C2Sѡȡ����ָ��Ϊ(130)��2��Ϊ29.78�㣬��-C2Sѡȡ�ľ���ָ��Ϊ ��2��Ϊ32.17�㣬���������4��ͼ6��ʾ�����ݱ�4��ͼ6��֪����1350 �棬����ʱ����ӳ�����-C2S�����ߴ���������ٽ������ƣ����������ڱ���ʱ��̵������£��ս���ᄃ��ṹ�����ƣ��Ǿ����ʶ࣬�ӳ���30 min����-C2S�����������ƣ�ͬʱ����Na+�Ĺ������ã���-C2S���������Ǿ����������࣬�����ߴ�������ű���ʱ����ٶ��ӳ�����ӷ�����������Na+���������٣���-C2S��������ͷǾ�������С����-C2S��ʼ�������-C2Sת������-C2S�����ߴ翪ʼ��С��˵���ӳ�����ʱ�䣬������Ca2+��ɢ��SiO2����;����У��ӿ��սᷴӦ���̣�ʹ�ս��������ᾧ�����ߡ�
��2��Ϊ32.17�㣬���������4��ͼ6��ʾ�����ݱ�4��ͼ6��֪����1350 �棬����ʱ����ӳ�����-C2S�����ߴ���������ٽ������ƣ����������ڱ���ʱ��̵������£��ս���ᄃ��ṹ�����ƣ��Ǿ����ʶ࣬�ӳ���30 min����-C2S�����������ƣ�ͬʱ����Na+�Ĺ������ã���-C2S���������Ǿ����������࣬�����ߴ�������ű���ʱ����ٶ��ӳ�����ӷ�����������Na+���������٣���-C2S��������ͷǾ�������С����-C2S��ʼ�������-C2Sת������-C2S�����ߴ翪ʼ��С��˵���ӳ�����ʱ�䣬������Ca2+��ɢ��SiO2����;����У��ӿ��սᷴӦ���̣�ʹ�ս��������ᾧ�����ߡ�
��4 ��ͬ����ʱ�����ս�����и������߿��;�����С
Table 4 FWHM and grain size of phases in sintered products for different durations
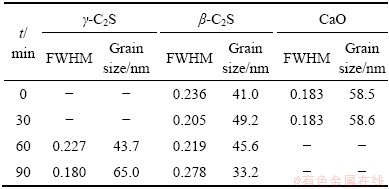

ͼ6 ��ͬ����ʱ�����ս������C2S����������ܽᾧ��
Fig. 6 Unit cell volume and total crystallinity of C2S in sintered products for different durations
�Ա���ʱ�䷶ΧΪ0~90 min�ս�������FT-IR��������һ��̽������ʱ���C2S�����Լ�����ṹ��Ӱ�죬�����ͼ7��ʾ����ͼ7��֪�����ű���ʱ����0 min�ӳ���90 min�����շ�ǿ���������ߣ������ӳ�����ʱ��������C2S�������ᾧ�����ӣ��������ӣ���930 cm-1�Լ�815 cm-1���γ����˦�-C2S������ʶ�״���847 cm-1������844 cm-1����һ���̶ȵķ�λƫ�ƣ����-C2S�ڸò��δ��ı���848 cm-1 Si��O���Գ���������һ�£�499 cm-1����O��Si��O���Գ�������ƫ�Ƶ�495 cm-1�����巶Χ��խ��˵���ӳ�ʱ�����������Ʀ�-C2S���ͣ�ͬʱ�������ڦ�-C2S��Na2O�ĺ������ڽ��¹����и�������ת���ɦ�-C2S��996 cm-1Ϊ��-C2S�������״������շ�ǿ�ȱ仯���-C2S�ĺ����仯һ�£�499 cm-1���״�ΪO��Si��O���Գ������������շ��ǿ�ȳ��Ƚ��ͺ��������ƣ��汣��ʱ����0 min���ӵ�90 min����λ���Ƶ�����ƶ�����495 cm-1�����������-C2S��ͼ��λ�����Ͻ����XRD�������һ�¡�

ͼ7 ��ͬ����ʱ�����ս����FT-IR����ͼ��
Fig. 7 FT-IR spectra of sintered products for different durations
���ս���������Һ(NaOHŨ��Ϊ60 g/L(��Na2O��)��Na2CO3Ũ��Ϊ50 g/L(��Na2O��)��Al2O3Ũ��Ϊ58 g/L����Ӧ�¶�80 �棬��Ӧʱ��1 h��Һ�̱�Ϊ10)���з�Ӧ���������C2S��Ӧ�ʣ�C2S�ķ�Ӧ����ʽ����Ӧ��(��)�ֱ��ʽ(2)~(5)����������ͼ8��ʾ����ͼ8�ɿ��������ű���ʱ����ӳ���C2S��Ӧ����12.57%�½���7.77%��������ʱ�����30 minʱ��C2S��Ӧ���½����������������ս�����е���Ҫ����Ϊ��-C2S�Լ��Ǿ����ʣ���-C2S����Һ�еļӦ��ɵġ��������ű���ʱ�����ӵ�90 min���ս����Ľᾧ�����ߣ������ɽ��ȶ��Ħ�-C2S����ˣ�C2S��Ӧ�ʼ��罵�ͣ�˵����-C2S������Ȧ�-C2S�������ȶ���
2CaO��SiO2(s)+2NaOH(l)=Na2SiO3(l)+2Ca(OH)2(s) (2)
3Ca(OH)2(s)+2NaAl(OH)4(l)=3CaO��Al2O3��6H2O(s)+2NaOH(l) (3)
3CaO��Al2O3��6H2O(s)+nNa2SiO3(l)=3CaO��Al2O3��nSiO2��(6-2n)H2O(s)+2nNaOH(l)+nH2O (4)
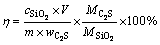 (5)
(5)
ʽ�У���Ϊ������Ƶķ�Ӧ�ʣ�%��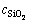 Ϊ��Һ�ж�������Ũ�ȣ�g/L��VΪ��Һ�������mL��mΪԭ��������g��
Ϊ��Һ�ж�������Ũ�ȣ�g/L��VΪ��Һ�������mL��mΪԭ��������g�� Ϊԭ���й�����Ƶĺ�����%��
Ϊԭ���й�����Ƶĺ�����%��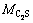 Ϊ���������Է���������
Ϊ���������Է���������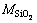 Ϊ����������Է���������
Ϊ����������Է���������
ͼ9��ʾΪ��ͬ����ʱ���ս���ﷴӦ����XRD�ס���ͼ9���Կ�����������ʱ�����30 minʱ�����ڴ�ʱ��-C2S�����϶�����Һ�еļ����Ӧ��ʹ�÷�Ӧ����Ҫ����ΪCaCO3�����ű���ʱ����ӳ����ս�����г����˽��ȶ��Ħ�-C2S����ˣ���Ӧ����CaCO3������֮���ͣ���-C2S�������ߡ�

ͼ8 ��ͬ����ʱ�����ս������C2S��Ӧ��
Fig. 8 Reaction rate of C2S of sintered products for different durations
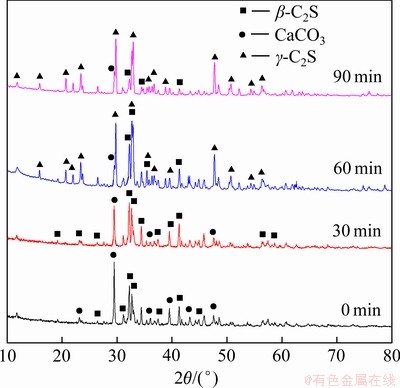
ͼ9 ��ͬ����ʱ���ս���ﷴӦ��XRD��
Fig. 9 XRD patterns of residues of sintered products for different durations
3 ����
1) ��CaO-SiO2��Ԫϵ�У�CaCO3��ʼ�ֽ��¶�Ϊ715 �棬�ս������Ҫ����Ϊ��-C2S����CaO-SiO2-Na2O��ϵ�У�CaCO3��ʼ�ֽ��¶Ƚ��͵�702 �棬�ս������Ҫ����Ϊ��-C2S��Na2O�����ۼ��ı�C2S���͵����á�
2) �ս�����Ц�-C2S�ͦ�-C2S�������������ֱ�Ϊ845 cm-1��930 cm-1������ս��¶ȣ��ٽ���-C2S���-C2Sת������ʹ��״��-C2S�������٣��ʷ�ɢ�ԵĿ���״��-C2S���������࣬�ᾧ�����ߡ�
3) �ӳ�����ʱ��ٽ���-C2S���-C2Sת����ʹ�ս�����ڼ���Һ�е��ȶ�����ߣ���-C2S������Ȧ�-C2S��������ȶ���
REFERENCES
[1] LI H, CHANG J. Stimulation of proangiogenesis by calcium silicate bioactive ceramic[J]. Acta Biomaterialia, 2013, 9(2): 5379-5389.
[2] LIN K L, CHANG J, ZENG Y, QIAN W J. Preparation of macroporous calcium silicate ceramics[J]. Materials Letters, 2004, 58(15): 2109-2113.
[3] RICARDO S,FRANCO Z. Recycling of hydrated cement pastes by synthesis of ����H-C2S[J]. Cement and Concrete Research, 2017, 100: 398-412.
[4] ZHOU X, MU Y D, LIU Z C, WANG F Z. Fabrication and characterization of a novel carbonated 0-3 piezoelectric ��-C2S composite[J]. Ceramics International, 2018, 44(11): 13426-13429.
[5] WANG D G, ZHANG Y, HONG Z R. Novel fast-setting chitosan/��-dicalcium silicate bone cements with high compressive strength and bioactivity[J]. Ceramics International, 2014, 40(7): 9799-9808.
[6] AHMAD O, SOODEH A. Reconstruction of radial bone defect in rat by calcium silicate biomaterials[J]. Life Sciences, 2018, 201: 45-53.
[7] LEE Y L, WANG W H, LIN F H, LIN C P. Hydration behaviors of calcium silicate-based biomaterials[J]. Journal of the Formosan Medical Association, 2017, 116(6): 424-431.
[8] LINK T, BELLMANN F, LUDWING H M, BEN H M. Reactivity and phase composition of Ca2SiO4 binders made by annealing of alpha-dicalcium silicate hydrate[J]. Cement and Concrete Research, 2015, 67(1): 131-137.
[9] EYSEL W, HAHN T. Polymorphism and solid solution of Ca2GeO4 and Ca2SiO4[J]. Crystalline Materials, 1970, 131: 322-341.
[10] SMITH D K, MAJUMDAR A, ORDWAY F. The crystal structure of ��-dicalciumsilicate[J]. Acta Crystallographica, 1965, 18(4): 787-795.
[11] �ž���, ������, ֣����, ���ľ�, ��ΰ, ���, ����ͨ. �����ѶԹ�������γɵ�Ӱ��[J]. ����������ѧѧ��(��Ȼ��ѧ��), 2006, 22(3): 424-427.
ZHANG Ju-song, ZHANG Tian-hua, ZHENG Wan-rong, WANG Wen-jun, JIN Jian-wei, BAI Hong-bin, SUI Zhi-tong. The Influence of titania on bicalcium silicate formation[J]. Journal of Shenyang Jianzhu University (Natural Science),2006, 22(3): 424-427.
[12] �� ��, �����, �� ��. V5+��Cr3+���Ӷ�C2S�ྦྷ�͵�Ӱ�����[J]. ���ϴ�ѧѧ��(��Ȼ��ѧ��), 2011, 25(4): 350-353.
ZHONG Xun, JIAN Shou-wei, KE Kai. Influence of V5+ and Cr3+ doping on polymorphic forms of C2S[J]. Journal of Jinan University (Natural Science), 2011, 25(4): 350-353.
[13] MAITI S C, GHOROI C. Influence of catalytic nano-additive for stabilization of ��-dicalcium silicateand its hydration rate with different electrolytes[J]. Cement and Concrete Research, 2017, 98: 111-121.
[14] �� ǧ, �� ��, ������, ���ܸ�, �� ��, �� ��. Ba2+���Ӳ��Ӷ�C2S�ṹ�ȶ��Ե�Ӱ��[J]. �ͻ����, 2016, 50(4): 265-268.
ZOU Qian, MA Yan, YU Xi-tang, WANG Zhou-fu, LIU Hao, LIU Qi. Effect of Ba2+ doping on stability of C2S structure[J]. Naihuo Cailiao, 2016, 50(4): 265-268.
[15] ������, ����ΰ, ������, �ں���, Ϳ�ӷ�, ��ʫ��. ������������ϵĸ��³ɿ���������������[J]. �й���ɫ����ѧ��, 2014, 24(6): 1664-1670.
PAN Xiao-lin, DONG Kai-wei, HOU Xian-lin, YU Hai-yan, TU Gan-feng, BI Shi-wen. High-temperature metallogenic mechanism and leaching property of calcium aluminate clinker with B2O3[J]. The Chinese Journal of Nonferrous Metals, 2014, 24(6): 1664-1670.
[16] �� ��, �� ��. ���η�Ӧ���������������ܳ��ʵ�Ӱ��[J]. �����, 2003(10): 10-12.
GUO Qin, WANG Jun. Effect of secondary reaction on dissolution rate of alumina in clinker[J]. Light Metals, 2003(10): 10-12.
[17] �ں���, ������, �� ��, ��ʫ��, ������. ���õ�����Ⱥ�����Դ�ɷ����ɷ������������ķ���: �й�, 201210069963.8[P]. 2014-07-16.
YU Hai-yan, PAN Xiao-lin, WANG Bo, BI Shi-wen, GU Song-qing. Method for producing alumina by using dry or semi-dry method of aluminum resources that low-aluminum silicon ratio: China, 201210069963.8[P]. 2014-07-16.
[18] TIAN Y P, PAN X L, YU H Y, TU G F. Formation mechanism and crystal simulation of Na2O-doped calcium aluminate compounds[J]. Transactions of Nonferrous Metals Society of China, 2016, 26(3): 848-858.
[19] OHAMED B M, SHARP J H. Kinetics and mechanism of formation of tricalcium aluminate, Ca3Al2O6[J]. Thermochimica Acta, 2002, 388: 105-114.
[20] κ��˧, ��ŵ��, �� ��, ���ӽ�, �� ��, ��һ��, �¼���. ʯī�ĵ������յ����Ʊ��ྦྷ�象Ĥ[J]. �˹�����ѧ��, 2017, 46(9): 1709-1713.
WEI Li-shuai, CHEN Nuo-fu, ZHANG Hang, WANG Cong-jie, HE Kai, BAI Yi-ming, CHEN Ji-kun. Preparation of polycrystalline silicon thin film by AIC on graphite substrate[J]. Journal of Synthetic Crystals, 2017, 46(9): 1709-1713.
[21] ����, ������. �����ӶԦ�-C2S�ȶ��Ե�Ӱ�켰������о�[J]. ������ѧ��, 1985, 13(4): 425-432.
FENG Xiu-ji, LONG Shi-zong. Effect of minor ions on the stability of ��-C2S and its mechanism[J]. Journal of Silicate, 1985, 13(4): 425-432.
Mineral transition behavior of dicalcium silicate doped with Na2O during sintering
PAN Xiao-lin1, 2, PEI Jian-nan1, ZHANG Can1, YU Hai-yan1, 2
(1. School of Metallurgy, Northeastern University, Shenyang 110819, China;
2. Key Laboratory for Ecological Metallurgy of Multimetallic Mineral, Ministry of Education, Northeastern University, Shenyang 110819, China)
Abstract: In order to clarify the influence of alkali on the sintering behavior of dicalcium silicate in the production of alumina by the sinter process, the phase transformation, crystal structure and stability of dicalcium silicate (C2S) in the presence of Na2O during the high-temperature sintering process under different sintering conditions were investigated by TG-DSC, XRD, FT-IR and SEM methods, providing theoretical basis for the low-sodium lime sinter process. In the CaO-SiO2 binary system, the main phase of the sintered product is ��-C2S. In the CaO-SiO2-Na2O system, the decomposition temperature of CaCO3 is reduced by Na2O, and the main phase is ��-C2S. Na2O acts as the role of flux and can alter the C2S crystal forms. In the presence of Na2O, the characteristic peak of infrared spectroscopy of ��-C2S and ��-C2S in the sintered product are 845 cm-1 and 930 cm-1, respectively. The increase of sintering temperature and the extension of holding time promote the phase transformation of blocky ��-C2S to granular ��-C2S, decrease the content of ��-C2S, increase the content of ��-C2S, and increase the crystallinity of the sintered product. The stability of the sintered product in the alkali solution is improved, and the ��-C2S solid solution is more stable than the ��-C2S solid solution.
Key words: dicalcium silicate; sintering process; mineral transition; crystal structure; stability
Foundation item: Project(2018YFC1901903) supported by the National Key Research and Development Program of China; Project(51674075) supported by the National Natural Science Foundation of China
Received date: 2019-11-07; Accepted date: 2020-06-23
Corresponding author: PAN Xiao-lin; Tel: +86-24-83686460; E-mail: panxl@smm.neu.edu.cn
(�༭ �� ��)
������Ŀ�������ص��з��ƻ�������Ŀ(2018YFC1901903)��������Ȼ��ѧ����������Ŀ(51674075)
�ո����ڣ�2019-11-07�������ڣ�2020-06-23
ͨ�����ߣ������֣������ڣ���ʿ���绰��024-83686460��E-mail��panxl@smm.neu.edu.cn