���±�ţ�1004-0609(2008)06-1143-09
����������ϸ��������Ԫ����ѧ��̬���о���չ
�� �����Ľ��������������ųɹ������
(���ϴ�ѧ ��Դ�ӹ������﹤��ѧԺ ����ұ��������ص�ʵ���ң���ɳ 410083)
ժ Ҫ������������ϸ��������ұ��������о���Ϊ�㷺��ϸ�����㷺�ֲ��ں��������ḻ�Ļ����С�����������ϸ�������£�������������ԭ������(����������)����һϵ����̬ת��ʹ��������ϸ�����ڡ�����ͻ����������д����Ų�ͬ��̬�ֲ���������ϸ��ϸ�������ϸ��������������ʽ���ۣ���ԭ������ɱ�ϸ�������������Σ��������м�̬��Ϊ����������������εȡ��й�����������ϸ�������������̬�о�ʮ��ȱ������һ����չ����������ϸ��������Ԫ����ѧ��̬���о�����Ϊ����ϸ�������������Ƽ�����Ľ��������IJ����ṩ�������ݡ�
�ؼ��ʣ�����������ϸ������ѧ��̬��Ԫ����㣻�������ܽ�
��ͼ����ţ�Q 939 ���ױ�ʶ�룺A
Research progress of sulfur chemical speciation impacted by acidophilic sulfur-oxidizing bacteria
HE Huan, XIA Jin-lan, PENG An-an, ZHANG Cheng-gui, QIU Guan-zhou
(Key Laboratory of Biometallurgy of Ministry of Education of China, School of Resources Processing and Bioengineering, Central South University, Changsha 410083, China)
Abstract: Acidophilic sulfur-oxidizing bacteria (SOB) are the mostly studied bioleaching bacteria which exists widely in the elemental sulfur and sulfides-containing environments. Under impaction by SOB, the solid sulfur and other reduced sulfides (including metal sulfides) are distributed in different chemical speciations inside or outside the cells as well as in the pertinent environmental deposit. The sulfur globules may be stored intra-cellularly after the solid sulfur is activated and transported by the bacteria. The reduced sulfur compounds, with polythiosulfate and/or elemental sulfur as the main transients, are finally oxidized to sulfuric acid. The chemical speciation of elemental sulfur impacted by various SOB was very poorly investigated, further research may provide theoretical support to the elucidation of sulfur metabolism of acidophilic SOB.
Key words: acidophilic sulfur-oxidizing bacteria; chemical speciation; elemental sulfur layer; sulfur globule; sulfur colloid
����������ϸ���ǽ�����������������е���Ҫ���ܾ�[1-2]���Խ������ˣ��㶫÷�ݡ���ɽ���Ƹ���ͭ������Կ��ˮ�Ϳ����е�������̬�����Ե��о���������Щ�����е�ϸ����Ҫ���ܹ����������ͻ�ԭ�������ϸ��[3-5]������ɸѡ�õ�������������ܳ��йصĹ��ܾ��꣬��Ҫ���������������������꣬����������������˾�(Acidithiobacillus ferrooxidans)��������������˾�(Acidithiobacillus thiooxidans)�����ᰢ������˾�(Acidithiobacillus albertensis)���Լ��ж��������������꣬������ϲ����˾�(At. caldus)��[6-8]�����⣬�����ϵ�[9-10]���������ڳ�ĸ��º�����Ȫ��ɸѡ�õ����꼫���������������꣬����������������˾�(Sulfobacillus thermosulfidooxidans), ���Ƚ�����Ҷ��(Sulfolobus metallicus)���������������(Acidianus manzaensis)�ȡ��������ʵ���������Щ�����������������������Ⱦ������Դٽ���������������ܳ����������õĹ�ҵӦ��ǰ��[6-10]������������ϸ���Ĺ�ͬ�ص������ᡢ���Ե�����ͻ�ԭ������(����������Σ���������Σ����������������ε�)��Ϊ��Դ���ʽ���ר�Ի���Ի���������������ԭ��������������ϸ�������£�Ԫ������ϸ��ϸ���������Բ�ͬ��ѧ��̬�ֲ����еı�ת����Ϊ�������ڵĵ����ʺ�ø����ɳɷ֣��е������ܽ���ʽɢ����ϸ���л���������[11]���е���������ʽ������ϸ������[12]����������������У�Ԫ�����ڽ��������[1]������Һ��[13]�����Ź㷺�ֲ����ɼ�������������ϸ���Ի�ԭ��������������ü�������Ľ������̣�����ϸ��ϸ��������Ԫ����Ļ�ѧ��̬ת�����̣���ˣ�������������ϸ��������Ԫ����ĸ�����̬չ���о������ڽ�ʾ�Ͳ����������������ܳ���������ķ�����̬ת�����ɣ�Ϊ��һ�����������������������½����������ܳ������ṩ�������ݣ��Լ�Ϊ��һ���о��Ͳ�����������������л;���춨������
1 ����������ϸ��ϵͳ������
���������ḻ�Ļ����У��纬����Ȫ����ɽ�ڡ�����ú������ȣ�������ϸ����������������Ԫ��ѭ���Լ�ά�ֻ�����Ⱥ������Եȷ���������Ҫ���á���Ȼ���ܹ�����Ԫ����������൱�ḻ������Ⱥ�ṹ���ܵ��������أ��纬�������༰��Ũ�ȡ��¶ȡ���ȡ�����ǿ�ȡ��л����ȵȵ�Ӱ��[14] �����1��ʾ���ڼ������Ի����£�������Դ�������ƶ����pHֵһ�����3��������Ⱥ��ͬ�����ж����ԡ������������¶ȿɽ����Ƿ�Ϊ����(��40 ��)���ж�����(40~60 ��)�ͼ�������(��60 ��)����������ϸ��[15-16] ��
����������ϸ����Ҫ��������˾���(Acidithiobacillus����дΪAt.)ϸ����������������������˾�(At. ferrooxidans)��������������˾�(At. thiooxidans)�Ͱ�����������˾�(At. albertensis)��[17]��������У���At. ferrooxidans)�����������ͻ�ԭ�������⣬�����ֻ�����õ�����ͻ�ԭ������������At. ferrooxidans��������뵽������������ϸ���������о���Ա��Ϊ��ϸ������Ҫ�����ܾ����������о��Ƚ�ȫ�棬Ŀǰ����At. ferrooxidansr�����������л;����Ϊ�о��ȵ�[18-19]��
������������У���������������л�Ϳ��������ֽ⣬������ϵ�¶ȿɿ���������50 �����ϣ���ˣ�һЩ��������ϸ���������棬���ж���������ϸ��ȴ���Ժܺ���������Щϸ����Ҫ��һЩ������������ר�Ի��������ϸ�������У���������ϸ����ҪΪ������������������(Leptospirillum ferrooxidans)����ϸ��ֻ��ʹ�������������������¶�Ϊ45 �棬�����ܽϸ�Ũ��������[20]����������ϸ������Ҫ�����˾�(Sulfobacillus spp.)��ϲ��������˾�(At. caldus)[3]��(Sulfobacillus)����������������������������Ȼ�ԭ�����ﻯ���������������ܹ������л�������м�����������[21-23]��At. caldus��Acidithiobacillus����Ωһ�ж����Ⱦ���DOPSON��[24]�о����֣�����At. caldus��Sulfobacillus thermosulfidooxidans��Ͻ������������ʱ�����������в����ĵ���������������αȵ���ʹ�ô�������S. thermosulfidooxidansʱҪ�ͣ���˵��At. caldus��Ч�ٽ������������̡�
������������������ϸ����Ϊ��ϸ���������ܹ����������������������û�ԭ�����������Ŀǰ�ѷ��봿����4�����������1��ʾ�����Ƿֱ�����Ҷ��(Sulfolobus)���������(Metallosphaera)�����������(Acidianus)����Ҷ����(Stygiolobus)��������ξ���(Sulfurisphaera)����Ҷ��Sulfolobus���о��϶���������������¶�Ϊ55~80 �棬����pHֵ 0.9~5.8�����Ի�ԭ������ͼ��л�����Ի�����������������[25]���������MetallosphaeraΪ�ϸ���������Ի�����Ӫ���ĸ�����Ⱦɫ����ϸ���������õ����������������������H2��Ϊ��Դ������������Acidianus(��ǰ����ΪDesulfurolobus)Ϊ�������������¼�������������ϸ����Ŀǰ��Stygiolobus��Sulfurisphaera������һ���֣��ֱ�ΪAzoricus��Ohwakuensis������Stygiolobus azoricusΪר��������������Sulfurisphaera ohwakuensis�ܹ����м��������������������������±������ӵ�����[26-27]��
��1 ���봿�����ܹ����û�ԭ�����������������ϸ��
Table 1 Isolated acidophilic sulfur-oxidizing bacteria making use of reductive sulfur compounds
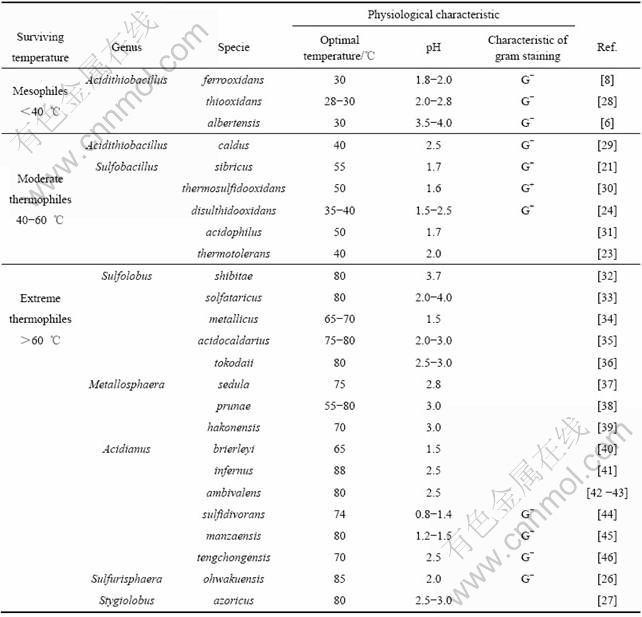
����������ϸ�����������¶ȿɷ�Ϊ���¡��ж����Ⱥͼ�������ϸ����16S rRNA����������ϸ��ϵͳ��������ͼ1��ʾ���Աȷ������֣�����������ϸ����ϵͳ�����������Ҳ���Է�Ϊ3���飬���ϵ��·ֱ����ϸ�����¾�����״���е��ж����Ⱦ��ͼ������Ⱦ��еĹ�ϸ�����ɼ�ϸ������������������������Ŵ�����֮��ȷʵ���������е���ϵ��
2 ϸ����������ѧ��̬
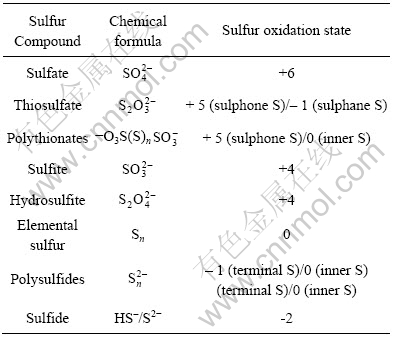
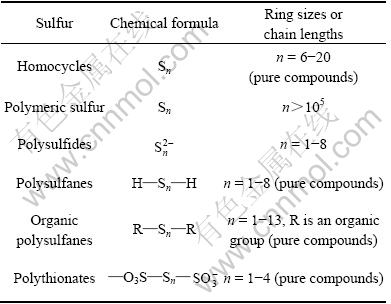
Ԫ��������Ȼ������������л�����ʽ���ڡ����2��ʾ��������ʽ���������Ե��ʡ�����������εȶ��ֲ�ͬ����̬���ڡ��л�������Ҫ�Ǻ���������װ��ᡢ�����ᡢ�����ᡢ�����ļ����������Ҫ�ֲ���ԭ�͡�ú���������ڡ���3��ʾΪ������Ļ�ѧ�ṹ[47]���ֱ�Ϊ����״��Sn(n = 6~20)����״�ۺ��� Sn (n��105)���������  (n = 1~8)���������H��Sn��H(n = 1~8)������л�����R��Sn��R (RΪ�л������ţ�n = 1~13), ���������ξۺ����CO3S��Sn��
(n = 1~8)���������H��Sn��H(n = 1~8)������л�����R��Sn��R (RΪ�л������ţ�n = 1~13), ���������ξۺ����CO3S��Sn�� (n = 1~4)������n��ʾĿǰΪֹ�ܹ��õ��Ĵ�������ԭ�Ӹ���������������ϸ������������(�������Ȫ�����Կ�ˮ����������)����ѭ���з�������Ҫ���á���ԭ��������������ϸ��(�������������ϸ��������������ϸ����)�����£�����������ĵ�������м������Щ�������ʸ�����̬�������е�ֱ����������ʽ�γɾۼ��������ϸ�����ڻ����⣻�е��ڽ���������γ���ˮ����㣻��Ԫ�����Ը���������ʽ������Һ�С�
(n = 1~4)������n��ʾĿǰΪֹ�ܹ��õ��Ĵ�������ԭ�Ӹ���������������ϸ������������(�������Ȫ�����Կ�ˮ����������)����ѭ���з�������Ҫ���á���ԭ��������������ϸ��(�������������ϸ��������������ϸ����)�����£�����������ĵ�������м������Щ�������ʸ�����̬�������е�ֱ����������ʽ�γɾۼ��������ϸ�����ڻ����⣻�е��ڽ���������γ���ˮ����㣻��Ԫ�����Ը���������ʽ������Һ�С�

ͼ1 ����16S rRNA����������ϸ��ϵͳ������
Fig.1 Phylogenetic tree based on 16S rRNA gene-sequence/accession number in brackets is gene bank of each strain
��2 �����Ҫ�����P���ϼ�
Table 2 Main sulfur compounds and their oxidation states
��3 ������Ļ�ѧ��̬
Table 3 Chemical speciation of elemental sulfur species
2.1 ���ܽ�������
��ԭ��������Ա�����������ϸ�����������������Ԫ������������������ӣ�����Щ����£�Ԫ����ȴ�Ծۺ��������ˮ���������ϸ�����ڻ������⡣����һ������֮ǰ����ѧ�߱�������ԭ��������������ϸ�������¿�ͨ��ij�ֻ�����������ʽ������ϸ��ϸ�����ڣ����������в����о���Ա���ֹ����ϸ������ɫ��ϸ���ڽ���������������������������ʱ���������Ϊ�м�������ĩ�˲���������ۣ��������о��ֶεľ������Լ�����̬�Ķ����ԣ�����ľ��廯ѧ��̬һֱ��������������[48-50]��Ŀǰ����������ϸ��(��Ҫ�ǹ����ϸ��)ϸ�����������̬�������ֲ�ͬ����ʶ��PRANGE��[12, 49]��Ϊ�������ϸ��������ɫ����ɫ��ϸ������������״������ڡ���ijЩ������ϸ������ȴ�Ի���״������ڣ���PICKERING ��[50]��Ϊ����ͬ��������ϸ������������Լ���״S8���ڡ���������ʹ�õļ���ֶ���ͬ����ΪX���߽��߽ṹ���ף�ͨ���Ա�ԭλ��������Ʒ����ͱ�������Ʒ(��������״S8����״�����һϵ��������-2~6������)ͼ�ײ��죬�Ӷ��Ʋ�������Ʒ������̬�����������������о������ִ��ڲ��죬PRANGE����ӫ��ģʽ����PICKERING������ģʽ�������о������ϲ����Ƿ��Ӱ�쵽�����о�������������
���Ի�����������ϸ��ͬ���������û�ԭ������������������������������ͬ���۲쵽�������������ʻ��ۡ�ROJAS��[11]���˹���ĥ������100 nm��Ļ�����Ĥ����At. ferrooxidans����������羵�о��������������裬�۲쵽���������ܽ������ֽ���״��ϸ��������������ɢ���ڰ���ϸ�����л����������γɵ����������ֱ�Ӵ��ݸ��´���ϸ�������Ƕ�����Ļ�ѧ��̬���������KNICKERBOCKER��[51]�о����֣�At. thiooxidans�ڵ�����������ʱ�����������ˮ�Է������Ա仯������ɨ��羵�۲쵽�������һ���л���ǣ�����һ���ܽ�״���ʣ���δ���������ܽ�״���ʵľ��廯ѧ��̬��PRANGE��[12]����X�������ս��˽ṹ����ԭλ��At. ferrooxidans���������������Һ���γ��������Ծ�������ʽ���ڣ�����ڽṹ���п������CO3S(S)n (nΪ��ԭ����Ŀ)��XIA��[6]ͨ������������۲쵽At. albertensis�������������������ʱ�����е��������ʴ��ڣ���������BRYANT��[52]�����������ʼ������ƣ��п�����ϸ������������������й�����廯ѧ��̬�����һ����������֤��
(nΪ��ԭ����Ŀ)��XIA��[6]ͨ������������۲쵽At. albertensis�������������������ʱ�����е��������ʴ��ڣ���������BRYANT��[52]�����������ʼ������ƣ��п�����ϸ������������������й�����廯ѧ��̬�����һ����������֤��
��ѧ���������ܽ�������Ȼ������Ǹ������ ���������γɵ�һ�ֽ���״���ʣ������ֱ����Լ0.1~1.0 ��m����Ҫ��S8����(��ˮ�ܽ�)������������ˮĩ����״������(��ˮ�ܽ�)��ɣ����������ܽ�������ͨ����ѧ�ֶ��Ʊ�[53]���뻯ѧ�ֶ��Ʊ������ܽ���ȣ�������ϸ�����������������γɵ������ܽ��ڽ�������ߴ��뽺���ȶ��Թ�ϵ������������ԣ����ڿ����ܶȺͱ�������ˮ�Եȷ�����ܲ��ϴ��磺ϸ�������ܽ������ܶ����Ե���(��ѧ)б�����ܽ������ܶȣ�ϸ�����������ˮ�Ժã���б�������ȴ��ˮ[50]��
Ŀǰ���й�������ϸ�������µ�����������ܽ����γɺͽ�����̼�����ƻ��������OHMURA��[54]���֣�At.ferrooxidans�ڵ�������Դ����������ʱ��ϸ����ë����һ�����ϵ���(40kDa)���õ���ͨ�������γɶ��������ʽʹAt. ferrooxidans �������������ı����ϡ�ROHWERER��[55]��������ʵ���������S8�ȱ��Ȼ��������ģʽ�����У����Ӧ�������˷�Ӧ�Լ���״�ṹ��S8����ϸ����ĵ���S����Ĥ�����ϵ�����RSH(���������ڴ����Ĺ�����)��Ӵ�����γ���״���������л����ϵ�RSnH(n��2)��Ȼ��ת�˵�ϸ�����ʺ����˫��ø�������γ���Ҫ����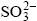 �����ǣ�ϸ�������Ƿ���ѭ��һģʽȴ����������ҵ�ĿǰΪֹҲδ���뵽����ת����صĹؼ����ס�
�����ǣ�ϸ�������Ƿ���ѭ��һģʽȴ����������ҵ�ĿǰΪֹҲδ���뵽����ת����صĹؼ����ס�
2.2 ��������е�Ԫ�����
�������Ի����£���������H+��Fe3+�����£���Ҫ�����������;���������;�����ֽ⣻����ϸ��ͨ��������ԭ���������ṩ����������������ͬʱά�ֽ����н������Ӳ��Ͻ�������Ҫ�ĸ������Ӻ����ӡ�����������ܽ�;��������FeS2��MoS2��WS2�Ȳ����������������ܽ⣬����ȫ����Fe3+��Ԫ��S����������ֱ�����е�6������ȫ����ת�ƣ��γ�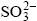 ��������Ԫ�ط��뵽��Һ��ȥ���������ܽ�;����������ZnS��PbS��FeAsS��CuFeS2��MnS2��CuS��Cu2S��NiS��CoS��CdS���ڶ����������������ܽ⣬������Fe3+��H+��Э���µĶԽ���������������ã������������ܽ⣬���д���ת��Ϊ��������ӣ��������ɵ�
��������Ԫ�ط��뵽��Һ��ȥ���������ܽ�;����������ZnS��PbS��FeAsS��CuFeS2��MnS2��CuS��Cu2S��NiS��CoS��CdS���ڶ����������������ܽ⣬������Fe3+��H+��Э���µĶԽ���������������ã������������ܽ⣬���д���ת��Ϊ��������ӣ��������ɵ�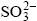 �͵���S�����⣬���������ȱFe3+����������Ľ���������п���������ӹ������ܽⲢ�ͷų�����[1]��
�͵���S�����⣬���������ȱFe3+����������Ľ���������п���������ӹ������ܽⲢ�ͷų�����[1]��
����������ϸ�������ʹ���ѧ���������У�����������γ���ˮ��Ԫ�����Ӱ����������ĵ绯ѧ���ʣ��谭������Ľ�һ���ֽ�� �������ӽ���[1]��BEVILAQUA��[56]�о�����At. ferrooxidans����������ͭ��Ĺ����У�ͭ���ӽ���������С��X��������������ֿ�������в���Ԫ����Ϊ�������ʣ����Ĵ���Ӱ�쵽��ͭ���ӵĽ���Ч�ʡ�SHI��[57]ͨ��X��������������֣�At. ferrooxidans������п������п������ѻ�������Ҫ���Ϊ����Ϊ���п�����Ӱ��ϸ������Ч�������ء�FOWLER��[58]�о���At. ferrooxidans������Һ������п���Ч�����֣�����ϸ������ϵ��п���ӵĽ��������Ը���δ����ϸ����ϵ����δ����ϸ������ϵ������п���ӵĽ�������������γ�һ������Ĥ����Ĥ�Ĵ�����ֹ��Fe3+����п�������������п���ӽ�����FALCO��[59]���û�ѧ������L. ferrooxidans������ͭ��ʱ�����ֿ�������������γɣ�����Ӱ���˽���Ч����KLAUBER��[60]����X���߹��������(XPS)�����о���ͭ��ѧ���������п������Ԫ������̬���о�������֣�������������Ҫ�ɶ�����͵����ɣ����Ƕ�������廯ѧ��̬����ȷ����HARMER��[61]����XPS��ɨ����������о������������ͭ����̣������ͭ��ѧ�������̷�Ϊ3�����裺1) ͨ���������轫������������ͭ���������ͷŵ���Һ�У�ʹ��һ�����γɶ�����2) ���л�ԭ��Ӧ���ò���Ӧ���ͷ������ӣ����γɱ���S2-�Ͷ���������3) ��ͨ�������ع������γɾ����������������ӵĽ�һ���ͷš����ּ�������һ���������������һ����֤��
2.3 �����������Ļ�����
���Ի����£���������к�ǿ�Ļ�ѧ���ԣ�����ͨ������������ϸ�����ܽ�����������ԭ��������ϸ�������£�����һϵ��������ԭ��Ӧ���ձ�ɸ������������Һ�С��о���������ͬ������ϸ������ͬ�¶Ⱥ���ȵȻ��������Լ���ʼ��������ȶ���Ӱ�쵽�����̬�ֲ���
SCHIPPERS��[13, 62]���÷����ЧҺ��ɫ�����Ӷ�ɫ�ױȽ��о���L. ferrooxidans��At. ferrooxidans��L. ferrooxidans��At. caldus��������Լ��������ӷֱ�����������Ч����������֣�L. ferrooxidans������ϵ�д������������Ρ����������κʹ������������е�����ռ10%������������2%������������1%�����м����������뵥�����������Һ����ʱ�Ľ��������ͬ����������At. ferrooxidans����ʱ��������Һ�н����������������(ռ����1%)��δ�������������Σ�������L. ferrooxidans��At. caldus��Ͻ��������������Һ�п������������������Ӵ��ڡ�������ΪAt. ferrooxidans��At. caldus���ܴ�л���ܼ�ʱ���������������������ɵ��м������L. ferrooxidans���ܴ�л������ˣ����������л�������������εȶ����м��̬�����
HALLBERG��[63]�о���ͬ��ż���������Ƽ���At. caldus������ͬ��ԭ�������Ӱ�죬�����������ż�����ʻ����ȱ���(Carbonyl cyanide m-chlorophenyl-hydrazone)��2��4-����������(2, 4-dinitrophenol)�������������������û���κ�Ӱ�죬�������������Ρ�������������������ȴ��ǿ���������á�N-�һ��������ǰ�(N- Ethylmaleimide)��������������Ρ����������Ρ������������������Ľ�һ��������2-����-4-�ǻ����-N-������(2-heptyl-4-hydroxyquinoline-N-oxide)����ֹ��������Ρ����������Ρ��������������������Ľ�һ���������������Ƽ��ͽ�ż�������ã���Ӧ��ϵ�пɼ����۵ĸ����м���
��ԭ��������At. ferrooxidans ���ڵ����������л����������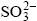 �����
�����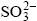 û�б����������������ڻ���, ���ϸ�������������ö�Ӱ��ϸ�����������, ϸ�����ڴ��ڽ��
û�б����������������ڻ���, ���ϸ�������������ö�Ӱ��ϸ�����������, ϸ�����ڴ��ڽ��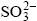 ���Ե�øϵͳ��������ϸ������
���Ե�øϵͳ��������ϸ������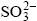 ��Ҫ����������-����������ԭø������
��Ҫ����������-����������ԭø������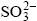 ��������ϸ����������������εĹ����л�������������μ��������������Σ��ӹ�����Acidianus ambivalens �з����Ĥ������������-��øQ ������ԭø(thiosulfate: quinone oxidoreductase: TQO) �����軯����-����Ϊ��������ʱ������
��������ϸ����������������εĹ����л�������������μ��������������Σ��ӹ�����Acidianus ambivalens �з����Ĥ������������-��øQ ������ԭø(thiosulfate: quinone oxidoreductase: TQO) �����軯����-����Ϊ��������ʱ������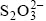 ��Ϊ
��Ϊ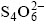 ��At. ferrooxidans �ڵ�������Դ����������ʱ��������ø(Rhodanese)���������ø��һ�������������ת��ø(thiosulfate thiotransferase, TST)��ר�Ŵ��
��At. ferrooxidans �ڵ�������Դ����������ʱ��������ø(Rhodanese)���������ø��һ�������������ת��ø(thiosulfate thiotransferase, TST)��ר�Ŵ��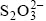 �е�S��S��ѧ��, ����S��
�е�S��S��ѧ��, ����S��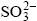 ��һ����Ϊ����������������������ˮ��ø���������������Σ���������о��������ǰ��һ�£����磬STEUDEL��[64]��1987 ���о�����At. ferrooxidans������������ˮ��ø��Ҫ������Ϊ
��һ����Ϊ����������������������ˮ��ø���������������Σ���������о��������ǰ��һ�£����磬STEUDEL��[64]��1987 ���о�����At. ferrooxidans������������ˮ��ø��Ҫ������Ϊ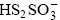 ��
��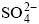 ����MEULENBERG��[65]1992�귢��Acidithiobacillus sp.ˮ�������Ҫ��
����MEULENBERG��[65]1992�귢��Acidithiobacillus sp.ˮ�������Ҫ��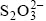 ��
��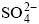 ��S0������SUGIO��[18, 66]��1996���о�����At. ferrooxidans Funis2-1ˮ�������Ҫ��
��S0������SUGIO��[18, 66]��1996���о�����At. ferrooxidans Funis2-1ˮ�������Ҫ��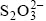 ��
��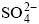 ��
��
3 ����
������ͻ�ԭ������������������ϸ�������£�����������ĵ�������м������Щ�滯ѧ��̬�������е�ֱ����������ʽ�γɾۼ�����������Һ�У��е�ͨ��ij��δ֪������������ʽ������ϸ��ϸ�����ڣ�����һЩ�ڽ���������γ���ˮ��Ԫ����㣬Ӱ����������ĵ绯ѧ���ʴӶ��谭������Ľ�һ���ֽ�ͽ������ӽ�������Щ�Ը�����������Ӷ�������Һ�У������й������������������£�������һЩ�������ù�ҵӦ��ǰ�������������������������£������������ľ��������̬ת���ı������١�
�����ڹ��������ϸ���л�������ѧ��̬�����������������й������γɺͽ���ľ������Ŀǰ������������������ϵ��������ϸ����Ϊ���滷�����⣬������Ŵ�ѧ������ͨ�������¹����ϸ��������������ϸ�����ںܴ���Ŀǰ�Ը���ϵ��������ϸ������������̬���о����������ڻ�����ͻ�ͭ��Ƚ��������о���������������ޡ����Ի����£���������������ͨ��������ϸ������øϵ��ɣ�����ϸ���Ե��������������ͳ�����������һֱ������δ�������⡣ϸ����Ԫ�����������ù��̾���ϸ��������Ԫ����ѧ��̬ת����̣�����ϸ����������øϵ������ء���һ����չ����������������Ԫ������̬�о����������ڽ�ʾ�Ͳ����������������ܳ���������ķ�����̬ת�����ɣ��Ӷ�Ϊ��һ�����������������������½����������ܳ������ṩ�������ݣ��Լ�Ϊ��һ���о��Ͳ�����������������л;���춨������
REFERENCES
[1] ROHWERDER T, GEHRKE T, KINZLER K, SAND W. Bioleaching review part A: Progress in bioleaching: fundamentals and mechanisms of bacterial metal sulfide oxidation[J]. Appl Microbiol Biotechnol, 2003, 63(3): 239-248.
[2] ROHWERDER T, SAND W. Oxidation of inorganic sulfur compounds in acidophilic prokaryotes[J]. Eng Life Sci, 2007, 7(4): 301-309.
[3] HE Zhi-Guo, XIAO Sheng-mu, XIE Xue-hui, ZHONG Hong, HU Yue-hua, LI Qing-hua, GAO Feng-lin, LIU Jian-she, QIU Guan-zhou. Molecular diversity of microbial community in acid mine drainages of Yunfu sulfide mine[J]. Extremophiles, 2007, 11(2): 305-314.
[4] YANG Yu, WAN Ming-xi, SHI Wu-yang, PENG Hong, QIU Guan-zhou, LIU Xue-duan. Bacterial diversity and community structure in acid mine drainage from Dabaoshan Mine, China[J]. Aquatic Microb Ecol, 2007, 47: 141-151.
[5] YIN Hua-qun, QIU Guan-zhou, WANG Dian-zuo, CAO Lin-hui, DAI Zhi-min, WANG Jie-wei, LIU Xue-duan. Comparison of microbial communities in three different mine drainages and their efficiency of bioleaching to the low grade of chalcopyrite[J]. J Cent South Univ Technol, 2007, 14: 460-466.
[6] XIA Jin-lan, PENG An-an, HE Huan, YANG Yu, LIU Xue-duan, QIU Guan-zhou. A new strain Acidithiobacillus albertensis BY-05 for bioleaching of metal sulfides ores[J]. Trans Nonferrous Metals Soc China. 2007, 17(1): 168-175.
[7] QIU Guan-zhou, FU Bo, ZHOU Hong-bo. Isolation of a strain of Acidithiobacillus caldus and its rolein bioleaching of chalcopyrite[J]. World J Microbiol Biotechnol, 2007, 23: 1217-1225.
[8] �� ��, �Ľ���, ������, �����. �㶫÷�ݽ������ѡ�����Խ�����Ľ���[J]. �����о���Ӧ��. 2007, 1: 182-186.
HE Huan, XIA Jin-lan, PENG An-an, QIU Guan-zhou. Breeding of a strain YS-1 from Meizhou, Guangdong provance and its bioleaching trials for metal sulfides ores[J]. Materials Research and Application, 2007, 1: 182-186.
[9] ������, ��һ��, �� ��, �ųɹ�, �����. �����������˾�һ�¾���ķ��������[J]. ����ʦ����ѧ��Ȼ��ѧ��. 2007, 30(4): 104-108.
DING Jian-nan,YU Yi-zun, HE Huan, YIN Hua-qun, ZHANG Cheng-gui, QIU Guan-zhou. Isolation and identification of a new strain in Sulfobacillus thermosuffidooxidans[J]. Acta Scientiarum Naturalium Universtatis Normalis Hunanensis, 2007, 30(4): 104-109.
[10] ������. ���ָ��½�����ķ���������������û�����DZ���о�[D]. ��ɳ: ���ϴ�ѧ, 2007.
DING Jian-nan. Isolation, identification of thermophilic leaching microorganisms and studies on their bioleaching mechanism and potential [D]. Changsha: Central South University, 2007.
[11] ROJAS J, GIERSIG M, TRIBUTSCH H. Sulfur colloids as temporary energy reservoirs for Thiobacillus ferrooxidans during pyrite oxidation[J]. Arch Microbiol, 1995, 163: 352-356.
[12] PRANGE A, CHAUVISTRE R, MODROW H, HORMES J, TR?PER H G, DAHL C. Quantitative speciation of sulfur in bacterial sulfur globules: X-ray absorption spectroscopy reveals at least three different species of sulfur[J]. Microbiology, 2002, 148: 267-276.
[13] SCHIPPERS A, ROHWERDER T, SAND W. Intermediary sulfur compounds in pyrite oxidation: implications for bioleaching and biodepyritization of coal[J]. Appl Microbiol Biotechnol, 1999, 52: 104-110.
[14] ELSHAHED S M, SENKO M J, NAJAR F Z, KENTON S M, ROE A B, DEWERS T A, SPEAR J R, KRUMHOLZ L R. Bacterial diversity and sulfur cycling in a mesophilic sulfide-rich spring[J]. Appl Environ Microbiol, 2003, 69(9): 5609-5621.
[15] JOHNSON D B. Biodiversity and ecology of acidophilic microorganisms[J]. FEMS Microbiol Ecol, 1998, 27: 307-317.
[16] ���ɷ�, �ܺ鲨, �� ��, �����. ��ͬ��Դ�������ж���������ϸ�������Է���[J]. ����ѧ��, 2007, 47(3): 381-386.
LIU Fei-fei, ZHOU Hong-bo, FU Bo, QIU Guan-zhou. Bacterial diversity analysis of moderately thermophilic microflora enriched by different energy sources[J]. Acta Microbiologica Sinica, 2007, 47(3): 381-386.
[17] DONOVAN P K, WOOD A P. Reclassification of some species of Thiobacillus to the newly designated genera Acidithiobacillus gen. nov. Halothiobacillus gen. nov. and Thermithiobacillus gen. nov.[J]. Int J Syst Evol Microbiol, 2000, 50: 511-516.
[18] �ųɹ�, �Ľ���, �� ��, �����. ����������ϸ����������չ[J]. ���\��ͨ��, 2007, 1: 59-65.
ZHANG Cheng-gui, XIA Jin-lan, WANG Jing, QIU Guan-zhou. A model of sulfur oxidation system of Acidithiobacillus spp.[J]. Biotechnology Bulletin, 2007, 1: 59-65
[19] �ųɹ�, �Ľ���, �����. ��������������˾���������ϵͳ�о���չ[J]. �й���ɫ����ѧ��, 2007, 16(7): 1239-1249.
ZHANG Cheng-gui, XIA Jin-lan, QIU Guan-zhou. Progress in research on Fe2+ oxidation system of Acidithiobacillus ferrooxidans[J]. The Chinese Journal of Nonferrous Metals, 2007, 16(7): 1239-1249.
[20] RAWLINGS D E, TRIBUTSCH H, HANSFORD G S. Reasons why 'Leptospirillum'-like species rather than Thiobacillus ferrooxidans are the dominant iron-oxidizing bacteria in many commercial processes for the biooxidation of pyrite and related ores[J]. Microbiology, 1999, 145: 5-13.
[21] MELAMUD V S, PIVOVAROVA T A, TOUROVA T P, T V KOLGANOVA, OSIPOV G A, LYSENKO A M, KONDRAT'EVA T F, KARAVAIKO G I. Sulfobacillus sibiricussp. Nov., a new moderately thermophilic bacterium[J]. Microbiology, 2003, 72(5): 605-612.
[22] GHAURI M A, KHALID A M, SUSAN G, HEAPHY S, GRANT W D. Phylogenetic analysis of different isolates of sulfobacillus spp. isolated from uranium-rich environments and recovery of genes using integron-specific primers[J]. Extremophiles, 2003, 7: 341-34.
[23] BOGDANOVA T I, TSAPLINA I A, KONDRAT'EVA T F. Sulfobacillus thermotolerans sp. nov, a thermotolerant, chemolithotrophic bacterium[J]. Int J Syst Evol Microbiol, 2006, 56: 1039-1042
[24] DOPSON M, LINDSTROM E B. Potential Role of thiobacillus caldus in arsenopyrite bioleaching[J]. Appl Environ Microbiol, 2003, 71: 31-36.
[25] BROCK T D, BROCK K M, BELLY R T, WEISS R L. Sulfolobus: A new genus of sulfur-oxidizing bacteria living at low pH and high temperature[J]. Arch Microbiol, 1972, 84: 54-68.
[26] KUROSAWA N, ITOH Y H, IWAI T. Sulfurisphaera ohwakuensis gen. nov., sp. Nov., a novel extremely thermophilic acidophile of the order sulfolobales[J]. Int J Syst Bacteriol, 1998, 48: 451-456.
[27] SEGERER A H, TRINCONE A, GAHRTZ M, STETTER K O. Stygiolobus azoricus gen. nov., sp. nov. represents a novel genus of anaerobic, extremely thermoacidophilic archaebacteria of the order Sulfolobales[J]. Int J Syst Bacteriol, 1991, 41(4): 495-501.
[28] SUZUK I I, CHAN C W, TAKEUCHI T L. Oxidation of elemental sulfur to sulfite by Thiobacillus thiooxidans cells[J]. Appl Envirom Microbiol, 1992, 58(11): 3767-3769.
[29] �� ӧ, ��ž�, �ֽ�Ⱥ, �����, ������. һ���ж����������������˾��ķ����ϵͳ��������[J]. ����ѧ��, 2004, 44(3): 382-385.
LIU Ying, QI Fang-jun, LIN Jian-qun, TIAN Ke-li, YAN Wang-ming. Isolation and phylogenetic analysis of a moderately thermophilic acidophilic sulfur oxidizing bacterium[J]. Acta Microbiologica Sinica, 2004, 44(3): 382-385.
[30] �˾�ʯ, ������. Ӱ��Sulfobacillus thermosulfidooxidans���������������������о�[J]. ����ۺ�����, 2002, 3: 38-41.
DENG Jing-shi, RUAN Ren-man. Studies on Influencing factors of growth and ferrous iron oxidation of Sulfobacillus thermosulfidooxidans[J]. Multipurpose Utilization of Mineral Resources, 2002, 3: 38-41.
[31] KINNUNEN P M, PUHAKKA J A. Characterization of iron- and sulphide mineral-oxidizing moderately thermophilic acidophilic bacteria from an indonesian auto-heating copper mine waste heap and a deep south african gold mine[J]. J Ind Microbiol Biotechnol, 2004, 31(9): 409-414.
[32] GROGAN D, PALM P, ZILLIG W. Isolate B12, which harbours a virus-like element, represents a new species of the archaebacterial genus Sulfolobus, Sulfolobus shibatae, sp. nov.[J]. Arch Microbiol, 1992, 154: 594-599.
[33] QUN X S, SINGH R K, CONFALONIERIB F, ZIVANOVIC Y, ALLARDE G, AWAYEZA M J, CURTISC B A, MOORSE A D, ERAUSOG G, FLETCHERC C, PAUL M K. The complete genome of the crenarchaeon Sulfolobus solfataricus P2[J]. PNAS, 2001, 98(14): 7835-7840.
[34] DOPSON M, SUNDKVIST J E, LINDSTROM E B. Toxicity of metal extraction and flotation chemicals to Sulfolobus metallicus and chalcopyrite bioleaching[J]. Hydrometallurgy, 2006, 81: 205-213.
[35] CHEN L M, BR?GGER K, SKOVGAAR M, KURT H, NAOKI N, TAKAHIDE K, TOSHIAKI U, AKIHIKO Y, TAIRO O. REDDER P, She Qun-xin, TORARINSSON E, GREVE B, AWAYEZ M, ZIBAT, KLENK H P, GARRETT R A. The Genome of Sulfolobus acidocaldarius, a model organism of the crenarchaeota[J]. J Bacteriol, 2005, 187(14): 4992-4994.
[36] TOSHIHARU S, TOSHIO I, TAKETOSHI U. Sulfolobus tokodaii sp. nov. (Sulfolobus sp. strain 7), a new member of the genus sulfolobus isolated from beppu hot springs, Japan[J]. Extremophiles, 2002, 6: 39-44.
[37] ITOH Y H, KUROSAWA N, UDA I, SUGA A, TANOUE S, ITOH T, HORIUCHI T, ITOH T. Metallosphaera sedula TA-2, a calditoglycerocaldarchaeol deletion strain of a thermoacidophilic archaeon[J]. Extremophiles, 2001, 5: 241-245.
[38] FUCHS T, HUBER H, TEINER K, BURGGRAF S, STETTER K O. Metallosphaera prunae sp. nov., a novel metal-mobilizing, thermoacidophilic archaeum, isolated from a uranium-mine in germany[J]. Syst Appl Microbiol, 2007, 18: 560-566.
[39] KUROSAWA N, ITOH Y H, ITOH T. Reclassification of Sulfolobus hakonensis takayanagi et al. 1996 as Metallosphaera hakonensis comb. nov. based on phylogenetic evidence and DNA G+C content[J]. Int J Syst Evol Microbiol, 2003, 53: 1607-1608.
[40] KONISHI Y, TOKUSHIGE M, ASAI S, SUZUKI T. Copper recovery from chalcopyrite concentrate by acidophilic thermophile Acidianus brierleyi in batch and continuous-flowstirred tank reactors[J]. Hydrometallurgy, 2001, 59: 271-282.
[41] SEGERER A, NEUNER A, KRISTJANSSON J K, STETTER K O. Acidianus infernus gen. nov., sp. nov., and acidianus brierleyi comb. nov.: Facultatively aerobic, extremely acidophilic thermophilic sulfur-metabolizing archaebacteria[J]. Int J Syst Bacteriol, 1986, 36(4): 559-564
[42] FUCHS T, HUBER H, BURGGRAF S, et al. 16S rDNA-based phylogeny of the archaeal order Sulfolobales and reclassification of Desulfurolobus ambivalens as Acidianus ambivalens comb. nov[J]. Syst Appl Microbiol, 1996, 19(1): 56-60.
[43] ZILLIG W, YEATS S, HOLZ I, BOECK A, RETTENBERGER M, GROPP F, SIMON G. Desulfurolobus ambivalens, gen. nov., sp. nov., an autotrophic archaebacterium facultatively oxidizing or reducing sulfur[J]. Syst Appl Microbiol, 1986, 8(3): 197-203.
[44] PLUMB J J, HADDAD C M, GIBSON J A E, FRANZMANN PD. Acidianus sulfidivorans sp. nov., an extremely acidophilic, thermophilic archaeon isolated from a solfatara on Lihir Island, Papua New Guinea, and emendation of the genus description[J]. Int J Syst Evol Microbiol, 2007, 57: 1414-1423.
[45] YOSHIDA N, NAKASATO M, OHMURA N, ANDO A, SAIKI H, ISHII M, IGARASHI Y. Acidianus manzaensis sp. nov., a novel thermoacidophilic archaeon growing autotrophically by the oxidation of H2 with the reduction of Fe3+[J]. Curr Microbiol, 2006, 53(5): 406-411.
[46] HE Z G, ZHONG H, LI Y. Acidianus tengchongensis sp. nov., a new species of acidothermophilic archaeon isolated from an acidothermal spring[J]. Curr Microbiol, 2004, 48: 159-163.
[47] STEINBUCHEL A. Microbiology monographs[M]. Berlin Heidelberg: Springer-Verlag, 2006: 21-51.
[48] WILFRED E K, ARIE D K, ALBERT J H J. Biologically produced sulfur[J]. Topics Curr Chem, 2003, 230: 167-188.
[49] PRANGE A, ARZBERGER I, ENGEMANN C, et al. In situ analysis of sulfur in the sulfur globules of phototrophic sulfur bacteria by X-ray absorption near edge spectroscopy[J]. Biochim Biophys Acta, 1999, 1428: 446-454.
[50] PICKERING I J, GEORGE G N, YU E Y, BRUNE D C, TUSCHAK C, OVERMANN J, BEATTY J T, PRINCE R C. Analysis of sulfur biochemistry of sulfur bacteria using X-ray absorption spectroscopy[J]. Biochemistry, 2001,40: 8138-8145.
[51] KNICKERBOCKER C, NORDSTROM D K, SOUTHAM G. The role of ''blebbing'' in overcoming the hydrophobic barrier during biooxidation of elemental sulfur by Thiobacillus thiooxidans[J]. Chem Geol, 2000, 169: 425-433.
[52] BRYANT R D, MCGROARTY K M, COSTERTON J W, LAISHLEY E J. Isolation and characterization of a new acidophilic Thiobacillus species (T. albertis)[J]. Can J Microbiol, 1983, 29: 1159-1170.
[53] STEUDEL R. Aqueous sulfur sols[J]. Topics in Current Chemistry, 2003, 230: 153-166.
[54] OHMURA N, TSUGITA K, KOIZUMI J I. Sulfur-binding protein of flagella of Thiobacillus ferrooxidans[J]. J Bacteriol, 1996, 178(19): 5776-5780.
[55] ROHWERDER T, SAND W. The sulfane sulfur of persulfides is the actual substrate of the sulfur-oxidizing enzymes from Acidithiobacillus and Acidiphillum spp.[J]. Microbiology, 2003, 149: 1699-1709.
[56] BEVILAQUA D, LEITE A, GARCIA O, TUOVINEN O H. Oxidation of chalcopyrite by Acidithiobacillus ferrooxidans and Acidithiobacillus thiooxidans in shake flasks[J]. Process Biochem, 2002, 38(4): 587-592.
[57] SHI S Y, FANG Z X. Bioleaching of marmatite flotation concentrate by Acidithiobacillus ferrooxidans and Leptospirillum ferrooxidans[J]. Trans Nonferrous Metal Soc China, 2004, 14(3): 569-575.
[58] FOWLER T A, CRUNDWELL F K. Leaching of zinc sulfide by Thiobacillus ferrooxidans: bacterial oxidation of the sulfur product layer increases the rate of zinc sulfide dissolution at high concentrations of ferrous ions[J]. Appl Environ Microbiol, 1999, 65(12): 5285-5292.
[59] FALCO L, POGLIANI C A. Comparison of bioleaching of covellite using pure cultures of Acidithiobacillus ferrooxidans and Acidithiobacillus thiooxidans or a mixed culture of Leptospirillum ferrooxidans and Acidithiobacillus thiooxidans[J]. Hydrometallurgy, 2003, 71: 31-36.
[60] KLAUBER C, PARKER A, WILHELM V B, WATLING H. Sulphur speciation of leached chalcopyrite surfaces as determined by X-ray photoelectron spectroscopy[J]. Int J Min Proc, 2001, 62: 65-94.
[61] HARMER S L, THOMAS J E, FORNASIERO D, GERSON A R. The evolution of surface layers formed during chalcopyrite leaching[J]. Geochim Cosmochim Acta, 2006, 70(17): 4392-4402.
[62] SCHIPPERS A, JOZSA P G, SAND W. Sulfur chemistry in bacterial leaching of pyrite[J]. Appl Environ Microbiol, 1996, 62(9): 3424-3431.
[63] HALLBERG K B, DOPSON M, LINDSTRO E B. Reduced sulfur compound oxidation by Thiobacillus caldus[J]. J Bacteriol, 1996, 178(1): 6-11
[64] STEUDEL R, HOLDT G, CHEM D, THOMAS G, HAZEU I W. Chromatographic separation of higher polythionates SnO [stack62?] (n = 3, ???, 22) and their detection in cultures of Thiobacillus ferroxidans; molecular composition of bacterial sulfur secretions[J]. Ang Chem Int Ed, 1987, 26(2): 151-153.
[65] MEULENBERG R, PRONK JT, HAZEU W, BOS P, KUENEN JG. Oxidation of reduced sulphur compounds by intact cells of Thiobacillus acidophilus[J]. Arch Microbiol, 1992, 157(2): 161-168.
[66] SUGIO T, KANAO T, FURUKAWA H, NAGASAWA T, BLAKE R C. Isolation and identification of an iron-oxidizing bacterium which can grow on tetrathionate medium and the properties of a tetrathionate-decomposing enzyme isolated from the bacterium[J]. Ferment Bioeng, 1996, 82(3): 233-238
������Ŀ�������ص�����о���չ�滮������Ŀ(2004CB619201)��������Ȼ��ѧ�������о�Ⱥ��������Ŀ(50321402)��������Ȼ��ѧ����������Ŀ(50674101)
�ո����ڣ�2007-11-05�������ڣ�2008-03-24
ͨѶ���ߣ��Ľ��������ڣ���ʿ���绰��0731-8836944��E-mail: jlxia@mail.csu.edu.cn
(�༭ ������)