��轵ĸ�ЧҺ��ɫ��ָ��ͼ��
¬��÷,������
(���ϴ�ѧ ��ѧ����ѧԺ,���� ��ɳ,410083)
ժҪ: ���ø�ЧҺ��ɫ��-���������м����������(HPLC-DAD)����ҩ��轵���˼����ܲ�����ȡҺ������ָ��ͼ���о����о��������:��������������Ƶ�Һ��ɫ��ָ��ͼ����ȡ�������к�ǿ��������,�������˼���ȡҺ��Һ��ɫ��ָ��ͼ��Ʒ�ֽ���ʶ��Ч���Ϻ�,����������ܲ�����ȡҺ��Һ��ɫ��ָ��ͼ�������������α��ʶ�����ģʽ�Ľ���;����,���ṩ����˼������ܲ��ص��������,��Ϊ���Է����Լ���ͬ�����з��ʶ���ṩ��һ�������ݡ�
�ؼ���: ���; ��ЧҺ��ɫ��; ��˼�; ����ܲ���; ָ��ͼ��
��ͼ�����:R282.5 ���ױ�ʶ��:A ���±��: 1672-7207(2005)02-0248-05
High Performance Liquid Chromatography Fingerprint of Fructus Lycii
LU Hong-mei, LIANG Yi-zeng
(School of Chemistry and Chemical Engineering, Central South University, Changsha 410083, China)
Abstract: The fingerprint of betaine and carotenoids extract of Fructus Lycii was studied using high performance liquid chromatography-diode array detector(HPLC-DAD). The results show that HPLC fingerprint for quality controlling of Fructus Lycii intensively depends on extraction method. For identifying different species of Fructus Lycii, the HPLC fingerprint of betaine extract is better than that of carotenoids extract, while the HPLC fingerprint of carotenoids extract contributes to telling true one from false one, and setting up common pattern of fingerprint of Fructus Lycii. Different ways should be chosen to deal with concrete problem in quality control of Traditional Chinese medicines. And the Ultraviolet spectra of betaine and carotenoids extract of Fructus Lycii were given, which provided basis for identifying peaks in different samples and qualitative analysis.
Key words: Fructus Lycii; HPLC; betaine; carotenoids; fingerprint
���(Fructus Lycii)��Ϊһ�ִ�ͳ������ҩ��,�ڹ�������ȫ���緶Χ�ڵõ����൱�㷺��Ӧ�á��ִ�ҩ��ѧ�о���Ϊ,��轾�����������ߡ���ͻ�䡢��˥�ϡ�����������ƣ�͡���Ŀ�Լ�����Ѫ֬�͵��̴��ȹ��ܡ��������70~80��[1-3],��ζ�����зֱ�ѡ��,Ŀǰ��û��һ�ֿ�ѧ�ķ����������ٵȽ�������ӵ�ԭ��״��������Ϲ���Ϊ4��[4],����������ԭ��״������������ӵķ�������������Ӱ�졣�������о�����DNA������ϸ����̬ѧ�Լ�������ȷ��������������зֱ�[5],����Щ�����в����졣
Ŀǰ,���Ƕ���ҩ���������ƴ���Ƕ���ҩ�������е�ij����Ч�ɷֻ�ָ���Գɷֽ��ж��ԡ���������,���������ַ���������ȫ��ط�ӳ��ҩ������������ҩָ��ͼ���Ƕ�ij����ҩ�Ļ��г�ҩ���ʵ�������,����һ���ķ����ֶ�,�õ��ܹ���ʾ����ҩ�Ļ��г�ҩ���Ե�ɫ�����ͼ�ס���ҩָ��ͼ����2���ص�:һ��ͨ��ָ��ͼ��������,����Ч������Ʒ����α�����;����ͨ��ָ��ͼ����Ҫ�����������������ȷ��,����Ч���Ʋ�Ʒ������,ȷ����Ʒ���������һ�¡�Ŀǰ,ָ��ͼ���ѳ�Ϊ���ʹ��ϵĿ�����ҩ����Ȼҩ������������Ч�ֶΡ��ڴ�,��������轵���Ҫ���Գɷ�[6]�е�����ܲ��ء���˼����ȡҺΪ��������轵Ļ�ѧָ��ͼ����̽�֡�
1 ʵ ��
1.1 �������Լ�
��Ҫ������:Agilent 1100 HPLC-DAD ϵͳ,�������������������ѹ�ݶȱá����������м����(DAD),HP Chemstationɫ����վ��
��Ҫ�Լ���:����(ɫ�״�);���ȼ���(ɫ�״�);�״�������ૡ�ʯ���Ѻ�̼��þ(��Ϊ������); �������1(L Chinense Mill,�ҹ���Ҫ��Ұ����,�ձ�ҩ�佫��涨Ϊ��Ʒ���)���������2(Lycium barbarum L,�ҹ���Ҫ����������,�й�ҩ��2000����1���涨��Ϊ��Ʒ���),����۽����ѧ�ṩ;�������3�������³�����ҵ��˾���ز��ֲ�����轡�
1.2 �����Ʊ�
1.2.1 ��˼���ȡҺ���Ʊ�
��˼����ȡ����������[7-12],ȡ0.2 g���������,����20 mL�״�,�������³�����30 min,��3000 r/min���ٶ�����3 min,�������ü״��ظ���ȡ3�Ρ���ѹŨ��,ˮ�ܽⶨ�ݡ���0.45 ��m����Ĥ,��Ϊ��轵���˼���ȡҺ����Ʒ��
1.2.2 ����ܲ�����ȡҺ���Ʊ�
����ܲ��ص���ȡ����������[13-18],ȡ10.0 g���������1.0 g̼��þһ�����,����50 mL����ૺͼ״����Һ(�����Ϊ1��1),������15 min ,��3000 r/min���ٶ�����6 min,����50 mLʯ����(�г�30~60 ��)��50 mL�����Ȼ�����Һ,���÷ֲ�,����ʯ�����ظ���ȡ2��,�ռ��ϲ���Һ,��35 ���ѹ����,����ö��ȼ����ܽⶨ�ݡ���0.45 ��m ����Ĥ,��Ϊ��轵�����ܲ�����ȡҺ����Ʒ��
1.3 ��������
1.3.1 ��˼���ȡҺ�ķ���
ɫ����ΪAgilent Zorbax NH2����(��ߡ�ֱ��Ϊ250 mm��4.6 mm,��������Ϊ5 ��m);������Ϊˮ-������Һ(�����Ϊ15��85),����Ϊ1.0 mL/min,���ݶ�ϴ��,�¶�Ϊ20 ��,�����Ⲩ��Ϊ190~380 nm,������Ϊ10 ��L��
1.3.2 ����ܲ�����ȡҺ�ķ���
ɫ����ΪHypersil ODS C18��(��ߡ�ֱ��Ϊ250 mm��4.0 mm,��������Ϊ5 ��m),������Ϊ����-���ȼ�����Һ(�����Ϊ60��40),����Ϊ1.0 mL/min, ���ݶ�ϴ��,�¶�Ϊ20 ��,����ɼ���Ⲩ��Ϊ360~780 nm,������Ϊ10 ��L��
2 ʵ����
2.1 ��˼���ȡҺ��ָ��ͼ����
��Ⲩ��Ϊ195 nmʱ,3����������˼���ȡҺ��ɫ��ͼ��ͼ1��ʾ����ͼ1�ɼ�,����1������2������3��ɫ�����ϴ�,������2������3�ķ����һ��,��ָ��ͼ��������һ��,���,�ɶ��Ե���Ϊ����2������3ͬ��һ��Ʒ�֡�
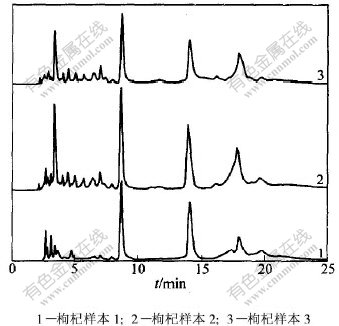
ͼ 1 �����˼���ȡ���ɫ��ͼ
Fig. 1 Chromatogram of betaine extract of Fructus Lycii
��Ե�������ɫ������˵,��ЧҺ��ɫ��-���������м����������(HPLC-DAD)��������Ϊ��ά����,������ͬʱ�����˹�����ɫ����Ϣ���������ṩ��ѧ���ʵĴ���������Ϣ,��ɫ���������ṩ������Ϣ����Ȼ,����������Ƶú�,��ѧ���ʵı���ʱ��Ի�ѧ���ʵĶ���Ҳ�Ǻ��а�����,����,��ָ��ͼ���о���,������������,����ʵ������֮�����ȫ��Ư�ƻ���������,�������Dz�������ά�����еĹ�����Ϣ��Ϊָ��ͼ���о��ṩ���µ���Ϣ��
ͼ2��ʾΪ����2��ɫ����������,���а���17����,ͼ3��ʾΪ��˼���ȡ��ɫ����12������������,��Ϊ��˼�Ķ��Թ����ṩ�����������ݡ�
2.2 ����ܲ�����ȡҺ��ָ��ͼ����
��Ⲩ��Ϊ456 nmʱ,3���������������ܲ�����ȡҺ��ɫ��ͼ��ͼ4��ʾ��
��ͼ4�ɼ�,3������������ܲ�����ȡҺ��ɫ��ͼ������,���ݱ�ʵ���ҵ���ҩָ��ͼ����������������,�������Դ���90%��������Ϊ��7��������轵Ĺ��з��������,���,�ɽ��������ܲ�����ȡ���HPLCͼ��Ϊָ��ͼ����ҩ����α�ļ�����
������1Ϊ��,ͼ5��ʾΪ����ܲ�����ȡҺ��ɫ��;ͼ6��ʾΪ����������ܲ�����ȡҺ��ÿ�����������ס�

ͼ 2 ��˼���ȡҺ��ɫ��ͼ
Fig. 2 Chromatogram of betaine extract of Fructus Lycii
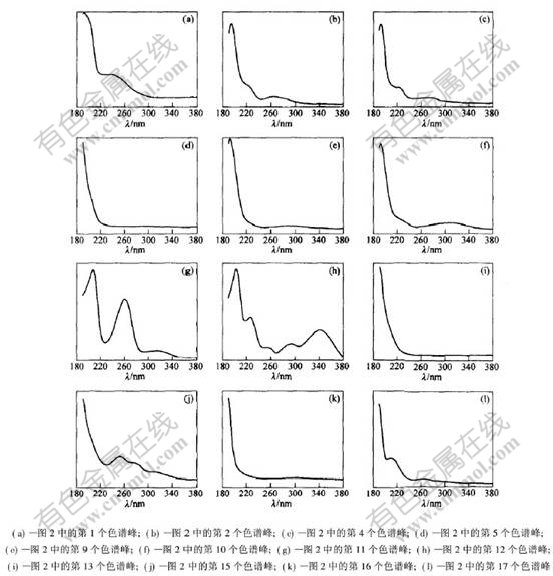
ͼ 3 ��˼���ȡҺ���������
Fig. 3 UV spectra of betaine extract of Fructus Lycii
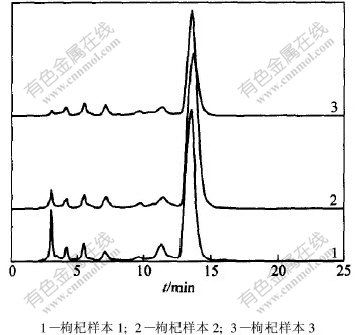
ͼ 4 �������ܲ�����ȡ���ɫ��ͼ
Fig. 4 Chromatogram of carotenoids extract of Fructus Lycii

ͼ 5 ����ܲ�����ȡҺ��ɫ��ͼ
Fig. 5 Chromatogram of carotenoids extract of Fructus Lycii
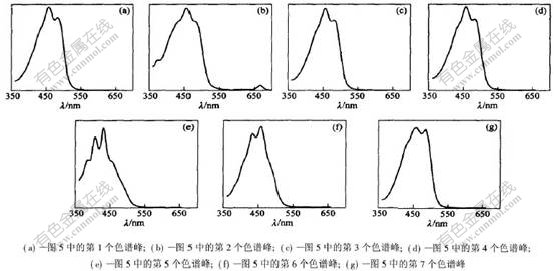
ͼ 6 ����ܲ�����ȡҺ���������
Fig. 6 UV spectra of carotenoids extract of Fructus Lycii
3 �� ��
�����2����ȡ�������õ�ɫ��ָ��ͼ������,�������ܲ�����ȡҺ�������õ�ָ��ͼ��֮������С(��ͼ4),˵������������ȡ�������ҳ���轵������Է�,Ϊ��Ч������Ʒ����α�ṩ��һ��������;����,��ָ��ͼ���о��ij�����,�轨��ҩ�ĵIJ�ͬ������ҩ��ָ��ͼ����ģʽ����ͼ4���Կ���,��轵Ĺ��з������,���,�������ַ�����������ģʽ�����ס�����������ȡҺ����Ʒ��ָ��ͼ�ײ���ܴ�(��ͼ1),�����÷�ӳ����轸�����֮��IJ��졣���,����˼���ȡҺ����载��������ļ�����������ܲ�����ȡҺ����载����������������ʡ���ͼ1�ɿ���,����˼���ȡҺָ��ͼ��Ҫ����һ�����ָ��ͼ�Ĺ���ģʽ�Ƿdz����ѵġ���������������������ȱ����Ҫ�����ݻ��۵������,ͨ����������ģʽ,�ƶ������������Ա�,����˼���ȡҺ���з���,�������൱������,����������ܲ�����ȡҺ��ָ��ͼ����Ժ�����
�����ָ��ͼ���о�����,����һ�̶ֹ�����ȡ�����ͷ�����������ָ��ͼ���о�����һ����ȱ�ݡ���Ϊ���ò�ͬ��ȡ�������õ���ָ��ͼ���ܴӲ�ͬ���淴ӳ��ҩ�ĵ�����,�Ӷ�������ȫò,������ÿһ��ָ��ͼ��������Ӧ����������1��ָ��ͼ��һ����ѷ�ӳһ��ҩ�ĵ���������,���ܽ���о���������һϵ�����⡣
4 �� ��
a. ��ҩ��轵�Һ��ɫ��ָ��ͼ����ȡ�������к�ǿ��������,�������˼���ȡҺ��Һ��ɫ��ָ��ͼ����Ʒ�ֵ�ʶ��Ч���Ϻ�,����������ܲ�����ȡҺ��Һ��ɫ��ָ��ͼ�������������α��ʶ�����ģʽ�Ľ�����
b. ��ЧҺ��ɫ������һ����Ҫ����ҩָ��ͼ���о�����,������ʵ��Ӧ����,����һ�̶ֹ�����ȡ�ͷ�����������ָ��ͼ���о�,ȱ����ѧ�ԡ����,�ڽ�����ҩָ��ͼ���о�ʱ,��θ��ݾ�������ѡ��ͬ��������ָ��ͼ��,��ָ��ͼ���о��б����������⡣
�����:
[1]TATSUYA F, JUN Y, HIROYOSHI O. Phylogeny and Biogeography of the Genus Lycium(Solanaceae): Inferences from Chloroplast DNA Sequences[J]. Molecular Phylogenetics and Evolution, 2001,19(2):246-258.
[2]BERNARDELLO L, LUJ�BN M C. Pollen Morphology of Tribe Lycieae: Grabowskia, Lycium, Phrodus(Solanaceae)[J].Review of Palaeobotany and Palynology,1997,96(3):305- 315.
[3]�ν�,�ִ�̩,������. ��轹�ʵ��ѧ�ɷ��о��ſ�[J]. �й�Ұ��ֲ����Դ,1997,16(1):8-11.
HE Jin, YAN Chun-tai, LIANG Yun-xiang. A Review of Studies on Ingredient of Fructus Lycii[J]. Chinese Wild Plant Resources, 1997, 16(1):8-11.
[4]������,������,������,��. ���������ԭ��״��FTIR��������[J]. ����ѧ�������, 2001, 20(6): 787-789.
SUN Su-qin, WANG Mi-qu, LIANG Xi-yun, et al. A Rapid Method for the Identification of four Different Features of Gouqizi by FTIR Spectrometry[J]. Spectroscopy and Spectral Analysis, 2001, 20(6): 787-789.
[5]����,������,������,��. ���������ֲ��ĺ���ָ��ͼ��������ټ����о�[J].����ѧ�������, 2004, 24(6): 679-681.
PENG Yong, SUN Su-qin, ZHAO Zhong-zhen, et al. A Rapid Method for Identification of Genus Lycium by FTIR Spectroscopy[J]. Spectroscopy and Spectral Analysis, 2004, 24(6): 679-681.
[6]����,����,������. ��轼���轶����о�(��)[J]. ʳƷ��ѧ,1996,17(9):9-12.
LI Zhong, LUO Qiong, ZHANG Sheng-hua. The Study in Fructus Lycii and Lycium Barbarum Polysaccharides[J]. Food Science, 1996,17(9):9-12.
[7]YOUNG G S, KYUNG H C, JONG M K, et al. Determination of Betaine in Lycium Chinense Fruits by Liquid Chromatography-electrospray Ionization Mass Spectrometry[J]. Journal of Chromatography A, 1999, 857(2):331-335.
[8]MAR H M H, RIDKY W T, GARNER C S, et al. A Method for the Determination of Betaine in Tissues Using High Performance Liquid Chromatography[J]. Journal of Nutritional Biochemistry, 1995, 6(7): 392-398.
[9]EICHENBERGER W, GRIBI C, GFELLER H, et al. Gas Chromatographic-mass Spectrometric Identification of Betaine Lipids in Chroomonas Salina[J]. Phytochemistry, 1996, 42 (4): 967-972.
[10]KATO M, SAKAI M, ADACHI K, et al. Distribution of Betaine Lipids in Marine Algae[J]. Phytochemistry, 1996, 42(5): 1341-1345.
[11]WOOD V K, BONHAM C C, MILES D, et al. Characterization of Betaines Using Electrospray MS/MS[J]. Phytochemistry, 2002, 59(7): 759-765.
[12]K�aNZLER K, EICHENBERGER W. Betaine Lipids and Zwitterionic Phospholipids in Plants and Fungi[J]. Phytochemistry, 1997, 46(5):883-892.
[13]HART J D, John K S. Development and Evaluation of an HPLC Method for the Analysis of Carotenoids in Foods, and the Measurement of the Carotenoid Content of Vegetables and Fruits Commonly Consumed in the UK[J]. Food Chemistry, 1995, 54(1):101-111.
[14]JORDI O, ANDREU P. Chromatographic Determination of Carotenoids in Foods[J]. Journal of Chromatography A, 2000, 881(2): 543-555.
[15]RODRIGUEZ-AMAYA B D. Some Considerations in Generating Carotenoid Data for Food Composition Tables[J]. Journal of Food Composition and Analysis,2000, 13(4): 641-647.
[16]SU Qing, ROWLEY K G, BALAZS D H N. Carotenoids: Separation Methods Applicable to Biological Samples[J]. Journal of Chromatography B, 2002, 781(2): 393-418.
[17]DAVOLI P, WEBER W S R. Identification and Quantification of Carotenoid Pigments in Aeciospores of the Daisy Rust Fungus, Puccinia Distincta[J]. Phytochemistry, 2002, 60(3): 309-313.
[18]BURNS J, FRASER D P, BRAMLEY M P. Identification and Quantification of Carotenoids, Tocopherols and Chlorophylls in Commonly Consumed Fruits and Vegetables[J]. Phytochemistry, 2003, 62(6): 939-947.
�ո�����:2004-04-26
������Ŀ:������Ȼ��ѧ����������Ŀ(20235020, 20175036),����ʡ��Ȼ��ѧ����������Ŀ(04JJ3081)
�����:¬��÷ (1976-),Ů,����������,��ʿ�о���,������ҩָ��ͼ����Ч�о�
������ϵ��: ¬��÷,Ů,��ʿ�о���;�绰: 0731-8830824;E-mail: lu_hongmei225@126.com