����������������Ƥ������������Cu2+������
������1, 2����ѧ��1���� ɯ1�����컪1
(1. ���ϴ�ѧ ұ���ѧ�빤��ѧԺ������ ��ɳ��410083��
2. ����ҽѧԺ ����ѧԺ������ ������750004)
ժ Ҫ���������������Ƥ(OP)Ϊԭ�ϣ����Ҵ����������ƺ��Ȼ��ƴ������õ�2�ָ�������Ƥ����������SOP��SCOP�������������ڶ�Cu2+���������о���ҺpHֵ������������������ʱ���Cu2+��ʼ����Ũ�ȶ�SOP��SCOP�������ܵ�Ӱ�졣���������Cu2+������Ƥ�����������ϵ��������ʿ죬��������������ѧ����������SOP��SCOP��Cu2+�����������߷���Langmuirģ�ͣ�����Langmuirģ�ͼ���SOP��SCOP�������������ֱ�Ϊ50.17 mg/g��72.73 mg/g, ����δ���Ե�OP����������(44.28 mg/g)�����Ժ������Ƥ�������������������ظ�ʹ��5�����ϡ�����Ƥ�������Դ�����ѧ�ȶ�����ߣ�����������ǿ�����������õ�Cu2+��������
�ؼ��ʣ�����Ƥ��Cu2+����ѧ���ԣ�����
��ͼ����ţ�X703.1 ���ױ�ʶ�룺A ���±�ţ�1672-7207(2009)04-0857-06
Adsorption of Cu2+ by saponified and cross-linked orange peel
FENG Ning-chuan1, 2, GUO Xue-yi1, LIANG Sha1, TIAN Qing-hua1
(1. School of Metallurgical Science and Engineering, Central South University, Changsha 410083, China;
2. School of Basic Medical Science, Ningxia Medical College, Yinchuan 750004, China)
Abstract: Two kinds of biosorbents (SOP and SCOP) were prepared by treating orange peel (OP) with ethanol, sodium hydroxide and calcium chloride and were used to adsorb Cu2+ from aqueous solution. Equilibrium isotherms and kinetics were obtained and the effects of solutions pH, biosorbent dosage, adsorption time and initial Cu2+ concentration were studied in batch experiments. Equilibrium was well described by Langmuir isotherms and kinetics was found to fit pseudo-second order type adsorption kinetics. According to the Langmuir equation, the maximum adsorption capacities of SOP and SCOP for Cu2+ are 50.17 and 72.73 mg/g, respectively, which are higher than untreated OP (40.28 mg/g). The loaded biosorbent is regenerated using HCl solution and can be used repeatedly for five times with little loss of adsorption capacity. The results show that additional chemical treatments of the orange peel by ethanol, sodium hydroxide and calcium chloride increase the adsorption capacity of Cu2+.
Key words: orange peel; Cu2+; chemical treatment; adsorption
������ɫ������ҵ�ķ�չ���ؽ�����Ⱦ�������ء������е��ؽ�������ͨ������;��������ˮ�壬����ˮ���и����������ĸ�����������ˮ��������壬�����˵Ľ�������Σ������ȥˮ���ؽ������ӵķ����ܶ࣬���õ���������������������ӽ������ͻ���̿�������ȡ���ʮ�������������о�����̽���������۸�Ч����������������ࡢ���ࡢ��ũҵ������������ؽ�����ˮ��Ⱦ[1-2]��������������һ�����˵���������ˮ�������������������۵�������϶��ؽ��������������������˵�Ũ���ؽ�����ˮ�Ĵ���[3]�����Ҿ����������ߣ������ٶȿ���ŵ㡣��������������������һ�֣������зḻ�Ĺ�������ά�ء�����ά�صȶ�����߷��ӻ������ľ����[4]��������Щ���ӱ��溬�д����ǻ����Ȼ��Ȼ��Թ����ţ�����ͬ�ؽ�������ͨ�����ӽ��������ϵȷ�ʽ��ϣ��Ӷ���������Һ���ؽ������ӵľ�����Ϊ�������ø�������������ʣ�������ѧ�߽����������о�[5-8]��P��rez-Ma??n ��[6]�ø�������ȥˮ��Һ�е��ӣ�Ajmal��[8]������Ƥ��ȥ��ˮ�е�������ֱ�Ӳ��ø����������������������������ϵ͡����ڿ������л����ʵ��ܽ������ˮ�л�ѧ���������ӵ�����[9-10]��
�����������о���ͨ�����������ữ�������ȷ� ��[11, 13]���Ը��������и��Դ�����ʹ����Թ����ŵ���Ŀ��ߣ�ȥ���������ӵ�������ǿ���о��������Ը������ȷ������ʽ��л�ѧ���ԣ����Ը������ǵ�������ѧ���ܣ���߶��ؽ����������������ڴˣ���������������ƤΪ���壬���Ҵ����������ƺ��Ȼ��ƴ������õ���2�ָ�������Ƥ����������SOP��SCOP�������������ڶ�Cu2+��������ͨ��ʵ��Ƚ�δ����������Ƥ��������Ƥ���ȶ����Լ�����ˮ��Һ��Cu2+���������о�Cu2+�ڸ�������Ƥ�����������ϵ���������������ƽ��ʱ�䡢��ʼŨ�ȵȶ�����������Ӱ�죬����������������ѧ�����·��̡�
1 ʵ ��
1.1 �������Լ�
����Ϊ��ASAP 2010ȫ�Զ�������(���� MICROMER ITICS)��JSM-5600LVɨ���������(�ձ�����)������130Bԭ�����շֹ��ȼ�(��������)��PHS-3C��ȼ�(�Ϻ��״�)��SHA-Cˮԡ��������(�����ٻ�)�������ظ���ط��ⶨ��������ѧ������(COD)��
�Լ�Ϊ��CuSO4��5H2O��HCl��NaOH�ȣ���Ϊ��������
1.2 ��������Ƥ�������������Ʊ�
1.2.1 δ�����ĸ�����Ƥ(OP)
����Ƥ(OP)������ˮ������ˮϴ������80 �����������㶨�����飬����Ϊ420 ��m��ɸ������ ���á�
1.2.2 ��ˮ�Ҵ�-NaOH����������Ƥ������(SOP)
ȡ50 g OP��250 mL��ˮ�Ҵ���125 mLŨ��Ϊ0.5 mol/L��NaOH��Һ��125 mLˮ��ϣ����ݲ����裬24 h��ˮϴ��pHֵ�����ԣ����Ĺ��ˣ���70 ����24 h����������SOP��
1.2.3 ��ˮ�Ҵ�-NaOH-CaCl2����������Ƥ������(SCOP)
ȡ50 g OP��250 mL��ˮ�Ҵ���125 mL 0.5 mol/L NaOH��125 mL 1.6 mol/L CaCl2��Һ��ϣ����ݲ����裬24 h��ˮϴ��pHֵ�����ԣ����ˣ���70 ����24 h����������SCOP��
1.3 ʵ�鷽��
��100 mL��ƿ�м���������������Cu2+��Һ25 mL���ܱ�ƿ���Է�ʵ�����������仯���������ˮԡ����������ÿ��20~30 min��0.1 mol/L HCl��0.1 mol/L NaOH������ҺpHֵ����֤�������ȶ���pHֵ�½��С���Ԥ��ʱ�䣬���ķ��벢���ˣ���ԭ�����շֹ��ȼƲⶨ��Һ��Cu2+ƽ��Ũ�ȡ�����ʽ������������

1.3.1 pH����
ȡCu2+����Ũ��Ϊ50 mg/L����Һ25 mL����0.10 g������, ����Cu2+��Һ��pHֵ�ֱ�Ϊ2.5��3.5��4.5��5.0��5.5��6.0����25 �������2 h�����ķ��룬�ⶨ��Һ��Cu2+����Ũ�ȡ�
1.3.2 ��������������
ȡCu2+����Ũ��Ϊ50 mg/L����Һ25 mL���ֱ����0.050��0.075��0.100��0.125��0.150 g������, ����Cu2+��Һ��pHֵΪ5.3����25 �������2 h�����ķ��룬�ⶨ��Һ��Cu2+����Ũ�ȡ�
1.3.3 ����ѧ����
ȡCu2+����Ũ��Ϊ50 mg/L����Һ25 mL����0.10 g������, ����Cu2+��Һ��pHֵΪ5.3����25 �������ͬʱ���(0~120 min)�����ķ��룬�ⶨ��Һ��Cu2+����Ũ�ȡ�
��������������ѧ���о��У�ͨ����һ���Ͷ�������ѧ���̶��������ݽ���ģ�⣬����������������Ũ��������ʱ��ı仯��ϵ����������ѧ���̵����Ա���ʽΪ��
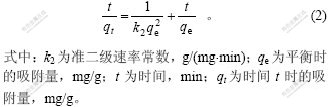
1.3.4 ������������
ȡCu2+����Ũ��Ϊ25~800 mg/L����Һ25 mL����0.10 g������, ����Cu2+��Һ��pHֵΪ5.3����25 �������2 h�����ķ��룬�ⶨ��Һ��Cu2+����Ũ�ȡ�
��Langmuir��Freundlich���̶�ʵ�����ݽ���ģ�⡣Langmuir����Ϊ��
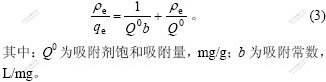 Q0��b�ɷֱ��ɦ�e/qe�Ԧ�e��ֱ�߷��̵�б��(1/Q0)�ͽؾ�(1/(Q0b))�����
Q0��b�ɷֱ��ɦ�e/qe�Ԧ�e��ֱ�߷��̵�б��(1/Q0)�ͽؾ�(1/(Q0b))�����
Freundlich������
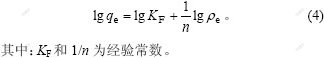 n��KF�ֱ���lg qe��lg ��e��ֱ��б��(1/n)�ͽؾ�(lg KF)�����
n��KF�ֱ���lg qe��lg ��e��ֱ��б��(1/n)�ͽؾ�(lg KF)�����
1.3.5 ������ʵ�鷽��
���ﵽ����ƽ�����������������Һ���ķ��룬���������м���25 mL 0.1 mol/L HCl��������3 h�����ˣ��ⶨ��Һ��Cu2+����Ũ�ȡ�������������ˮϴ�����ԣ���ɡ��������������������ʹ�á�
2 ���������
2.1 ��������������
ͼ1��ʾΪOP��SOP��SCOP��SEM����ͼ1�ɿ�����OP��SOP��SCOP�ı����϶����������SOP��SCOP�ı����δ���Ե�OP�ֲڡ����ɶ���ף����ֱ���ṹ���������������̵Ľ��С���BET�����OP��SOP��SCOP�ıȱ�������ֱ�Ϊ0.83��1.17��1.49 m2/g��

(a) OP; (b) SOP; (c) SCOP
ͼ1 OP��SOP��SCOP��SEM��
Fig.1 SEM images of OP(a), SOP(b) and SCOP(c)
2.2 ����Ƥ���Դ�����Cu2+�������ܵ�Ӱ��
������OP��SOP��SCOP��Cu2+������Ч�����������1���������������Ƥ���Ժ��Cu2+��ȥ������ߣ�������Ϊ�����Ҵ����������ƺ��Ȼ��ƵĴ����������������������Ŀ�϶�ʺͱȱ���������˸���Ļ���λ�㡣����Ƥ��������ά�ء�����ά�صȸ߷��������⣬�����зḻ�Ĺ�������������Ҫ���Ϊ������ȩ�ᣬ���в����Ȼ����������������������ƺ��Ȼ��ƵĴ������������İ�����ȩ�ᱻ����[14]���Ȼ�����Ŀ���ӣ�����������ߡ����⣬�����Ե�SOP��SCOP���������Һ����ɫ��������dz��ɫ������δ���Ե�OP���������Һ������ԵĻ�ɫ���Ҿ�SOP��SCOP��������Һ�Ļ�ѧ������COD��OP���������ҺCOD�����½���������Ϊδ����OP�ڽ�����Һ�н���ʱ���д�����ɫ�����ʼ��������л���������������Һ��COD�ܸߣ������Ե�SOP��SCOP��ɫ�������Լ��������л����ھ��Ҵ����������ƺ��Ȼ��ƴ��������дֱ���ȥ��ʹ�������Ļ�ѧ�ȶ�����ߣ�COD�������͡�
��1 ����Ƥ���Դ���������Cu 2+��Ӱ��
Table 1 Effects of orange peel pretreatment on Cu2+ adsorption
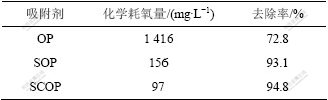
ע��pHֵΪ5.3�������¶�25 �棬��������Ϊ4 g/L������ʱ��Ϊ2 h����ʼCu2+����Ũ��Ϊ50 mg/L��
���Ҵ�-NaOH����������Ƥ������SOP�뾭�Ҵ�-NaOH-CaCl2����������Ƥ������SCOP��Ȼ����ͬ�����¶�50 mg/L Cu2+��Һ����������������ͬ����SCOPʹ������Һ��COD���ͣ���ѧ�ȶ��Ը�ǿ���������������Ʊ������У�SCOP��SOP����ϴ�Ӵ�����
2.3 ���(pH)��������Ӱ��
ͼ2��ʾΪ��ҺpHֵ��OP��SOP��SCOP�������ܵ�Ӱ�졣���Կ�����pHֵ��OP����������Ӱ��ϴ���SOP��SCOP��������Ӱ���С������ҺpHֵ�ϵ�ʱ�����������͡���pHֵ��2.5����4.5ʱ������������֮���ӡ��Ժ�����pHֵ�ļ�����������������������(SCOP)�����Ӻ���(SOP)��OP���������������pHֵΪ5.0ʱ���˺���pHֵ���ӣ������������������͡���������Ϊ�ϵ�pHֵ��H+������Ũ�Ⱥͻ�Խϸߣ����������������γ��˾����������Ӷ��������ϵ�[8]������pHֵ������H+������Ũ�Ƚ��ͣ���¶������Ĵ�����ɵĻ��ţ������ڽ�����������Ũ�Ƚӽ��������ڻ���λ����[15]��
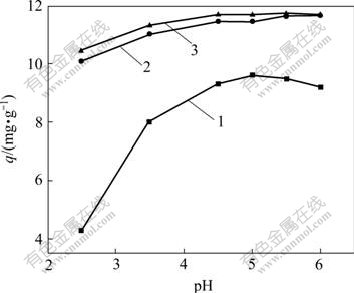
1��OP; 2��SOP; 3��SCOP
�����¶�Ϊ25 �棬��������Ϊ4 g/L������ʱ��Ϊ2 h��
��ʼCu2+����Ũ��Ϊ50 mg/L
ͼ2 pHֵ��Cu2+������Ӱ��
Fig.2 Effects of pH on adsorption of Cu2+
2.4 ����������������Ӱ��
ͼ3��ʾΪOP��SOP��SCOP�ļ�������������Ӱ�졣���Կ���������������Ͷ���������ӣ����������ӡ������������ﵽ4 g/L������������������ʱ�������������������������������ӣ������������͡������������������������ʹ��Һ���������������࣬����λ�����࣬�����������ߣ�����������������Ҳ�����������������žۣ���С������������������⣬�ڸ�����������Ũ���£����ӵ������Ҳ����ʹһЩ�������������Ͻ�Ϊ��ɢ�Ľ������ӽ���[16]������������������͡�����[17-18]��Ҳ�����ƵĽ������ʵ��ѡ����������Ϊ4 g/L��

1��OP; 2��SOP; 3��SCOP
pHֵΪ5.3�������¶�Ϊ25 �棬����ʱ��Ϊ2 h��
��ʼCu2+����Ũ��Ϊ50 mg/L
ͼ3 ����������������Ӱ��
Fig.3 Effects of biosorbent dosage on adsorption of Cu2+
2.5 ��������ѧ
��25 ��ʱ��������������ʱ��ı仯��ͼ4�����Կ�����OP��SOP��SCOP���������ʺܿ죬��20 min�ڻ����ﵽ����ƽ�⡣������������������ʱ��ѡΪ2 h����ȷ���ﵽ����ƽ�⡣
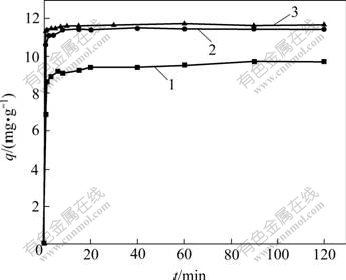
1��OP; 2��SOP; 3��SCOP
pHֵΪ5.3�������¶�Ϊ25 �棬������Ϊ4 g/L��
��ʼCu2+����Ũ��Ϊ50 mg/L
ͼ4 Cu2+����������ѧ����
Fig.4 Adsorptions kinetics curves of Cu2+
����������ѧ���̶��������ݽ���ģ�⣬�������2���ӱ�2���Կ��������������Ժܺõ�����������ѧ���̽���ģ�⣬���ϵ������0.999 8���ϣ���qe��ʵ��ֵ������ֵ����С�����ʾ����������ѭ������Ӧ�������������ʱ���ѧ����������[19]��
��2 ������Ӧ����ѧ����
Table 2 Kinetic parameters of pseudo-second-order equation for Cu2+ adsorption

2.6 ������������
ͼ5��ʾΪ25 ��ʱ��OP��SOP��SCOP�ĵ����������ߡ����Կ���������������Һ��Cu2+����Ũ�ȵ����Ӷ����ӣ��������ﵽ����ƽ�⡣��Langmuir�� Freundlich��������ģ�Ͷ�ͼ5�����ݽ���ģ�⣬�������3���ɱ�3�ɿ�����OP��SOP��SCOP��Cu2+������������Langmuirģ�͡�Langmuir��������ʽ�ǵ����Ӳ�����ģʽ����ʾ�������������Խ������ӵ������Ի�ѧ����Ϊ����������״̬�����ڵ�������[20]������Langmuir��������ʽ����OP��SOP��SCOP�ı����������ֱ�Ϊ44.28��50.17��72.73 mg/g����Ȼ����ѧ���Ժ������������Ķ�ס����ɽṹΪ�����ķ����ṩ�˾�ı������ʹ�ڶ������λ������������ӽӴ��Ļ��ᣬʹ��������Ѹ�ٷ���������λ�����ӣ�ʹ���Cu2+������������ǿ�����������������Ʊ������У��Ȼ��Ƶļ���ʹ��SCOP������������SOP�ı������������ߣ�������Ǹ����ӵĴ���ʹ���Գɷְ�����ȩ����ܽ�Ƚ��͡�
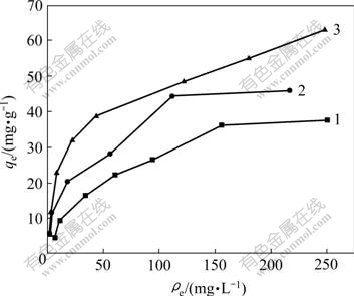
1��OP; 2��SOP; 3��SCOP
pHֵΪ5.3�������¶�Ϊ25 �棬��������Ϊ4 g/L��
����ʱ��Ϊ2 h
ͼ5 Cu2+��������������
Fig.5 Adsorptions isotherms curves of Cu2+
��3 Langmuir��Freundlich���̵IJ��������ϵ��
Table 3 Conform parameters of Langmuir and Freundlich equation

2.7 ��������
�о���������Cu2+��SOP��SCOP���������������Ѿ�����Cu2+����������������0.1 mol/L��HCl��Һ�У���3 h�����ˣ������������������ȥ����ˮϴ�����ԣ���ɣ�����ʹ�ã������ͼ6����ͼ6�ɿ�����������������������������������飬�����������ͺ��٣������Ժ�����Ƥ���������ٿ���ѭ��ʹ��5�����ϡ�

pHֵΪ5.3�������¶�Ϊ25 �棬��������Ϊ4 g/L��
����ʱ��Ϊ2 h����ʼCu2+����Ũ��Ϊ50 mg/L
ͼ6 SOP��SCOP������-�Ѹ�ѭ��ʵ����
Fig.6 Adsorption-desorption cycles results of SOP and SCOP
3 �� ��
a. �Է�����������ƤΪ���壬���Ҵ����������ƺ��Ȼ��ƴ������õ���2�ָ�������Ƥ����������SOP��SCOP���ȱ�����ⶨ����ò�������������SOP��SCOP��δ���Ե�OP�������ɡ���ף��и���ıȱ���������������ڶ�Cu2+��������ȥ������ߣ���ѧ�ȶ�����ǿ�������ǿ��������ظ�ʹ�ã����������õ���������
b. ��ҺpHֵ��Ӱ��������������Cu2+��������Ҫ���أ��������pHֵΪ5.0~5.5��Cu2+�������������ϵ��������ʿ죬20 min�ʹﵽ����ƽ�⡣��������ѧ��������������ѧ���̺ܺõ����������������߽����������Langmuir�������Ч��������Freundlich�������Ч��������Langmuir���̼����OP��SOP��SCOP�ı����������ֱ�Ϊ44.28��50.17��72.73 mg/g��
�ο����ף�
[1] Ozsoy H D, Kumbur H. Adsorption of Cu(��) ions on cotton boll[J]. Journal of Hazardous Materials B, 2006, B136: 911-916.
[2] Ma W, Tobin J M. Determination and modelling of effects of pH on peat biosorption of chromium, copper and cadmium[J]. Journal of Biochemistry Engineering, 2004, 18(1): 33-40.
[3] Wang X S, Qin Y. Equilibrium sorption isotherms for Cu2+ on rice bran[J]. Process Biochemistry, 2005, 40(2): 677-680.
[4] ����. ����Ƥ���ۺ�����[J]. ʳƷ�뷢��ҵ, 2005, 31(7): 145-146.
ZANG Yu-hong. Research on the extracting condition of useful substances from the orange peels[J]. Food and Fermentation Industries, 2005, 31(7): 145-146.
[5] Biswas B K, Inoue K, Ghimire K N, et al. The adsorption of phosphate from an aquatic environment using metal-loaded orange waste[J]. Journal of Colloid and Interface Science, 2007, 312(2): 214-223.
[6] P��rez-Mar��n A B, Zapata V M, Ortu?o J F, et al. Removal of cadmium from aqueous solutions by adsorption onto orange waste[J]. Journal of Hazardous Materials B, 2007, B139: 122-131.
[7] Annadurai G, Juang R S, Lee D J. Adsorption of heavy metals from water using banana and orange peels[J]. Water Science and Technology, 2003, 47(1): 185-190.
[8] Ajmal M, Rao R A K, Ahmad R, et al. Adsorption studies on Citrus reticulata (fruit peel of orange): removal and recovery of Ni(��) from electroplating wastewater[J]. Journal of Hazardous Materials B, 2000, B79: 117-131.
[9] Noeline B F, Manohar D M, Anirudhan T S. Kinetic and equilibrium modelling of lead(��) sorption from water and wastewater by polymerized banana stem in a batch reactor[J]. Separation and Purification Technology, 2005, 45(2): 131-140.
[10] Gaballah I, Goy D, Allain E, Kilbertus G, et al. Recovery of copper through decontamination of synthetic solutions using modified barks[J]. Metallurgical and Materials Transactions B, 1997, B28: 13-23.
[11] Dhakal R P, Ghimire K N, Inoue K. Adsorptive separation of heavy metals from an aquatic environment using orange waste[J]. Hydrometallurgy, 2005, 79(3/4): 182-190.
[12] ������, ��ѧ��, �� ɯ, ��. ����Ƥ��ѧ���Լ����Cu(��)���ӵ���������[J]. �й���ɫ����ѧ��, 2008,18(S1): 148-154.
FENG Ning-chuan, GUO Xue-yi, LIANG Sha, et al. Biosorption of Cu2+ on modified orange peel[J]. The Chinese Journal of Nonferrous Metals, 2008,18(S1): 148�C154.
[13] Li X, Tang Y, Xuan Z, Liu Y, et al. Study on the preparation of orange peel cellulose adsorbents and biosorption of Cd2+ from aqueous solution[J]. Separation and Purification Technology, 2007, 55(1): 69-75.
[14] Marshall W E, Johns M M. Agricultural by-products as metal adsorbents: sorption properties and resistance to mechanical abrasion[J]. Journal of Chemical Technology and Biotechnology, 1996, 66(2): 192-198.
[15] Aksu Z. Equilibrium and kinetic modelling of cadmium(��) biosorptions by C. vulgaris in a batch system: Effect of temperature[J]. Separation and Purification Technology, 2001, 21(3): 285-294.
[16] Monahar D M, Anoop Krishnan K, Anirudhan T S. Removal of mercury(��) from aqueous solutions and chlor-alkal industry wastewater using 2-mercaptobenzimidazole-clay[J]. Water Research, 2002, 36(6): 1609-1619
[17] ?zer A, ?zer D, ?zer A. The adsorption of copper(��) ions on to dehydrated wheat bran(DWB): determination of the equilibrium and thermodynamic parameters[J]. Process Biochemistry, 2004, 39(12): 2183-2191.
[18] Chen G , Zeng G , Tang L, et al. Cadmium removal from simulated wastewater to biomass byproduct of Lentinus edodes[J]. Bioresource Technology, 2008, 99(15): 7034-7040.
[19] ?zacar M, ?engil ? A. Adsorption of reactive dyes on calcined alunite from aqueous solutions[J]. Journal of Hazardous Material B, 2003, B98: 211-224.
[20] ������, ���Ƽ, �˿˼�. ���ӻ�ʣ����������Ⱦ�ϵ����ܼ�����[J]. ����ѧ��, 2007, 58(15): 1290-1295.
CUI Long-zhe, WU Gui-ping, DENG Ke-jian. Adsorption performance and mechanism of binding of dye by protonated coke waste[J]. Journal of Chemical Industry and Engineering (China), 2007, 58(15): 1290-1295.
�ո����ڣ�2008-09-15�������ڣ�2008-11-27
������Ŀ��������Ȼ��ѧ����������Ŀ(50774100)
ͨ�����ߣ���ѧ��(1966-)���У����ϳ�ɳ�ˣ����ڣ�������Դѭ���뻷�������о����绰��0731-88836207��E-mail: xyguo@mail.csu.edu.cn