DOI��10.19476/j.ysxb.1004.0609.2017.08.25
300 kA���������������������ܽ�ģ��
�� ï�������ã��� ������ Զ������Ԩ�������
(���ϴ�ѧ ��Դ��ѧ�빤��ѧԺ����ɳ 410083)
ժ Ҫ������������Ϲ����У��������������ȡ���顢�ܽⲢ�ܵ������봫���ܽ���Ƶ��ۺ����á�����OpenFOAM����ƽ̨����Ч�������������ܽ�Ŀ��ƻ��ƣ������������ú����Ϻ�ĵ�����¶���Ӧ���������������������������ȡ���������ܽ����ģ�ͣ�����Rosin-Rammler�ֲ������������Ϻ����������������������ֲ�����ʵ��300 kA���������������ܽ���̽�����ֵģ�⡣���������ǰ18 s�������ܽ�50%(��������)�����ڿ����ܽ�Σ�һ����������144 s������ʣ��Լ1.5%(��������)��������δ�ܽ⣬δ�ܽ�����ۼ������ڵ��۵ײ��γɳ������������������ܽ����ȵ�����£�������λ�õ�����¶���ǰ1 s�����½����������¶ȿ��ٻ�������60 s֮����������ơ�
�ؼ��ʣ���飻�������ܽ⣻���ȣ����ʣ������ֲ�����ֵģ��
���±�ţ�1004-0609(2017)-08-1738-10���� ��ͼ����ţ�TF821���� ���ױ�־�룺A
��������Ϊ����������е���Ҫԭ�ϣ����ܽ�����ɢ�Ŀ���ֱ�Ӿ����˵��յ��ȶ���[1]�����������۵�������ͻ���ϵ�л���������⼼�����豸����˸��ߵ�Ҫ���ر���300 kA��500 kA���������۵�Ӧ�ã��������߶���С�����������ܽ�����ɢ��Ϊ���ѣ������Ľ�鲻�ܼ�ʱ�ܽ���������۵ף���α�֤�������ܹ������Ϻ���ٵ��ڵ�������ܽ���ɢ������ؽ����������⡣
�������й�ҵ���ڵĸ���ǿ��ʴ�Ȳ����������ֳ�����ֱ���о���������ʵ�ʵ����е��ܽ���̣���Ҫ������������ʯӢ�۶����������ܽ���ɽ����о�[2-4]�����ż���������ѧ�ط�չ��Ŀǰ������һЩѧ�߿�ʼ����ֵģ��ĽǶ����о�ʵ�������������������ܽ���ɢ���̡�ղˮ���[5]������������������Ũ�ȷֲ�������ֵģ�⣬�о��ó�������������������ɢ����Ҫ������������ɴٽ���������ȫ�۵���ɢ��POI��[6]��VERHAEGHE��[7]��Ϊ�������ܽ����������������Ũ�Ȳ�Դ�������������ʿ����ܽ�ģ�ͣ���LILLEBUEN��[8]��BEREZIN��[9]����Ϊ���ȶ�Ϊ�����������ܽ����Ҫ���ã���������������ȿ����ܽ�ģ�͡��ż���[10]�ڿ������������Բ����ȶ��������ܽ��Ӱ�죬ͨ��ʵ����ϵõ���һ���������ܽ�ͨ��ģ�͡�ZHAN��[11-12]���˫������Ⱥ��ƽ��ģ��(TPPBM)����500 ��m��Ϊ���������������������ܽ�Ĵ��ȡ����ʿ��ƻ��ƽ�������ֵģ�⡣����Ե�[13-14]����500 kA���������������˹��̵Ķ���ֶ�����ģ�ͣ����۷������������Ϲ����е����������������Ũ�ȷֲ������о�δ��������������ܽ⡣�����ֵ�[15]�о����Ϲ����е�����¶ȼ���ƽ��ı仯���ƣ����������������Ե����ϻ��ƻ�������ƽ�⡣TAYLOR��[16]����ʵ��Ԥ��ɽ�400 ��m�Ŀ���������Ϊ���ֿ��ƻ������õ���������������Ԩ��[17]�����������������������ܽ�Ĵ��ʿ���ģ�ͺ�������ģ�ͣ��о��ó������������ܽ������������ļ��ٶ�Ѹ�ټ�С����ï��[18]��ϸ�о��������ȡ����ʵ������ܽ���ƻ��ƣ��������������������Ƶ��ٽ�ֱ������С��560 ��m�������������ܽ��ܴ��ʻ��ƿ��ƣ�����560 ��m�������������ܽ��ܴ��Ȼ��ƿ��ơ�Ȼ���������о����ǻ����������ģ�ͽ�����ֵģ�⣬����Ϊ���������Ϻ�˲ʱ���������У���δ��ʵ�ʲ۽��з�����֤����δ�����ڲ�ͬ�������������ܽ��ܵ��Ŀ��ƻ��Ʋ�ͬ������д���һ�������о���
����������OpenFOAM��Դ����ƽ̨���ֱ������������������ܽ�ģ���봫���ܽ�ģ�ͣ����������������������������ȡ�������Ͽ����µ��ܽ����ģ�飬�ۺϿ����������ú����Ϻ���¶���ӦЧӦ����ʵ��300 kA���������������������ܽ���̽�����⣬���۷���һ����������144 s�������������ܽ����ʣ�δ�ܽ�����ֲ��Լ�������¶ȵı仯��
1 ����ģ��
1.1 ����������ģ��
����������300 kA������Ϊ�о�����������Ϊ��ɢ��������������Ҫ���������Ե������������������������ܽ���̽�����ֵģ�⡣����Һ���������ڵ�����е��ܽ�Ӱ���С��������Һ��ļ��㣬ȡ�����������Ϊ�����������������µĵ�����������ڳ���Ͷ���Գƣ���������ѡȡһ�����ϵ���Ϊ�о������ܽ�����������Ҫ���������ϵ���Χ������������Ӱ�����ȷ�Լ�Ϊ���ټ�����õ�ǰ���£�ѡȡ��۽��м��㣬�����ڶ���ԳƵİ�������ۡ����۾���������1��ʾ����۳ߴ�Ϊ3840 mm��7400 mm��180 mm����������ģ�ͼ����ϵ�ʾ��ͼ��ͼ1��2��ʾ��
��1 ��������ز���
Table 1 Parameters of aluminum electrolytic cell

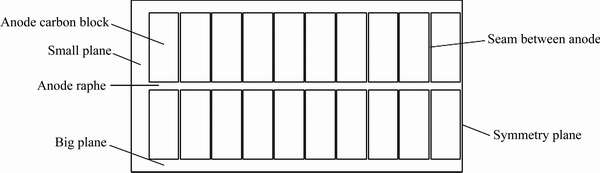
ͼ1 �����ۼ�������
Fig. 1 Computation domain of aluminum electrolytic cell
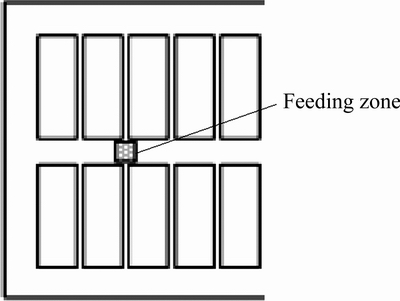
ͼ2 ������������ʾ��ͼ
Fig. 2 Schematic diagram of alumina feeding zone
1.2 ��������
ʵ�����������У��������������ܽ�����ܶ�����ص�Ӱ�죬�ڽ���ģ�����ʱ�������¼���[19]��
1) ��������̿������ģ���������ˮƽ��
2) ���Բ۰��Ӱ�죻
3) ������Һ��Ե�����˶���Ӱ�죻
4) ���Խ����γɹ��̣��������Ϻ�������Ѹ���γɽ�顣
5) ���Ե�������������������Լ������Ե���ʵļ��ȣ��ص��ע���������ܽ���̡�
2 ��ѧģ��
2.1 ��������
�������������µ���ʵ��������̣�����Ҫ�������������Լ�����������������֮�䶯��������Ӱ�죬�������¶������̣�
 (1)
(1)
 (2)
(2)
 (3)
(3)
ʽ�У���Ϊʱ�䣬s��uΪ������ٶ�ʸ����m/s����LΪ����ʵ��ܶȣ�kg/m3����Ϊ����ʶ����ȣ�Pa��s��u��v��w�ֱ�����ٶ�ʸ��u��x��y��z����ķ�����m/s��S�ǹ���Դ����������������������������������ʶ���������Smt�ȣ�����Smt������ʾ��
 (4)
(4)
ʽ�У�VcellΪ��Ԫ���������m3������Ϊʱ�䲽����s��uSe��uSs�ֱ�Ϊ�����������ij��ٶȺ��������������ٶȣ�m/s��ͨ�����������������Ķ����仯���Եó�����ʶ����任�����Դ˶Ե���ʶ������̽�����⡣
2.2 �����˶���ҷ��ģ��
�ڶ������塪�����������������У�ҷ���������ڿ�������Ҫ��������ҷ���Ĵ�С�������С����������������˶��ٶ��Լ�ҷ��ϵ���йأ�ҷ����ʽ������ʾ[20]��
 (5)
(5)
ʽ�У�uL��uP�ֱ�Ϊ��������ٺ��������������٣�m/s �� ����ʾ������������������m2��CDΪҷ��ϵ������������������ŵ���йأ�����������£�
����ʾ������������������m2��CDΪҷ��ϵ������������������ŵ���йأ�����������£�
 (6)
(6)
����������������ͨ���Ե��������������������������������յķ������������������˶�������ţ�ٵڶ����ɣ�
 (7)
(7)
 (8)
(8)
ͨ������(5)~(8)���̵�������⣬�ɻ������������ÿһʱ�̵�λ���Լ��ٶȣ����������������˶��켣��
2.3 ���˷���
�������������ڵ���ʺ���������Ũ�����˷������£�
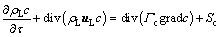 (9)
(9)
ʽ�У�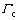 Ϊ������Ũ����ɢϵ����m2/s��Sc����������������λ���йأ���ǰ��������û������������ʱ��ScΪ0����������������ʱ��Sc���ܽ������йأ�����Ԫ�����������������������ĵ�λʱ���ܽ�����
Ϊ������Ũ����ɢϵ����m2/s��Sc����������������λ���йأ���ǰ��������û������������ʱ��ScΪ0����������������ʱ��Sc���ܽ������йأ�����Ԫ�����������������������ĵ�λʱ���ܽ�����
�������ڵ�����е��ܽ������һ�����ȹ��̣���ɵ�����¶ȵ��½��������������������£�
 (10)
(10)
ʽ�У���Ϊ����ϵ����W/(m��K)��STͬSc���ƣ���������������������ʱ��ST��ʾ��Ԫ����λʱ�������������������������ܽ�ʱ���յ�������
2.4 �����¶ȼ���
���о�ѡȡ�ij�ʼ����ʳɷ����2��ʾ���������͵�[21]�ľ�����㣬��ʼʱ�̳����¶�Ϊ950 �档
��2 ����ʳɷֱ�[22]
Table 2 Composition of electrolyte (mass fraction, %)[22]

2.5 �ܽ�ģ��
���������ܽ��ܴ����봫�������ܽ���ƵĿ��ƣ��о��ó�С��560 ��m�������������ܽ��ܴ��ʻ��ƿ��ƣ�����560 ��m�������������ܽ��ܴ��Ȼ��ƿ��ƣ������봫���ܽ���ƻ����Ƶ������Լ�560 ��m�ٽ�ֱ���ĵó��������[17-18, 23]��
�ڴ��ʻ����£�����������������ģ�ͱ���ʽ���£�
 (11)
(11)
�ڴ��Ȼ����£�����������������ģ�ͱ���ʽ���£�
 (12)
(12)
ʽ�У�kΪ����ϵ����m/s��hΪ��������ϵ����W/(m2��K)��CAlΪ�����������ݣ�J/(kg��k)����HdissΪ�������ܽ��ȣ�J/kg�� Ϊ������ܶȣ�kg/m3��
Ϊ������ܶȣ�kg/m3�� Ϊ�����������ܶȣ�kg/m3��wsatΪ�����������������Ũ�ȣ�%��wΪ����������Ũ�ȣ�%��TLΪ����ʵ����¶ȣ�K��TliqΪ����ʳ����¶ȣ�K��
Ϊ�����������ܶȣ�kg/m3��wsatΪ�����������������Ũ�ȣ�%��wΪ����������Ũ�ȣ�%��TLΪ����ʵ����¶ȣ�K��TliqΪ����ʳ����¶ȣ�K��
3 ���������������ֲ�
3.1 �����������ۼƷֲ�����
�ڼ�������֮ǰ������������������40~200 ��m�ķ�Χ�ڣ�һ���������ʣ��������������������̵���ʰ����γɽ��������ⲿ�ֽ����������ϴ����Լ10~15 mm[24]���������ʵ�����������������ֲ����Բ����������������һ�����Rosin-Rammler�ֲ�(���R-R�ֲ�)���ֲ������ı���ʽΪ[25-27]��
 (13)
(13)
ʽ�У�RΪ�ۻ������ֲ�����ʾ����ijһ�������ۻ���������ռ���п����������������ֳ�ɸ���ʣ��º�n�ֱ��������������ֲ��йص�ϵ����ָ����x��ʾ����������
�����ֳ����Եõ�������ǰ���������������ķֲ���ͨ�����Իع�ļ��㷽��������⣬������С���˷�ԭ�������ۻع��ߵĺû�[25]���Դ˻���ܽ�Ϊ��ȷ�������Ϻ����������������ֲ���R-R�ֲ�������
����ʽ(14)����δ�������ͽ������ĺ���[9]��
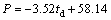 (14)
(14)
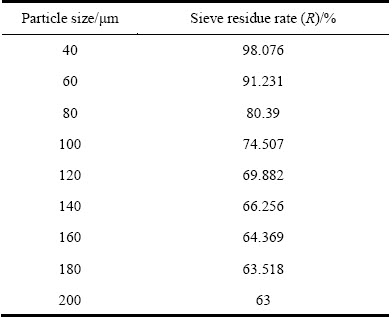
ʽ�У�PΪδ��������ռ�ĺ���(��������)��tdΪ��������ȫ�ܽ��ʱ�䣬һ��tdΪ6 min����PԼΪ37%����ʼ�����������������������ֲ�����[12]�Ǹ���ij�о�Ժ�����Ȳ����������Եó���Ȼ�����δ����������Լռ37%���������Ƴ����Ϻ��ɢ�õ�δ�������ֲ����������3��ʾ������ʵ�ʲ���ѡȡ���������������������������R-R�ֲ���������������ѡȡ���4�е���������һ��������⡣
�����Իع���㣬�ó����Ϻ������������ڵ�����е������ۼƷֲ�����Ϊ
 (15)
(15)
��3 �����������ֲ���
Table 3 Distribution of alumina particle
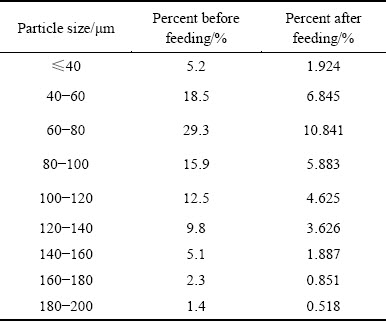
��4 ɸ���ʼ���
Table 4 Calculation of sieve residue rate
3.2 ���Ϻ��ʼ�����������ֲ�
ʵ���������м�������������������ڼƣ�Ŀǰ��ֵģ�Զ�ﲻ���˼���Ҫ����ˣ���Ҫ�����������������к�������һ�������������������һ����Ŀ��ʵ�����������������ڼ����ܽ��ʱ��ͨ������Դ��ķ�ʽ�������������ܽ����������������Ŀ��������Դ����õ�ʵ���������ܽ������¶ȳ��ļ��㷽ʽ��ͬ�����о��м�����������СΪ16 cm��16 cm��2 cm��������128���������ÿһʱ�䲽��(0.001 s)����128��������ÿ������ÿ������һ����������0.1 sʱ����ȫ������������������ģ�����ļ����������������ʱ���Լ������������������ʵ�ʿ������йأ�������ɺ����Щ������������ʵ�ʵ����м����1.8 kg������������
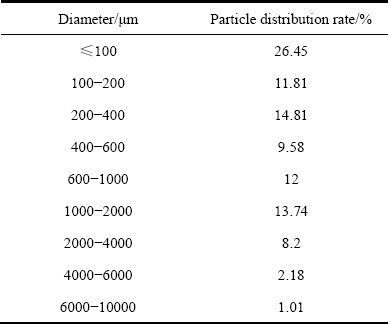
�����������ڼ�������֮ǰ���������������������100 ��m���ң������������ܽ���ٽ�ֱ��Ϊ560 ��m��ʵ��������������������һ����1~1.5 cm֮�䣬����ʱѡȡ���������Ϊ1cm������ǰ���Ѽ���ó���R-R�ֲ������������Ϻ�Ľ���δ�������������ۼƷֲ����м�������ƣ��õ����Ϻ�����������������ֲ�ͳ�Ʊ������5��ʾ����ģ��ʵ�������������ܽ�ʱ�����ڲ��ܰ���ʵ�ʵ�������������������ģ�⣬��ˣ���������ѡȡ����100��200��400��600��1000��2000��4000��6000��10000 ��m��ʵ�ֶ�ʵ�����������Ͻ�������е��ܽ�ģ�⡣
��5 ���Ϻ���������ֲ�ͳ�Ʊ�
Table 5 Distribution of particle size after feeding
4 �����������������ܽ����������
�������������Ҫ�������������������͵���������������������Ϻ���Ҫ�������������з죬��Ҫ�����ݹĶ������ö���ɢ����˱��Ľ��ص��ע300 kA���������������������������µ��ܽ���̡�
4.1 ���������µ���������ֲ�
��ȡCFX�����300 kA���������������ݵ�������[23]��ͨ��Դ�����ӵķ�ʽ���뵽����ʶ��������У��õ���ͼ3��ʾ���������������µ���������ֲ�ͼ��
��ͼ3�������Կ������������������µ�����������Ϊ0.55 m/s����������ڼ��Գ�����������λ���з����콻�Ӵ����˴���������ٽϴ���������������з�ĵ�����γɶԳ壬ʹ�õ�������½��裬�����������������Ŀ��ٷ�ɢ��
4.2 �����������ܽ����
�����ѵó���1.8 kg���������������ֲ���ģ���������������������������ܽ⼰���˹��̣��õ��������ۻ�����������ģ����������[28]�ĶԱ���ͼ4��ʾ��
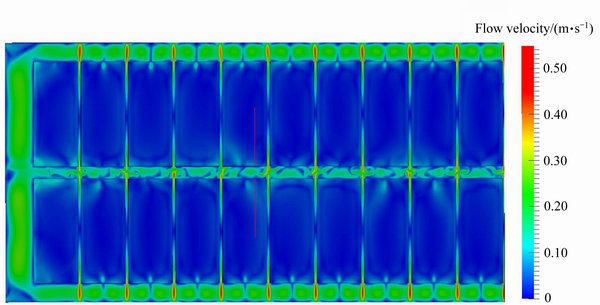
ͼ3 �������������µ���������ֲ�ͼ
Fig. 3 Electrolyte flow field distribution under effect of anode bubble
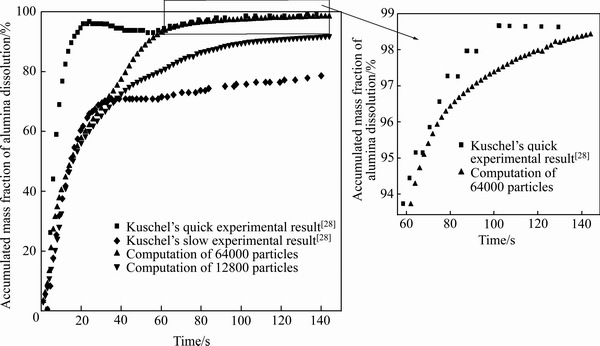
ͼ4 �������ۼ��ܽ���������
Fig. 4 Accumulated mass fraction of alumina dissolution
ͼ4��KUSCHEL��[28]��ʵ��Ϊ��һ���̶�ԲͲ�����м����������ģ��ʵ�ʵ����������KUSCHEL��[28]���������ܽ�ʵ���Ϊ�����������һ���ǿ����ܽ�ʵ�飬�����������ٷ�ɢ�ĵ��������У�Ŀ���Ǿ����ܵر��������������ۼ����γɽ�飬�ӿ��������ܽ⣻�ڶ�������ͨ�������裬�����˿�����ۼ�������������ܽ��ٶȽ�����ʵ�ʵ��۲����������ܽ��Ϊ���ѣ������뱾�ļ��㹤�����Ƶ�Kuschelʵ�������жԱȷ������ֱ�ѡ������12800�����������64000���������������1.8 kg�ܵ����������������о�����������Լ�������Ӱ�죬ѡ��ģ����������ʵ�ʵĿ��������з�����
��ͼ4���Կ�����ǰ30 s�У�12800�����������64000������������ܽ�ģ������KUSCHEL��[28]����ʵ�����ǺϽϺã�30~60 s֮�䣬12800��������64000���������ۼ��ܽ��������߸���KUSCHEL��[28]����ʵ��������������ܽ������߿����� 60 s��64000���������ܽ�������KUSCHEL��[28]����ʵ���������Ǻϣ���12800�������ܽ��ٶ�Ҫ������Ҳ�����ڿ����ܽ����ߡ����ģ������ʵ��������ԭ����Ҫ�����¼��㣺KUSCHEL��[28]����ʵ����Ϊ�������Ӧ�˿�����ۼ������������ģ���12800����64000������������ܽ�ͬ����������������飬��ˣ�ǰ30s����ģ������KUSCHEL��[28]����ʵ�����ӽ�����30~60 sʱ������ʵ������ֱ��Ϊ10 cm��С�������ģ�Ũ�Ȳ�ļ�С�Լ����ȶȽ��͵����������ܽ����ʼ�С������������ܽ������ʵ�ʵ��۳ߴ�ϴ��������Ķ������������������ܱ߲��������ʵ���ʲ��䣬ʹ������������Ũ�Ⱥ��¶ȵı仯�ݶȲ������ģ������������ܽ��������KUSCHEL��[28]����ʵ������60 s��64000�����������ģ������KUSCHEL��[28]�Ŀ���ʵ���Ǻϣ���ȻKUSCHEL��[28]�Ŀ���ʵ�龡���ܵ�ʹ�������������ȷ�ɢ�ؼ��������У����������ٲ��ֿ�������ۼ����γ�������飬��Щ�������ܽ��������64000�����������ģ������У�С������ǰ60 s���Ѿ��ܽ⣬ʣ��δ�ܽ�Ŀ�������Ϊ��Ľ���������ˣ���60 s֮��������ܽ������Ǻϡ����12800����64000��������������������ԭ����ģ�����������ʵ�ʿ������IJ�ͬ��ģ�������Խ�࣬һ��������������ʵ��������������Խ�٣�Խ�ӽ���ʵ�������������ˣ�64000������ģ����ӽ���ʵ�ʣ�����ʵ���ǺϽϺã�˵�����ô��ȴ������ģ�ͼ���ʵ�������������������ܽ��ǿ��еġ��������߽�ѡȡ64000�����������ģ�������о�300 kA�������е��ܽ������
KOBBELTVEDT[29]������������15 s�����ܽ���50%�����������䶨����һʱ���Ϊ�����ܽ�Ρ���ͼ4�п��Կ�������18 s�����������ܽ���50%����������KOBBELTVEDT[29]�Ŀ����ܽ�ʱ��ӽ�����ˣ����о��������300 kA�������У����Ϻ�ǰ18 sʱ�����Ϊ�����������ܽ�Ρ�64000���������ģ������������һ����������144 s����ʱ����Լ1.5%���ҵ�������δ�ܽ⣬��Щδ�ܽ���������������ּ����ڴ�Ľ������ϣ���Щ�������ܽ�����������ڵ��۵ײ��γɳ�����ͨ�����㣬300 kA�����۵�һ����������һ�����������ڽ�����Լ0.027 kg���������γɳ�������ʵ���������ϽϺã���˿���������ֵ����ķ���Ϊ�Ժ�����������������������ṩ����ָ����
δ�ܽ�����������ʾ��ͼ��ͼ5��ʾ��
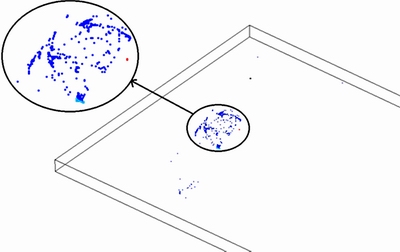
ͼ5 δ�ܽ�����������ʾ��ͼ
Fig. 5 Schematic diagram of undissolved alumina particle
4.3 ������������¶ȱ仯����
�����������������뵽����ʺ�����������������¶��½���Ϊ���ԣ���������ѡȡ������ƽ���¶���Ϊ�о������ڲ����ǵ������ȼ������ܱ�ɢ�ȵ�����£��о��������ܽ�����ȹ��̡�ͼ6��ʾΪ�����������ƽ���¶ȱ仯���ߡ�
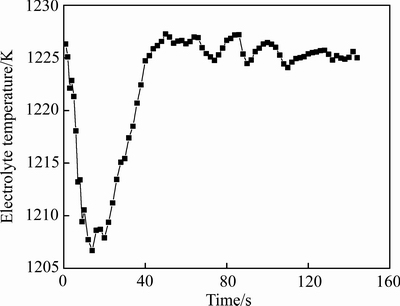
ͼ6 �����������ƽ���¶ȱ仯����
Fig. 6 Variation of average electrolyte temperature in feeding zone
��ͼ6��֪�������Ϻ��ǰ14 s���ң���ʱ���������������ܽ�Σ���ɢ��С���������ܽ���������ȣ�������¶��ɳ�ʼ��1233 K(960 ��)Ѹ���½����¶�����½���26 �棬�����������ʵ��ó��ĵ������10 s���ҽ��µ���͵㣬����¶��������Ľ���ӽ�[30-31]����14 s֮����ʵ��������������¶Ƚϵ͵ĵ���ʾ�������ɢ�����õ���Χ�¶Ƚϸߵĵ���ʲ���ʹ���������¶ȿ������ߡ����⣬��60 s֮���¶ȳ��������ƣ��������ڲ�������������������������δ�����ߣ��Լ�����ط��¶Ƚϵ͵ĵ��������������¶������ڱ��������ص��о��������ܽ�����ȹ��̣���Ҫͬʱ�����������ƽ��������ѶȽϴ���˺����˼��������Ե���ʵļ��ȣ���������������¶Ȳ�����������ʼ����¶�1233 K���������¶ȱ仯������ʵ�����ǽӽ��ģ��ȽϽ����ͼ7��ʾ��
ͼ7��ʾΪ������������¶��½����߶Ա�ͼ��ͼ��1~5�������ΪWALKER[30]��91 kA��ʽ���ϵ��������õ��IJ������ݣ���ʼ������¶�Ϊ985 �棬1�ŵ�λ�������������Һ������1 cm����2~5�����λ������������1 cm�������ȵ�żÿ��1 s��¼һ�����ݡ���ͼ7��֪��1��2����Ե��¶��½��Ͽ죬����½���90 �棬������������Ե�λ���������ϲ㣬���Ϻ���������ܽ�������ȣ������ȵ�ż����һЩ���������������̵ĵ�����γ�һ�����̲㣬ʹ�䲻����Һ������ֱ�ӽӴ����������������IJ�������������̲��¶Ƚϵͣ�ʹ���¶Ȳ������ݽϵͶ�ʧ�档ģ������3~5���Ե����ݱȽϷ��֣��¶ȱ仯���ɴ�����ͬ����Ϊ�ȼ�С����������½���26 �����ң��¶��½����ʱ����ʱ�����в����14 s��ģ���������¶�������ʵ���¶���������������������ڼ���ֵΪ���������ֵ��仯����������¶ȵĻ������ɵ����������Ϻ��µġ�
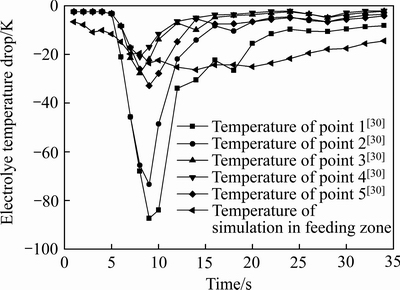
ͼ7 ������������¶ȱ仯����
Fig. 7 Change curves of electrolyte temperature in feeding zone
5 ����
1) ����OpenFOAM����ƽ̨�������������ú����Ϻ�ĵ�����¶���Ӧ����Һ���߱仯���������������е�����Լ�������������ŷ��-�������ռ���ģ�ͣ�������ʵ��300 kA�������������������Ĵ��ȴ�����Ͽ����µ��ܽ�ģ�ͣ�ģ������������ʵ��������ǺϽϺá�
2) ���������������Ͻ������ʺ�����������R-R�ֲ���ͨ�����Իع�ļ��㷽���Ƶ�������������������������ֲ�����Ϊ ��
��
3) �������������Ϻ���Ҫ�������������з죬��Ҫ�����ݹĶ������ö���ɢ��ģ���������������������������ܽ���̣���ǰ18 s���������ܽ���50%����������ɢ�õ�С���������ܽ⣬�������ܽ�Σ�30 s���ܽ�����������60 s����С�������ܽ���ȫ��ʣ���Ľ����������ܽ⣻һ����������144 s������ʣ��Լ1.5%��������δ�ܽ⣬��Щδ�ܽ�Ŀ����ۼ��γɳ�����
4) �������������ܽ����ȵ�����£�������λ�õ�����¶���ǰ14 s�����½�������ڵ�������������¸��������¶Ƚϸߵĵ���ʲ��䣬�¶ȿ��ٻ�����֮�������������ܽ������Լ�����ʵĶ�����ɢ��������������¶ȳ��仯��
5) ģ�������������ʵ�������ǺϽϺã���֤��ģ���ȷ�ԣ���ˣ�����������ֵ����ķ���Ϊ�Ժ�����������������������ṩ����ָ����
REFERENCES
[1] YANG You-jian, GAO Bing-liang, WANG Zhao-wen, SHI Zhong-ning, HU Xian-wei. Effect of physiochemical properties and bath chemistry on alumina dissolution rate in cryolite electrolyte[J]. JOM, 2015, 67(5): 973-983.
[2] �����, ʯ����, �߱���, ������. �����������ڱ���ʯ�е��ܽ�[J]. ������ѧѧ��(��Ȼ��ѧ��), 2003, 24(9): 832-834.
XU Jun-li, SHI Zhong-ning, GAO Bing-liang, QIU Zhu-xian. Dissolution of alumina in molten cryolite[J]. Journal of Northeastern University (Natural Science), 2003, 24(9): 832-834.
[3] ����, �߱���, �� ��, ������, ��ҫ��. ���ڱ���ʯ�����������ܽ�(��Ӱ�о�)[J]. ������ѧѧ��(��Ȼ��ѧ��), 1999, 20(4): 398-400.
YANG Zhen-hai, GAO Bing-liang, XU Ning, QIU Zhu-xian, LIU Yao-kuan. Dissolution of alumina in molten cryolite (A video recording study)[J]. Journal of Northeastern University (Natural Science), 1999, 20(4): 398-400.
[4] ROLSETH S, HOVLAND R, KOBBELTVEDT O. Alumina agglomeration and dissolution in cryolitic melts[C]// MANNWEILER U. Light Metals1994. San Francisco, CA: TMS, 1994: 351-357.
[5] ղˮ��, �� ï, ������, ������, ���. ������������������Ũ�ȷֲ�����ֵģ��[J]. �й���ɫ����ѧ��, 2014(10): 2658-2667.
ZHAN Shui-qing, LI Mao, ZHOU Jie-min, ZHOU Yi-wen, YANG Jian-hong. Numerical simulation of alumina concentration distribution in melts of aluminum reduction cells[J]. The Chinese Journal of Nonferrous Metals, 2014, 24(10): 2658-2667.
[6] POI N W, HAVERKAMP R G, KUBLER S. Thermal effects associated with alumina feeding in aluminium reduction cells[C]// MANNWEILER U. Light Metals1994. San Francisco, CA: TMS, 1994: 219-225.
[7] VERHAEGHE F, BLANPAIN B, WOLLANTS P. Dissolution of a solid sphere in a multicomponent liquid in a cubic enclosure[J]. Modelling and Simulation in Materials Science and Engineering, 2008, 16(4): 45007.
[8] LILLEBUEN B O R, BUGGE M, HOIE H. Alumina dissolution and current efficiency in Hall-Heroult cells[C]// BEARNE G. Light Metals2009. San Francisco, CA: TMS, 2009: 389-394.
[9] BEREZIN A I, ISAEVA L A, BELOLIPETSKY V M, POSKAZHOVA T V, SINELNIKOV V V. A model of Dissolution and Heating of Alumina Charged by Point-Feeding System in ��Virtual Cell�� program[C]// KVANDE H. Light Metals 2005. San Francisco, CA: TMS, 2005: 151-156.
[10] �ż���. ������ѧģ�͵������۶�̬���̼���Ԥ��ϵͳ�о�[D]. ��ɳ: ���ϴ�ѧ, 2011.
ZHANG Jia-qi. Principal electrolysis processes and corresponding prediction system for aluminum electrolysis cells based on mathematical models[D]. Changsha: Central South University, 2011.
[11] ZHAN Shui-qing, LI Mao, ZHOU Jie-min, YANG Jian-hong, ZHOU Yi-wen. CFD simulation of dissolution process of alumina in an aluminum reduction cell with two-particle phase population balance model[J]. Applied Thermal Engineering. 2014, 73(1): 803-816.
[12] ZHAN Shui-qing, LI Mao, ZHOU Jie-min, YANG Jian-hong, ZHOU Yi-wen. Analysis and modeling of alumina dissolution based on heat and mass transfer[J]. Transaction of Nonferrous Metal Society of China, 2015, 25(5): 1648-1656.
[13] �����. ���������������˶������������˹��̵���ֵģ���о�[D]. ��ɳ: ���ϴ�ѧ, 2012.
ZHANG He-hui. Numerical study of vortex flow of melts and transport process of alumina in aluminum reduction cells[D]. Changsha: Central South University, 2012.
[14] �� ��, ����, �����, �ź���, �� ˧, �� ��, ������. 500 kA���������������Ũ�ȳ�����ֵģ��[J]. �й���ɫ����ѧ��, 2015, 25(3): 799-805.
JIANG Nan, QIU Ze-jing, ZHANG He-hui, ZHANG Hong-liang, YANG Shuai, LI Jie, LIU Qing-sheng. Numerical simulation of alumina concentration field in 500 kA aluminum reduction cell[J]. The Chinese Journal of Nonferrous Metals, 2015, 25(3): 799-805.
[15] ������, �� ��, �� ��, ����ǧ, �� ��. ���������Ϲ��̶Ե�����¶ȳ���Ӱ��[J]. �й���ɫ����ѧ��, 2016, 26(2): 430-438.
DING Pei-lin, WANG Heng, HUANG Jun, WANG Zi-qian, CAO Bin. Effect of feeding in aluminum reduction cell on electrolyte temperature[J]. The Chinese Journal of Nonferrous Metals, 2016, 26(2): 430-438.
[16] TAYLOR M P, WELCH B J, MCKIBBIN R. Effect of convective heat transfer and phase change on the stability of aluminum smelting cells[J]. AICHE Journal, 1986, 32(9): 1459-1465.
[17] ����Ԩ, �� ï, �� Զ, �� ��. �����������ڴ��ʻ��ƿ����µ��ܽ�ģ��[J]. �����, 2015(5): 24-28.
HOU Wen-yuan, LI Mao, LI Yuan, BAI Xiao. Simulation of alumina particle dissolution under the control of mass transfer mechanism[J]. Light Metals, 2015(5): 24-28.
[18] �� ï, �� ��, �� Զ, ����Ԩ, ������. �������������ܽ���ƻ��Ƽ����ٽ�ֱ��[J]. �й���ɫ����ѧ��, 2016, 26(2): 456-462.
LI Mao, BAI Xiao, LI Yuan, HOU Wen-yuan, GAO Yu-ting. Control mechanisms and critical characteristics in dissolution of alumina particles[J]. The Chinese Journal of Nonferrous Metals, 2016, 26(2): 456-462.
[19] ��Сϼ. �������ڵ������������ֵģ���о�[D]. ��ɳ: ���ϴ�ѧ, 2005.
XIA Xiao-xia. Study on numerical simulation of the flow field in aluminum reduction electrolyte cells[D]. Changsha: Central South University, 2005.
[20] ������, �����, ������. ���̹��̹���ѧ������ˮ�ҵ�е�Ӧ��[M]. �人: �人������ѧ������, 2003: 146-148.
HU Dao-he, XU De-long, CAI Yu-liang. Gas-solid process engineering and its application in the cement industry[M]. Wuhan: Wuhan University of Technology Press, 2003: 146-148.
[21] ������, ������. ��ҵ��������۵���ѧģ�͵��о�[J]. �����, 1981(1): 15-22.
ZHANG Ming-jie, QIU Zhu-xian. Research on mathematical model of industrial aluminum electrolyte melting point[J]. Light Metals. 1981(1): 15-22.
[22] ������. �����[M]. ����: ��ѧ��ҵ������, 2006.
FENG Nai-xiang. Aluminum electrolysis[M]. Beijing: Chemical Industry Press, 2006.
[23] ����Ԩ. �������������������ܽ������ֵģ��[D]. ��ɳ: ���ϴ�ѧ, 2015.
HOU Wen-yuan. Numerical simulation of the dissolution process of alumina particle in aluminum electrolytic cell[D]. Changsha: Central South University, 2015.
[24] PETER N. Evolution of alpha phase alumina in agglomerates upon addition to cryolitic melts[D]. Trondheim: Norwegian University of Science and Technology, 2002.
[25] �� ��, Ҧ����, ������, ŷʢ��, κ����. ������ɭ-��ķ�շֲ������ķ۳���ɢ�ȷ���[J]. �����Ƽ���ѧѧ��, 2010, 32(9): 1101-1106.
LIU Jian, YAO Hai-fei, JIN Long-zhe, OU Sheng-nan, WEI Chuan-guang. Dust dispersion analysis based on the Rosen-Rammler distribution function[J]. Journal of University of Science and Technology Beijing, 2010, 32(9): 1101-1106.
[26] ֣����, �����, ��־��, �ų���, �� ��. ��ͬ�����ʽ��ú�����������ֲ������о�[J]. �ɿ��밲ȫ����ѧ��, 2007, 24(1): 96-100.
ZHENG Gang-biao, KANG Tian-he, YIN Zhi-hong, ZHANG Chi-ming, DUAN Jun. Research on dust size distribution of coal impacted with different forms[J]. Journal of Mining & Safety Engineering, 2007, 24(1): 96-100.
[27] ������. ����Rosin-Rammler�����ֲ��������о�[J]. ��ҵ��ȫ�����, 2000, 26(5): 6-8.
DAI Li-yan. Study on function of Rosin-Rammler particle size distribution[J]. Industrial Safety and Dust Control. 2000, 26(5): 6-8.
[28] KUSCHEL G I, WELCH B J. Further studies of alumina dissolution under conditions similar to cell operation[C]// ELWIN R. Light Metals 1991. New Orleans, Louisiana: TMS, 1991: 112-118.
[29] KOBBELTVEDT O. Dissolution kinetics for alumina in cryolite melts[D]. Trondheim: Norwegian University of Science and Technology Department of Electrochemistry, 1997.
[30] WALKER D I. Alumina in aluminum smelting and its behaviour after addition to cryolite-based electrolytes[D]. Toronto: University of Toronto, 1993.
[31] WELCH B J, KUSHEL G I. Crust and alumina powder dissolution in aluminum smelting electrolytes[J]. JOM, 2007, 59(5): 50-54.
Simulation of alumina particle dissolution in 300 kA aluminum electrolytic cell
LI Mao, GAO Yu-ting, BAI Xiao, LI Yuan, HOU Wen-yuan, WANG Yu-jie
(School of Energy Science and Engineering, Central South University, Changsha 410083, China)
Abstract: During the aluminum electrolytic feeding process, alumina particles will dissolve after absorbing heat, aggregation subject under the control of the mass and heat transfer mechanism. Based on the OpenFOAM computing platform, identifying the dominant mechanism controlling dissolution of alumina, considering the bubble effect and temperature response of electrolyte after feeding, the alumina, dissolution model coupled with heat and mass transfer were proposed. Based on the alumina particle size distribution calculated by Rosin-Rammler function, the actual dissolution process in electrolyte after feeding were simulated in 300 kA aluminum reduction cell. The simulation results show that the first 18 s is the quick stage of dissolution, in which about 50% of the quantity is dissolved. At the end of a feeding cycle 144 s, about 1.5% of the alumina is undissolved, the undissolved particle aggregates and forms sludge at the bottom of the cell. Only considering the alumina endothermic process, the electrolyte temperature in the feeding zone rapidly declines within the first 14 s, then, the temperature quickly is recovered and oscillated after 60 s.
Key words: aggregation; alumina dissolution; heat transfer; mass transfer; particle size distribution; numerical simulation
Foundation item: Project(2010AA065201) supported by the National High Research Development Program of China
Received date: 2016-05-03; Accepted date: 2017-02-21
Corresponding author: LI Mao; Tel: +86-13055169363; E-mail: limao89@163.com
(�༭ ����)
������Ŀ�����Ҹ����о���չ�ƻ�������Ŀ(2010AA065201)
�ո����ڣ�2016-05-03�������ڣ�2017-02-21
ͨ�����ߣ��� ï�������ڣ���ʿ���绰��13055169363��E-mail: limao89@163.com