DOI: 10.11817/j.issn.1672-7207.2015.11.053
微生物菌剂与冰草联合修复含油污染土壤
陈丽华1,周立辉2,雒晓芳1,杨琴2,潘和平1
(1. 西北民族大学 实验中心,甘肃 兰州,730030;
2. 长庆油田公司油气工艺研究院,陕西 西安,710018)
摘要:从陕西姬源油田污染严重的土壤中富集培养、筛选分离得到8株降解石油菌,向土壤中添加上述8株菌组成的混合菌剂,通过63 d盆栽试验,利用微生物菌剂与冰草联合作用修复石油污染土壤,测定土壤中降油率、微生物数量和脱氢酶活性;并采用气相-质谱联用仪(GC-MS)分析石油中正构烷烃组分的降解情况研究植物-微生物联合修复油污土壤。试验结果表明:植物与微生物菌剂联合作用修复能力大于单一植物修复能力,并且含油质量分数直接影响修复性能;经63 d植物与菌剂联合修复质量分数为3%含油土壤,降油率达81.48%,比单一植物降油高43.04%;土壤微生物数量、脱氢酶活性的增加有利于原油降油;微生物-植物联合作用对高碳数烷烃的降解作用大于低碳数烷烃的降解作用,15 d的降解率平均可达60%以上,加菌后正二十三烷和正三十三烷的降解率分别较对照组提高了34.7%和25.3%。
关键词:混合菌剂;冰草;降油率;微生物;脱氢酶活性;油污土壤
中图分类号:X53 文献标志码:A 文章编号:1672-7207(2015)11-4377-07
Bioremediation of oil-contaminated soil by microbial agents and ice grass
CHEN Lihua1, ZHOU Lihui2, LUO Xiaofang1, YANG Qin2, PAN Heping1
(1. Experimental Center, Northwest University for Nationalities, Lanzhou 730030, China;
2. Institute of oil-gas techniques, Companies of Changqing Oil Field, Xi’an 710018, China)
Abstract:Eight strains of oil-degradation bacteria were screened and isolated from oil contaminated soil at Jiyuan Oilfield of Shannxi Province of China. Different amounts of these bacteria were injected into soil polluted by crude oil; after being treated with potting experiment for 63 days, petroleum contaminated soil was degraded with petroleum-degrading bacterium in combination with wheat grass; petroleum degradation rates, microbial population, dehydrogenises activity were measured, and degradation of n-alkanes was analyzed by GC-MS. The results show that the combined effects of plant and microbial remediation ability are better than repair capacity of single plant, and oil mass fraction directly affects the repair performance. After 63 days of plant and microbial remediation, oil degradation rate of mass fraction of 3% contaminated soil reaches 81.48%, which is obviously 43.04% higher than that treated with single plant. Increased soil microbial biomass and dehydrogenase activity are beneficial to oil degradation. The effects of petroleum-degrading combined with bacterium-plant on high carbon number n-alkanes are better than those of low carbon number n-alkanes. The degradation rate of the mixed bacteria for high carbon normal alkanes is up to 60% on average after 15 days. The degradation rates of twenty-three alkanes and thirty-three alkanes increase by 34.7% and 25.3% than those of the control group used by bacteria, respectively.
Key words: mixed bacterial strains; ice grass; oil degradation rate; microbial; dehydrogenase activity; oil-contaminated soil
随着石油产品需求量的不断增加,石油及其制品通过多种途径进入环境,对土壤和水体造成了严重污染,并且威胁着人类的健康,石油污染土壤技术的研究及应用正日益受到广泛重视与关注。然而,生物修复技术被认为是一种绿色环保、无二次污染、高效、可彻底降解污染物的具有发展前景的石油污染修复方法[1]。该技术关键在于利用功能微生物可降解多种石油烃组分,研究如何最大程度强化菌群自身降解石油污染底物的能力,并对影响混合菌群降解性能的营养条件和环境因素进行试验研究[2]。但是,污染土壤的石油组分十分复杂,单一的细菌及真菌只能降解少数特定烃类或者只能降解到某一阶段,而混合菌种因菌群丰富,代谢途径多种,故能降解多种复杂有机物,包括石油烃类物质[3]。陈丽华等[4-5]研究表明混合菌株不仅可以降解正构烷烃,还能较好地促使藿烷化合物的生物转化,使不稳定立体构型向稳定性构型转化的演化特征。然而,植物修复技术又是一项正在开发研究中的生物修复新技术。但修复植物的筛选是植物修复技术首要解决的问题[6]。Zhou等[7]对石油污染土壤的植物修复、微生物-植物复合修复方面进行了系统的研究工作,采用蚯蚓对已修复的土壤的生物毒性进行检测。黄盼盼等[8-9]通过盆栽实验研究了土壤石油烃污染对玉米和水稻根生长情况影响, 并在土壤中接种经过筛选得到石油烃降解菌, 研究石油烃降解菌对石油烃毒性的影响以及对土壤中石油烃的降。张松林 等[10]通过紫花苜蓿对石油污染土壤进行人工植物修复试验,发现紫花首蓓对石油污染土壤有很好的修复效果。因此,本文作者利用微生物与植物联合的修复技术,首先筛选分离得到8株降解石油菌,然后向石油污染土壤中添加8株菌组成的混合菌剂,选取西北地区常见的野生植物冰草,通过盆栽试验,研究不同质量分数的石油污染土壤在植物与菌剂联合作用下的修复性能,并进行GC-MS分析,进一步从深层次上搞清问题的根源,以提高生物修复的针对性和有效性,最大程度发挥污染治理工程的投资效益和社会效益。
1 材料与方法
1.1 土样及原油
土样取自陕西姬塬油田,采集油田附近受石油污染的土壤为土样。石油为当地原油,饱和烃质量占原油总质量的68%~78%,芳烃占5%~15%,非烃占7%~13%,沥青质占5%左右。
1.2 混合菌剂
所用菌种为本实验室分离保存[11],分别为不动杆菌属(Acinetobacter) 1株,假单胞菌属(Pseudomonas)
4株,无色杆菌属 (Achromobacter)1株、热带假丝酵母菌(Candida tropicalis) 1株,诺卡氏菌属(Nocardioides)1株。将6株细菌按照60%(质量分数)和2株真菌按照40%(质量分数),采用三级扩大培养法配成菌悬液,将菌液吸附于锯末载体上,密封保存在室温下[4]。
1.3 微生物的生物量的测定
采用平板稀释涂布法测定菌剂中各类微生物的生物量[12]。
1.4 降油率的测定
降油率的测定方法参照文献[5]。用紫外分光光度法在225 nm处测得标准油样标准曲线,得标准方程式为:y=0.017x-0.012,相关系数R2为0.9987。该式反映了样品中石油类含量和吸光度之间的关系。式中:y表示用50 mL正己烷索氏提取含油油样所得提取液的有效吸光度,为量纲一参数;x表示样品的含油质量浓度,mg/L。
1.5 土壤中脱氢酶活性的测定
通过把土壤溶液离心后加入2, 3, 5-三苯基氯化四氮唑(TTC)和Tris溶液萃取后测定其吸光度,根据测得的吸光度和绘制的标准曲线计算出土壤中脱氢酶活性[5]。吸光度与TTC质量浓度的线性关系式为:y=0.0130x-0.0014,相关系数R2为0.9938。其中:y为不同质量浓度的TTC对应的吸光度,x为TTC的质量浓度(μg/mL)。
1.6 利用气相-质谱联用仪即GS-MC检测降解油样中正构烷烃组分
取降解15 d后土壤样品正己烷萃取液5 mL,经无水硫酸钠脱水,经过0.22 μm耐有机溶剂滤膜过滤后,取2 mL 氮气吹干,正己烷1 mL重新溶解后,利用GC-MS检测溶解液中正构烷烃质量[4-5]。用质量归一法计算出样品中正构烷烃系列化合物的质量。在石油混合物组分中相对分子质量相同物质的比较多,但每个物质的结构不同,在GC-MS离子源中,每个分子被电子流轰击打成碎片时,由于结构不同而出现各自的特征碎片离子。如正构烷烃的碎片离子为57,71,85,…,利用物质的特征碎片值可以从总离子流图中将正构烷烃同系列物质提取出来。
石油烃中正构烷烃物质的降解率R计算方法如下:R=(M1-Mi)/M1,式中:M1为对照组中各物质质量;Mi为第7 d和15 d残油中各物质质量。
1.7 实验设计
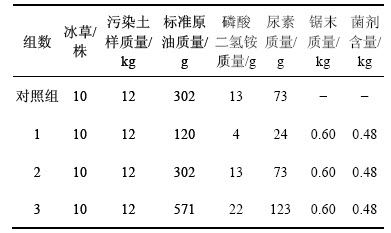
在直径为30 cm、高为50 cm的花盆中加入不同原油浓度的污染土样。实验设计4组,对照组中不加菌剂也不加锯末,其余处理与第2组完全一致;第1,2和3组中每盆种植冰草幼苗各10株,使原油质量分数分别达到1%,3%和5%,再分别加入质量分数为4%的菌剂,质量分数为5%的锯末,将土样充分混匀,最后加入尿素,磷酸二氢铵,使各盆土壤C,N和P质量比约为100:10:1。保持含水率约为20%,并添加适量液体有机肥,在同等试验条件下使冰草生长2月后长成壮株。每种处理设置3组平行,分别于第 1,4,7,12,17,20,27,34,41,48 和63 d测定石油类污染物降解率、脱氢酶活性、土壤中的微生物数量等。初始各组中原油质量以实际测定值为准,结果如表1所示。
表1 试验处理措施
Table 1 Experimental treatment measures
2 结果与讨论
2.1 降油植物的筛选
采用紫花苜蓿、冰草和小麦进行人工石油污染土壤的植物筛选试验,石油污染物质量分数为5%。图1所示为不同时间对3种植物株高的影响。从图1可知:质量分数为5%的石油污染土壤中,苜蓿、冰草和小麦的株高均有所增加,尤其对冰草株高的促进作用最明显,故后期的实验中选择冰草为降油试验的代表植物。
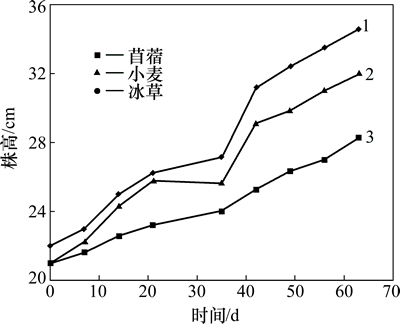
图1 不同时间对3种植物株高的影响
Fig. 1 Effect of different time on plant height of three plants
2.2 降油率随时间的变化
图2所示为原油的降解率随时间的变化情况。由图2(a)可见:0~14 d原油的降解不明显;在14 d左右有1个快速增长的趋势,30 d之后增长幅度逐渐减缓;在修复后期,加菌剂组的石油降解能力高于空白组降解能力,石油降解顺序为第2组、第1组、第3组、空白对照组,其中第2组的降油率最高为88.54%,第3组的降油率为81.24%,第1组的降油率为52.30%,而空白对照组的降油率仅为38.43%,明显低于其他各组降油率。其原因不仅与微生物作用有关,更与植物的协同作用分不开。修复初期,降油增幅不明显,因为冰草幼小,根系欠发达,移植后需要一段修复期,对营养物质的吸收能力大大降低;另外,初期加入微生物菌剂时,对土壤有一段适应过程,且石油污染物会抑制外源微生物的生长,导致微生物数量短期内呈减少趋势,未能发挥有效的降解作用[6]。经过一段适应期后,冰草新根系的生长对营养元素的需求量增大,此时微生物适应环境的能力大大提高,数量增多,从而提高了修复效果。植物的修复功能主要体现在植物根系的吸收,如果植物具有发达的根系,生长旺盛,穿透效果较好,给微生物提供较大的根表面积,修复效果就会好[13];根际植物与微生物联合作用可以促进根部污染物质的降解[14],壮年冰草横走或下伸的根状茎,须根系长而密集,转化及分解有机污染物的作用明显。 35 d后,降油增幅已不明显,呈波动状态。这是因为土壤中微生物群落结构已达到平衡,残油量不多,土壤中养分质量分数低,另外微生物代谢过程中有毒物质的积累过多而抑制了微生物的生长[13],大部分石油已被降解,土壤中的微生物数量呈现出下降的趋势,微生物降解作用不明显。含油质量分数太高不仅抑制微生物的数量,还会抑制植物的生长,并且降解效果也最差。
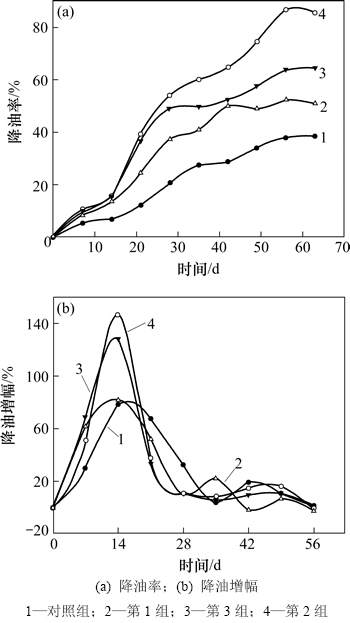
图2 降油率随时间的变化
Fig. 2 Relationship between oil degradation and time
2.3 降油与微生物数量之间的变化
根据油污土壤的生物修复研究结果[5, 14]可知:微生物的数量和脱氢酶活性可以作为微生物对底物适应性的指标,它们与石油烃的衰减有着良好的相关性。图3所示为降油率增长幅度与微生物数量之间的关系。由图3(a)可见:微生物数量变化和降油幅度呈现明显的相关性,微生物数量达到峰值时,降油增幅也最大;在实验初期(0~7 d),微生物数量均较低,降油率的增长幅度也较小;7~28 d 微生物迅速繁殖,石油降解速率迅速加快,增长幅度迅速增大。由于石油中大量存在着易于使这些菌株生长的各种烃类,使微生物可利用的营养成分充足,进而导致大量的繁殖生长,导致微生物数量迅速提高,石油降油率的增长幅度也迅速提高;28 d 后,土壤中的微生物数量呈下降趋势。由图3(b)可知:在同一含油质量分数(3%)下,加了质量分数为4%的菌剂后降油率的增长幅度大于不加菌剂的增长幅度。而且加菌剂情况下,在适当含油质量分数下,微生物繁殖更快,峰值出现提前14 d,降解效果比不加菌剂明显,降解率高43.04%。研究结果表明:适当质量分数下,石油能够促进植物根际区小分子有机酸、总糖和氨基酸的分泌,植物在石油胁迫下能够呈现积极的反应[15],微生物在适当质量分数下数量也相对较多,而高石油污染物会抑制土壤微生物的生长[6],降低微生物对石油污染物的降解作用。

图3 降油率增长幅度与微生物数量之间 的关系
Fig.3 Relationship between oil degradation rate increased and microbial number
2.4 降油与脱氢酶活性之间的关系
在多种情况下,微生物对石油污染物的降解或转化从脱氢开始,因此,可以利用脱氢酶的活性来反映石油降解微生物的活性。随着微生物在土壤中适应性的增强,微生物数量开始上升,脱氢酶活性也随着增加;但随着营养物质的减少和污染物的降解,可供利用的烃类组分和有机质质量分数逐渐减少,石油降解菌的生长受到抑制,数量减少,最终脱氢酶活性降低[14]。
图4所示为降油率的增长幅度与脱氢酶活性之间的关系。由图4可知:脱氢酶活性的变化随时间的增加呈现出一定的规律,在0~28 d降解过程中脱氢酶活性随着培养时间的增长而不断增强,当降解到28 d左右时土壤中的脱氢酶活性则随着培养时间下降。从图4(b)可以看出:空白组(单一植物降解)细菌的脱氢酶活性明显低于加菌剂-植物联合修复组脱氢酶活性。图4(a)中,含油质量分数较高时脱氢酶活性相对较低,且整体降油增长幅度也较低。 向土壤加入适量的混合菌剂,在7~28 d土壤所添加的氮肥、磷肥促进了冰草的生长,冰草的根系较发达,主要分布于0~15 cm的土层中,具横走或下伸的根状茎,从根部释放出的物质起到了改善和调节冰草与微生物的作用(根系分泌物作用和调控),微生物活性逐渐增强,脱氢酶活性总体也呈上升趋势,而微生物活性在土壤有机物的转化过程中起着很重要的作用,微生物活性增强有利于污染物的降解。在28 d左右脱氢酶活性达到了最高峰,此时微生物有效地降解了土壤中的石油烃类物质,再加上冰草根系发达吸收转化作用也增强,使得石油烃类物质不断消耗,脱氢酶活性逐渐减小,降油率的增长幅度也明显减弱。然而,目前实验还处于起步阶段,至于植物和微生物联合降解石油的深层次机理还有待于进一步研究。
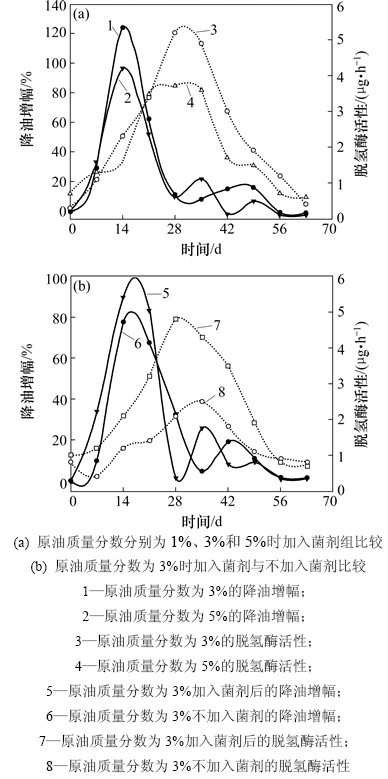
图4 降油率的增长幅度与脱氢酶活性之间的关系
Fig. 4 Relationship between oil degradation rate increased and the activity of dehydrogenase
2.5 植物-菌剂对原油组分降解的影响
图5所示为对照组和植物-混合菌剂组降解质量分数为3%的油污土壤后的正构烷烃离子流图。从图5可知:烃类占原油总质量的85%~100%,其中多半是直链烃,另外是支链烃,低碳数正构烷烃中姥鲛烷(Pr)和植烷(Ph)质量分数最高。
在饱和烃中,直链烷烃最容易被降解。从图5(b)可知:植物-菌剂联合作用对正构烷烃的降解效果明显,丰度下降显著;加菌后正构烷烃高峰区从nC23~nC30前移到nC18~nC22,加菌后微生物对高碳数正构烷烃的降解在前期占优势,长链降解为短链,在短链烷烃上具有叠加效应,故有明显的后峰前移现象。加菌后主峰前移明显,分别从nC25前移到nC20和nC19,而不加菌剂组降解中只有植物作用,主峰明显在后,C16~C30质量分数均较高,表明正构烷烃没有被强烈降解的特征。
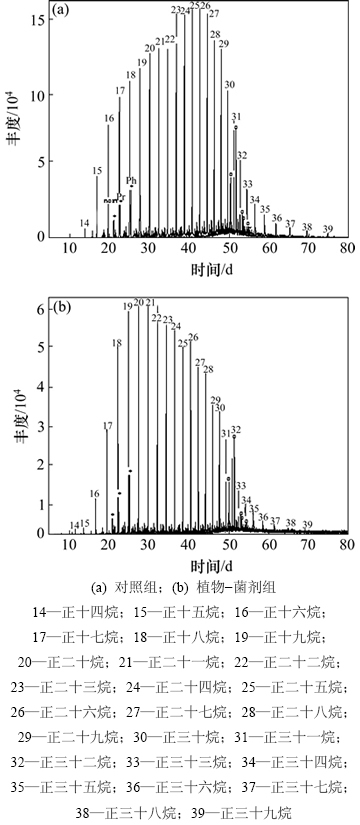
图5 降解前/后正构烷烃离子流图
Fig. 5 TIC of remaining N-alkanes after degradation
图6所示为正构烷烃被降解15 d后正十四烷到正三十九烷的降解趋势。在对正构烷烃各组分的降解中,微生物-植物联合作用对高碳数烷烃的作用大于低碳数烷烃,nC22~nC39烷烃降解率均明显高于不加菌剂组,总体15 d的降解率平均可达60%以上,而不加菌剂组的降解率仅为38%;加菌后正二十三烷和正三十三烷的降解率分别为49.9%和60.4%,较不加菌剂组分别提高34.7%和25.3%。植物-菌剂降解正构烷烃的趋势与文献[5]中报道的正构烷烃的降解演化规律相符。另外,微生物在降解前期对中低碳数的正构烷烃利用率较低,利用多的为高碳数段,即在C31~C39碳数段由于微生物菌种之间表现了协同作用可以稳定共存,促进了该段正构烷烃的降解[16]。正构烷烃降解后的产物也为微生物提供充分可利用的碳源,更有利于微生物的生长,这也是微生物对正构烷烃降解率较高的一个原因[17]。
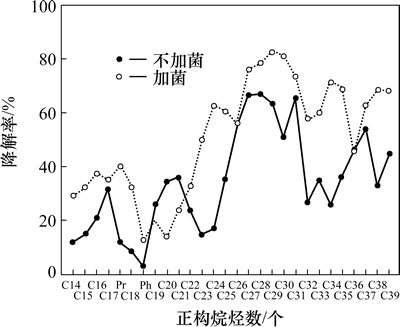
图6 正构烷烃的降解率
Fig. 6 Degradation rate of N-alkanes
3 结论
1) 植物与菌剂联合组的修复性能均高于单一植物组。土壤微生物数量、脱氢酶活性的增加有利于原油的降油。
2) 植物-菌剂联合组的降解效果明显,丰度下降显著;加菌剂后主峰前移明显,分别从nC25前移到nC20和nC19,而不加菌剂组降解中只有植物作用,主峰明显在后,C16~C30质量分数均较高,表明正构烷烃没有被强烈降解的特征。
3) 微生物-植物对高碳数烷烃的降解作用大于低碳数烷烃的降解作用,正二十三烷和正三十三烷的降解率分别较对照组提高了34.7%和25.3%。
参考文献:
[1] Kishore E D, Ashis K M. Crude petroleum-oil biodegradation efficiency of Bacillus subtilis and pseudomonas aeruginosa strains isolated from a petroleum-oil contaminated soil from North-East India[J]. Bioresource Technology, 2007, 98(7): 1339-1345.
[2] 徐金兰, 黄廷林, 唐智新, 等.石油污染土壤生物修复高效菌的降解特性[J]. 石油学报, 2009, 25(4): 570-576.
XU Jinlan, HUANG Tinglin, TANG Zhixin, et al. Characteristics of highly efficient petroleum-degrading bacteria in bioremediation of oil-contaminated soil[J]. Acta Petrolei Sinica, 2009, 25(4): 570-576.
[3] Lu L, Huggins T, Jin S, et al. Microbial metabolism and community structure in response to bioelectrochemically enhanced remediation of petroleum hydrocarbon-contaminated soil [J]. Environmental science & Technology, 2014, 48(7): 4021-4029.
[4] 陈丽华, 马金珠, 雒晓芳. 添加混合菌剂对石油污染土壤的降解研究[J]. 中南大学学报(自然科学版), 2012, 43(11): 4581-4589.
CHEN Lihua, MA Jinzhu, LUO Xiaofang, et al. Degrading of petroleum contaminated soil by injected mixed oildegradation bacterial strains[J]. Journal of Central South University (Science and Technology), 2012, 43(11): 4581-4589.
[5] 雒晓芳, 陈丽华, 王冬梅, 等. 石油降解菌株的分离鉴定及降油特性[J]. 微生物学杂志, 2012, 32(5): 11-17.
LUO Xiaofang, CHEN Lihua, WANG Dongmei, et al. Isolation and identification and degrading characteristics of oil- degradation bacterial strain[J]. Journal of Microbiology, 2012, 32(5): 11-17.
[6] 张海玲, 周立辉, 陈丽华, 等. 修复黄土塬区石油污染土壤的微生物混合菌剂及修复方法: 中国, 201210272041.7 [P]. 2012-08-01.
ZHANG Hailing, ZHOU Lihui, CHEN Lihua, et al. The mixed microbial agent and repair method of bioremediation for petroleum contaminated soil in Loess Tableland: China, 201210272041.7 [P]. 2012-08-01.
[7] ZHOU Qixing, CAI Zhang, ZHANG Zhineng, et al. Ecological remediation of hydrocarbon contaminated soils with weed plant[J]. Journal of Resources and Ecology, 2011, 2(2): 212-221.
[8] 黄盼盼, 周启星. 石油污染土壤对蚯蚓的致死效应及回避行为的影响[J]. 生态毒理学报, 2012, 7(3): 48-53.
HUANG Panpan, ZHOU Qixing. Effects of petroleum- contaminated soil on lethality and avoidance behavior of the earthworm eisenia foetida[J]. Asian Journal of Ecotoxicolog, 2012, 7(3): 48-53.
[9] 马强, 张旭红, 林爱军, 等. 土壤石油烃污染的植物毒性及植物-微生物联合降解[J]. 环境工程学报, 2009, 3(3): 543-548.
MA Qiang, ZHANG Xuhong, LIN Aijun, et al. Plant toxicity and microorganisms-plant degradation for petroleum hydrocarbon contaminated in soil[J]. Journal of Environmental Engineering, 2009, 3(3): 543-548.
[10] 张松林, 董庆士, 周喜滨, 等. 人为石油污染土壤紫花苜蓿田间修复试验[J]. 兰州大学学报(自然科学版), 2008, 44(1): 47-50.
ZHANG Songlin, DONG Qingshi, ZHOU Xibin, et al. Field medicago sativa L. phytoremediation on the artificial oil-polluted soil[J]. Journal of Lanzhou University (Science and Technology), 2008, 44(1): 47-50.
[11] 雒晓芳, 陈丽华, 王冬梅, 等. 复合微生物菌剂对石油污染土壤的修复[J ].生态学杂志, 2013, 32(9): 2433-2438.
LUO Xiaofang, CHEN Lihua, WANG Dongmei, et al. Remediation of oil-contaminated soil by compound microbial preparation[J]. Chinese Journal of Ecology, 2013, 32(9): 2433-2438.
[12] 沈萍, 陈向东. 微生物学实验[M]. 4版. 北京: 高等教育出版社, 2007: 28-34.
SHEN Peng, CHEN Xiangdong, Microbiology experiment[M]. 4th ed. Beijing: Higher Education Press, 2007:28-34.
[13] Sarkar D, Ferguson M, Datta R, et al. Bioremediation of petroleum hydrocarbons in contaminated soils: Comparison of biosolids addition, carbon supp lamentation, and monitored natural attenuation[J]. Environmental Pollution, 2005, 136(1): 187-195.
[14] 刘继朝, 崔岩山, 张燕平, 等. 植物与微生物对石油污染土壤修复的影响[J]. 生态与农村环境学报, 2009, 25(2): 80-83.
LIU Jichao, CUI Yanshan, ZHANG Yanping, et al. Effect of plants and microorganisms on remediation of petroleum contaminated soil[J]. Journal of Ecoloy and Rural Environment, 2009, 25(2): 80-83.
[15] 史德青, 张建, 祝威, 等.胜利油田含油污泥的植物修复研究[J]. 环境污染与防治, 2012, 30(8): 52-55.
SHI Deqing, ZHANG Jian, ZHU Wei, et al. Phytoremediation of oily sludge of Shengli oil field[J]. Environmental Pollution and Control, 2012, 30(8): 52-55.
[16] 顾传辉, 陈桂珠. 石油污染土壤生物降解生态条件研究[J]. 生态科学, 2000, 19(4): 67-71.
GU Chuanhui, CHEN Guizhu. Research of bioremediation condition of petroleum contaminated soil[J]. Ecologic Science, 2000, 19(4): 67-71.
[17] Dubinsky E A, Conrad M E, Chakraborty R, et al. Succession of hydrocarbon-degrading bacteria in the aftermath of the deepwater horizon oil spill in the gulf of mexico[J]. Environmental science & Technology, 2013, 47(19): 10860- 10867.
(编辑 罗金花)
收稿日期:2015-01-29;修回日期:2015-03-29
基金项目(Foundation item):中国石油长庆油田分公司基金资助项目(14AQ-FW-014);国家自然科学基金地区资助项目(41361070);甘肃省自然科学基金资助项目(1308RJZA187);甘肃省教育厅项目(2014B-010)(Project (14AQ-FW-014) supported by the Fund of Chinese Petroleum Changqing Oilfield Company; Project (41361070) supported by National Natural Science Foundation of Area; Project (1308RJZA187) supported by the Natural Science Foundation of Gansu Province;Project (2014B-010) supported by Education Project of Gansu Province)
通信作者:陈丽华,博士,教授,从事土壤石油污染机理与修复研究;E-mail: 673126749@qq.com