文章编号:1004-0609(2013)S1-s0336-07
外科植入物用Ti6Al7Nb和Ti13Nb13Zr合金组织与性能
王卫民,罗斌莉
(西安赛特金属材料开发有限公司,西安 710016)
摘 要:在工业生产条件下,研究Ti6Al7Nb和Ti13Nb13Zr合金的组织、性能和生物相容性;并将Ti6Al7Nb、Ti13Nb13Zr合金与无毒对照组材料在动物体内、体外实验结果进行对比,评价了合金的生物相容性。结果表明:2种合金铸锭的化学成分及其棒、丝材组织与性能均满足GB 23102―2008、ISO 5832―11、ASTM F1295标准要求;生物学性能实验证明,合金不含毒性组元,生物相容性好,是理想的外科植入物材料;其中,Ti6Al7Nb合金的多种形式植入件的近百例临床使用表明疗效良好,适合临床应用。
关键词:外科植入物;Ti6Al7Nb;Ti13Nb13Zr;组织;性能;生物相容性
中图分类号:TG146.2+3 文献标志码:A
Microstructure and mechanical properties of Ti6Al7Nb and Ti14Nb13Zr alloys for surgical implants
WANG Wei-min, LUO Bin-li
(Xi’an Saite Metal Material Co., Ltd., Xi’an 710018, China)
Abstract: Under the commercial run condition, the preparation technology, microstructure, mechanical properties, biological properties and clinical application of Ti6Al7Nb and Ti13Nb13ZrZr alloys were investigate. The results show that the chemical composition, microstructure and properties of bar and sheet meet the challenge of GB23102―2008, ISO5832―11 and ASTM F1295. The alloys possess nontoxic component and better biological compatibility. So, it is preferable surgical implant. The hundreds clinical experimental results show that Ti6Al7Nb has excessively curative effect.
Key words: surgical implants; Ti6Al7Nb; Ti13Nb13Zr; microstructure; properties; biological compatibility
Ti6Al7Nb和Ti13Nb13Zr合金是目前为止研究开发和临床应用最为成功的2种新型外科植入物用钛合金材料[1-5]。Ti6Al7Nb合金由瑞士Sulzer医学技术公司研制开发,工业生产过程与英国IMI钛公司合作进行。它以无毒元素Nb替代有毒元素V,消除了植入物潜在毒性,并具有与Ti6Al4V合金一样的力学性能及疲劳性能。继美国推出ASTM―1295标准后,国际标准化委员会也于1993年颁布了ISO5832―11国际标准;我国于2007年将该合金列入了GB/T13810《外科植入物用钛及钛合金加工材》标准中,2008年12月国家正式颁布GB23102―2008《外科植入物金属材料用Ti6Al7Nb合金加工材》标准[6-8]。
Ti13Nb13Zr合金是美国20世纪90年代研制的仅含有Nb和Zr无毒合金元素、具有低弹性模量、高强度和韧性、优良的抗腐蚀性能和生物相容性的近β型生物医用钛合金。该合金更适合用作软体硬组织修复的替代材料;美国的加工材标准为ASTM F1713―43。我国将Ti13Nb13Zr合金列入国标化学成分标准,牌号TC26,但还没有专门的外科植入物加工材标准。2种合金在国际上均已获得广泛的临床应用[9-10]。
本文作者结合国内用户对Ti6Al7Nb合金植入物产品临床应用取证的需求和国外用户对Ti13Nb13Zr合金加工材的需求,研究了2种合金在工业生产条件下的热加工、热处理工艺、组织性能及材料的生物相容性。
1 实验
1.1 实验方案
原料选用0级海绵钛、纯铝豆、海绵锆,2种合金的Nb元素都以Ti-Nb(Nb质量分数为58.8%)中间合金形式加入。合金按名义成分配料,Ti-Nb中间合金用铝箔分包多个合金包分层添加在电极中,含40%(质量分数)的Ti-Nb中间合金车削与海绵钛混合均匀后直接压制在电极中。电极采用2 000t油压机压制,真空等离子焊箱焊接,在1.5 t电弧炉上经二次真空自耗熔炼制成直径为460 mm的铸锭。
在铸锭的头、中、尾3个部位上取样进行化学成分分析;在距离铸锭的头部120 mm处端面的中心处位置、1/2处位置、3/4处位置共9个点取样进行成分均匀性分析。
铸锭开坯锻造在1 600 t快锻机上进行,锻造温度为1 100~1 250 ℃。对开坯锻造制备的直径220 mm坯料随后下料,用于不同规格棒坯的生产;制定了较大规格(直径为30~75 mm)合金棒材和小规格(直径为2.5~30 mm)棒、丝材、制备工艺及成品热加工工艺、热处理工艺试验方案(如表1所列),以保证产品满足用户对Ti6Al7Nb和Ti13Nb13Zr合金材料不同规格和相应标准的要求。
材料的物理性能、金相组织观察、力学性能、骨植入试件均在成品上取样。
表1 实验方案
Table 1 Experimental scheme

1.2 组织与性能检测
金相试样采用HF、HNO3、H2O(体积比为1:3:10)的腐蚀剂腐蚀,采用NIKON金相显微镜分析试样的显微组织。采用MTS810拉伸试验机测试试样的室温拉伸性能。
2种合金的生物学性能实验以大白兔和豚鼠为实验对象,进行了体外细胞毒性(GB/T 16886.5―2003)、骨植入试验(GB/T 16886.6―1997)。其中,骨植入试验是将直径×长度为1.5 mm×6 mm,光洁度高于0.8 μm的Ti6Al7Nb和Ti13Nb13Zr合金试件和对照样品植入大白兔体内1~26周,使用光学显微镜分别观测了1周、4周、12周和26周的显微组织;体外细胞毒性、等试验还使用了T-1000电子天平、CO2培养箱、酶标仪、2135切片机等仪器设备。
2 结果与讨论
2.1 铸锭的化学成分及均匀性分析
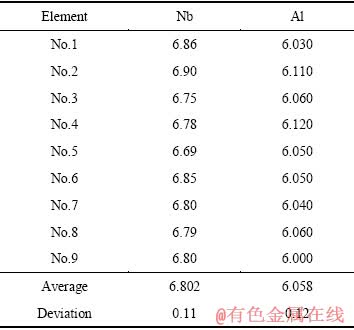
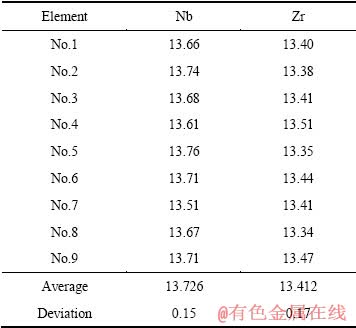
表2和3所列分别为2种合金的工业化生产铸锭头、中、尾的化学成分;为了考核合金的成分均匀性,试验还对合金铸锭头部120 mm处端面主成分的均匀性进行了分析,结果见表4和5。
从表2和3可以看出,2种合金铸锭头、中、尾的主成分偏差很小,杂质含量也在正常水平。从表4和5可知:Ti6Al7Nb合金主成分Nb最大偏差为0.11%、Al最大偏差为0.12%;Ti13Nb13Zr合金主成分Nb最大偏差为0.15%、Zr最大偏差为0.17%。合金成分没有偏析,符合国家及国际标准要求。分析结果表明,2种合金生产采用的添加NbTi中间合金及其配料方法,以及制定的熔炼工艺路线合理可行。
2.2 热加工对显微组织和性能的的影响
国外用户需求的Ti13Nb13Zr合金材料和国内用户对Ti6Al7Nb合金植入件的临床应用研究需求,涉及到合金各种规格棒、丝材冶金半成品产品,而医用热加工钛合金产品,要获得满足标准要求的均匀细小的等轴组织,优化热加工工艺是关键[11]。
表2 Ti6Al7Nb合金铸锭的化学成分
Table 2 Composition of Ti6Al7Nb alloy (mass fraction, %)
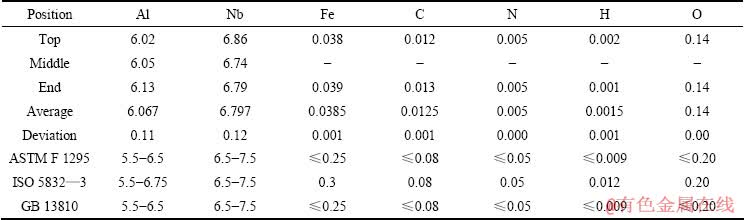
表3 Ti13Al13Nb合金铸锭的化学成分
Table 3 Composition of Ti13Nb13 Zr alloy (mass fraction, %)
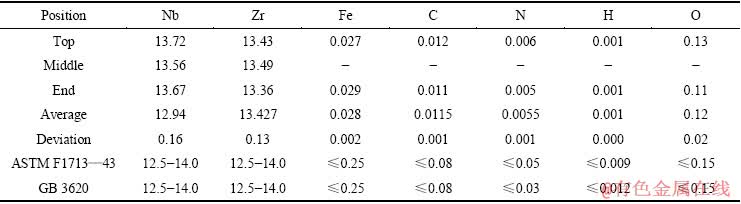
表4 Ti6Al7Nb合金铸锭端面化学成分
Table 4 Composition of Ti6Al7Nb alloy (mass fraction, %)
生产和研究按试验方案进行了热加工工艺试验,大规格棒坯生产采用了特殊的温度梯度组合变形工艺(工艺1A);小规格棒材在两相区较低温度轧制加工,并控制道次变形量(工艺2B)[12-14]。2种合金按表1工艺方案1、2制备的棒坯及精锻棒、轧棒均获得评级要求的等轴显微组织,2种合金热加工状态典型的显微组织照片见图1~3。不同规格棒材的力学性能见表6。
表5 Ti13Nb13Zr合金铸锭端面化学成分
Table 5 Composition ofTi13Nb13Zr alloy (mass fraction, %)
2.3 热处理对显微组织和性能影响
研究表明,Ti6Al7Nb合金在700 ℃退火时,α相发生再结晶,形成初生α+少量β转变组织;当温度升高到800 ℃时,组织晶粒已完全等轴化;当温度为900 ℃时,在加热过程中,相当数量的α相转变成针状β相,形成典型的双态组织;当加热温度在1 000 ℃时,组织呈现魏氏组织特征,具有明显的β片状组织和清晰的β晶界。图4所示为Ti6Al7Nb合金800 ℃和1 000 ℃退火态典型的显微组织照片。

图1 Ti6Al7Nb和Ti13Nb13Zr合金棒坯的横断面金相组织
Fig. 1 Metallographs of Ti6Al7Nb (a) and Ti13Nb13Zr (b) alloy bar blank

图2 Ti6Al7Nb和Ti13Nb13Zr合金精锻棒金相照片
Fig. 2 Microstructures of Ti6Al7Nb (a) and Ti13Nb13Zr (b) forging alloys

图3 Ti6Al7Nb和Ti13Nb13Zr合金轧棒显微组织
Fig. 3 Microstructures of Ti6Al7Nb (a) and Ti13Nb13Zr (b) alloy
表6 Ti6Al7Nb和Ti13Nb13Zr合金棒材的室温拉伸性能
Table 6 Mechanical properties of foreign Ti6Al7Nb and Ti13Nb13Zr alloy bars
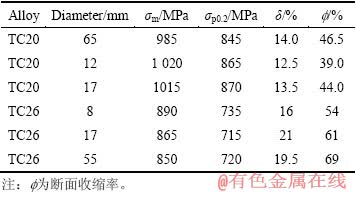
与此对应,在700~900 ℃下退火,组织为等轴再结晶α+(β)转变组织。在相变点以上的1 000 ℃加热时,由于形成了粗大的片状魏氏组织,使合金材料的塑性降低(表7)。因此,Ti6Al7Nb合金退火处理温度应为700~900 ℃。
Ti13Nb13Zr合金为近β合金,合金的α+β→β转变温度为735 ℃。工业生产中采用了780 ℃、1~2 h固溶退火和(780 ℃、1 h)+(500 ℃、4~6 h)固溶时效工艺,其成品典型显微组织和性能见图5及表8。
2.4 合金的物理性能
2种合金的相变点、密度、硬度、弹性模量、冲击韧性列于表9。由表9可知,Ti13Nb13Zr合金具有更低的弹性模量,弹性模量更接近人骨。

图4 Ti6Al7Nb合金不同退火温度的金相组织
Fig. 4 Metallographs of Ti6Al7Nb alloy at different annealing temperatures
表7 不同退火温度Ti6Al7Nb合金退火后的室温拉伸性能
Table 7 Mechanical properties of Ti6Al7Nb alloy bars at different annealing temperatures
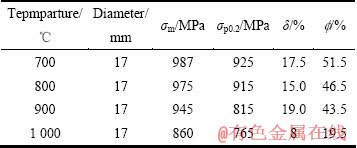
2.5 合金的断裂韧性
2种合金的断裂韧性见表10。从表10可知:2种合金的断裂韧性相当。
2.6 合金的疲劳性能
2种合金的物理性能列于表11。可见:2种合金的疲劳性能也相当。

图5 Ti13Nb13Zr合金固溶及固溶时效的显微组织
Fig. 5 Microstructure of annealing Ti13Nb13Zralloy
表8 Ti13Nb13Zr合金固溶和固溶时效态的室温拉伸性能
Table 8 Mechanical properties of Ti13Nb13Zr alloy bars after solution and ageing
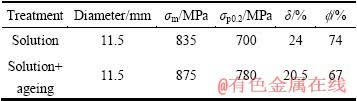
表9 Ti6Al7Nb和Ti13Nb13Zr合金的物理性能
Table 9 Physical properties of Ti6Al7Nb and Ti13Nb13Zr alloy

2.7 生物相容性评价
通过对比Ti6Al7Nb和Ti13Nb13Zr合金和无毒对照组材料在动物体内、体外实验的结果,客观评价了2种合金的生物相容性。2种合金的生物相容性(炎细胞密度和纤维膜的厚度)和生物毒性试验结果见表12和13。
体外细胞毒性试验结果表明,2种合金对豚鼠的膜腔细胞和Hela细胞的形态无明显影响,RGR水平分别为100和101,细胞毒性反应级别为0(标准要求不大于1级),符合要求。
表10 Ti6Al7Nb和Ti13Nb13Zr合金的断裂韧性
Table 10 Fracture toughness property of Ti6Al7Nb and Ti13Nb13Zr alloys

表11 Ti6Al7Nb和Ti13Nb13Zr合金的疲劳韧性
Table 11 Fatigue property of Ti6Al7Nb and Ti13Nb13Zr alloy

骨植入试验检测结果表明,植入1周样品局部反应评价计分为0.71分;植入4周为1.04分;植入12周为1.76分;植入26周为0分;刺激等级均为无刺激。组织学切片显微镜检查结果表明,植入26周后,Ti6Al7Nb和Ti13Nb13Zr合金试样周围形成较薄纤维囊壁,膜厚已符合美国材料学会(ASTM)测定外科植入材料委员会(F4)提出的标准。组织学切片显微镜检查试验组织见图6。
表12 Ti6Al7Nb和Ti13Nb13Zr合金的生物相容性
Table 12 Biology Compatibility of Ti6Al7Nb and Ti13Nb13Zr

表13 Ti6Al7Nb和Ti13Nb13Zr合金的生物毒性
Table 13 Bitoxicity of Ti6Al7Nb and Ti13Nb13Zr
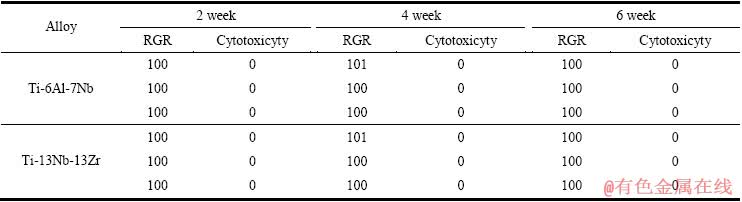
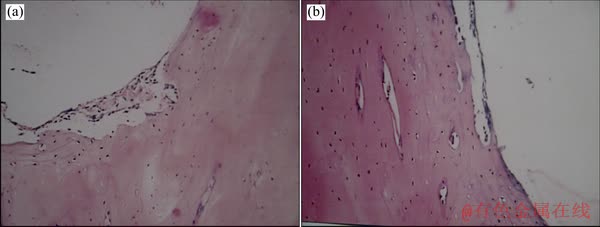
图6 Ti6Al7Nb和Ti13Nb13Zr合金种植体组织学切片
Fig. 6 Microstructures of Ti6Al7Nb (a) and Ti13Nb13Zr (b) alloys after 26 weeks
2.8 应用
医疗器械生产厂用本研究提供的Ti6Al7Nb合金棒、丝材制作了内固定螺丝、股骨头组合髋关节、脊柱矫形固定系统等外科植入件并应用于临床治疗和取证。至2012年12月,已完成临床手术近百例,治疗效果良好。为国内临床研究提供Ti13Nb13Zr合金棒材400 kg,为国外用户提供成品棒丝材近1 500 kg。
3 结论
1) 研制生产的Ti6Al7Nb和Ti13Nb13Zr合金化学成分、显微组织和力学性能均达到GB/T 13810―2007、GB 23102―08、ASTM F 1295、ISO 5832―3标准的要求。
2) 在工业生产条件下通过控制配料方法、熔炼、热加工及热处理工艺,可获得成分均匀、无偏析、组织性能优良的Ti6Al7Nb和Ti13Nb13Zr合金加工材。
3) 生物毒性实验结果表明,Ti6Al7Nb和Ti13Nb13Z合金具有优良的生物相容性。已研制生产的多种Ti6Al7Nb和Ti13Nb13Z合金植入器件临床应用百例,效果良好。
REFERENCES
[1] ITO Y, OKAZAKI Y, ITO A, TATEISHI T. New titanium alloys for medical implants[C]//Titanium’95: Science and Technology. London:The Instiute of Materials, 1996: 1776-1783.
[2] MISHRA A K, DAVIDSON J A, POGGIE R A, KOVACS P, FITZGERALD T J. Biocompatible titanium alloy[C]//EYLON D, BOYER R R, KOSS D A. Beta Titanium Alloy in 1990’s, Warrendale, PA: TMS, 1993: 61.
[3] WANG K, GUSTAVSON L, DUMBLETON J. The characterization of Ti-12Mo-6Zr-2Fe―A new biocompatible titanium alloy developed for surgical implants[C]//EYLON D, BOYER R R, KOSS D A. Beta Titanium Alloy in 1990’s, Warrendale, PA: TMS, 1993: 61-63.
[4] SEMLITSCH M, WEBER H, STEGER R. Experience with Ti-6Al-7Nb alloy for joint replacements’ titanium[C]//Proc 8th Int Conf on Titanium. Birmingham: The Institute of Materials, 1995: 1742-1743.
[5] BOYER R, COLLINGS E W, WELSCH G. Materials properties hand book: Titanium alloys[M]. Kinsman: ASM International, 1994.
[6] 魏寿庸, 何 瑜, 陈占乾, 白晓环. 外科植入用Ti-6Al-7Nb钛合金的工艺、组织和性能[J]. 金属学报, 2002, 38(1): 132-134.
WEI Shou-yong, HE Yu, CHEN Zhan-qian, BAI Xiao-huan. The Process,microstructure and properties of Ti-6Al-7Nb alloy used in surgical implant[J]. Acta Metallurgica Sinica, 2002, 38(1): 132-134.
[7] 王桂生, 许国栋, 魏寿庸, 李渭清. 外科植入用钛合金Ti-6Al-7Nb的研究[J]. 稀有金属, 2001, 25(5): 395-397.
WANG Gui-sheng, XU Guo-dong, WEI Shou-yong, LI Wei-qing. The study of Ti-6Al-7Nb alloys for surgical implant[J]. Chinese Journal of Rare Metals, 2001, 25(5): 395-397.
[8] 牛中杰, 曹继敏, 杨冠军, 王廷询. Ti-6Al-7Nb钛合金热加工与热处理工艺研究[J]. 钛工业进展, 2006, 23(1): 24-27.
NIU Zhong-jie, CAO Ji-min, YANG Guan-jun, WANG Ting-xun. Study on heat machining and heat treatment process of Ti-6Al-7Nb alloy[J]. Titanium Industry Progress, 2006, 23(1): 24-27.
[9] 付艳艳, 周 廉, 于振涛, 王克光. Ti-13Nb-13Zr合金加工性能和显微组织研究[J]. 稀有金属, 2004, 28(1): 39-43.
FU Yan-yan, ZHOU Lian, YU Zhen-tao, WANG Ke-guang. Mechanical properties and microstructures of Ti-13Nb-13Zr alloy[J]. Chinese Journal of Rare Metals, 2004, 28(1): 39-43.
[10] 黄永光. 外科植入用钛合金材料及其标准化[J]. 金属学报, 2002, 38: 530-532.
HUANG Yong-guang. Titanium alloy materials for surgical implant application and standardization[J]. Acta Metallurgica Sinica, 2002, 38: 530-532.
[11] 张 翥, 惠松骁, 刘 伟. 高强高韧TB10钛合金棒材研究[J].稀有金属, 2006, 30(2): 221-225.
ZHANG Zhu, HUI Song-xiao, LIU Wei. High strength and high toughness TB10 titanium alloy bars[J]. Chinese Journal of Rare Metals, 2006, 30(2): 221-225.
[12] 王卫民, 林邵华, 李 雷, 曹继敏. 外科植入物用Ti6Al4V(ELI)合金棒材的成分、组织和力学性能[J]. 中国有色金属学报, 2010, 20(1): 555-559.
WANG Wei-min, LIN Shao-hua, LI Lei, CAO Ji-min. Composition, microstructure and mechanical properties of Ti6Al4V(ELI) alloy bars for surgical implants[J]. The Chinese Journal of Nonferrous Metals, 2010, 20 (1): 555-559.
[13] 王卫民, 林邵华, 曹继敏, 张占英. 热加工工艺对医用TC4合金棒材显微组织的影响[J]. 钛工业进展, 2012, 29 (3): 14-18.
WANG Wei-ming, LIN Shao-hua, CAO Ji-min, ZHANG Zhan-ying. Effect of thermal processing on microstructure of medical TC4 alloy bars[J]. Titanium Industry Progress, 2012, 29(3): 14-18.
[14] 王卫民, 林海峰, 罗斌莉, 杨华斌, 曹继敏. 外科植入物用Ti-6A1-7Nb合金板、棒丝材制备及性能表征[J]. 钛工业进展, 2013, 30(2): 11-16.
WANG Wei-min, LIN Hai-feng, LUO Bin-li, YANG Hua-bin, CAO Ji-min. Preparation and properties characterization of Ti-6Al-7Nb alloy plates, bars and wires used for surgical implants[J]. Titanium Industry Progress, 2013, 30(2): 11-16.
(编辑 赵 俊)
收稿日期:2013-07-28;修订日期:2013-10-10
通信作者:王卫民,高级工程师;电话:029-86527655;E-mail:wwm631018@163.com