DOI: 10.11817/j.ysxb.1004.0609.2020-35823
报废动力电池镍钴锰酸锂三元正极材料高温氢还原-湿法冶金联用回收有价金属
郭苗苗1, 2, 3, 4,席晓丽1, 2,张云河3, 4, 5,余顺文3, 4,龙小林3, 4,蒋振康3, 4, 5,聂祚仁1, 2,许开华3, 4, 5
(1. 北京工业大学 材料与制造学部,北京 100124;
2. 工业大数据应用技术国家工程实验室,北京 100124;
3. 荆门市格林美新材料有限公司,荆门 448124;
4. 国家电子废弃物循环利用工程技术研究中心,荆门 448124;
5. 格林美股份有限公司,深圳 518101)
摘 要:通过高温氢还原和湿法冶金联用的方法回收报废动力电池镍钴锰酸锂三元正极材料中的镍、钴、锰以及锂金属,并对其回收机理及工艺进行研究。结果表明:报废三元正极材料经过高温氢气还原后,在层状镍钴锰酸锂结构中的锂迁移到表面,变成LiOH、LiOH・H2O和少量的Li2CO3;镍钴锰由之前的Co2+、Ni3+和Mn4+分别还原成了Co0、Ni0和 MnO,其在还原水洗后物料的表面相分别为Ni(OH)2和Co(OH)2及MnO;还原后的LiOH、LiOH・H2O和少量的Li2CO3经过水浸、酸洗、沉淀后,可得纯度为99.5%的Li2CO3,实现了锂与镍、钴、锰的分离;还原后的镍、钴和MnO经过硫酸酸浸后,镍、钴和锰浸出率分别为96.88%、97.23%和99.78%。浸出后溶液经氧化沉淀及萃取分离,锰沉淀分离率为98.46%,萃取分离后氯化钴和氯化镍溶液杂质含量低于10 mg/L。
关键词:镍钴锰酸锂;三元正极材料;报废;氢气还原;回收;机理
文章编号:1004-0609(2020)-06-1415-12 中图分类号:X705 文献标志码:A
动力锂离子电池自1991年发明以来,因其广泛应用在3C、电动工具、电动汽车、储能等领域,发展迅速[1-2]。特别是近几年燃油汽车逐渐被新能源动力汽车取代,动力电池车的市场比例逐年上升,大量三元动力电池进入消费端,也因此产生了大量的报废动力电池[3]。
报废的动力电池中含有大量的有价金属,随意丢弃及处理,不仅造成钴、镍、锰、锂等资源的极大浪费,还会严重污染环境[3-4],因此,亟需开发出一种绿色无污染的、可大规划工业化的处理方法。大量文献报道了报废动力电池回收及资源化方法[5-6],归纳起来可分为湿法[5-10]、火法[11-12]、生物法[13]及几种方法联用法[14-15]。以上处理方法中,生物法浸出时间长,在重金属离子种类多且含量高时,细菌的繁殖和生存都很困难,产业化效率低[13];火法处理工艺设备成本高、能耗大且需要投入庞大的尾气处理系统,产业化应用受限[11-12];废旧电池湿法处理工艺的研究及应用最为广泛,文献及专利统计中占比为57.25%[3]。但报废镍钴锰三元正极材料(以下简称三元正极材料)中Co3+和Mn4+很难被硫酸、盐酸、草酸、柠檬酸、氨基磺酸、磷酸等完全溶解,需在溶解酸中加入还原剂把+3价钴和+4价镍还原成低价,才能完全溶解[7-8]。浸出溶液中的镍、钴、锰、锂4种有价金属可以通过共沉淀法制备镍钴锰化合物[16-19],也可以通过沉淀法、萃取法、氧化还原等方法进行分离[7-10]:共沉淀法制备的化合物单一,后续产品应用范围有限;镍钴锰锂可通过湿法工艺分离成4种金属盐类,应用范围广,但4种金属的分离步骤长,导致整体金属特别是锂金属回收率低及产品纯度不高,且废水量大[15, 20]。为了实现镍钴锰锂金属的选择性溶解及分离,HU等[15]利用高温褐煤还原和湿法冶金结合的方法,采用褐煤还原报废的三元正极材料,使三元材料在高温阶段还原成钴、镍、MnO和Li2CO3,把溶液中需要加还原剂还原的步骤改为褐煤还原,然后以通入CO2的水浸出以上还原后的混合物,Li2CO3转变为LiHCO3溶解,剩余的镍钴锰在浸出渣中,实现了锂的选择性溶解及与镍、钴、锰的分离,但是此方法还原及锂浸出方式复杂,锂浸出液含量低至4.365 g/L,锂的浸出率也只有84.7%,并且酸浸提镍钴锰后固体尾渣中过量褐煤残留的碳含量高达95.6%,为含有镍钴锰的危险废物,需无害化处理。
为了进一步解决以上选择性浸出工艺中锂收率低、简化镍、钴、锰、锂的回收工艺,本研究采用高温氢还原和湿法冶金联用工艺,报废镍钴锰酸锂三元正极粉经过高温氢还原成Co0、Ni0、MnO和LiOH或LiOH・H2O,采用纯水选择性浸出锂离子,少量的草酸溶液洗涤滤渣,随后用碳酸钠沉淀出碳酸锂产品,分离锂与镍、钴、锰金属。通过XRD及XPS的分析,研究还原前后三元正极粉的各种金属的存在物相结构以及还原前后颗粒表面锂、镍、钴、锰有价金属的存在形态及价态,阐明锂、镍、钴、锰离子的迁移过程以及其浸出机理;最后通过沉淀、萃取等湿法冶金方法分离及回收镍、钴、锰金属,实现了废旧锂离子电池中有价金属的完全分离及回收。
1 实验
1.1 实验原料与实验方法
本实验的报废三元动力电池来自于荆门市格林美新材料有限公司,经过拆解、破碎、正负极分离、过筛、除铁、除铝等除杂步骤,最后报废正极粉的组成及含量如表1所示,实验具体步骤如图1所示,所有试剂都是工业纯,没有进一步提纯。
表1 处理后报废三元正极材料组成
Table 1 Composition of waste ternary cathode materials after treatment (mass fraction, %)
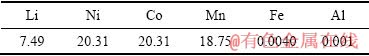

图1 报废三元正极材料有价金属回收工艺流程图
Fig. 1 Process flow diagram of recovering valuable metals from waste ternary cathode materials
实验的高温氢还原在双管推杆炉中还原,还原气体为摩尔比3:1的氢气和氮气混合气,固定还原时间为3h,考察不同还原温度对还原结果的影响。湿法冶金实验在50 L反应釜中进行:水浸锂实验取10 kg氢气还原后的报废三元正极材料,加入40 L的水,在常温条件下,以100 r/min的搅拌速度搅拌0.5 h(搅拌时间的实验除外),抽滤,滤液备用;渣再投入反应釜中,加入40 L的水,用草酸固体调节酸洗液的pH,以100 r/min搅拌转速搅拌洗涤0.5 h,抽滤,渣用于酸浸钴镍锰金属,洗液和滤液合并用于锂的沉淀;锂沉淀过程为取以上洗液和滤液40 L溶液,用碳酸钠固体调节溶液的pH为14,抽滤,洗涤,烘干,得到碳酸钠固体粉末;除锂后的洗渣烘干,称取5 kg,加入50 L反应釜,加入过量系数不等的3 mol/L的稀硫酸,定容到20 L,常温,100 r/min搅拌2 h,过滤分离得到渣及镍钴锰的硫酸溶液;之后在20 L的镍钴锰溶液中,用0.5 mol/L的氢氧化钠溶液缓慢滴入调节溶液pH,然后升温到50 ℃,加入化学计量比的高锰酸钾沉淀锰,过滤分离固体和镍钴溶液;镍钴溶液进入混合室体积为200 mL的连续萃取槽中用P507进行连续逆流萃取,通过调节萃取的油相比、萃取级数,使得钴镍及少量的锰全萃取,然后用5 mol/L的盐酸进行反萃,调节反萃的有机相和反酸比例以及反萃级数,来控制出料的氯化钴、氯化镍及氯化锰的浓度及杂质含量,得到杂质含量低的氯化钴、氯化镍及少量氯化锰溶液。
1.2 实验表征方法
通过等离子发射光谱仪(日本岛津,ICPE-9810)检测不同金属离子的含量或者浓度。pH计(梅特勒-托利多,S210)用来检测和调控浸出或反应过程中的pH。XRD(日本岛津XRD-6100,铜靶)用来分析各种中间产物及产品的物相及结构。废旧LiNi1/3Co1/3Mn1/3O2及其还原后产物的形貌及元素分布通过扫描电子显微镜(SEM,美国QUANTA 250FEG)和其附带能量色散仪(EDS,EDAX Genesis-SiLi)检测。报废LiNi1/3Co1/3- Mn1/3O2正极材料通过激光粒度仪(LS-800)测试粒度,比表面积通过比表面仪(NOVA4000e,JS00087)检测。X射线光电子能谱仪(XPS,英国,Axis Supra)用来分析各种物料中各元素的价态及表面物相。
2 结果与讨论
2.1 报废镍钴锰酸锂三元正极材料分析
报废镍钴锰酸锂三元正极材料经过除铁及除铝后,含量如表1所示,正极粉中的镍钴锰含量分别为20.31%、20.31%和18.75%,计算镍钴锰的摩尔比为1.01:1.01:1,基本符合LiNi1/3Co1/3Mn1/3O2中镍钴锰的元素比。锂含量为7.49%,铁和铝的含量低于50 mg/kg,说明经处理之后,铁、铝含量较低,本研究重点在于锂、镍、钴、锰元素回收。LiNi1/3Co1/3Mn1/3O2正极粉激光粒径测试粒度为10 μm,比表面积为3.8 m2/g,振实密度为2.46 g/cm3,为致密的球形颗粒,且因LiNi1/3Co1/3Mn1/3O2粉中镍、钴、锰的价态分别为+2、+3、+4价,需要把Co3+和Mn4+还原成低价才能被被酸完全溶解,因此采用高温氢还原-湿法冶金联用工艺流程[7]。
2.2 氢气还原机理分析
2.2.1 还原温度对报废三元材料物相结构影响分析
LiNi1/3Co1/3Mn1/3O2粉中镍、钴、锰的价态分别为+2、+3、+4价,而其在水溶液中的稳定价态为+2价,为了将粉体中镍、钴、锰完全浸出到溶液中,需要将材料中高价态的金属还原成+2价或更低价。图2所示为不同还原温度还原的报废LiNi1/3Co1/3Mn1/3O2正极粉的XRD谱。从图2中可知,350 ℃时与还原前晶相一致,属于LiMO2层状结构(M=Ni, Co, Mn),即尚未发生明显的还原反应[21-22]。而450 ℃时出现多种物相,包括钴、镍单质、MnO及 LiOH、LiOH・H2O、Li2CO3等[15],据此判断可能的反应方程式如下:
6LiNi1/3Co1/3Mn1/3O2+7H2→2Co+2Ni+2MnO+6LiOH+4H2O (1)
LiOH非常容易吸水,上述反应发生后LiOH可直接吸收还原过程产生的H2O,或物料移出还原设备后吸收空气中的水分形成LiOH・H2O。原始物料为LiNi1/3Co1/3Mn1/3O2并不含碳,且还原过程中气氛为H2/N2混合气,并无CO2,因此,物相中少量的Li2CO3 推测为还原后物料接触空气中CO2反应产生[23-24],方程式如下:
2LiOH+CO2→Li2CO3+H2O (2)
当还原温度上升至550 ℃之后,开始出现LiMnO2 物相,MnO衍射峰减弱,在650 ℃时,MnO物相对应的衍射峰消失,LiMnO2峰强度增加,表明更高温度下,活泼的LiOH、MnO开始反应形成锰酸锂[25],可能发生反应方程式如下:
2LiOH+2MnO→ 2LiMnO2+H2 (3)
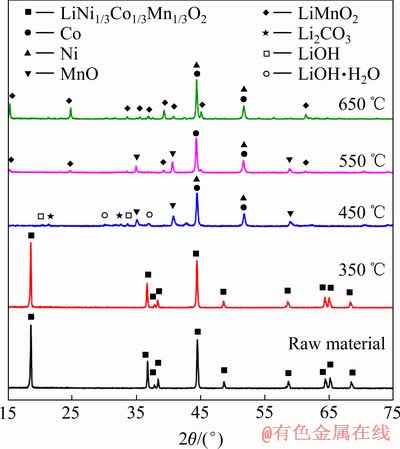
图2 不同还原温度对LiNi1/3Co1/3Mn1/3O2正极材料物相的影响
Fig. 2 Effects of different reduction temperatures on phase of LiNi1/3Co1/3Mn1/3O2 cathode materials
2.2.2 氢还原报废三元材料锂表面价态及物相分析
图3所示为450 ℃还原报废三元正极材料刻蚀前后的XPS谱。由图3所示的Li 1s图谱可知,还原后的三元正极锂在刻蚀前后结合能为54.9 eV,可推测锂为+1价。然而根据还原后样品C 1s的图谱,可知表面主要存在两种碳,一种是被污染的碳,其结合能在284.8 eV左右,另一种碳的结合能在289.8 eV,归属于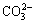 中的碳,故推测表面可能有Li2CO3[26];但是还原后的样品经过刻蚀之后,C 1s图谱发生了显著的变化,表面的污染碳峰基本消失,而碳酸根的碳峰继续存在,但是强度已经减弱,说明刻蚀之后表面的碳酸盐浓度发生了变化,同时也进一步证明了表面碳酸锂的存在,并且深度超过10 nm。由O 1s图谱可见,氧的结合能为531.21 eV 可能是
中的碳,故推测表面可能有Li2CO3[26];但是还原后的样品经过刻蚀之后,C 1s图谱发生了显著的变化,表面的污染碳峰基本消失,而碳酸根的碳峰继续存在,但是强度已经减弱,说明刻蚀之后表面的碳酸盐浓度发生了变化,同时也进一步证明了表面碳酸锂的存在,并且深度超过10 nm。由O 1s图谱可见,氧的结合能为531.21 eV 可能是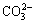 中的氧,也可能是OH-的氧,在不同文献中[27-29],碳酸锂的锂和氢氧化锂的锂的结合能稍微有区别,在55.1~55.3 eV;在刻蚀之后,绝大多数的氧继续以碳酸盐和氢氧根的形式存在,但是在528.1 eV左右出现了一个小峰,根据文献[27],这个小峰是锂的化合物Li2CO3和LiOH在氩刻蚀过程中转化为Li2O的氧晶格峰。这也充分说明了经过还原后,三元正极材料表面的锂主要为LiOH和Li2CO3,Li2CO3由LiOH和CO2反应而得,深度超过了10 nm。
中的氧,也可能是OH-的氧,在不同文献中[27-29],碳酸锂的锂和氢氧化锂的锂的结合能稍微有区别,在55.1~55.3 eV;在刻蚀之后,绝大多数的氧继续以碳酸盐和氢氧根的形式存在,但是在528.1 eV左右出现了一个小峰,根据文献[27],这个小峰是锂的化合物Li2CO3和LiOH在氩刻蚀过程中转化为Li2O的氧晶格峰。这也充分说明了经过还原后,三元正极材料表面的锂主要为LiOH和Li2CO3,Li2CO3由LiOH和CO2反应而得,深度超过了10 nm。
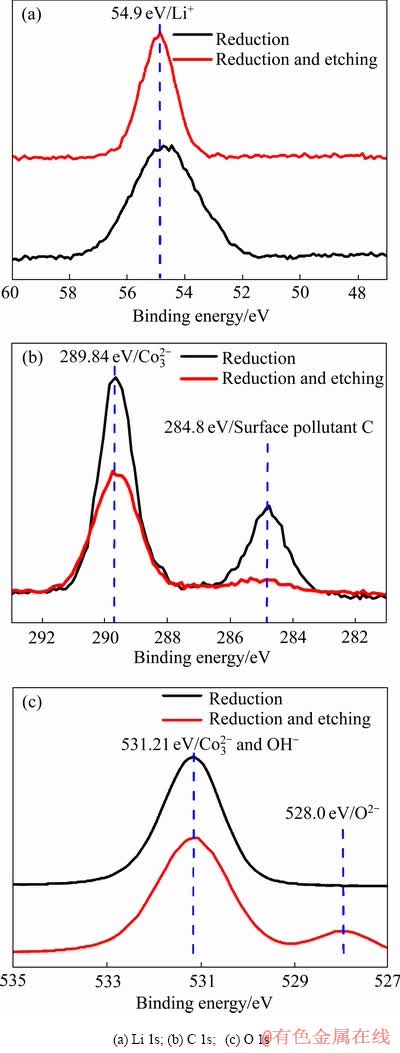
图3 450 ℃还原报废三元正极材料刻蚀前后XPS谱
Fig. 3 XPS spectra of waste ternary cathode materials under reduction at 450 ℃ before and after etching
2.2.3 氢还原报废三元材料表面镍、钴、锰价态及物相分析
图4所示为废正极粉原料、原料经过还原以及还原水洗后的XPS谱。由图4可知,原料中镍、钴、锰 2p3/2的结合能分别为854.8、779.7和642.3 eV,和文献报道的三元材料中+2镍、+3钴、+4锰价态分布一 致[7, 21, 30]。 报废正极粉经过还原后,表面探测不到镍、钴和锰的峰,而是被锂完全覆盖。该还原后的正极粉经过水洗去掉表面覆盖的锂之后,材料表面的镍、钴、锰2p3/2的结合能发生了偏移,镍和钴分别为856.0 eV和781.4 eV,分别对应了Ni(OH)2和Co(OH)2[31],可能是还原之后的钴粉和镍粉在氢氧化锂水溶液中,表面生成了碱式盐;而锰的峰偏移至641.5 eV,表明了锰的价态为+2价,推测是以一氧化锰氧化物的形式存在,和图2中不同还原温度对LiNi1/3Co1/3Mn1/3O2正极材料物相的XRD的结果一致,没有发生表面变化。
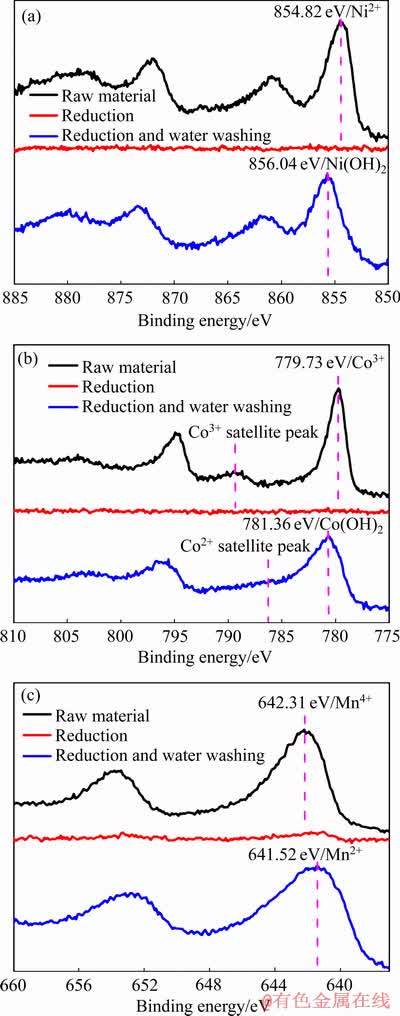
图4 报废正极粉原料、还原后、还原水洗后的Ni 2p、Co 2p和Mn 2p 的XPS谱
Fig. 4 XPS spectra of Ni 2p(a), Co 2p(b), and Mn 2p(c) of waste cathode materials (untreated, after reduction, and after reduction and washing)
2.2.4 氢还原对报废三元正极材料表面元素迁移的影响
图5所示为450 ℃氢气还原报废LiNi1/3Co1/3- Mn1/3O2 正极材料前后的EDS谱。由图5可知,报废三元正极材料中镍、钴、锰是均匀分布的,经过氢气还原后,宏观球形形貌被破坏,同时镍钴锰的分布变得不均匀,和文献报道一致[15],在还原过程中破坏了原有的微观均匀层状结构,生成了钴、镍金属和锰的氧化物,有部分合金聚集,意味着还原过程中发生了镍、钴、锰的迁移,有利于镍钴锰固体混合物的酸浸出。同时,由图4可知,原料在被还原之后,表面只有锂的峰,说明在高温还原过程中,材料表面被锂所覆盖,也说明了锂由原来层状结构中间迁移到了表面,便于后面的水浸出工艺浸出锂。
2.3 锂回收工艺及其机理分析
2.3.1 不同还原温度对锂浸出效率的影响
图6所示为经过不同还原温度还原后的正极材料在固液比(g/mL)为1:10、常温水溶液中的浸出率。由图6可见,在水浸出条件下,钴、镍、锰金属浸出率低于0.08%,几乎不浸出;在450 ℃之前,锂的浸出率随着还原温度的升高而提高;到450 ℃时,锂的浸出率最大为93.61%,正极材料还原温度升高至650 ℃时,锂在水溶液中的浸出率下降至69.08%,这是在不同还原温度下报废正极三元材料还原出的物相不同所致。由图2可知,在不同还原温度下,锂存在物相及形态发生变化;在原料及350 ℃还原条件下,锂以LiNi1/3Co1/3Mn1/3O2的形式存在,镶嵌在LiNi1/3Co1/3- Mn1/3O2层状结构之间,在充放电过程中,在正负极电势差下实现来回迁移。在纯水中,报废正极材料中锂的浸出率为0.2%,几乎不溶于水。经过350 ℃焙烧后,锂虽然还是以LiNi1/3Co1/3Mn1/3O2的形式存在,但部分锂在高温还原过程中以氢氧化锂形式迁移到了LiNi1/3Co1/3Mn1/3O2表面,废弃三元物料经过不同处理方式处理后镍、钴、锰的XPS也说明这一点(见图4);氢氧化锂在水中的溶解度很大,所以有16%的锂被浸出。在450 ℃还原条件下,锂以LiOH和LiOH・H2O及 Li2CO3存在,对比图7可发现,水洗后Li2CO3和LiOH峰消失,只有少许LiOH・H2O峰存在,说明450 ℃还原的LiNi1/3Co1/3Mn1/3O2中的锂大部分转变为可溶的LiOH,有少部分被空气中二氧化碳沉淀的Li2CO3,在水浸出时,锂的浸出率高达93.61%。在550 ℃之后,锂开始少量转变成LiMnO2,同时有部分锂迁移到表面,有90%的锂溶解在水中。在650 ℃之后,锂转化为LiMnO2的比例增加,锂在水溶液中的浸出率迅速下降到69.08%。

图5 450 ℃氢气还原报废LiNi1/3Co1/3Mn1/3O2 正极材料前后的EDS谱
Fig. 5 EDS images of waste LiNi1/3Co1/3Mn1/3O2 cathode materials before and after reduction at 450 ℃ by hydrogen
2.3.2 不同水浸出时间对锂浸出效率的影响
图8所示为不同水浸时间对锂浸出率的影响。对锂的水浸时间进行优化,在常温下,当水固比为4:1时,水浸出时间0.5、1、2和4 h的浸出率都在91%~94%之间,浸出时间的延长并不能增加锂的浸出率,所以最优水浸出时间为0.5 h,浸出液锂浓度为15.93 g/L,镍浓度为0.3 mg/L,钴浓度为0.7 mg/L,锰浓度为1.7 mg/L。由此可见,水浸工艺的原辅料简单易得,浸出时间短,锂回收杂质含量低,效率也高。

图6 不同还原温度的正极材料水浸出锂的浸出率
Fig. 6 Leaching rate of aqueous lithium from cathode materials at different reduction temperatures
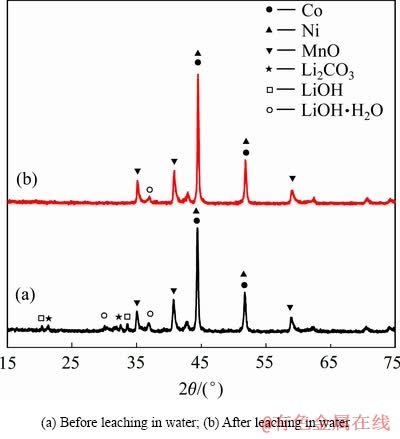
图7 450 ℃还原样品的水洗前后的XRD谱
Fig. 7 XRD patterns of waste LiNi1/3Co1/3Mn1/3O2 cathode materials under reduction at 450 ℃ before and after washing
2.3.3 酸洗对锂浸出效率的影响
经过最佳还原条件450 ℃ 还原和4:1的固液比的水浸0.5 h之后,LiNi1/3Co1/3Mn1/3O2正极粉组成锂、钴、镍、锰的含量分别为0.69%、29.51%、29.87%和27.21%,锂在固体残余物中的含量仍然偏高,为提高整体锂的回收率,在液固比为4:1的条件下,加入H2C2O4固体调节不同pH值洗涤效果如图9所示。由图9可见,在草酸水洗条件下,镍、钴、锰的溶解率小于0.05%,几乎不溶解;而随着pH降低,锂的溶解率由pH=8时的65%,提高到pH=5时的97.5%和pH=4时的97.24%,这是因为锂能溶于草酸,而镍、钴、锰不溶于草酸。随着草酸用量增加,pH降低,锂溶解越多,pH=5为最佳酸洗条件。经过以上工艺优化,剩余的固体渣中锂含量最低可降至0.02%。

图8 不同水浸时间对锂浸出率的影响
Fig. 8 Effect of different leaching time on lithium leaching rate

图9 不同pH条件下草酸洗涤效果
Fig. 9 Oxalic acid washing effect under different pH conditions
2.3.4 锂的沉淀回收
上述两步水洗的溶液和酸洗的溶液混合,用碳酸钠调节pH=14,得出碳酸锂的XRD谱如图10所示,和纯碳酸锂的晶型一致[32],纯度为99.5%。
2.4 镍钴锰的回收工艺及其机理分析
2.4.1 硫酸加入量对镍、钴、锰浸出效果的影响
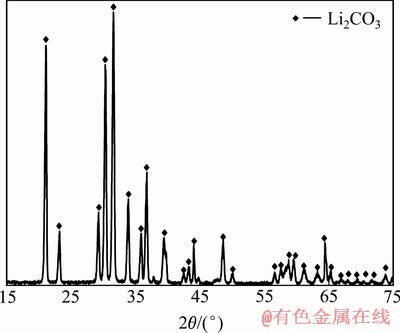
图10 回收的Li2CO3的XRD谱
Fig. 10 XRD pattern of recycled Li2CO3
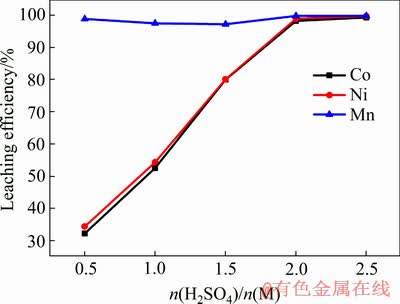
图11 硫酸加入过量比对镍钴锰元素的浸出率影响
Fig. 11 Effect of excess ratio of sulfuric acid added on leaching rate of Ni, Co and Mn
图11所示为镍钴锰固体混合物浸出效果图。由图11可见,在硫酸加入过量比为2时,镍、钴和锰的浸出率分别为96.88%、97.23%和99.78%。在硫酸加入过量比低于2时,明显可见MnO比钴、镍粉优先溶解。由图2、3和4可知,经过还原后,报废三元正极材料的球形结构被破坏,且镍、钴、锰由之前的+2、+3、+4还原成了低价的0(主相)和+2(表面)价态、0(主相)和+2(表面)价态、及+2价的MnO(主相和表面)。因此,在不加还原剂的条件下,硫酸能完全溶解镍钴锰的混合固体,又因为氧化物比金属盐更加容易溶于酸,所以在酸量不够的条件下,优先溶解MnO。
2.4.2 高锰酸钾沉淀锰的影响因素
酸浸之后,溶液中的Co2+浓度为21 g/L,Ni2+浓度为21 g/L,Mn2+浓度为19 g/L,锂离子含量为20 mg/L,pH=0.5。镍钴锰的三元混合溶液通过高锰酸钾氧化Mn2+为MnO2沉淀而和钴镍进行分离,具体方程式如(4)[6]所示:
3Mn2++ +2H2O→5MnO2+4H+ (4)
+2H2O→5MnO2+4H+ (4)
图12所示为高锰酸钾氧化过程中pH对金属沉淀效果的影响。由图12可见,按照如上化学方程式中的Mn2+和MnO4-的摩尔比加入KMnO4的溶液,在原始溶液pH条件下,Mn2+的沉淀率为95.95%,钴镍的沉淀率分别为1.95%和2.3%,这个可能是MnO2沉淀过程中的夹杂包裹导致的钴、镍沉淀。用0.5 mol/L的NaOH慢慢滴入浸出溶液调节溶液的pH,随着pH的增加,Mn2+的沉淀率逐渐上升至98%以上,基本上完全沉淀;同时,钴镍的沉淀率也随着pH的升高而逐渐增加,这是因为Ni2+的起始沉淀pH为2,Co2+的起始沉淀pH为3,随着pH增加,部分钴镍沉淀。综合考虑钴镍锰的沉淀率,选择pH为1进行高锰酸钾氧化沉淀锰的条件。

图12 高锰酸钾氧化过程中pH对金属沉淀效果的影响
Fig. 12 Effect of pH on metal precipitation in potassium permanganate oxidation process
2.4.3 萃取分离镍钴工艺
经过沉淀除Mn后,溶液中钴镍的浓度分别为10.14 g/L和10.3 g/L,锰的浓度为200 mg/L。为进一步分离钴镍,并降低溶液中锰浓度,研究中采用萃取工艺,选择P507作为萃取剂,探索并优化了萃取过程中负载有机相与水相比值(相比,即O/A)、萃取级数等关键工艺参数。
图13所示为相比对萃取率的影响。当萃取级数固定为4级、原始溶液pH=1,有机相组成为25% P507+75% 磺化煤油、萃取时间为5 min时,钴、镍、锰等金属的萃取率随着相比增加而提升;当O/A=4时,各种金属元素的萃取率基本达到最大值,其中钴为98.9%、镍为97.3%、锰为98.4%;继续提升O/A,萃取率增加有限,为减少有机相投入与消耗,故选择O/A=4。图14所示为萃取级数对萃取率的影响。由图14可知,当固定其他工艺参数时,级数增加上述三种金属的萃取率随之增加;级数≥3时,萃取率增加幅度有限。因此,选择萃取级数为3级,此时各元素萃取率分别为钴97.4%、镍96.1%、锰97.5%。
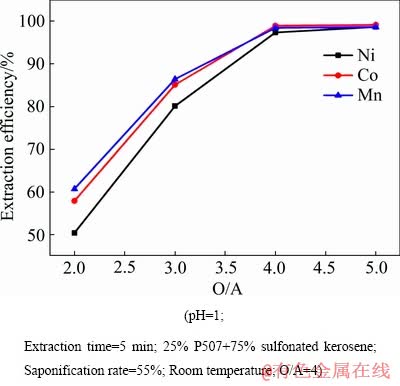
图13 相比对萃取率的影响
Fig. 13 Effect of phase ratio on extraction rate

图14 萃取级数对萃取率的影响
Fig. 14 Effect of extraction order on extraction rate

图15 钴、镍、锰反萃段相比及反萃级数对反萃率的影响
Fig. 15 Effects of phase ratio and reverse extraction order on different metal reverse extraction rates
图15所示为钴、镍、锰反萃段相比及反萃级数对反萃率的影响,其中图15(a)、(c)、(e)所示为相比对钴、镍、锰反萃率的影响,图15(b)、(d)、(f)所示为反萃级数对钴、镍、锰反萃率的影响。由图 15(a)、(c)、(e)可见,随着O/A比增加,反萃率逐渐下降;由图15(b)、(d)、(f)可见,随着反萃级数的增多,反萃率逐步提升。综合考虑成本、钴镍分离系数等因素,钴、镍、锰的反萃过程相比宜分别控制在5、4、8;反萃级数分别选择8级、10级、5级。经过萃取分离后,氯化钴溶液的钴含量为60 g/L,杂质含量为锰 7 mg/L和镍 2 mg/L;氯化镍浓度为57.8 g/L,杂质含量为锰 5 mg/L和钴 4 mg/L,满足材料再制备的氯化钴及氯化镍对原料要求。
3 结论
1) 经过高温氢还原及湿法冶金联用方法,探索出一种报废正极材料处理方法并优化了工艺,该方法中锂、镍、钴、锰的回收方法高效易行,具有产业化的潜力。
2) 报废正极材料经过450 ℃氢气还原3 h后,在层状镍钴锰酸锂中的锂迁移到表面,变成LiOH、LiOH・H2O和少量的Li2CO3;还原后表面的LiOH、LiOH・H2O和少量的Li2CO3,经过水浸+酸洗后,锂的浸出率可达到97.5%,最后沉淀可得纯度为99.5%的Li2CO3,实现了锂与镍、钴、锰的分离;
3) 报废正极材料经过氢气还原之后,镍钴锰由之前的+2、+3、+4价分别还原成了Ni0、Co0及Mn2+的MnO,并且发生金属迁移,其经过水洗后物料的表面相分别为Ni(OH)2和Co(OH)2及MnO;然后经过2倍硫酸酸浸后,镍、钴、锰浸出率分别为96.88%,97.23% 和99.78%。
4) 上述硫酸镍钴锰溶液在pH=1时,加入化学计量比的高锰酸钾沉淀锰,得到锰的沉淀分离率为98.46%;萃取分离后,氯化钴和氯化镍溶液中杂质含量低于10 mg/L,满足电池材料对原料的要求。
REFERENCES
[1] CHAGENES A, POSPIECH B. A brief review on hydrometallurgical technologies for recycling spent lithium-ion batteries[J]. Journal of Chemical Technology & Biotechnology, 2013, 88(7): 1191-1199.
[2] CHOI J W, AURBACH D. Promise and reality of post-lithium-ion batteries with high energy densities[J]. Nature Reviews Materials, 2016, 1(4): 1-16.
[3] ZENG Xian-lai, LI Jin-hui, SINGH N. Recycling of spent lithium-ion battery: A critical review[J]. Critical Reviews in Environmental Science and Technology, 2014, 44(10): 1129-1165.
[4] MESHRAM P, PANDEY B D, MANKHAND T R. Extraction of lithium from primary and secondary sources by pre-treatment, leaching and separation: A comprehensive review[J]. Hydrometallurgy, 2014, 150: 192-208.
[5] 余海军, 谢英豪, 张铜柱. 车用动力电池回收技术进展[J]. 中国有色金属学报, 2014, 24(2): P448-460.
YU Hai- jun, XIE Ying- hao, ZHANG Tong- zhu. Technical progress on power batteries recovery for electric vehicle[J]. The Chinese Journal of Nonferrous Metals, 2014, 24(2): 448-460.
[6] 吴 越, 裴 锋, 贾路路, 刘晓磊, 张文华, 刘 平. 废旧锂离子电池中有价金属的回收技术进展[J]. 稀有金属, 2013, 37(2): 320-329.
WU Yue, PEI Feng, JIA Lu- lu, LIU Xiao- lei, ZHANG Wen hua, LIU Ping. Overview of recovery technique of valuable metals from spent lithium ion batteries[J]. Chinese Journal of Rare Metals, 2013, 37(2): 320-329.
[7] HE Li-po, SUN Shu-ying, SONG Xing-fu, YU Jia-guo. Leaching process for recovering valuable metals from the LiNi1/3Co1/3Mn1/3O2 cathode of lithium-ion batteries[J]. Waste Management, 2017, 64: 171-181.
[8] WAN Rong-chi, LIN Yu-chuan, WU She-huang. A novel recovery process of metal values from the cathode active materials of the lithium-ion secondary batteries[J]. Hydrometallurgy, 2009, 99(3/4): 194-201.
[9] PANT D, DOLKER T. Green and facile method for the recovery of spent lithium nickel manganese cobalt oxide (NMC) based lithium ion batteries[J]. Waste Management, 2017, 60: 689-695.
[10] ZHANG X, ZHANG Xi-hua, CAO Hong-bin, XIE Yong-bing, NING Peng-ge, AN Hui-jiao, YOU Hai-xia, NAWAZ F. A closed-loop process for recycling LiNi1/3Co1/3Mn1/3O2 from the cathode scraps of lithium-ion batteries: Process optimization and kinetics analysis[J]. Separation and Purification Technology, 2015, 150: 186-195.
[11] TRAGER T, FRIEDRICH B, WEYHE R. Recovery concept of value metals from automotive lithium-ion batteries[J]. Chemie Ingenieur Technik, 2015, 87(11): 1550-1557.
[12] XIAO Song-wen, REN Guo-xing, XIE Mei-qiu, PAN Bing, FAN You-qi, WANG Feng-gang, XIA Xing. Recovery of valuable metals from spent lithium-ion batteries by smelting reduction process based on MnO-SiO2-Al2O3 slag system[J]. Journal of Sustainable Metallurgy, 2017, 3(4): 703-710.
[13] XIN Ya-yun, GUO Xing-ming, CHEN Shi, WANG Jing, WU Feng, XIN Bao-ping. Bioleaching of valuable metals Li, Co, Ni and Mn from spent electric vehicle Li-ion batteries for the purpose of recovery[J]. Journal of Cleaner Production, 2016, 116: 249-258.
[14] SUN L, QIU K Q, Vacuum pyrolysis and hydrometallurgical process for the recovery of valuable metals from spent lithium-ion batteries[J]. Journal of Hazardous Materials, 2011, 194: 378-384.
[15] HU Jun-tao, ZHANG Jia-liang, LI Hong-xu, CHEN Yong-qiang, WANG Cheng-yan. A promising approach for the recovery of high value-added metals from spent lithium-ion batteries[J]. Journal of Power Sources, 2017, 351: 192-199.
[16] LI Jian-gang, ZHANG Qian, HE Xiang-ming. Preparation of LiNi1/3Co1/3Mn1/3O2 cathode materials from spent Li-ion batteries[J]. Transaction of Nonferrous Metals Society of China, 2007, 17(S1-B): s897-s901.
[17] 陈 亮, 唐新村, 张 阳, 瞿 毅, 王志敏. 从废旧锂离子电池中分离回收钴镍锰[J]. 中国有色金属学报, 2011, 21(5): 1192-1198.
CHEN Lian, TANG Xin- cun, ZHANG Yan, QU Yi, WANG Zhi- min. Separation and recovery of Ni, Co and Mn from spentlithium ion batteries[J]. The Chinese Journal of Nonferrous Metals, 2011, 21(5): 1192-1198.
[18] WEI Chu, YA Li-zhang, XIA Chen, YAO Guo-huang, CUI Hong-you, WANG Min, WANG Jing. Synthesis of LiNi0.6Co0.2Mn0.2O2 from mixed cathode materials of spent lithium-ion batteries[J]. Journal of Power Sources, 2019, 449: 227567.
[19] YUN Yan-wang, TIAN Yu-wang, LI Jue-wu, MIN Xiao-bo, LIU-Hui, WEN Ding-qiang, KE Yong, WANG Zhong-bing, TANG Yi-wei, FU Hai-kuo. Recovery of valuable metals from spent ternary Li-ion batteries: Dissolution with amidosulfonic acid and d-glucose[J]. Hydrometallurgy, 2019, 190: 105162.
[20] 陈若葵, 李长东, 唐红辉, 谭群英, 王 杜. 一种从废旧锂离子电池中回收锂的方法. 中国, ZL104745823A[P]. 2015-03-12.
CHEN Ruo-kui, LI Chang-dong, TANG Hong-hui, TAN Qun-ying, WANG Du. Method for recycling lithium from waste lithium ion battery: China, 104745823A[P]. 2015-03-12.
[21] ZHANG X, XIE Y, CAO H, NAWAZ F, ZHANG Y. A novel process for recycling and resynthesizing LiNi1/3Co1/3Mn1/3O2 from the cathode scraps intended for lithium-ion batteries[J]. Waste Management, 2014, 34(9): 1715-1724.
[22] PENG Le-le, ZHU Yue, KHAKOO U, CHEN Da-hong, YU Gui-hua. Self-assembled LiNi1/3Co1/3Mn1/3O2 nanosheet cathodes with tunable rate capability[J]. Nano Energy, 2015, 17: 36-42.
[23] ZILBERMAN P. The CO2 absorber based on LiOH[J]. Acta Medica Marisiensis, 2015, 61(1): 4-6.
[24] KIMURA K, SAKAMTO T, MUKAI T, IKEUCHI Y, YAMASHITA N, ONISHI K, ASAMI K, YANAGIDA M. Improvement of the cyclability and coulombic efficiency of Li-ion batteries using Li[Ni0.8Co0.15Al0.05]O2 cathode containing an aqueous binder with pressurized CO2 gas treatment[J]. Journal of The Electrochemical Society, 2018, 165(2): A16-A20.
[25] ZHOU Hui, LI Ying-shun, ZHANG Jiao-long, KANG Wen-pei, YU DY W. Low-temperature direct synthesis of layered m-LiMnO2 for lithium-ion battery applications[J]. Journal of Alloys and Compounds, 2016, 659: 248-254.
[26] POVEY A F, SHERWOOD P M A. Covalent character of lithium compounds studied by X-ray photoelectron spectroscopy[J]. Journal of the Chemical Society, Faraday Transactions 2: Molecular and Chemical Physics, 1974, 70(0): 1240-1246.
[27] WOOD K N, TEETER G. XPS on Li-battery-related compounds: Analysis of inorganic SEI phases and a methodology for charge correction[J]. ACS Applied Energy Materials, 2018, 1(9): 4493-4504.
[28] AURBACH D, POLLAK E, ELAZARI R, SALITRA G, KELLEY C S, AFFINITO J. On the surface chemical aspects of very high energy density, rechargeable Li-sulfur batteries[J]. Journal of The Electrochemical Society, 2009, 156(8): A694- A702.
[29] AN S J, LI Jian-lin, SHENG Yang-ping, DANIEL C, WOOD D L. Long-term lithium-ion battery performance improvement via ultraviolet light treatment of the graphite anode[J]. Journal of The Electrochemical Society, 2016, 163(14): A2866- A2875.
[30] CHO T H, PARK S M, YOSHIO M, HIRAI T, HIDESHIMA Y. Effect of synthesis condition on the structural and electrochemical properties of Li[Ni1/3Mn1/3Co1/3]O2 prepared by carbonate co-precipitation method[J]. Journal of Power Sources, 2005, 142(1/2): 306-312.
[31] BIESINGER M C, PAYNE B P, GROSVENOR A P, LAU L W M, GERSON A R, SMART, R S C. Resolving surface chemical states in XPS analysis of first row transition metals, oxides and hydroxides: Cr, Mn, Fe, Co and Ni[J]. Applied Surface Science, 2011, 257(7): 2717-2730.
[32] ZHOU Zhi-yong, LIANG Fan, QIN-Wei, FEI Wei-yang. Coupled reaction and solvent extraction process to form Li2CO3: Mechanism and product characterization[J]. AIChE Journal, 2014, 60(1): 282-288.
Recovering valuable metals from waste ternary cathode materials of power battery by combined high temperature hydrogen reduction and hydrometallurgy
GUO Miao-miao1, 2, 3, 4, XI Xiao-li1, 2, ZHANG Yun-he3, 4, 5, YU Shun-wen3, 4, LONG Xiao-lin3, 4, JIANG Zheng-kang3, 4, 5, NIE Zuo-ren1, 2, XU Kai-hua3, 4, 5
(1. College of Materials Science and Engineering, Beijing University of Technology, Beijing 100124, China;
2. National Engineering Laboratory for Industrial Big-data Application Technology, Beijing 100124, China;
3. GEM Jingmen New Material Co., Ltd., Jingmen 448124, China;
4. Chinese National WEEE Recycling Engineering Research Center, Jingmen 448124, China;
5. GEM Co., Ltd., Shenzhen 518101, China)
Abstract: The nickel, cobalt, manganese and lithium metals in the ternary cathode material of scrapped power battery were recovered by high temperature hydrogen reduction and hydrometallurgical method, and the recovery mechanism and process were studied. The results show that the Li in the layered Ni-Co-Mn oxide migrates to the surface and becomes LiOH, LiOH・H2O and a small amount of Li2CO3 after high temperature reduction. The Co2+, Ni3+ and Mn4+ are reduced to Co0, Ni0 and MnO, respectively. And the surface phases of the reduced materials are referred as Ni(OH)2, Co(OH)2 and MnO after Li leaching. The Li2CO3 with 99.5% in purity is obtained from the water leaching, acid washing, and precipitation processes of LiOH, LiOH・H2O and a small amount of Li2CO3, which realizes the separation of Li from Co-Ni-Mn. After the sulfuric acid leaching of the reduced Ni, Co and MnO, the leaching rates of Ni, Co and Mn are 96.88%, 97.23% and 99.78%, respectively. The precipitation and separation rate of Mn is 98.46% after the oxidizing precipitation and extraction separation of the leached solution, and the impurity contents in CoCl2 and NiCl2 solutions are less than 10 mg/L after the extraction separation.
Key words: LiNi1/3Co1/3Mn1/3O2; ternary cathode materials; waste; hydrogen reduction; recovery; mechanism
Foundation item: Project(2017.1.1-2019.12.31) supported by the Green Manufacturing System Integration Project 2017 from the Ministry of Industry and Information Technology, China
Received date: 2019-08-08; Accepted date: 2020-05-26
Corresponding author: XI Xiao-li; Tel: +86-10-67396638; E-mail: xixiaoli@bjut.edu.cn
(编辑 何学锋)
基金项目:工信部2017年绿色制造系统集成项目(2017.1.1-2019.12.31)
收稿日期:2019-08-08;修订日期:2020-05-26
通信作者:席晓丽 ,教授,博士;电话:010-67396638;E-mail:xixiaoli@bjut.edu.cn